




肾血管性高血压(renovascular hypertension,RVH)是各种原因造成肾动脉狭窄或阻塞后产生的继发性高血压,是仅次于肾脏疾病导致继发性高血压的第2位原因[1]。
近年来,关于雌激素在心血管疾病发生、发展过程中的作用,逐渐引起了研究者的关注。流行病学调查研究结果显示,女性绝经后与同年龄绝经前妇女相比,心脑血管疾病和高血压的发病率明显升高[2]。研究发现,雌激素对心血管疾病有保护作用,并参与血压的调节[3], 其作用主要通过下调肾素血管紧张素系统(renin angiotensin system,RAS)重要组分表达来实现[4]。我们前期研究发现,♂ RVH大鼠的血压水平低于♀,切除双侧卵巢导致雌激素低下后,血压下降并接近♂动物[5]。本研究通过检测RVH及雌激素低下合并RVH大鼠的血管组织中血管紧张素转化酶1(angiotensin converting enzyme 1,ACE1)、血管紧张素Ⅱ的1a型受体(angiotensin type 1a receptor,AT1aR)、血管紧张素Ⅱ的1b型受体(angiotensin type 1b receptor,AT1bR)、血管紧张素Ⅱ 2型受体(angiotensin type 2 receptor,AT2R)的mRNA,以及ACE1、AT1R、AT2R蛋白表达,探讨性别及雌激素水平对肾素血管紧张素系统的影响。
1 材料 1.1 实验动物10周龄的45只SD大鼠(♀30只,♂15只),体质量(180±20)g, 购自新疆医科大学实验动物中心,许可证号:SCXK(新)20160003。根据手术类型分为雄性手术组(2K1C-M)、雌性手术组(2K1C-F)、雌性去势组(2K1C-OVX),手术后常规喂养32周。
1.2 试剂雌二醇放射免疫分析试剂盒、血管紧张素Ⅱ(angiotensin Ⅱ,Ang Ⅱ)放射免疫分析试剂盒(北京北方生物技术研究所);戊巴比妥钠(Sigma公司);总蛋白抽提试剂盒和蛋白定量试剂盒(上海天根生物有限公司);ACE1、AT1R、AT2R抗体(美国Santa Cruz公司);HRP标记的二抗、免疫印迹增强化学发光试剂盒(尚柏生物医学技术有限公司);TRIzol、RNase inhibitor、Oligd(T)18、dNTPs、10×PCR buffer,均为TaKaRa公司产品。
1.3 仪器Powerlab生物信号处理系统(澳大利亚AD Instruments公司);蛋白电泳及转膜仪(美国Bio-Rad公司);UV-2802紫外分光光度计(上海尤尼柯仪器有限公司);Real time PCR仪(ABI公司);数码凝胶图像处理系统(上海天能)。
2 方法 2.1 两肾一夹(two-kidney one-clip,2K1C)RVH动物模型的制备30只SD大鼠,♀♂各半,以戊巴比妥钠40 mg·kg-1腹腔注射麻醉,分离左侧肾动脉,套U型银夹子(内径为0.25 mm)以狭窄肾动脉,术后分层缝合切口,后肢肌肉注射青霉素钠(每只80 000 U)预防感染,完成2K1C手术。
2.2 高血压合并雌激素低下动物模型的制备♀SD大鼠(15只)做左侧肾动脉狭窄手术的同时,分离双侧卵巢,结扎卵巢动脉后切除双侧卵巢(ovariectomized,OVX),手术后给予青霉素(每只80 000 U)预防感染,完成2K1C-OVX手术。麻醉清醒前注意保温,以防冻死,清醒后在SPF级实验室自由进水、进食,常规喂养32周。
2.3 大鼠动脉血压的测定术后32周后,戊巴比妥钠按40 mg·kg-1腹腔注射麻醉,充满肝素化生理盐水的PE50导管插入右侧颈总动脉;将导管接压力换能器,信号输入至Powerlab生物信号处理系统测动物的收缩压(systolic blood pressure,SBP)和舒张压(diastolic blood pressure,DBP)。以SBP>18.62 kPa为筛选标准,血压高于此标准入选,剔除低者。
2.4 标本留取将符合标准的动物取2 mL血,室温下静置0.5~1 h后, 300 r·min-1离心10 min,取上清液,置-80 ℃冰箱保存。取血2 mL迅速注入含酶抑制剂(3.0 mmol·L-1 EDTA二钠20 μL、3.4 mmol·L-1 8-羟基喹啉20 μL、3.2 mmol·L-1二巯基丙醇10 μL)的抗凝管中,摇匀,300 r·min-1、4 ℃离心15 min,将上清液置于-80 ℃冰箱保存,用放射免疫法按说明书测雌二醇和Ang Ⅱ的浓度。
2.5 qPCR法检测大鼠血管组织中ACE1、AT1aR、AT1bR、AT2R的mRNA表达取各组大鼠动脉组织100 mg,在液氮中磨成粉状,加入1 mL TRIzol试剂,氯仿抽提和乙醇沉淀方法准备总RNA。检测RNA样品在260 nm和280 nm处的吸光度。在AMV逆转录酶的作用下,以2.0 μg总RNA为模板,逆转录成cDNA,总反应体系为25 μL,所得cDNA于-20 ℃冻存。引物序列见Tab 1。待测样品均作复管,每次实验均以不加模板的PCR体系作为阴性对照。反应条件为:94 ℃,5 min(热启动),94 ℃,30 s(变性),65 ℃,30 s(退火),72 ℃,30 s(延伸),40个循环。结果用MJ opticon monitor软件分析。
| Gene | Primer sequence(5′to3′) | Product size/bp | |
| ACE1 | Forward | GATTGCAGCCGGGCAACTTT | 137 |
| Reverse | CTCCTCCGTGATGTTGGTGT | ||
| AT1aR | Forward | CTCTGCCACATTCCCTGAGTT | 212 |
| Reverse | CTTGGGGCAGTCATCTTGGA | ||
| AT1bR | Forward | TCAAGCTGTGATTCTGTCCCA | 246 |
| Reverse | GCTACAACTTCAATCAAACAACAGC | ||
| AT2R | Forward | AGGGCCCTAAAAAGGTGTCC | 77 |
| Reverse | AGGAAGGGTTGCCAAAAGGA |
称取0.1 g胸主动脉组织,剪碎组织,加入0.5 mL组织裂解液(RIPA)进行裂解, 4 ℃、12 000×g离心10 min, 取上清液,用Bradford法测定所提取的蛋白浓度。将样品适当稀释后,95 ℃变性5 min,冷却后-20 ℃冻存。SDS-PAGE电泳分离,转移至PVDF膜上,以封闭液室温封闭膜1 h后,加入一抗ACE1(1 :2 000)、AT1R(1 :1 000)、AT2R(1 :500)、内参β-actin(1 :500),4 ℃孵育过夜。用HRP结合的二抗在室温孵育1 h,DAB试剂直接在PVDF膜上显色。采用Imagetool凝胶图像分析软件对PVDF膜扫描分析,以每组目的蛋白表达的面积灰度值与β-actin表达的面积灰度值的比值作为半定量分析值。
2.7 数据统计所有数据采用x±s表示,运用SPSS 17.0统计软件进行统计学分析,t检验用于组间比较。
3 结果 3.1 各组大鼠血压、Ang Ⅱ浓度及雌激素水平的比较2K1C-F组的收缩压明显高于2K1C-M组和2K1C-OVX组(P < 0.05),各组动物的舒张压差异无统计学意义;与2K1C-F组比较,2K1C-M组、2K1C-OVX组的Ang Ⅱ含量明显升高(P < 0.01);与2K1C-M组相比,2K1C-OVX组的收缩压及Ang Ⅱ含量差异无统计学意义。与2K1C-F组相比,切除卵巢之后雌激素含量降低,但差异无统计学意义。见Tab 2。
| Group | SBP/kPa | DBP/kPa | E2/ng·L-1 | Ang Ⅱ/ng·L-1 |
| 2K1C-F | 23.94±2.98 | 17.69±2.01 | 13.54±11.56 | 0.87±0.09 |
| 2K1C-M | 22.74±2.18* | 17.29±1.84 | 3.42±1.93* | 1.23±0.12** |
| 2K1C-OVX | 21.41±3.39* | 16.62±2.87 | 9.80±4.70# | 1.15±0.06** |
| *P < 0.05, **P < 0.01 vs 2K1C-F; #P < 0.05, ##P < 0.01 vs 2K1C-M | ||||
Tab 3结果显示,与2K1C-F组比较,2K1C-M组的ACE1、AT1aR、AT1bR、AT2R mRNA表达明显上调(P < 0.05),2K1C-OVX组的ACE1、AT1bR mRNA表达明显上调(P < 0.05),AT2R明显下调(P < 0.05);与2K1C-M组比较,2K1C-OVX组ACE1、AT1bR、AT2R的mRNA水平明显下调(P < 0.05), AT1aR也下调,但差异无统计学意义。与2K1C-F组比较,2K1C-M组,2K1C-OVX组的AT1aR/AT2R和AT1bR/AT2R比值均明显升高,与2K1C-M组比较,2K1C-OVX组的AT1aR/AT2R比值明显下降,AT1bR/AT2R比值明显升高。
| Group | ACE1 | AT1aR | AT1bR | AT2R | AT1aR/AT2R | AT1bR/AT2R |
| 2K1C-F | 1.000±0.022 | 1.003±0.082 | 1.003±0.082 | 1.000±0.022 | 1.005±0.101 | 1.005±0.101 |
| 2K1C-M | 3.301±0.233* | 1.477±0.104* | 3.394±0.240* | 1.167±0.082* | 1.266±0.003** | 2.911±0.004** |
| 2K1C-OVX | 1.555±0.290*# | 1.370±0.240 | 1.573±0.275*# | 0.714±0.125*# | 1.916±0.004**## | 2.204±0.007**## |
| *P < 0.05, **P < 0.01 vs 2K1C-F; #P < 0.05 vs 2K1C-M | ||||||
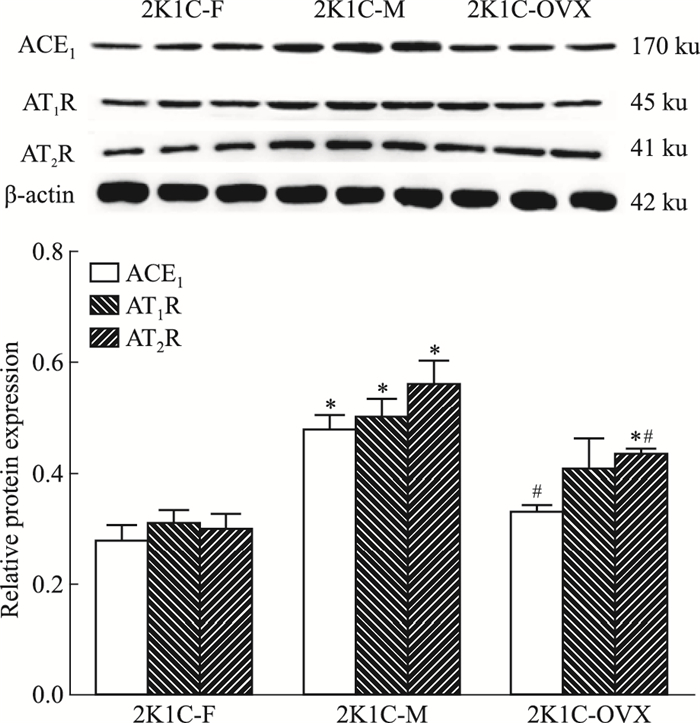
如Fig 1所示,与2K1C-F组比较,2K1C-M组ACE1、AT1R、AT2R的蛋白表达明显上调(P < 0.05),2K1C-OVX组AT2R的蛋白表达明显上调(P < 0.05),ACE1、AT1R的相对表达量显示上调趋势,但差异无统计学意义;与2K1C-M组比较, 2K1C-OVX组ACE1、AT2R的蛋白表达明显降低(P < 0.05),AT1R也降低,但差异无统计学意义。
|
| Fig 1 Protein expression of ACE1, AT1R, AT2R in vascular tissue(x±s, n=3) *P < 0.05 vs 2K1C-F; #P < 0.05 vs 2K1C-M |
本研究选用RVH动物模型,制作这种动物模型最常用的方法是两肾一夹(2K1C)[6], 此模型的成模原理主要是激活肾素血管紧张素醛固酮系统,模型建立成功后比较稳定,重复性也较好。
本研究发现,2K1C-F组的血压高于2K1C-M组和2K1C-OVX组。在前期研究中我们发现,2K1C-F组的内皮素(endothelin-1,ET-1)的含量大于2K1C-M组和2K1C-OVX组[5],推测NO-内皮素系统的变化可能是♀动物的血压高于♂的原因,但雌激素促进ET-1释放的机制尚不确定。雌性2K1C-F组Ang Ⅱ的含量,ACE1、AT1R的mRNA及蛋白表达均低于2K1C-M组,提示RAS的mRNA及蛋白表达均有性别差异性,以及雌激素可下调ACE1-Ang Ⅱ-AT1R轴的活性。文献研究结果表明,RAS的各个组分在女性和男性中的表达都有差异[7-8],且雌激素可下调组织中ACE1和AT1R受体的表达[9]。Ang Ⅱ主要作用于两种受体:血管紧张素Ⅱ1型受体(AT1R)和血管紧张素Ⅱ2型受体(AT2R)。Ang Ⅱ与AT1R结合,产生血管收缩、水钠潴留、醛固酮释放、升高血压等生理效应。对于AT2R的生理作用有争议,但越来越多的证据表明,AT2R引起的生理效应与AT1R相反,AT2R具有舒张血管和对抗AT1R介导的收缩血管作用[10]。有研究报道,♀自发性高血压动物主动脉中,AT1R的mRNA表达水平明显高于♂和去卵巢组,AT2R的表达反而雌性的低于雄性和去卵巢组,但雌性动物AT1R/AT2R的比值明显低于雄性和去卵巢组[11]。本研究发现,2K1C-F组中AT2R的mRNA表达水平明显低于2K1C-M组,但2K1C-F组AT1aR/AT2R、AT1bR/AT2R比值明显低于2K1C-M组和2K1C-OVX组,表明雌激素下调AT1R表达的影响大于AT2R。
本研究发现,卵巢切除后雌激素水平降低,且Ang Ⅱ含量及ACE1、AT1R的表达升高。研究发现,大鼠卵巢切除后不仅上调ACE1、AT1R的表达,且下调AT2R的表达[12]。实验表明,与同龄男性比较,绝经后女性RAS基因表达水平增加[13]。但在我们实验中可能是因为2K1C-OVX组的雌激素浓度仍然高于2K1C-M组,导致了2K1C-M组的RAS表达高于2K1C-OVX组。
综上所述,RVH大鼠血管组织中Ang Ⅱ的含量,AT1R、AT2R、ACE1的mRNA及蛋白表达存在性别及雌激素水平差异性:切除卵巢的RVH大鼠和♂RVH大鼠的ACE1-Ang Ⅱ-AT1R轴的mRNA及蛋白表达量均高于♀RVH大鼠。但血管组织中RAS的性别差异性和雌激素差异性不能解释血压的差异性。
| [1] |
Feng M T, W H, Jiang W W, et al. Epidermal growth factor receptor involvement in cardiovascular remodeling in renovascular hypertensive rats[J]. Chin Pharmacol Bull, 2016, 32(5): 625-31. |
| [2] |
Kamel H, Navi B B, Sriram N, et al. Risk of a thrombotic event after the 6-week postpartum period[J]. N Engl J Med, 2014, 370(14): 1307-15. doi:10.1056/NEJMoa1311485 |
| [3] |
Prabhushankar R, Krueger C, Manrique C. Membrane estrogen receptors: their role in blood pressure regulation and cardiovascular disease[J]. Curr Hypertens Rep, 2014, 16(1): 408-9. doi:10.1007/s11906-013-0408-6 |
| [4] |
Bukowska A, Spiller L, Wolke C, et al. Protective regulation of the ACE2/ACE gene expression by estrogen in human atrial tissue from elderly men[J]. Exp Biol Med, 2017, 242(14): 1412-23. doi:10.1177/1535370217718808 |
| [5] |
邬利娅·伊明, 阿瓦古丽·达吾提, 帕提古丽·阿布拉, 等.性别对肾血管性高血压大鼠血压及靶器官损伤的影响[J].新疆医科大学学报, 2018, 41(4): 389-93. Yiming W, Dawuti A, Abula P, et al. Gender specific effect in development of renovascular hypertension[J]. J Xinjiang Med Univ, 2018, 41(4): 389-93. http://www.cnki.com.cn/Article/CJFDTotal-XJYY201804001.htm |
| [6] |
Baylis C. Nitric oxide synthase derangements and hypertension in kidney disease[J]. Curr Opin Nephrol Hypertens, 2012, 21(1): 1-6. |
| [7] |
Schneider M P, Wach P F, Durley M K, et al. Sex differences in acute ANG Ⅱ-mediated hemodynamic responses in mice[J]. Am J Physiol Regul Integr Comp Physiol, 2010, 299(3): R899-906. doi:10.1152/ajpregu.00638.2009 |
| [8] |
Sullivan J C, Bhatia K, Yamamoto T, et al. Angiotensin(1-7) receptor antagonism equalizes angiotensin Ⅱ-induced hypertension in male and female spontaneously hypertensive rats[J]. Hypertension, 2010, 56(4): 658-66. doi:10.1161/HYPERTENSIONAHA.110.153668 |
| [9] |
Dean S A, Tan J, O'Brien E R, et al. 17beta-estradiol downregulates tissue angiotensin-converting enzyme and ANG Ⅱ type 1 receptor in female rats[J]. Am J Physiol Regul Integr Comp Physiol, 2005, 288(3): R759-66. doi:10.1152/ajpregu.00595.2004 |
| [10] |
Duke L M, Evans R G, Widdop R E. AT2 receptors contribute to acute blood pressure-lowering and vasodilator effects of AT1 receptor antagonism in conscious normotensive but not hypertensive rats[J]. Am J Physiol Heart Circ Physiol, 2005, 288(5): H2289-97. doi:10.1152/ajpheart.01096.2004 |
| [11] |
Silva-Antonialli M M, Tostes R C, Fernandes L, et al. A lower ratio of AT1/AT2 receptors of angiotensin Ⅱ is found in female than in male spontaneously hypertensive rats[J]. Cardiovasc Res, 2004, 62(3): 587-93. doi:10.1016/j.cardiores.2004.01.020 |
| [12] |
袁梦琪, 段争, 孙彦利, 等. 雌激素对低氧性肺动脉高压大鼠体内血管紧张素转换酶-血管紧张素Ⅱ-血管紧张素受体-1轴的影响[J]. 中华医学杂志, 2014, 94(22): 1696-700. Yuan M Q, Duan Z, Sun Y L, et al. Effects of estrogen on ACE-Ang Ⅱ-AT1 axis in ovariectomy and hypoxic pulmonary hypertensionrats[J]. Natl Med J Chin, 2014, 94(22): 1696-700. doi:10.3760/cma.j.issn.0376-2491.2014.22.005 |
| [13] |
Ramos-Filho A C, A Faria J, Calmasini F B, et al. The renin-angiotensin system plays a major role in voiding dysfunction of ovariectomized rats[J]. Life Sci, 2013, 93(22): 820-9. doi:10.1016/j.lfs.2013.09.008 |