

2. 陕西理工大学 中德天然产物研究所,陕西 汉中 723000;
3. 陕西理工大学 维生素D生理与应用研究所,陕西 汉中 723000
陈琛(1978-)男,博士,副教授,研究方向:天然药物资源开发利用,通讯作者,E-mail:cchen2008@yahoo.com
 ,
HUANG Jie-ru1,
QI Shan-shan3
,
HUANG Jie-ru1,
QI Shan-shan3
 ,
CHEN Chen1,2
,
CHEN Chen1,2
 ,
HE Jia1,
Zhao Ting1,
Pu Jing-fei1,
Zhao Man1
,
HE Jia1,
Zhao Ting1,
Pu Jing-fei1,
Zhao Man1
2. Chinese-German Joint Lab for Natural Product Research, Shaanxi University of Technology, Hanzhong, Shaanxi 723000, China;
3. Vitamin D Research Institute, Shaanxi University of Technology, Hanzhong, Shaanxi 723000, China
骨质疏松是糖尿病常见的慢性并发症之一,糖尿病患者中有50%合并骨质疏松症[1-2]。糖尿病性牙槽骨丢失是糖尿病的慢性并发症之一,主要表现为牙槽骨骨量减少,骨组织显微结构受损,骨脆性增加,骨密度降低,易发骨折[3]。红景天是我国的传统中药红景天的活性成分,具有抗氧化、抗炎、降血糖、神经保护等诸多功效[4-6]。我们前期的研究表明,其对糖尿病性骨质疏松症具有保护作用[7],但其对糖尿病性牙槽骨丢失是否具有保护作用,目前尚未见报道。本实验通过红景天提取物(含红景天苷20%)干预治疗,观察糖尿病大鼠牙槽骨结构变化及相关骨代谢因子的变化,探讨其对糖尿病大鼠牙槽骨丢失的影响,以期为糖尿病性牙槽骨丢失的防治提供理论依据。
1 材料与方法 1.1 实验动物SPF级3月龄♀未孕SD大鼠40只,体质量(230~246) g,由成都达硕实验动物中心提供,许可证号:SCXK(川)2015-030。分笼饲养,自由饮水,动物房温度(22~26) ℃,适应性饲养1周后进行实验。
1.2 试剂与仪器红景天提取物(其中红景天苷含量20%),购自陕西森弗天然制品有限公司;链脲佐菌素,购自阿拉丁公司;钙标准品,购自Sigma公司;大鼠碱性磷酸酶(alkaline phosphatase,ALP)、骨保护素(osteoprotegerin,OPG)、核因子NF-κB配体的受体激活剂(receptor activator of nuclear factor kappa-Β ligand,RANKL)检测试剂盒,均购自南京建成生物工程公司。血糖计、血糖试纸(罗氏公司);酶标仪(Biotek);AAS-900T原子吸收光谱仪(美国PE公司);RM2235病理组织切片机(Leica公司);高速离心机(Eppendorf)。
1.3 糖尿病大鼠模型的构建将大鼠禁食12 h,腹腔一次性注射链脲佐菌素(60 mg·kg-1),于造模后3 d及造模后1周,所有大鼠于尾静脉采血,测定全血血糖并记录。若2次血糖值均≥16.7 mmol·L-1,表明糖尿病造模成功。空白组大鼠给予柠檬酸缓冲液腹腔注射。
1.4 动物分组及给药糖尿病模型构建成功后,对上述动物进行重新分组,分别为空白组(Control)、模型组(Model)、红景天组(RRE),每组10只,红景天组灌胃给予红景天提取物150 mg·kg-1·d-1,连续给药8周。
1.5 血清生化检测大鼠给药8周末,尾静脉采血测定空腹血糖,腹腔注射10 g·L-1戊巴比妥钠麻醉后,采集眼眶静脉血,4 000 r·min-1离心10 min,分离血清,分别按照试剂盒说明书检测血清ALP、OPG、RANKL,采集实验数据,计算OPG/RANKL比值。
1.6 血钙检测采用火焰原子吸收法进行血钙测定。钙稀释液:盐酸:乙二醇:水以体积比0.5 :5 :94.5混合。供试样:吸取60 μL血清加到5.94 mL钙稀释液中;空白样:5.94 mL钙稀释液。按仪器工作条件测定空白、标准溶液和供试样的吸光度,仪器自动进行标准曲线的绘制,具体方法见参考文献[8]。
1.7 骨组织病理分析给药第8周末,颈椎脱臼处死大鼠,取各组大鼠牙槽骨,固定于4%多聚甲醛24 h后,经10% EDTA(pH 8.0)脱钙28 d,常规脱水并进行石蜡切片(5 μm),HE染色,显微观察各组大鼠牙槽骨结构、骨小梁宽度、骨小梁分离度等。
1.8 破骨细胞的组织化学染色采用抗酒石酸酸性磷酸酶(tartrate-resistant acid phosphatase,TRAP)法[9]对牙槽骨组织石蜡切片进行组织化学染色,观察并计数牙槽骨中破骨细胞数量。
1.9 统计学处理利用SPSS 17.0统计软件对数据进行单因素组间方差分析和比较,结果以x±s表示。
2 结果 2.1 各组大鼠血糖、血清ALP和Ca检测结果如Tab 1所示,模型组血糖、血清ALP较空白组明显升高(P < 0.01),血清Ca均较空白组明显降低(P < 0.05);给予红景天提取物8周后,大鼠血糖、血清ALP水平较模型组明显降低(P < 0.01),血清Ca水平较模型组明显升高(P < 0.05)。
| Group | Blood glucose /mmol·L-1 |
ALP/ U·L-1 |
Ca/ mg·L-1 |
| Control(n=10) | 5.67±0.36 | 924.80±56.73 | 96.53±5.21 |
| Model(n=7) | 22.98±3.43** | 1433.33±104.24** | 69.82±4.50* |
| RRE(n=10) | 12.13±2.35## | 1047.82±75.71## | 87.94±5.12# |
| *P<0.05, **P<0.01 vs control; #P<0.05, ##P<0.01 vs model | |||
如Tab 2所示,模型组大鼠血清OPG水平较空白组明显降低(P<0.01),给予红景天提取物8周后血清OPG较模型组升高。RANKL的检测结果显示,模型组血清RANKL水平较空白组明显增加(P<0.01),给予红景天提取物8周后血清RANKL水平较模型组降低,且红景天组与空白组血清RANKL差异无显著性(P>0.05)。各组大鼠血清OPG/RANKL比值统计结果的变化趋势与OPG的变化趋势一致。
| Group | OPG/ ng·L-1 |
RANKL/ ng·L-1 |
OPG/ RANKL ratio |
| Control(n=10) | 4.89±0.47 | 1.25±0.20 | 3.89±0.33 |
| Model(n=7) | 2.17±0.23** | 2.23±0.38** | 1.24±0.19* |
| RRE(n=10) | 4.21±0.35## | 1.14±0.09## | 3.68±0.37# |
| *P<0.05, **P<0.01 vs control; #P<0.05, ##P<0.01 vs model | |||
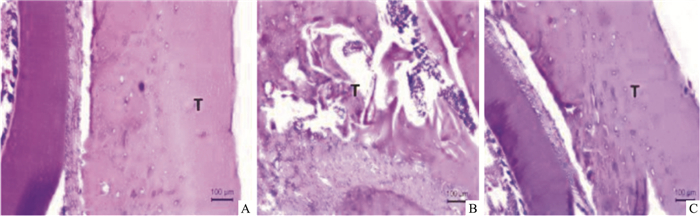
如Fig 1所示,空白组牙槽骨形态结构紧密;与空白组相比,糖尿病大鼠牙槽骨边缘见到活跃的破骨细胞性骨吸收陷窝,可见骨细胞呈扁平或星形,胞质嗜碱性,颌骨骨小梁较细小,髓腔显得宽大,骨小梁排列稀疏、变细变薄,间距增大,结构紊乱。红景天治疗组可见骨质疏松有所改善,颌骨内骨小梁变粗变大呈片状,交织成网状,断裂、吸收现象改善,骨细胞细密,分布均匀。
|
| Fig 1 Alveolar bone tissue morphology of rats in each group(HE staining×200) A: Control group; B: Model group; C: RRE group. T refers to trabecular bone. |
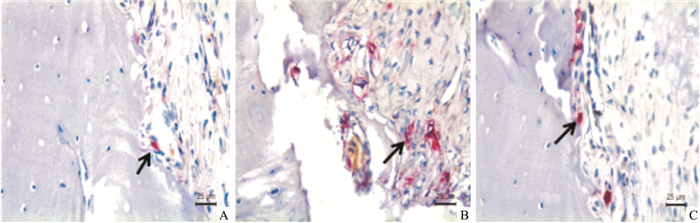
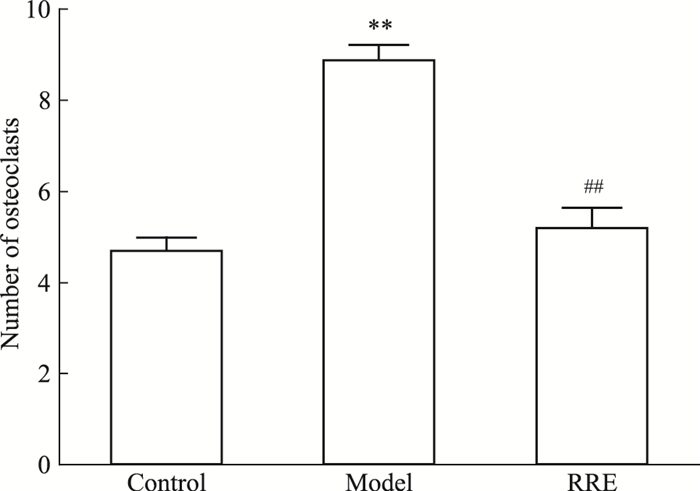
如Fig 2所示,破骨细胞由多核巨细胞组成,经TRAP染色后呈红色或暗红色,主要分布于骨髓腔边缘。经破骨细胞计数发现,模型组每高倍视野下破骨细胞数量较空白组明显增加,红景天治疗组破骨细胞数较模型组降低(P>0.05),见Fig 3。
|
| Fig 2 TRAP stain of osteoclasts in alveolar bone of rats in each group(TRAP staining×400) A: Control group; B: Model group; C: RRE group. The arrow points to the osteoclasts. |
|
| Fig 3 Number of osteoclasts inalveolar bone of rats in each group **P < 0.01 vs control; ##P < 0.01 vs model |
糖尿病牙槽骨骨质疏松是全身系统性骨质疏松的一个表现,它与牙周病、牙松动、牙脱落、口腔种植等口腔病变有密切的关系[10]。本次实验采用链脲佐菌素腹腔注射法构建的糖尿病性牙槽骨损伤大鼠模型,从牙槽骨组织形态及破骨细胞计数结果可以看出,模型组牙槽骨骨小梁的微观形态呈现出骨小梁稀疏、变薄变窄,骨小梁间距明显增大,说明牙槽骨微观结构被破坏,模型构建成功。
本研究通过建立链脲佐菌素诱导的牙槽骨丢失模型,发现红景天提取物对于糖尿病性牙槽骨丢失具有保护作用,通过组织病理学观察发现,其可有效治疗糖尿病性牙槽骨丢失,模型大鼠给予红景天提取物8周后,牙槽骨结构明显改善,牙槽骨破骨细胞数量明显降低。血糖检测发现,其具有明显降血糖功效,这与以往报道一致。
血清骨代谢检测发现,红景天提取物给药8周后,血清Ca、OPG含量明显增加,血清ALP、RANKL水平较模型组明显降低。ALP存在于成骨细胞中,可通过分解磷酸酯的无机磷促进骨矿物质沉积,骨形成与ALP的活性度相关[11]。本实验结果表明,模型组ALP含量高于正常对照组,说明骨组织中骨转换加快,红景天治疗后ALP水平降低,表明红景天提取物可抑制骨转换。
OPG-RANKL双分子系统是一个在生理和病理条件下调节成骨细胞生成和骨吸收的关键因子,OPG是破骨细胞生成抑制因子,RANKL是破骨细胞分化的诱导因子。血清OPG以及OPG/RANKL比值升高时,说明骨形成增加而骨吸收减少[12-14]。本实验结果显示,模型大鼠OPG水平及OPG/RANKL比值降低,给予红景天治疗后,OPG水平及OPG/RANKL比值升高。上述结果证实红景天提取物对糖尿病性牙槽骨损伤具有保护作用,其机制可能是通过调节OPG/RANKL系统以及ALP,从而促进骨形成,抑制骨吸收。
| [1] |
Schacter G I, Leslie W D. Diabetes and bone disease[J]. Endocrinol Metab Clin N Am, 2017, 46(1): 63-85. |
| [2] |
Piscitelli P, Neglia C, Vigilanza A. Diabetes and bone: biological and environmental factors[J]. Curr Opin Endocrinol Diabetes Obes, 2015, 22(2): 439-45. |
| [3] |
刘梅, 张君, 王旭霞. T1DM、T2DM糖尿病大鼠牙槽骨骨密度变化的相关性实验研究[J]. 山东大学学报(医学版), 2011, 49(9): 53-5. Liu M, Zhang J, Wang X X. Changes of the mineral density of the alveolar bone between T1DM and T2DM rats[J]. J Shandong Unive(Health Sci), 2011, 49(9): 53-5. |
| [4] |
Li F, Tang H, Xiao F, et al. Protective effect of salidroside from Rhodiolae Radix on diabetes-induced oxidative stress in mice[J]. Molecules, 2011, 16(2): 9912-24. |
| [5] |
赖文芳, 张小琴, 洪海棉, 等. 红景天苷对大鼠局灶性脑缺血/再灌注损伤的神经保护作用[J]. 中国药理学通报, 2015, 31(6): 775-80. Lai W F, Zhang X Q, Hong H M, et al. Neuroprotective effects of salidroside on focal cerebral ischemia-reperfusion injury in rat[J]. Chin Pharmacol Bull, 2015, 31(6): 775-80. doi:10.3969/j.issn.1001-1978.2015.06.008 |
| [6] |
Zhang J K, Yang L, Meng G L, et al. Protection by salidroside against bone loss via inhibition of oxidative stress and bone-resorbing mediators[J]. PLoS One, 2013, 8: e57251. doi:10.1371/journal.pone.0057251 |
| [7] |
Zheng H X, Qi S S, Chen C. Salidroside improves bone histomorphology and prevents bone loss in ovariectomized diabetic rats by upregulating the OPG/RANKL ratio[J]. Molecules, 2018, 23: 2398. doi:10.3390/molecules23092398 |
| [8] |
祁珊珊, 王永吉, 辛薇. SD大鼠绝经后骨质疏松疾病动物模型的构建[J]. 临床与实验病理学杂志, 2016, 32(1): 49-53. Qi S S, Wang Y J, Xin W. An animal model establishment of SD rat with women's postmenopausal osteoporosis[J]. J Clin Exp Pathol, 2016, 32(1): 49-53. |
| [9] |
Deng B, Jia L, Tan H, et al. Effects of sangu decoction on osteoclast activity in a rat model of breast cancer bone metastasis[J]. Evid-Based Compl Alt Med, 2012, 23(9): 381904. |
| [10] |
Tervonen T, Karjalainen K, Knuuttila M, et al. Alveolar bone loss in type 1 diabetic subjects[J]. J Clin Periodontol, 2000, 27(8): 5-9. |
| [11] |
祁琳, 王川, 梅国华, 等. 低氧状态下红景天苷经HIF-1α信号通路调节人成骨样MG-63细胞表型表达的研究[J]. 中国药理学通报, 2017, 33(6): 836-43. Qi L, Wang C, Mei G H, et al. Effect of salidroside on regulating phenotypic expression of human osteoblast-like MG-63 cells through HIF-1α signal passway[J]. Chin Pharmacol Bull, 2017, 33(6): 836-43. doi:10.3969/j.issn.1001-1978.2017.06.018 |
| [12] |
Indridason O S, Franzson L, Sigurdsson G. Serum osteoprotegerin and its relationship with bone mineral density and markers of bone turnover[J]. Osteoporos Int, 2005, 16(4): 417-23. doi:10.1007/s00198-004-1699-x |
| [13] |
Boyce B F, Xing L. Biology of RANK, RANKL, and osteoprotegerin[J]. Arthritis Res Ther, 2007, 9: S1. |
| [14] |
Boyce B F, Xing L. Functions of RANKL/RANK/OPG in bone modeling and remodeling[J]. Arch Biochem Biophys, 2008, 15: 139-46. |