

2. 天津中医药大学天津市现代中药重点实验室-省部共建国家重点实验室培育基地,天津 301617
李楠(1982-),女,博士,助理研究员,研究方向:中药制剂,通讯作者,E-mail:linan20080402@163.com
2. Tianjin State Key Laboratory of Modern Chinese Medicine-Province and Ministry Co-Established State Key Laboratory Cultivation Base, Tianjin University of Traditional Chinese Medicine, Tianjin 301617, China
随着环境的日益恶化以及大气层的不断破坏,辐射地球的紫外线(ultraviolet rays,UV)强度越来越大。皮肤长期暴露于紫外线下导致皮肤老化,大量实验研究表明,氧化应激是UV造成皮肤损伤的重要原因。当皮肤受到UV辐射时,皮肤内形成大量活性氧(reactive oxygen species,ROS)。正常情况下,体内ROS的产生和清除处于动态平衡,UV反复照射破坏了氧化和抗氧化防御系统平衡[1]。高水平的ROS等氧化物可引起表皮角质层和真皮层内细胞脂质、核酸、蛋白质等大分子损伤,影响相关信号通路传导。
转录因子NF-E2相关因子2(NF-E2-related factor 2,Nrf2)是调控细胞对抗外源性有害物质和氧化损伤的关键转录因子。Nrf2通过与抗氧化反应元件(antioxidant response element,ARE)相互作用,诱导抗氧化蛋白表达。Nrf2-ARE是机体抵抗内外界氧化损伤的防御性转导通路[2-3]。正常生理情况下,细胞质中的Nrf2与Keap1结合,并处于活性相对抑制状态。在应激状态下,Nrf2与Keap1解离转位至细胞核,启动下游超氧化物歧化酶(superoxide dismutase,SOD)等基因和蛋白表达,从而维持机体氧化还原平衡。Nrf2-ARE通过抑制ROS,从而阻止光老化的形成。
黄芩(Scutellaria baicalensis Georgi)是唇形科黄芩属多年生草本植物,具有清热燥湿、泻火解毒、止血等功效。黄芩的活性成分主要是黄酮类,包括汉黄芩素、黄芩素、黄芩苷等。汉黄芩素、黄芩素、黄芩苷均具有抗氧化、抗衰老的作用[4]。植物雌激素通过调节雌激素受体,促进细胞中核转录因子Nrf2入核[5-9],从而发挥抗氧化抗衰老作用[2, 10-12]。汉黄芩素、黄芩素、黄芩苷均为黄芩中植物雌激素类成分[12-13],它们是否能通过雌激素受体调节Nrf2-ARE信号通路,发挥抗氧化作用还有待明确。本研究通过建立基于Nrf2-ARE通路的报告基因筛选模型,筛选黄芩中基于雌激素受体发挥抗氧化作用的活性成分,并利用UVB造模后的HaCaT细胞进行验证。
1 材料 1.1 仪器FORMA3111 CO2恒温培养箱(美国Thermo公司);低温高速离心机(美国Beckman);HZQ-C空气浴振荡器(哈尔滨市东明医疗仪器厂);超净台(苏州佳宝净化工程有限公司);SH2B型紫外光疗仪(美国Sigma);DMIL倒置相差显微镜(德国LEICA);Infinite M200型多功能酶标仪(瑞士Tecan);VICTORTM X5多功能读板仪(Perkin Elmer);Flex Station3多功能酶标仪(美国Molecula Device)。
1.2 药物与试剂叔丁基对苯二酚(tertiary butylhydroquinone,tBHQ,Sigma);ICI 182780(Biotechne,批号:129453618);全反式维甲酸ATRA(Solarbio,批号:1228A023);ROS试剂盒、SOD测试盒(WST-8法),均购自碧云天;SOD测试盒(WST-1法),购自南京建成生物工程研究所;汉黄芩素(wogonin,批号:C19A8Q34235)、黄芩素(baicalein,批号:C20M8Y31962)、黄芩苷(baicalin,批号:P16S8F44143),购自上海源叶生物科技有限公司。DMEM培养基(Gibco);胎牛血清(Biological Industries);DMSO(Sigma);CCK-8试剂盒(日本Dojindo Lab);感受态细胞DH5α、质粒小提试剂盒(天根);萤火虫荧光素酶报告基因载体pGL4.37、海肾荧光素酶报告基因载体pRL-TK(Promega);氨苄西林、LB液体培养基(干粉)、LB固体培养基(干粉),购自Solarbio。
1.3 细胞株人肾上皮细胞系293T、人类永生化表皮细胞株HaCaT,来源为ATCC细胞库。
2 方法 2.1 质粒载体的转化与验证利用感受态细胞DH5α转化质粒pGL4.37,并加入到适量菌汤中,用无菌的涂布器取适量菌汤涂布于选择培养基上,倒置培养,37 ℃过夜。挑取单个菌粒,加入到含有适量肉汤的锥形瓶中,37 ℃、160 r·min-1过夜摇菌。从过夜摇菌的菌液中取1 mL于离心管中,做好标记。通过设计上游引物①:5′-GTGAATCGATAGTACTAACA-3′;上游引物②:5′-TCAACGAGTACGACTTCGTG-3′;下游引物①:5′-CCAAACTCATCAATGTATCT-3′三段引物,将质粒送华大基因公司测序,以进一步鉴定阳性克隆[5]。
2.2 质粒的提取及测定取“2.1”中阳性克隆的菌液,采用质粒小提试剂盒提取质粒。取1 μL质粒溶液,以DEPC水作空白对照。在紫外分光光度计上分别读取260 nm、280 nm波长下的吸光度值。
2.3 细胞培养复苏293T细胞,以10%胎牛血清的DMEM完全培养基,于37 ℃、5% CO2的培养箱中培养。
2.4 细胞活力实验使用CCK-8试剂盒考察不同浓度的汉黄芩素、黄芩素、黄芩苷对293T细胞活力的影响。取对数生长期的293T细胞,以3×104个/孔的密度接种于96孔细胞培养板中,贴壁生长达70%后,将1~100 μmol·L-1的汉黄芩素、黄芩素、黄芩苷,分别加入不同的细胞培养孔中,每孔100 μL,6个复孔,同时设置未加入药物的空白对照组。培养24 h后,吸弃细胞板中上清液,用PBS清洗2-3次,每孔加入100 μL PBS稀释的1×CCK-8工作液,37 ℃孵育1 h后,在酶标仪450 nm处测定吸光度(A值)。计算细胞存活率:细胞存活率(%)=
取对数生长期的293T细胞,以3×104个/孔的密度接种于96孔细胞培养板中,待细胞生长密度达到70%~80%时,使用PEI(1 g·L-1)转染试剂同时转染ARE荧光素酶报告质粒pGL4.37(每孔41 ng)和海肾荧光素酶报告质粒pRL-TK(每孔2.4 ng),培养24 h。培养结束后,各孔分别加入Nrf2激活剂tBHQ(10 μmol·L-1),不同浓度的黄芩苷、汉黄芩素、黄芩素和细胞基础培养基,培养6 h。弃上清液,D-Hank′s漂洗细胞,裂解后,用Dual-Luciferase检测系统检测。每组实验设6个复孔,重复3次。通过萤火虫荧光素酶活性与海肾荧光素酶活性对比,得到相对荧光素酶活性值。诱导表达倍数=(药物诱导的Luciferase/药物诱导的Renilla)/(基培对照组的Luciferase/基培对照组的Renilla)。
2.6 黄芩主要活性成分通过雌激素受体影响Nrf2-ARE通路发挥抗氧化作用预先给予浓度为1 μmol·L-1的雌激素受体抑制剂ICI 182780稀释液50 μL处理细胞1 h,再分别加入200 μmol·L-1的黄芩苷溶液50 μL,使黄芩苷最终浓度为100 μmol·L-1,继续培养6 h后,检测荧光,方法同“2.5”。
2.7 验证黄芩中主要活性成分的抗氧化作用 2.7.1 细胞模型的建立复苏HaCaT细胞,以10%胎牛血清的MEM完全培养基,于37 ℃、5% CO2的培养箱中培养,待细胞长到80%左右进行种板。抑制剂组预先给予浓度为1 μmol·L-1的雌激素受体抑制剂ICI 182780稀释液和1 μmol·L-1 Nrf2-ARE通路抑制剂ATRA[14]稀释液各50 μL处理HaCaT细胞1 h,再分别加入200 μmol·L-1的黄芩苷溶液50 μL,使黄芩苷最终浓度为100 μmol·L-1,给药组直接给予100 μmol·L-1的黄芩苷溶液100 μL,加入继续培养24 h后,造模。将预给药后的HaCaT细胞分别给予不同剂量的UV照射,设置空白对照组,24 h后分别收集细胞,检测细胞活性。光源采用美国Sigma公司的SH2B型紫外光疗仪,模拟UVB辐射皮肤损伤模型,光谱为280~320 nm,强度为60 mJ·cm-2。
2.7.2 UVB照射后HaCaT细胞ROS、SOD活性的检测使用ROS试剂盒考察空白组、模型组、给药组、抑制剂组的HaCaT细胞ROS活性。用无血清MEM培养基清洗细胞,每孔加入100 μL稀释好的DCFH-DA工作液,37 ℃、5% CO2细胞培养箱孵育30 min。用无血清MEM培养基洗涤细胞3次,每孔加入100 μL MEM培养基。在酶标仪中使用激发波长488 nm,发射波长525 nm检测荧光值。
使用SOD试剂盒考察空白组、模型组、给药组、抑制剂组的HaCaT细胞SOD活性。ICI 182780组采用WST-8检测法,ATRA组采用WST-1检测法。按说明书操作计算。
2.8 统计学处理采用SPSS 17.0统计分析软件进行数据处理,数据均以x±s表示,组间比较采用单因素方差分析。
3 结果 3.1 质粒载体转化的验证及质量的测定通过基因测序得2 098 bp,将该序列与已知质粒进行比对,同源性99%,其中测序序列结果中包含ARE序列,证明转化成功。质粒浓度为158.00 mg·L-1,纯度为1.97。
3.2 黄芩主要活性成分对293T细胞活力的影响如Fig 1所示,黄芩苷(1、10、100 μmol·L-1)组293T细胞活力与正常对照组相比差异无显著性,汉黄芩素和黄芩素1 μmol·L-1组293T细胞活力与正常对照组相比差异无显著性。1、10、100 μmol·L-1为黄芩苷对293T细胞的安全浓度,1 μmol·L-1为汉黄芩素和黄芩素的安全浓度。采用黄芩苷、汉黄芩素和黄芩素的安全浓度进行抗氧化活性的筛选。

|
| Fig 1 Effect of scutellarin, baicalein, baicalinon cell viability of 293T cells(x±s, n=6) **P < 0.01 vs control |
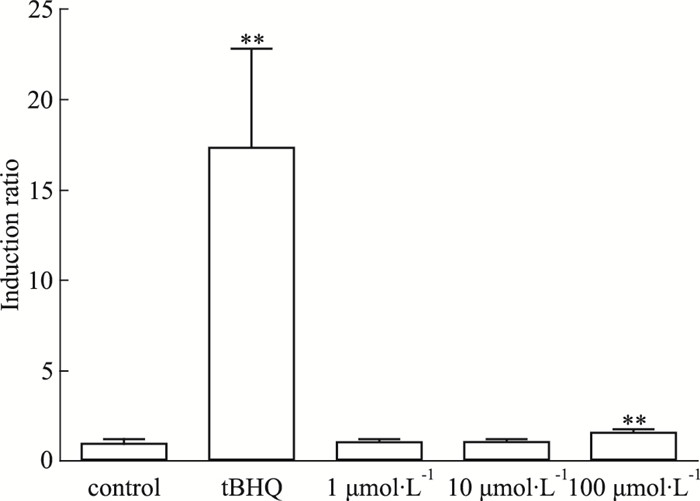
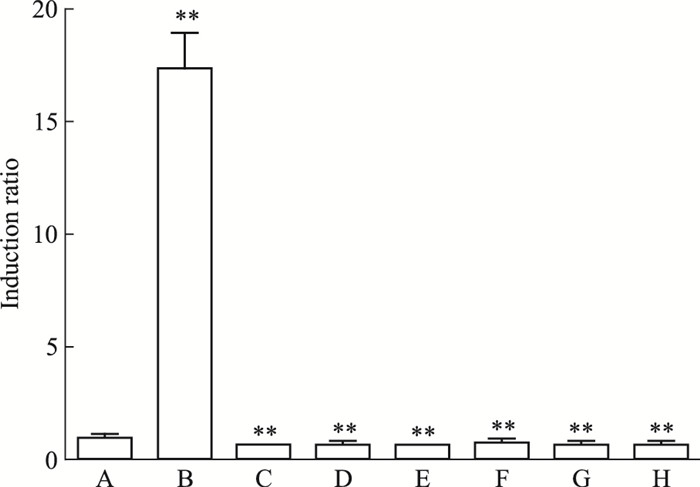
分别将黄芩苷(1、10、100 μmol·L-1),汉黄芩素(0.2、0.5、1 μmol·L-1)和黄芩素(0.2、0.5、1 μmol·L-1)加入转染了质粒DNA的293T细胞中,检测报告基因的活性。Fig 2结果显示,100 μmol·L-1黄芩苷可明显激活293T细胞中的Nrf2-ARE通路,诱导表达倍数为空白组的(1.56±0.01)倍(P<0.01);黄芩苷(1、10 μmol·L-1)诱导表达倍数与空白组比较差异均无显著性。如Fig 3所示,汉黄芩素和黄芩素0.2、0.5、1 μmol·L-1 3个浓度的诱导表达倍数均小于1,无抗氧化活性。
|
| Fig 2 Effect of baicalin on luciferase inductionin 293T cells(x±s, n=6) **P < 0.01 vs control |
|
| Fig 3 Effect of scutellarin, baicalein onluciferase induction in 293T cells(x±s, n=6) A:Control; B:tBHQ; C:0.2 μmol·L-1 of scutellarin; D: 0.5 μmol·L-1 of scutellarin; E: 1 μmol·L-1 of scutellarin; F: 0.2 μmol·L-1 of baicalein; G: 0.5 μmol·L-1 of baicalein; H: 1 μmol·L-1 of baicalein.**P < 0.01 vs control |
如Fig 4所示,预给予雌激素受体特异性抑制剂ICI 182780后,诱导表达倍数下降至(1.02±0.23)倍,抗氧化作用基本消失。

|
| Fig 4 Effect of ICI 182780 on luciferase-upregulationby baicalin in 293T cells(x±s, n=6) **P < 0.01 vs control |
Tab 1结果显示,与模型组比较,黄芩苷(100 μmol·L-1)对HaCaT细胞有明显的抗氧化作用。预给予雌激素受体特异性抑制剂ICI 182780后,ROS值升高,SOD值下降,抗氧化作用消失。表明黄芩苷可能通过雌激素受体发挥抗氧化作用。
| Group | ROS(n=6) | SOD/units(n=3) |
| Control | 31.09±1.28** | 0.32±0.01** |
| Model | 44.81±1.02 | 0.12±0.03 |
| Baicalin | 36.80±0.89** | 0.22±0.03** |
| ICI 182780 | 43.35±1.65 | 0.08±0.06** |
| **P<0.01 vs model | ||
Tab 2结果显示,与模型组比较,黄芩苷(100 μmol·L-1)对HaCaT细胞有明显的抗氧化作用。预给予Nrf2-ARE通路特异性抑制剂ATRA后,ROS值升高,SOD值下降,抗氧化作用消失。表明黄芩苷可能通过Nrf2-ARE通路发挥抗氧化作用。
| Group | ROS(n=6) | SOD/kU·L-1(n=3) |
| Control | 41.03±1.89** | 116.76±4.63* |
| Model | 49.56±1.42 | 58.56±9.46 |
| Baicalin | 41.56±1.18** | 109.34±42.65* |
| ATRA | 50.64±0.97 | 35.21±12.20 |
| *P<0.05, **P<0.01 vs model | ||
本研究采用基因载体pGL4.37-ARE与内对照报告基因载体pRL-TK共转染293T细胞,建立双荧光素酶报告基因系统,检测293T细胞中相关蛋白表达,并将其诱导表达倍数归一化,以消除实验中不同测试之间所固有的变化,从而筛选出可明显激活293T细胞中的Nrf2-ARE通路的活性成分黄芩苷,并为后续单体抗氧化成分的开发提供实验依据。
文献报道,黄芩苷可以下调Keap1表达、上调Nrf2蛋白水平,过量的Nrf2由胞质向核内转移,与ARE调控序列结合,启动下游SOD等基因和蛋白表达,从而清除氧自由基[10],实现抗氧化作用[6]。研究表明,黄芩苷(100 μmol·L-1)可缓解UVB照射所致HaCaT细胞内ROS的过量表达,提高SOD活性,从而达到对UVB照射导致的氧化应激的保护作用。预加入雌激素受体抑制剂和Nrf2-ARE通路抑制剂抗氧化作用消失,从而推断黄芩苷可能是通过雌激素受体调节Nrf2-ARE通路发挥抗氧化作用。
黄芩素与黄芩苷化学结构相似,但在本研究构建的筛选模型中,在考察浓度范围内黄芩素未表现出抗氧化作用。刘靖丽等[15]从密度泛函理论角度探讨了黄芩素和黄芩苷抗氧化活性与结构关系,认为C6位的酚羟基是黄芩苷黄芩素的最大反应活性位点。在非极性溶剂中,抗氧化活性取决于脱氢能力,脱氢能力越强,抗氧化能力越强,黄芩苷的脱氢能力强于黄芩素,所以黄芩苷的抗氧化活性大于黄芩素;在极性溶剂中,抗氧化活性取决于电离势,电离势越低,抗氧化活性越强,黄芩苷的电离势低于黄芩素,所以黄芩苷的抗氧化活性强于黄芩素。与本研究结果一致。
本研究成功建立了双荧光素酶报告基因系统,用于体外筛选具有抗氧化活性成分,并用UVB造模后的HaCaT细胞进行了验证。结果发现,黄芩中主要活性成分黄芩苷通过雌激素受体影响Nrf2-ARE通路,发挥抗氧化作用。
| [1] |
Liu Y, Chan F, Sun H, et al. Resveratrol protects human keratinocytes HaCaT cells from UVA-induced oxidative stress damage by downregulating Keap1 expression[J]. Eur J Pharmacol, 2011, 650(1): 130-7. doi:10.1016/j.ejphar.2010.10.009 |
| [2] |
邹海曼.杜仲和补骨脂中活性植物雌激素成分对ESF-1细胞抗衰老基因调控机制的研究[D].哈尔滨: 黑龙江中医药大学, 2013. Zou H M. Study on the regulation mechanism of anti-aging gene in ESF-1 cells by active phytoestrogens in Eucommia ulmoides Oliv[D]. Heilongjiang University of Traditional Chinese Medicine, 2013. http://cdmd.cnki.com.cn/Article/CDMD-10228-1013249932.htm |
| [3] |
曹玲娟, 龚慧, 颜苗, 等. Nrf2-ARE信号通路参与肝脏疾病病理机制研究进展[J]. 中国药理学通报, 2015, 31(8): 1057-61. Cao L J, Gong H, Yan M, et al. Advances in research on the pathogenesis of liver disease by Nrf2-ARE signaling pathway[J]. Chin Pharmacol Bull, 2015, 31(8): 1057-61. doi:10.3969/j.issn.1001-1978.2015.08.006 |
| [4] |
李凌霞, 赵晶, 党文军, 等. 归素膏对衰老小鼠皮肤SOD活性及MDA含量影响的实验研究[J]. 中国中医药科技, 2014, 21(6): 637-8. Li L X, Zhao J, Dang W J, et al. Experimental study on the effect of Guiyu cream on SOD activity and MDA content in aging mouse skin[J]. Chin J Tradit Med Sci Technol, 2014, 21(6): 637-8. |
| [5] |
邵帅, 马增春, 洪倩, 等. 基于Nrf2-ARE通路的抗辐射有效活性成分筛选研究[J]. 中国药理学通报, 2012, 28(1): 29-33. Shao S, Ma Z C, Hong Q, et al. Screening of radiation-resistant active ingredients based on Nrf2-ARE pathway[J]. Chin Pharmacol Bull, 2012, 28(1): 29-33. doi:10.3969/j.issn.1001-1978.2012.008 |
| [6] |
李航, 段惠军. Nrf2/ARE信号通路及其调控的抗氧化蛋白[J]. 中国药理学通报, 2011, 27(3): 300-3. Li H, Duan H J. Nrf2/ARE signaling pathway and its regulated antioxidant protein[J]. Chin Pharmacol Bull, 2011, 27(3): 300-3. |
| [7] |
李云霞, 林涛, 杨晓江. 植物雌激素在皮肤抗衰老中的作用及应用[J]. 中国美容医学, 2014, 23(21): 1850-1. Li Y X, Lin T, Yang X J. The role and application of phytoestrogens in skin anti-aging[J]. Chin J Aesthetic Med, 2014, 23(21): 1850-1. |
| [8] |
吴可, 赵文丽, 李月影, 等. Nrf2-ARE信号通路在左乙拉西坦抗癫痫中的作用[J]. 中国药理学通报, 2017, 33(10): 1462-6. Wu K, Zhao W L, Li Y Y, et al. The role of Nrf2-ARE signaling pathway in the antiepileptic effect of levetiracetam[J]. Chin Pharmacol Bull, 2017, 33(10): 1462-6. doi:10.3969/j.issn.1001-1978.2017.10.026 |
| [9] |
孟哲, 腾帅, 王琛, 等. 积雪草酸通过激活Nrf2抗氧化通路抑制自发性高血压大鼠心肌纤维化[J]. 中国药理学通报, 2018, 34(8): 1073-8. Meng Z, Teng S, Wang C, et al. Centella asiatica inhibits myocardial fibrosis in spontaneously hypertensive rats by activating the Nrf2 antioxidant pathway[J]. Chin Pharmacol Bull, 2018, 34(8): 1073-8. doi:10.3969/j.issn.1001-1978.2018.08.009 |
| [10] |
于佳佳.雌激素对Nrf2活化及HO-1, Cu/Zn-SOD表达的影响[D].长春: 东北师范大学, 2010. Yu J J. Effects of estrogen on Nrf2 activation and expression of HO-1 and Cu/Zn-SOD[D]. Changchun: Northeast Normal University, 2010. http://cdmd.cnki.com.cn/Article/CDMD-10200-2010178631.htm |
| [11] |
Bemneburg M, Plettenberg H, Medve-könig K, et al. Induction of the photoaging-associated mitochondrial common deletion in vivo in normal human skin[J]. J Invest Dermatol, 2004, 122(5): 1277-83. |
| [12] |
陈梦, 赵丕文, 赵笛, 等. 中药植物雌激素的药理作用研究进展[J]. 江苏中医药, 2017, 49(4): 82-5. Chen M, Zhao P W, Zhao D, et al. Advances in pharmacological studies of phytoestrogens in traditional Chinese medicine[J]. Jiangsu Tradit Chin Med, 2017, 49(4): 82-5. |
| [13] |
尹昭晔.杜仲的植物雌激素活性成分研究[D].天津: 天津大学, 2010. Yin Z Y. Study on phytoestrogens active components of Eucommia Ulmoides[D]. Tianjin: Tianjin University, 2010. http://cdmd.cnki.com.cn/Article/CDMD-10056-1011263433.htm |
| [14] |
Wang X J, Hayes J D, Henderson C J, et al. Identification of retinoic acid as an inhibitor of transcription factor Nrf2 through activation of retinoic acid receptor alpha[J]. Proc Natl Acad Sci USA, 2007, 104(49): 19589-94. doi:10.1073/pnas.0709483104 |
| [15] |
刘靖丽, 崔莹超. 黄芩素和黄芩苷抗氧化活性与结构关系的密度泛函理论研究[J]. 云南民族大学学报(自然科学版), 2017, 26(6): 461-4. Liu J L, Cui Y C. The density functional theory studies on the relationship between antioxidant activity and structure of Baicalein and Baicalin[J]. Yunnan Minzu Univ(Natural Sci Ed), 2017, 26(6): 461-4. doi:10.3969/j.issn.1672-8513.2017.06.006 |

