

2. 南华大学附属湘潭医院病理科,湖南 湘潭 411101;
3. 永州职业技术学院基础医学系,湖南 永州 425100;
4. 南华大学附属第二医院病理科,湖南 衡阳 421001
苏琦(1945-),男,教授,博士生导师,研究方向:胃癌发生与防治的分子机制,通讯作者,E-mail: suqi1945@163.com
2. Dept of Pathology, the Affiliated Xiangtan Hospital, University of South China, Xiangtan, Hunan 411101, China;
3. Dept of Basic Medicine, Yongzhou Vocational Technical College, Yongzhou, Hunan 425100, China;
4. Dept of Pathology, the Second Affiliated Hospital, University of South China, Hengyang, Hunan 421001, China
胃癌是全球最常见的恶性肿瘤之一,据2018年全世界185个国家统计的最新报告,每年新发病例100万,死亡78.3万,发生率与死亡率分别居于第5位与第3位[1]。我国是胃癌高发地区,每年约新发67.9万,死亡49.8万,发生率与死亡率仅次于肺癌,由于患者就诊时大多已发生侵袭转移,常规手术和化疗效果较差,故5年生存率低[2]。因此,研发高效低毒药物与胃癌的早期诊断对提高胃癌的治疗效果,延长患者的生存期至关重要[3]。
二烯丙基二硫(diallyl disulfide,DADS)作为大蒜中烯丙基硫化物的一种脂溶性的有效成分,对多种肿瘤均有明显的抑制作用[4]。近年来,microRNAs(miRNAs)在肿瘤中的作用引起人们高度关注。miRNAs在肿瘤中通过与靶基因mRNA的3′非编码区完全或不完全结合,表现为癌基因或抑癌基因作用[3]。本研究采用miRNA芯片与qRT-PCR,检测与鉴定DADS抑制人胃癌MGC803细胞的差异miRNAs表达。
1 材料与方法 1.1 细胞培养人胃癌MGC803、BGC823、MKN28、SGC7901、HGC27细胞,以及正常胃黏膜上皮GES-1细胞,由本实验室保存,置于含10%小牛血清的RPMI 1640培养基中,37 ℃、5% CO2、饱和湿度的培养箱内传代培养。取对数生长期的细胞用于实验。
1.2 试剂DADS为Fluka公司产品; miRCURYTMArray Power标记试剂盒,由上海康成生物公司提供; qPCR miRNA试剂盒,购自上海吉玛公司; RPMI 1640培养液,购自Hyclone公司; 胎牛血清,购自四季青生物公司。
1.3 microRNA芯片检测30 mg·L-1 DADS处理24 h的MGC803细胞与未处理的MGC803细胞,分别取1×106~1×107细胞,加1 mL的RNA抽提试剂TRIzol,裂解后抽提RNA,检测RNA纯度及完整性。制备荧光标记探针:采用miRCURYTMArray Power标记试剂盒,用标记酶将Hy3TM或Hy5TM荧光基团标记miRNA,得到用于与芯片杂交的荧光探针。芯片杂交:在标准条件下,使用PhalanxTM的热收缩杂交袋,将标记号的探针和miRCURYTM芯片杂交。GenePix4000B芯片扫描仪扫描芯片的荧光强度,并将实验结果转化成数字型数据保存,用配套软件对原始数据进行分析运算。
1.4 qPCR检测用RNA抽提试剂盒抽提组织与细胞总RNA,qPCR miRNA试剂盒逆转录合成cDNA存于-80 ℃。miR-200b:5′-UAAUACUGCCUG GUAAUGAUGA-3′; miR-22:5′-AAGCUGCCAGUUGA AGAACUGU-3′; 所有miRNA序列由美国Exiqon公司合成。采用美国Illumina公司(Eco)qRT-PCR仪检测。PCR扩增反应体系:2×SYBR Mix 10 μL,Taq DNA polymerase 0.2 μL,MiR-PCR primers 0.4 μL,miRNA RT product 2.0 μL,灭菌蒸馏水7.4 μL。上机:95.0 ℃,3 min; 95.0 ℃,12 s; 62.0 ℃,35 s; (62.0~95.0) ℃,15 s,共40个循环。反应结束后,软件自动分析并显示循环阈值(CT)和实时定量荧光动态曲线。
1.5 临床胃癌标本收集南华大学附属第一医院在无任何辅助治疗的情况下,手术中的27例配对的原发胃癌和邻近的非胃癌组织。所有组织标本HE染色,经两名独立病理学家诊断。所有患者均获得知情同意书,并经华南大学研究伦理委员会批准。
1.6 统计学处理采用SPSS 16.0软件进行统计学分析,结果均以x±s表示,两组间比较用t检验,多组间比较用单因素方差分析。
2 结果 2.1 DADS作用MGC803细胞miRNAs差异表达microRNA芯片检测显示,30 mg·L-1 DADS处理24 h的MGC803细胞的差异miRNAs表达中,发现7个miRNA上调,5个miRNA下调(Fig 1、Tab 1)。

|
| Fig 1 MGC803 cells treated by DADS detected by miRNA chip |
| miRNA | Fold change | P value |
| Upregulated miRNAs | ||
| hsa-miR-200b | 5.453 | 0.0000 |
| hsa-miR-22 | 4.786 | 0.0000 |
| hsa-miR-7 | 2.536 | 0.0006 |
| hsa-miR-143 | 1.851 | 0.0099 |
| hsa-miR-138 | 1.711 | 0.0079 |
| hsa-miR-34a | 1.856 | 0.0127 |
| hsa-miR-150 | 0.924 | 0.0028 |
| Downregulated miRNAs | ||
| hsa-miR-222 | 0.247 | 0.0000 |
| hsa-miR-21 | 0.286 | 0.0049 |
| hsa-miR-15b | 0.313 | 0.0072 |
| hsa-miR-182 | 0.474 | 0.0039 |
| Has-miR-18a | 1.669 | 0.0014 |
进一步采用qRT-PCR验证上调miRNAs。Fig 2结果显示,30 mg·L-1 DADS处理人胃癌MGC803细胞后,miR-200b、miR-22、miR-7、miR-143、miR-138、miR-34a、miR-150等表达较未处理组明显上调(P < 0.05),与miRNA芯片检测结果一致。

|
| Fig 2 Up-regulated miRNAs in gastric cancer cells detected by qPCR(x±s, n=3) *P < 0.05 vs mock |
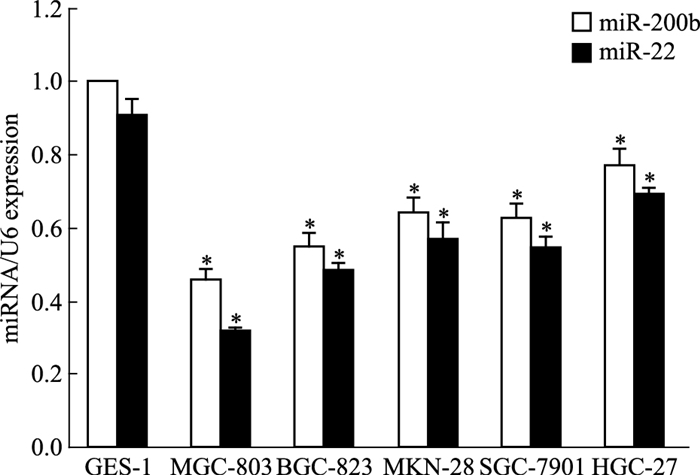
根据DADS处理人胃癌MGC803细胞后,miR-200b与miR-22上调最明显,因此,采用qPCR进一步验证miR-200b与miR-22是否在各种人胃癌细胞表达上调。Fig 3检测结果显示,miR-200b与miR-22在MGC-803、BGC-823、MKN-28、SGC-7901、HGC-27等各种人胃癌细胞表达较正常人胃癌GES-1细胞明显下调(P < 0.05)。
|
| Fig 3 Expression of miR-200b and miR-22 in gastric cancer cells detected by qPCR(x±s, n=3) *P < 0.05 vs GES-1 |
为了明确miR-200b与miR-22在胃癌组织的表达情况,采用qPCR检测。Fig 4结果显示,miR-200b与miR-22在胃癌组织中表达较正常胃组织明显下调(P < 0.05)。

|
| Fig 4 Expression of miR-200b and miR-22 in gastric cancer detected by qPCR(x±s, n=3) *P < 0.05 vs normal |
研究发现,黄酮类化合物白杨黄素具有抑制胃癌细胞增殖的作用,白杨黄素可改变miRNAs的表达,上调miR-22、miR-34a、let-7a、miR-9、miR-126,下调miR-21、miR-18a、miR-221,可能是其作用的分子机制[5]。本研究采用microRNA芯片检测结果显示,DADS处理人胃癌MGC803细胞的差异miRNAs表达中,miR-200b、miR-22、miR-7、miR-143、miR-138、miR-34a、miR-150等表达上调,而miR-21、miR-222、miR-15b、miR-182、miR-18a等表达下调。且qPCR验证7个上调的miRNA在DADS处理MGC803细胞较未处理组明显上调,与芯片检测结果一致。进一步检测上调最为明显miR-22与miR-200b在各组胃癌细胞和组织中表达明显下调。
研究显示,胃癌组织中miR-22的表达率较正常组织明显降低,表明miR-22可能是早期检测胃癌的良好诊断生物标志物[6]。有研究证明,胃癌患者血清中miR-22的水平较健康对照组明显降低,相反,miR-21的水平明显高于对照组。生物信息学分析显示,Sp1是miR-21靶点,而PTEN是miR-22的靶点,提示其是胃癌潜在的生物标志物[3]。幽门螺杆菌感染是慢性炎症导致胃癌发生的主要原因,而NLRP3在炎症发生过程中起着至关重要的作用。幽门螺杆菌感染可抑制miR-22的表达,促进NLRP3的表达,从而引发了上皮细胞失控的增殖和胃癌发生。然而,miR-22可直接靶向NLRP3,在体内外降低其致癌作用。因此,miR-22抑制NLRP3并维持胃微环境稳态的机制,可作为胃癌干预的潜在靶点[7]。我们发现,miR-22在胃癌中表达下调,与临床分期和淋巴结转移有关,miR-22可通过靶向metadherin抑制MGC803细胞侵袭与转移[8]。DADS可上调miR-22,通过Wnt-1通路明显抑制MGC803细胞增殖与迁移侵袭[9]。
miR-200b是一种在肿瘤进展过程中具有多效作用的microRNA与治疗靶点。miR-200b通过诱导G2期阻滞和凋亡,抑制食管鳞状细胞癌(ESCC)细胞的生长。CDK2和PCNA相关因子(PCNA-associated factor, PAF)是miR-200b直接的靶点,ESCC中CDK2和PAF水平均较正常组织明显升高,与miR-200b的频繁缺失和生存率明显降低有关[10]。Zheng等[11]采用荟萃分析1 271例食管癌、3467例胃癌和1517例结直肠癌患者,鉴定59个miRs,发现miR-200b与胃肠癌患者预后不良相关。在173例胃癌标本中,miR-200b低表达组的预后明显低于miR-200b高表达组,并与腹膜转移相关。癌症相关成纤维细胞(cancer-associated fibroblasts,CAFs)可促进miR-200b的表观遗传改变,降低miR-200b的表达,增加胃癌细胞侵袭和迁移[12]。胃癌组织和正常组织的miRs差异表达图谱显示,miR-200家族在胃癌中表达下调,且miR-200家族在癌组织中的表达明显低于非癌组织,与组织学分级和血管内侵袭有关。因此,miR-200家族可能成为胃癌的预后预测因子与治疗靶点[13]。miR-200b是胃癌、乳腺癌、卵巢癌、胶质瘤等多种肿瘤的抑制因子。miR-200b在胶质瘤组织中下调与预后不良相关,可能是神经胶质瘤预后的潜在生物标志物[14]。我们研究显示,miR-200b在胃癌组织中表达下调与患者临床分期、T分期、淋巴结转移及生存率明显相关。miR-200b高表达可直接靶向DNMT3A、DNMT3B和SP1,引起DNMT1、DNMT3A和DNMT3B表达降低,反过来通过启动子DNA低甲基化,导致p16、RASS1A1和E-cadherin重新表达,提示miR-200b可能成为胃癌预后的标志物与治疗的靶点[15]。
综上所述,DADS诱导人胃癌MGC803细胞的差异miRNAs表达,有7个miRNA明显上调,5个miRNA下调,DADS可上调MGC803细胞miR-200b与miR-22表达。然而,DADS是否能够通过上调miR-7、miR-143、miR-138、miR-34a、miR-150和下调miR-21、miR-222、miR-15b、miR-182、miR-18a,抑制胃癌细胞增殖与迁移侵袭,尚待进一步研究。
| [1] |
Bray F, Ferlay J, Soerjomataram I, et al. Global cancer statistics 2018: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries[J]. CA Cancer J Clin, 2018, 68(6): 394-424. doi:10.3322/caac.v68.6 |
| [2] |
Chen W, Zheng R, Baade P D, et al. Cancer statistics in China, 2015[J]. CA Cancer J Clin, 2016, 66(2): 115-32. doi:10.3322/caac.21338 |
| [3] |
Huang Y, Zhu J, Li W, et al. Serum microRNA panel excavated by machine learning as a potential biomarker for the detection of gastric cancer[J]. Oncol Rep, 2018, 39(3): 1338-46. |
| [4] |
Yi L, Su Q. Molecular mechanisms for the anti-cancer effects of diallyl disulfide[J]. Food Chem Toxicol, 2013, 57: 362-70. doi:10.1016/j.fct.2013.04.001 |
| [5] |
Mohammadian F, Pilehvar-Soltanahmadi Y, Alipour S, et al. Chrysin alters microRNAs expression levels in gastric cancer cells: possible molecular mechanism[J]. Drug Res(Stuttg), 2017, 67(9): 509-14. |
| [6] |
Jafarzadeh-Samani Z, Sohrabi S, Shirmohammadi K, et al. Evaluation of miR-22 and miR-20a as diagnostic biomarkers for gastric cancer[J]. Chin Clin Oncol, 2017, 6(2): 16. doi:10.21037/cco |
| [7] |
Li S, Liang X, Ma L, et al. MiR-22 sustains NLRP3 expression and attenuates H. pylori-induced gastric carcinogenesis[J]. Oncogene, 2018, 37(7): 884-96. doi:10.1038/onc.2017.381 |
| [8] |
Tang Y Y, Liu X P, Su B, et al. microRNA-22 acts as a metastasis suppressor by targeting metadherin in gastric cancer[J]. Mol Med Rep, 2015, 11(1): 454-60. doi:10.3892/mmr.2014.2682 |
| [9] |
唐云云, 唐仪, 刘芳, 等. 二烯丙基二硫上调miR-22通过Wnt-1通路抑制人胃癌细胞增殖与迁移侵袭[J]. 中国药理学通报, 2017, 33(8): 1141-6. Tang Y Y, Tang Y, Liu F, et al. Upregulation of miR-22 through Wnt pathway suppress the proliferation, migration and invasion in human gastric MGC803 cells by DADS[J]. Chin Pharmacol Bull, 2017, 33(8): 1141-6. doi:10.3969/j.issn.1001-1978.2017.08.020 |
| [10] |
Zhang H F, Alshareef A, Wu C, et al. miR-200b induces cell cycle arrest and represses cell growth in esophageal squamous cell carcinoma[J]. Carcinogenesis, 2016, 37(9): 858-69. doi:10.1093/carcin/bgw079 |
| [11] |
Zheng Q, Chen C, Guan H, et al. Prognostic role of microRNAs in human gastrointestinal cancer: A systematic review and meta-analysis[J]. Oncotarget, 2017, 8(28): 46611-23. |
| [12] |
Kurashige J, Mima K, Sawada G, et al. Epigenetic modulation and repression of miR-200b by cancer-associated fibroblasts contribute to cancer invasion and peritoneal dissemination in gastric cancer[J]. Carcinogenesis, 2015, 36(1): 133-41. doi:10.1093/carcin/bgu232 |
| [13] |
Chang L, Guo F, Huo B, et al. Expression and clinical significance of the microRNA-200 family in gastric cancer[J]. Oncol Lett, 2015, 9(5): 2317-24. doi:10.3892/ol.2015.3028 |
| [14] |
Liu Q, Tang H, Liu X, et al. miR-200b as a prognostic factor targets multiple members of RAB family in glioma[J]. Med Oncol, 2014, 31(3): 859. doi:10.1007/s12032-014-0859-x |
| [15] |
Tang H, Deng M, Tang Y, et al. miR-200b and miR-200c as prognostic factors and mediators of gastric cancer cell progression[J]. Clin cancer Res, 2013, 19(20): 5602-12. doi:10.1158/1078-0432.CCR-13-1326 |

