


2. 宁夏医科大学 临床医学院,宁夏 银川 750004;
3. 宁夏医科大学 总医院产前诊断中心,宁夏 银川 750004
 ,
ZHANG Hui1,
DING Ning1,
WANG Yan-hua1,3,
WU Kai1,
CAO Jun2,
WANG Qing-qing1,
LIU Kun2,
ZHANG Hui-pin3,
JIANG Yi-deng1
,
ZHANG Hui1,
DING Ning1,
WANG Yan-hua1,3,
WU Kai1,
CAO Jun2,
WANG Qing-qing1,
LIU Kun2,
ZHANG Hui-pin3,
JIANG Yi-deng1

2. College of Clinical Medicine, Ningxia Medical University, Yinchuan 750004, China;
3. General Hospital, Ningxia Medical University, Yinchuan 750004, China
妊娠期高血压疾病(hypertension disorder complicating pregnancy, HDCP)是导致孕产妇并发症和围生儿发病及死亡的常见原因,且发病机制复杂[1]。近年来研究发现,胎盘功能异常是造成HDCP的重要原因之一[2]。在妊娠过程中,胎盘滋养细胞凋亡和增殖不但影响胎盘的生理功能,甚至对整个妊娠过程及结局产生不良影响[3]。内质网被认为是细胞内诱导细胞凋亡发生的场所[4],持续或强烈的内质网应激反应可能会诱导细胞发生凋亡[5]。葡萄糖调节蛋白78 (glucose regulated protein 78,GRP78)作为内质网的重要分子伴侣,在蛋白质折叠和转运过程及内质网应激反应中都发挥着重要的作用[6]。此外,p53凋亡刺激蛋白2(apoptosis stimulating protein 2 of p53,ASPP2)是p53结合蛋白家族促凋亡成员,参与细胞生长、凋亡、损伤应激等一系列的生理反应,能够通过调节促凋亡靶基因的转录来促进细胞凋亡[7-8]。然而,关于ASPP2在HDCP胎盘滋养细胞凋亡中作用机制的研究,目前尚未见报道。因此,如能阐明ASPP2调控GRP78在胎盘滋养细胞凋亡中的作用,将为进一步研究HDCP的发病机制提供理论依据。
1 材料与方法 1.1 材料 1.1.1 试剂胎牛血清、RPMI 1640培养基,购自Gibco公司; N-硝基-L-精氨酸甲酯(N-nitro-L-arginine methyl ester,L-NAME),购自Sigma公司; Annexin V-FITC/PI细胞凋亡检测试剂盒,购自贝博公司; 总RNA提取试剂盒,购自北京天根生物技术有限公司; 逆转录和qRT-PCR试剂盒,购自Thermo Fisher公司; 蛋白提取试剂盒、蛋白定量试剂盒、吖啶橙/溴化乙锭染色试剂盒,购自南京凯基有限公司; caspase-12、GRP78、ASPP2抗体,均购自Abcam公司; 辣根过氧化物酶(HRP)标记的二抗,购自北京中杉金桥有限公司; 引物委托上海生工公司合成; ASPP2干扰腺病毒,购自上海汉恒生物科技有限公司。
1.1.2 仪器超净工作台(苏州安泰空气技术有限公司); 电泳仪、凝胶成像仪(美国伯乐公司); 荧光定量PCR仪(上海枫岭生物技术有限公司); 流式细胞仪(美国BD公司); 激光扫描共聚焦显微镜(日本Olympus公司)。
1.2 方法 1.2.1 细胞培养人胎盘滋养细胞株HTR-8/SVneo,购自上海瑞鹿生物技术有限公司。用含10%胎牛血清的RPMI 1640培养基培养,置于37 ℃、5% CO2的培养箱中培养。当细胞密度达到80%时,以0 μmol·L-1 L-NAME和100 μmol·L-1 L-NAME干预的人胎盘滋养细胞分别作为对照组(Control)和L-NAME组,干预48 h后,收集细胞用于后续实验。
1.2.2 ASPP2干扰腺病毒感染胎盘滋养细胞在光学显微镜下观察,确定胎盘滋养细胞处于生长对数期后,弃去旧培养液,吸取2 mL RPMI 1640纯培养基换液,向其中加入15 μL ASPP2干扰腺病毒液充分混匀,置于37 ℃、5% CO2的细胞培养箱内培养4 h后,弃培养基,加入配好的培养液(含10%胎牛血清及1%青链霉素双抗)继续培养48 h。
1.2.3 流式细胞术检测胎盘滋养细胞凋亡水平用不含EDTA、不含酚红的胰蛋白酶消化胎盘滋养细胞后,1 000 r·min-1离心5 min,收集细胞。用冷PBS洗涤细胞2次,1 000 r·min-1、4 ℃离心5 min收集细胞。用400 μL 1×Annexin V结合液悬浮细胞,浓度约为1×109·L-1。加入5 μL Annexin V-FITC染色液,轻轻混匀后,于4 ℃避光孵育15 min,然后加入10 μL PI染色液轻轻混匀,于4 ℃避光孵育5 min。使用400目的滤膜过滤后,立即用流式细胞仪检测。以FITC和PI荧光作双参数点图,细胞分为4个象限:左下象限为活细胞,右下象限为早期凋亡细胞,右上象限为晚期凋亡细胞,左上象限为机械损伤和死亡细胞。
1.2.4 吖啶橙/溴化乙锭染色检测胎盘滋养细胞凋亡水平人胎盘滋养细胞培养同上,待细胞进入对数生长期后,分别加入0、100 μmol·L-1 L-NAME干预细胞48 h后,收集细胞,用PBS将细胞浓度调至1×1010·L-1,取细胞悬液100 μL,加入吖啶橙/溴化乙锭染料各2 μL混匀,荧光显微镜下观察凋亡细胞。
1.2.5 qRT-PCR检测ASPP2 mRNA的表达根据RNA提取剂盒说明书,提取人胎盘滋养细胞总RNA。GenBank数据库查询ASPP2的基因序列并设计引物:ASPP2上游引物:5′-ATTGAATCAAGAGCAGAATGCC-3′, 下游引物:5′-CAGCTCATTAACACGCTTATCC-3′。PCR扩增程序:95 ℃ 5 min,95 ℃ 10 s,59 ℃ 30 s,72 ℃ 30 s,72 ℃ 10 min,共45个循环,并以内参GADPH为对照进行平衡,同体系扩增目的基因的相对量根据公式2-△△Ct计算, △△Ct=[CtASPP2(待测样本)-CtGADPH(待测样本)]-[CtASPP2(校正样本)-CtGADPH(校正样本)]。
1.2.6 Western blot检测caspase-12、GRP78和ASPP2的蛋白表达按全蛋白提取试剂盒提取胎盘滋养细胞全蛋白,每组取30 μg总蛋白进行SDS-PAGE凝胶电泳,25 V恒压转膜9 min,5%的脱脂奶粉封闭2 h,与抗caspase-12、GRP78和ASPP2抗体4 ℃孵育过夜,HRP标记的二抗室温孵育2 h,于凝胶成像分析仪上成像分析,以β-actin为内参,计算caspase-12、GRP78和ASPP2与β-actin内参灰度值的比值,进行分析。
1.2.7 免疫荧光染色检测GRP78的蛋白表达将细胞接种于激光共聚焦小皿中,感染ASPP2干扰腺病毒,并用100 μmol·L-1 L-NAME干预48 h后,4%多聚甲醛固定30 min,含有0.2% Triton X-100的PBS透化5 min,山羊血清工作液封闭1 h,然后与抗GRP78的抗体4 ℃孵育过夜。PBS洗涤后,用FITC偶联的二抗37 ℃温育1 h,细胞核用DAPI复染,PBS洗涤后,在共聚焦显微镜下观察。
1.3 统计学处理与分析采用Prism 5.0统计软件对实验数据进行分析整理,以x±s表示,两样本均数间比较采用Student's t检验,多个样本之间比较采用One-way ANOVA检验。
2 结果 2.1 L-NAME对胎盘滋养细胞凋亡的影响Annexin V-FITC/PI双标记流式细胞术检测发现,与对照组相比,L-NAME组人胎盘滋养细胞凋亡水平增加(P<0.05)。吖啶橙/溴化乙锭染色发现,对照组细胞呈现均匀的绿色或橙色(自然凋亡细胞),而L-NAME组少数细胞呈现鲜绿色,多数细胞呈鲜亮的橙色斑点(晚期凋亡细胞)。同时Western blot检测发现,caspase-12蛋白表达水平与对照组相比明显增加(P<0.05)。见Fig 1。

|
| Fig 1 Effect of L-NAME on apoptosis of placental trophoblast cells A:Flow cytometry was used to detect the apoptosis of placental trophoblast cells; B:Apoptosis rate of placental trophoblast cells(x±s, n=3); C:AO/EB assay was used to detect the apoptosis of placental trophoblast cells (×100); D:Expressions of caspase-12 were detected by Western blot (x±s, n=4). *P < 0.05 vs control group. |
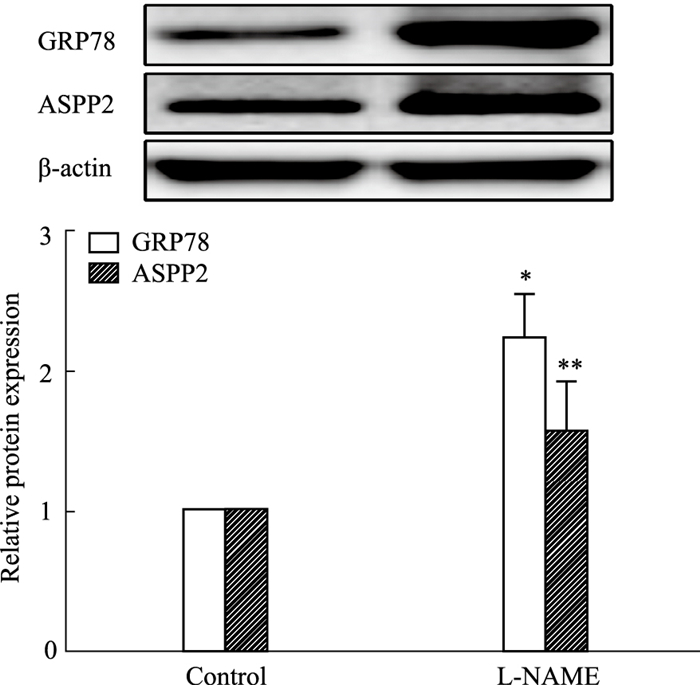
Fig 2的Western blot检测结果显示,与对照组相比,L-NAME组GRP78和ASPP2蛋白表达水平均明显升高(P<0.05,P<0.01)。
|
| Fig 2 Expression of GRP78 and ASPP2 protein in placental trophoblast cells(x±s, n=4) *P < 0.05, **P < 0.01 vs control group |
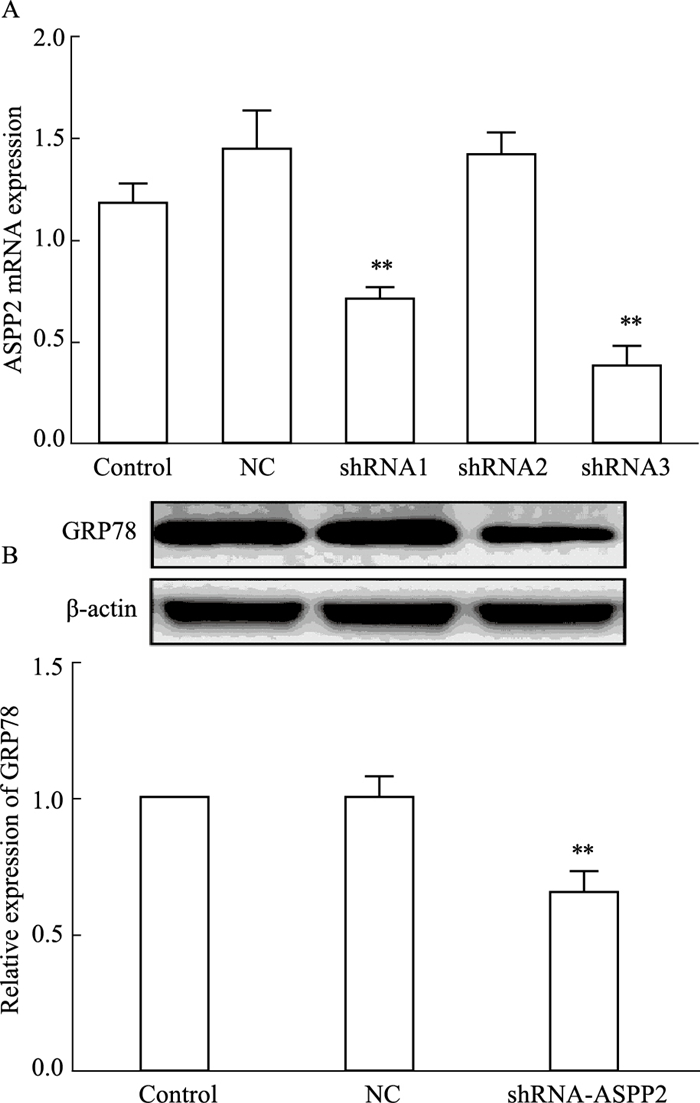
qRT-PCR和Western blot分别检测ASPP2、GRP78 mRNA与蛋白表达水平,Fig 3结果显示,与NC组相比,shRNA1和shRNA3表达降低(P<0.01),但shRNA3效果最明显,后续实验均选用shRNA3-ASPP2;干扰ASPP2后,GRP78蛋白表达水平明显降低(P<0.01)。
|
| Fig 3 Transfection of ASPP2 interference adenovirus and protein expression of GRP78 in placental trophoblast cells(x±s, n=3) A:After placental trophoblast cells transfect interference control (NC group) and ASPP2 interference adenoviral fragment (shRNA1, shRNA2, shRNA3), qRT-PCR was used to detect ASPP2 mRNA expression; B:Western blot was used to detect GRP78 protein expression after interference with ASPP2 expression. **P < 0.01 vs NC group. |
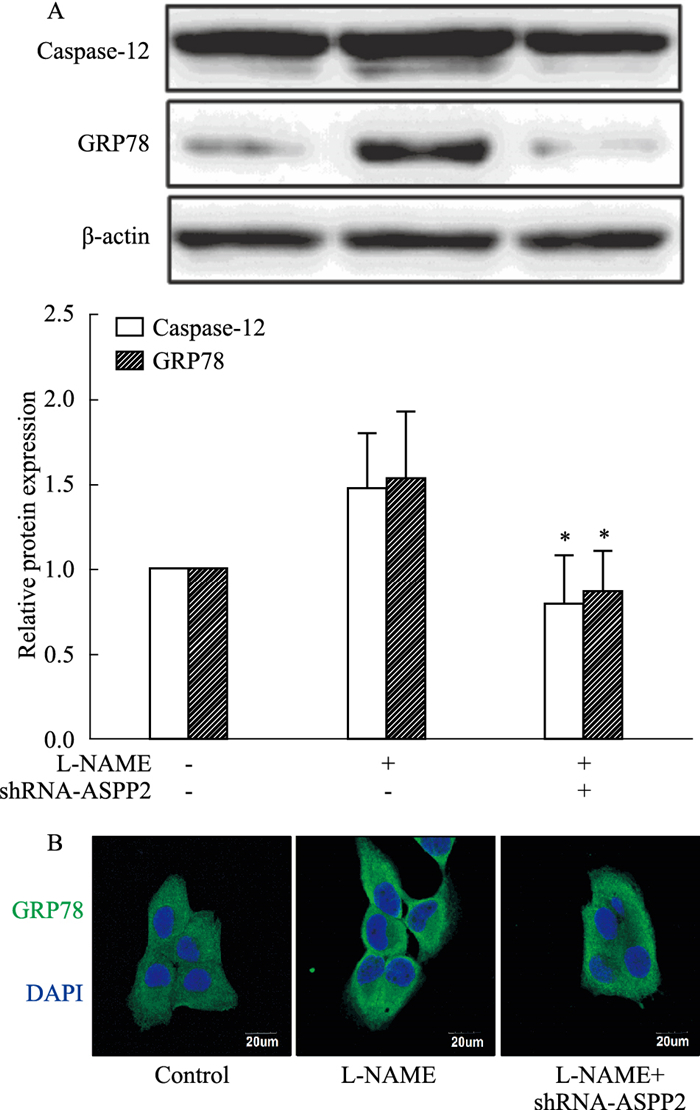
Fig 4结果显示,与L-NAME组相比,L-NAME+shRNA-ASPP2组caspase-12、GRP78蛋白表达水平明显降低(P<0.05)。同时,免疫荧光染色也显示GRP78蛋白表达水平降低。
|
| Fig 4 Effect of ASPP2 on caspase-12 and GRP78 in placental trophoblast cells A:Western blot was used to detect caspase-12 and GRP78 protein expression(x±s, n=4); B:Immunofluorescence was used to detect GRP78 protein expression (×1 000). *P < 0.05 vs L-NAME group. |
HDCP是产科常见的一种并发症,在孕产妇中发病机率较高,严重时甚至会导致孕产妇、胎儿或新生儿死亡[9]。目前,对于HDCP的发病机制尚不明确。研究发现[10],多数病例在妊娠20周以后会出现一过性高血压、蛋白尿等症状,但这些症状会随着分娩结束而消失,因此,母胎界面或胎盘的功能成为越来越多人的研究重点。胎盘是哺乳动物妊娠期间由胚胎的绒毛膜和母体子宫内膜联合长成的母子间交换物质的过渡性器官,可以分泌多种激素及细胞因子,而胎盘滋养细胞在其中发挥着重要的功能,因此,胎盘滋养细胞功能的异常与HDCP密切相关[11]。同时,随着有关凋亡在人体疾病发病机制方面的深入研究,近年来胎盘滋养细胞凋亡与HDCP的关系倍受关注。有研究报道[12],HDCP子痫前期患者血清NO表达水平明显低于正常妊娠组,提示妊娠期间NO分泌不足可能是HDCP的重要致病因素之一。在本研究中,我们用一氧化氮合酶抑制剂L-NAME干预人胎盘滋养细胞,从而模拟HDCP微环境。实验结果显示,L-NAME干预48 h后,人胎盘滋养细胞凋亡水平明显增加,同时caspase-12蛋白的表达水平也明显增加,表明胎盘滋养细胞凋亡是导致HDCP的重要环节。
内质网应激反应是机体对环境刺激所产生的自我保护反应,在各种疾病的发病机制中发挥关键作用,并且与多种基因的表达调控相关,而长期刺激导致的内质网应激反应会导致细胞调节功能失衡,进而引起细胞凋亡[13]。GRP78作为内质网上的重要分子伴侣,在蛋白质折叠和转运过程及内质网应激反应中发挥重要作用,是细胞内质网应激反应的敏感标记物[14]。本研究结果显示,L-NAME干预胎盘滋养细胞后,GRP78蛋白的表达水平明显增加,表明L-NAME诱导胎盘滋养细胞凋亡过程中确实存在内质网应激反应。ASPP2是ASPP细胞凋亡调节家族中结构最完整的家族成员,作为p53结合蛋白家族的一个促凋亡成员,可以通过将p53引导至促凋亡基因的启动子而与其结合,并增强p53的凋亡能力。有研究报道[15],ASPP2可以通过p53非依赖的形式增强DRAM和Bax的表达,进一步促进肿瘤细胞的凋亡。但是有关ASPP2在胎盘滋养细胞凋亡方面的研究还未见报道。本实验结果显示,L-NAME干预胎盘滋养细胞后,ASPP2蛋白的表达水平明显增加,表明ASPP2可能参与胎盘滋养细胞凋亡的过程。那么,ASPP2是否通过调节内质网应激反应,从而影响胎盘滋养细胞的凋亡呢?研究发现,感染ASPP2干扰腺病毒后,GRP78蛋白的表达水平明显降低,同时用L-NAME干预胎盘滋养细胞后,caspase-12和GRP78蛋白的表达水平也明显降低,提示通过下调ASPP2降低GRP78的表达,可以抑制L-NAME诱导的胎盘滋养细胞凋亡,进一步表明ASPP2可能通过内质网应激反应参与了胎盘滋养细胞凋亡的调控。
HDCP的发病机制复杂,并受多种复杂而精细的调控。本实验发现,ASPP2可能参与胎盘滋养细胞凋亡的发生过程,同时内质网应激反应作为外源性引发胎盘滋养细胞凋亡的重要靶点,在HDCP的发生发展中应该被重点关注,这可能为进一步研究HDCP的发病机制指明了新的方向。
( 致谢: 本实验在宁夏血管损伤与修复研究重点实验室完成,感谢各位老师、同学在实验过程中给予的支持与帮助。)
| [1] |
王颖, 李梅, 解冰洁, 等. 妊娠期高血压疾病对小于胎龄儿的影响及潜在交互作用研究[J]. 中华流行病学杂志, 2016, 37(9): 1283-7. Wang Y, Li M, Xie B J, et al. Influence of hypertension disorder complicating pregnancy and its interaction with other factors on incidence of small for gestational age[J]. Chin J Epidemiol, 2016, 37(9): 1283-7. doi:10.3760/cma.j.issn.0254-6450.2016.09.020 |
| [2] |
韩瑾, 张蒙, 许遵鹏, 等. 孕早期血清胎盘生长因子在妊娠期高血压疾病筛查中的应用[J]. 中国妇幼健康研究, 2016, 27(6): 698-701. Han J, Zhang M, Xu Z P, et al. Application of first-trimester serum placental growth factor in the screening for gestational hypertension[J]. Chin J Woman Child Health Res, 2016, 27(6): 698-701. doi:10.3969/j.issn.1673-5293.2016.06.009 |
| [3] |
Wierzba W, Tyszko P, Kanecki K, et al. Proliferation and apoptosis of human placental cells exposed to aromatic hydrocarbons[J]. Ginekol Pol, 2017, 88(12): 686-91. doi:10.5603/GP.a2017.0122 |
| [4] |
Xiong J, Ding N, Gao T, et al. Hypermethylation of endoplasmic reticulum disulfide oxidase 1α leads to trophoblast cell apoptosis through endoplasmic reticulum stress in preeclampsia[J]. J Cell Biochem, 2018, 119(10): 8588-99. doi:10.1002/jcb.27101 |
| [5] |
李忠生, 于常艳, 陈宵, 等. 喹乙醇致肾脏毒性的内质网应激相关凋亡途径研究[J]. 卫生研究, 2015, 44(3): 444-50. Li Z S, Yu C Y, Chen X, et al. Research on olaquindox induced endoplasmic reticulum stress related apoptosis on nephrotoxicity[J]. J Hygiene Res, 2015, 44(3): 444-50. |
| [6] |
Wang Y, Wang J H, Zhang X L, et al. Endoplasmic reticulum chaperone glucose-regulated protein 78 in gastric cancer:an emerging biomarker[J]. Oncol Lett, 2018, 15(5): 6087-93. |
| [7] |
Liu K, Jiang T, Ouyang Y, et al. Nuclear EGFR impairs ASPP2-p53 complex-induced apoptosis by inducing SOS1 expression in hepatocellular carcinoma r[J]. Oncotarget, 2015, 6(18): 16507-16. |
| [8] |
Wang S, Yang L, Bai R, et al. Interaction of p53 and ASPPs regulates rhesus monkey embryonic stem cells conversion to neural fate concomitant with apoptosis[J]. Cell Cycle, 2018, 17(9): 1146-53. doi:10.1080/15384101.2018.1464848 |
| [9] |
曲垟霖, 王巍, 王强. 妊娠期高血压疾病血压控制水平与妊娠结局相关综述分析[J]. 中国妇幼保健, 2018, 33(11): 26325. Qu Y L, Wang W, Wang Q. A review of the relationship between blood pressure control level and pregnancy outcome in hypertensive disorder complicating pregnancy[J]. Maternal Child Health Care China, 2018, 33(11): 2632-5. |
| [10] |
Beukers F, Cranendonk A, de Vries J I, et al. Catch-up growth in children born growth restricted to mothers with hypertensive disorders of pregnancy[J]. Arch Dis Child, 2013, 98(1): 30-5. doi:10.1136/archdischild-2012-302510 |
| [11] |
毛彩艳, 张辉, 李旭生, 等. FABP4在妊娠期高血压疾病胎盘滋养细胞免疫炎症反应中的作用研究[J]. 中国药理学通报, 2017, 33(8): 1126-31. Mao C Y, Zhang H, Li X S, et al. Effect of FABP4 on placental trophoblastic immune inflammatory response in patients of hypertensive disorder complicating pregnancy[J]. Chin Pharmacol Bull, 2017, 33(8): 1126-31. doi:10.3969/j.issn.1001-1978.2017.08.017 |
| [12] |
胡方慧, 邹晓红, 杨云, 等. 内皮素-1及一氧化氮在妊娠高血压疾病子痫前期患者血清中的表达[J]. 中国社区医师, 2017, 33(31): 102-3. Hu F H, Zou X H, Yang Y, et al. Expression of endothelin-1 and nitric oxide in serum of patients with gestational hypertension preeclampsia[J]. Chin Community Doctors, 2017, 33(31): 102-3. doi:10.3969/j.issn.1007-614x.2017.31.63 |
| [13] |
许文虎, 金春子, 王晓龙, 等. 内质网应激信号通路在棕榈酸诱导的血管内皮细胞凋亡中的作用[J]. 中国药理学通报, 2017, 33(12): 1668-72. Xu W H, Jin C Z, Wang X L, et al. Role of endoplasmic reticulum stress signaling pathway in high fat-induced cell apoptosis in vascular endothelial cells[J]. Chin Pharmacol Bull, 2017, 33(12): 1168-72. |
| [14] |
Xiong Z, Jiang R, Li X, et al. Different roles of GRP78 on cell proliferation and apoptosis in cartilage development[J]. Int J Mol Sci, 2015, 16(9): 21153-76. |
| [15] |
Song X, Du J, Zhu W, et al. Identification and characterization of an apoptosis-stimulating protein of p53 (ASPP) gene from Branchiostoma belcheri:insights into evolution of ASPP gene family[J]. Fish Shellfish Immunol, 2016, 49: 268-74. |