

2. 北京大学人民医院,北京 100044
2. Peking University People′s Hospital, Beijing 100044, China
糖尿病是一种临床常见的代谢性疾病。国际糖尿病联盟预计2040年全球将有6.42亿糖尿病患者,其中85%~95%为2型糖尿病(type 2 diabetes mellitus,T2DM)[1]。糖尿病发病率的急剧升高与不健康的饮食及生活习惯、吸烟和肥胖等密切相关,研究表明睡眠障碍也应被视为一个重要的危险因素。
睡眠障碍指睡眠时间不足或睡眠中存在异常问题,包括入睡困难、恶梦、早醒、片段化睡眠、昼夜节律失调、睡眠呼吸障碍等。多项研究证明,睡眠障碍和糖尿病之间存在一种双向关系:一方面,T2DM患者的睡眠问题远多于非糖尿病患者; 另一方面,睡眠障碍也会增加糖尿病患病风险,或者影响血糖水平,使病情进一步恶化[2, 3]。
1 睡眠障碍对T2DM的影响睡眠过程主要分为非快眼动睡眠和快眼动睡眠,前者即所谓深睡眠,占睡眠总时长的15%~20%。深睡眠阶段人体的交感神经兴奋性降低,迷走神经兴奋性增高,表现为心率减慢、血压降低、生长激素释放增加、大脑的葡萄糖利用率降低、下丘脑-垂体-肾上腺(hypothalamic pituitary adrenal,HPA)轴的活性被抑制。而睡眠障碍会导致夜间交感神经系统活性升高、肾上腺皮质分泌增多,使机体对胰岛素的敏感性降低[4]。目前研究显示,睡眠时间和睡眠质量均与T2DM相关。
1.1 睡眠时间与T2DM近期多项Meta分析显示,睡眠时间与糖尿病的发生风险呈“U型”关系,每日7~8 h的风险最低,过短或过长的睡眠均会导致患病风险增加[5-7]。进行4晚睡眠剥夺的成年人,外周脂肪组织的胰岛素敏感性比对照组减少了约30%[8]。此外,睡眠时间异常也会影响昼夜节律,而睡眠昼夜节律在调节胰岛素分泌及胰岛素敏感性中也发挥重要作用[9]。
1.2 睡眠质量与T2DM睡眠呼吸障碍是一种严重影响睡眠质量的慢性疾病,其中阻塞型睡眠呼吸暂停(obstructive sleep apnea,OSA)的发病率最高,其特征是睡眠时间歇性部分或完全的上气道阻塞,导致低氧血症、高碳酸血症,甚至激醒。OSA使睡眠片段化,深睡眠比例下降,影响糖代谢、胰岛素敏感性和胰岛β细胞的功能[10]。有研究发现,OSA患者的糖尿病发病率有所增加,而糖尿病患者的OSA患病率也高于常人[11]。睡眠呼吸障碍还会影响血糖稳态,血糖波动过大会使糖尿病并发症的发生率明显升高。
持续气道正压通气可以使患者在睡眠期间保持上气道开放,避免呼吸暂停的发生。该治疗不仅能减少睡眠片段化和其他睡眠异常,而且可以维持血糖平衡,明显提高合并有OSA的T2DM患者的胰岛素敏感性,降低患者的HbA1c[12]。
2 睡眠影响T2DM的机制 2.1 交感神经系统研究显示,睡眠剥夺后,血清和尿中去甲肾上腺素和肾上腺素水平均有所增高,从而促进糖异生,导致血糖升高[13]。从机制上看,睡眠障碍会导致自主神经系统节律紊乱、低氧血症、高碳酸血症等,引起交感神经系统的过度激活,抑制胰岛素分泌,同时减少胰岛素介导的葡萄糖摄取。
2.2 HPA轴睡眠剥夺会影响HPA轴,使体内皮质醇、肾上腺素等胰岛素拮抗激素的分泌增加[14],导致外周组织对胰岛素的敏感性下降。交感神经系统也会刺激HPA轴,从而影响血糖水平。
2.3 食欲睡眠障碍可以间接通过改变食欲,影响T2DM的发生。睡眠不足或睡眠质量差会影响多种调节食欲的激素分泌,包括抑制食欲的瘦素、胰岛素和增加食欲的胃饥饿素、食欲素等[15, 16]。瘦素可以下调胰岛素的基因转录和分泌,提高周围组织对胰岛素的敏感性。胃饥饿素主要向下丘脑传递刺激食欲的信号,通过增加交感神经活性来减轻饱腹感,此外,还会促进脂肪形成、抑制脂肪分解、减少能量消耗,引起肥胖和胰岛素抵抗。食欲素通过活化交感神经系统,增加肝糖原的合成,并促进骨骼肌和棕色脂肪组织摄取利用葡萄糖。食欲素缺乏会导致肝细胞内质网应激增强,引起肝胰岛素信号传导障碍和糖异生异常[17]。
2.4 褪黑激素褪黑激素是由哺乳动物松果体产生的一种胺类激素,其分泌主要受昼夜节律调控,交感神经兴奋会导致其释放减少。褪黑激素可调节胰岛素分泌,改善胰岛素活性[18]。短睡眠和睡眠障碍者体内褪黑激素合成和分泌紊乱,导致T2DM发病风险明显升高[19]。
褪黑素还能提高血清脂联素的水平[20],而脂联素是肝和外周组织的胰岛素敏化剂[21]。褪黑素及其代谢物也是有效的自由基清除剂,其抗氧化和抗炎作用可以改善β细胞功能障碍、减少β细胞凋亡。
3 T2DM影响睡眠睡眠受多种因素影响,糖尿病导致睡眠障碍的病因机制十分复杂。在糖尿病发展过程中,会出现多系统功能紊乱或器官损害,致使睡眠调控机制失衡。首先,糖尿病可影响中枢神经系统的神经递质,引起自主神经功能紊乱,影响患者睡眠[22]; 其次,糖尿病加重内分泌系统的紊乱,HPA轴功能亢进是已知的导致睡眠障碍的因素[23]; 另外,T2DM中高血糖、代谢性炎症、胰岛素抵抗等多种因素导致周围神经病变[24],这种慢性并发症也是造成睡眠障碍的重要原因。T2DM还与肥胖密切相关,肥胖易导致OSA和其他睡眠障碍。
此外,降糖药物使用过量或摄食过少时,患者夜间可能会出现低血糖,交感神经兴奋而导致患者惊醒; 高血糖会导致渗透性利尿作用增强,排尿频率增加; 糖尿病作为一种慢性疾病,易导致焦虑、抑郁等精神心理障碍,引起睡眠质量下降。
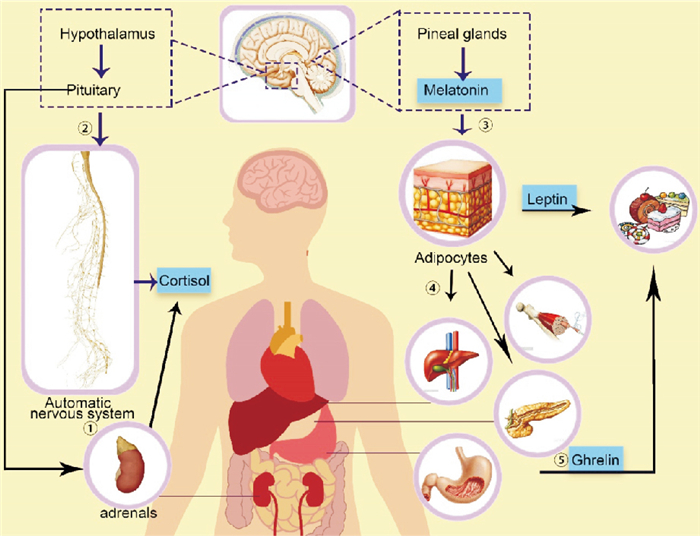
4 结语糖尿病与睡眠相互影响,T2DM患者睡眠障碍发生率较高,而睡眠障碍也会对血糖控制产生不良影响(Fig 1)。故在治疗上,一方面,改善睡眠质量、优化睡眠时间可以减轻胰岛素抵抗、稳定血糖水平; 另一方面,T2DM患者病情的缓解可改善机体代谢,提高睡眠质量。现阶段关于T2DM患者睡眠的研究仍处于探索期。目前进行的实验有一些不足之处:首先,问卷评价虽简单易行,但无法保证真实客观性; 多导睡眠图是确诊睡眠障碍的最佳标准,但价格昂贵、操作复杂。其次,进行抽样调查时,睡眠时间过长的参与者比例很小,易受偶然因素的影响; 另外,关于未成年糖尿病患者的研究还比较少。随着T2DM患病人数的激增,改善患者症状、提高生活质量迫在眉睫,通过改善睡眠延缓病情恶化的研究应当成为焦点。此外,关于糖尿病和睡眠障碍的机制尚不清楚,需要进一步的探索。而以上的论述提示,临床工作者在关注药物及饮食、运动管理的同时,应加强对患者睡眠状况的干预,良好的睡眠可能成为改善病情的关键所在。
|
| Fig 1 Glycemic control affected by sleep ① The hypothalamus secrets corticotropin releasing hormone(CRH), stimulating pituitary secretion of adrenocorticotropic hormone(ACTH). ACTH promotes adrenal secretion of cortisol, affecting the secretion and function of insulin. ② Under circadian regulation, hypothalamus affects the autonomic nervous system, regulating the secretion of cortisol. ③ The pineal glands secrete melatonin, increasing the secretion and function of insulin by directly acting on islet cells or by decreasing circulating free fatty acid levels. ④ Adipocytes produce leptin, regulating insulin secretion and improving the surrounding tissue on insulin sensitivity. ⑤ Ghrelin, secreted by the stomach, along with leptin regulate appetite, affecting the body′s intake of calories. |
| [1] |
Ogurtsova K, Da R F J, Huang Y, et al. IDF Diabetes Atlas: Global estimates for the prevalence of diabetes for 2015 and 2040[J]. Diabetes Res Clin Pract, 2017, 128: 40. doi:10.1016/j.diabres.2017.03.024 |
| [2] |
Resnick H E, Redline S, Shahar E, et al. Diabetes and sleep disturbances[J]. Diabetes Care, 2016, 26(3): 702-9. |
| [3] |
Seibert P S, Jennifer V, Codieann D H. The concomitant relationship shared by sleep disturbances and type 2 diabetes: developing telemedicine as a viable treatment option[J]. J Diabetes Sci Technol, 2013, 7(6): 1607. doi:10.1177/193229681300700621 |
| [4] |
Tan X, Chapman C D, Cedernaes J, et al. Association between long sleep duration and increased risk of obesity and type 2 diabetes: A review of possible mechanisms[J]. Sleep Med Rev, 2018, 40: 127-34. doi:10.1016/j.smrv.2017.11.001 |
| [5] |
Itani O, Jike M, Watanabe N, et al. Short sleep duration and health outcomes: a systematic review, meta-analysis, and meta-regression[J]. Sleep Med, 2017, 32: 246-56. doi:10.1016/j.sleep.2016.08.006 |
| [6] |
Lee S, Ng K Y, Chin W K. The impact of sleep amount and sleep quality on glycemic control in type 2 diabetes: a systematic review and meta-analysis[J]. Sleep Med Rev, 2017, 31: 91-101. doi:10.1016/j.smrv.2016.02.001 |
| [7] |
Ford E S, Wheaton A G, Chapman D P, et al. Associations between self-reported sleep duration and sleeping disorder with concentrations of fasting and 2-h glucose, insulin, and glycosylated hemoglobin among adults without diagnosed diabetes[J]. J Diabetes, 2014, 6(4): 338-50. doi:10.1111/jdb.2014.6.issue-4 |
| [8] |
Broussard J L, Ehrmann D A, Van Cauter E, et al. Impaired insulin signaling in human adipocytes after experimental sleep restriction: a randomized, crossover study[J]. Ann Intern Med, 2012, 157(8): 549-57. doi:10.7326/0003-4819-157-8-201210160-00005 |
| [9] |
Reutrakul S, Van Cauter E. Interactions between sleep, circadian function, and glucose metabolism: implications for risk and severity of diabetes[J]. Ann N Y Acad Sci, 2014, 1311(1): 151-73. doi:10.1111/nyas.2014.1311.issue-1 |
| [10] |
Melamed K H, Goldhaber S Z. Cardiology patient page. Obstructive sleep apnea[J]. Circulation, 2015, 132(5): e114-6. |
| [11] |
Arble D M, Bass J, Behn C D, et al. Impact of sleep and circadian disruption on energy balance and diabetes: a summary of workshop discussions[J]. Sleep, 2015, 38(12): 1849-60. doi:10.5665/sleep.5226 |
| [12] |
Mokhlesi B, Grimaldi D, Beccuti G, et al. Effect of one week of 8-hour nightly continuous positive airway pressure treatment of obstructive sleep apnea on glycemic control in type 2 diabetes: a proof-of-concept study[J]. Am J Respir Crit Care Med, 2016, 194(4): 516-9. doi:10.1164/rccm.201602-0396LE |
| [13] |
Faraut B, Nakib S, Drogou C, et al. Napping reverses the salivary interleukin-6 and urinary norepinephrine changes induced by sleep restriction[J]. J Clin Endocrinol Metab, 2015, 100(3): E416-26. doi:10.1210/jc.2014-2566 |
| [14] |
Guyon A, Balbo M, Morselli L L, et al. Adverse effects of two nights of sleep restriction on the hypothalamic-pituitary-adrenal axis in healthy men[J]. J Clin Endocrinol Metab, 2014, 99(8): 2861-8. doi:10.1210/jc.2013-4254 |
| [15] |
Hibi M, Kubota C, Mizuno T, et al. Effect of shortened sleep on energy expenditure, core body temperature, and appetite: a human randomised crossover trial[J]. Sci Rep, 2017, 7: 39640. doi:10.1038/srep39640 |
| [16] |
Krittanawong C, Tunhasiriwet A, Wang Z, et al. Association between short and long sleep duration and cardiovascular outcomes? A systematic review and meta-analysis[J]. Eur Heart J Acute Cardiovasc Care, 2017, 69S(11): 1798. |
| [17] |
Tsuneki H, Tokai E, Nakamura Y, et al. Hypothalamic orexin prevents hepatic insulin resistance via daily bidirectional regulation of autonomic nervous system in mice[J]. Diabetes, 2015, 64(2): 459-70. doi:10.2337/db14-0695 |
| [18] |
Agil A, Rosado I, Ruiz R, et al. Melatonin improves glucose homeostasis in young Zucker diabetic fatty rats[J]. J Pineal Res, 2012, 52(2): 203-10. doi:10.1111/jpi.2012.52.issue-2 |
| [19] |
Mcmullan C J, Schernhammer E S, Rimm E B, et al. Melatonin secretion and the incidence of type 2 diabetes[J]. JAMA, 2013, 309(13): 1388-96. doi:10.1001/jama.2013.2710 |
| [20] |
Yamauchi T, Kadowaki T. Adiponectin receptor as a key player in healthy longevity and obesity-related diseases[J]. Cell Metab, 2013, 17(2): 185-96. doi:10.1016/j.cmet.2013.01.001 |
| [21] |
周庆峰. 细胞因子类抗糖尿病药物研究进展[J]. 中国药理学通报, 2016, 32(6): 760-3. Zhou Q F. Research progress in anti-diabetic drugs of cytokine[J]. Chin Pharmacol Bull, 2016, 32(6): 760-3. doi:10.3969/j.issn.1001-1978.2016.06.005 |
| [22] |
Monti J M. The neurotransmitters of sleep and wake, a physiological reviews series[J]. Sleep Med Rev, 2013, 17(4): 313-5. doi:10.1016/j.smrv.2013.02.004 |
| [23] |
Barone M T, Menna-Barreto L. Diabetes and sleep: a complex cause-and-effect relationship[J]. Diabetes Res Clin Pract, 2011, 91(2): 129-37. doi:10.1016/j.diabres.2010.07.011 |
| [24] |
杨秀颖, 张莉, 陈熙, 等. 2型糖尿病周围神经病变机制研究进展[J]. 中国药理学通报, 2016, 32(5): 598-602. Yang X Y, Zhang L, Chen X, et al. Research progress of diabetic peripheral neuropathy mechanisms in type 2 diabetes[J]. Chin Pharmacol Bull, 2016, 32(5): 598-602. doi:10.3969/j.issn.1001-1978.2016.05.002 |

