

2. 中国医学科学院药物研究所, 药物靶点研究与新药筛选北京市重点实验室, 北京 100050
杨淬(1975-),男,博士,教授,研究方向:民族活性药物筛选,通讯作者,E-mail: yangynni@163.com
2. Institute of Materia Medica, Chinese Academy of Medical Sciences & Peking Union Medical College, Drug Targets & Screening Center-the Key Lab of Beijing, Beijing 100050, China
肿瘤是一类严重威胁人类健康的疾病。据我国2018年最新癌症报告显示,2014年全国恶性肿瘤新发病例数380.4万例,0~74岁累积死亡率为12.00%。肿瘤是多因素经过多个过程形成的,包括肿瘤的起始、发展、浸润、转移等[1-2]。目前,肿瘤的靶向治疗已成为肿瘤治疗的研究热点。与传统细胞毒化疗不同,肿瘤分子靶向治疗具有特异性抗肿瘤作用,并且毒性明显减少,开创了肿瘤治疗的新领域[3]。
在恶性肿瘤中,黑色素瘤是皮肤肿瘤中恶性程度最高的一种,具有容易出现远处转移、增长快、死亡率高、预后差的特点。因此,阐明黑色素瘤的分子机制,发现新的黑色素瘤治疗靶标及基于这些靶标的新药发现,对于黑色素瘤的治疗具有重要的意义[4]。
ST8α-N-乙酰基-神经氨酸α-2, 8-唾液酸转移酶1(ST8 alpha-N-acetyl-neuraminide alpha-2, 8-sialyltransferase 1, ST8Sia1)是唾液酸转移酶ST8Sia亚家族的6个成员(ST8Sia Ⅰ-Ⅵ)之一,又被称为神经节苷脂3合成酶(ganglioside GD3 synthase, GD3s)。ST8Sia1是神经节苷脂GD3和神经节苷脂GD2生物合成的唯一关键酶[5-6]。ST8Sia1的功能研究,对于GD3及其下游产物的生物合成以及肿瘤发生发展等,具有重要的意义。已有文献报道,ST8Sia1在肿瘤中高表达,特别是在神经外胚层来源的肿瘤中表达很高,如恶性胶质瘤、黑色素瘤等[7]。我们通过生物信息学分析,也发现了ST8Sia1在黑色素瘤中的高表达,但是ST8Sia1能否作为抗肿瘤靶点仍不确定。为了研究ST8Sia1在黑色素瘤中的功能及其作用机制,构建高表达ST8Sia1基因的表达载体显得非常重要。本研究主要利用基因工程技术,构建了两种不同的ST8Sia1基因过表达载体,并比较了不同载体在人黑色素瘤细胞WM451中的转染效率,挑选转染效率较高的载体,建立稳定高表达ST8Sia1的细胞株,并探讨ST8Sia1过表达对黑色素瘤细胞增殖的影响。本研究为进一步研究ST8Sia1基因在黑色素瘤中的生物学功能奠定了基础。
1 材料与方法 1.1 材料 1.1.1 细胞株人胚胎肾细胞293T购自中国科学院细胞库(上海);人黑色素瘤细胞WM451购自广州吉妮欧公司。
1.1.2 试剂ST8Sia1-myc-flag质粒,购自美国Origene公司(CAT # : RC223851);pEGFP-C1载体,购自上海唯地生物公司;pHBLV-CMV-MCS-3flag-EF1-ZsGreen-T2A-Puro载体,购自汉恒生物科技有限公司;限制性内切酶EcoR Ⅰ、Bgl Ⅱ、BamH Ⅰ、Xba Ⅰ,购自日本TaKaRa公司;DNA ladder购自美国Thermo Fisher Scientific公司;大肠杆菌菌株DH5α,购自美国Invitrogen公司;质粒DNA小、大量抽提试剂盒,购自北京康为世纪公司;凝胶回收试剂盒,购自上海捷瑞生物工程有限公司;琼脂糖、琼脂粉,购自上海生工生物工程有限公司;KOD-Plus Kit购自上海东洋纺生物科技有限公司;DMEM培养基、胎牛血清(FBS),购自美国Invitrogen公司;ST8Sia1多克隆抗体购自Abcam公司(CAT # : ab37806);GAPDH鼠单克隆抗体购自Proteintech公司(CAT # : 60004-1-Ig)。ST8Sia1引物由奥科鼎盛生物科技有限公司合成;碱基测序由睿博兴科测序公司完成。
1.1.3 仪器荧光定量PCR仪(美国ABI公司);CXY-6C电泳仪(北京六一仪器厂);细胞培养箱(美国Thermo公司);Tanon-1200凝胶成像系统(上海天能科技有限公司); 荧光显微镜(日本OLYMPUS公司)。
1.2 方法 1.2.1 不同ST8Sia1基因过表达载体构建 1.2.1.1 构建携带绿色荧光蛋白的ST8Sia1-pEGFP-C1重组质粒引物设计。从GenBank库中查找人ST8Sia1的mRNA序列,设计引物。h-ST8Sia1-forward primer: GAGAAG ATCTatgagcccctgcgggcgg;h-ST8Sia1-reverse primer: GCTCTA GATCAggaagtgggctggagtgaggta。
ST8Sia1片段PCR回收。PCR扩增ST8Sia1序列,体系(50 μL)为:10×PCR Buffer for KOD plus 5 μL, MgSO4 (25 mmol·L-1) 3 μL, dNTPs (2 mmol·L-1) 5 μL, 上游引物(10 μmol·L-1) 1.5 μL,下游引物(10 μmol·L-1) 1.5 μL,KOD plus DNA polymerase 1 μL,模板DNA(ST8Sia1质粒,100 ng· μL-1)1 μL, ddH2O 32 μL。将以上反应物轻轻混匀后进入扩增程序,即94 ℃ 2 min, 然后反复98 ℃ 10 s, 60 ℃ 30 s, 68 ℃ 45 s循环30次, 68 ℃ 10 min,4 ℃冷却后取出,琼脂糖凝胶回收目的条带, 大小约1 100 bp, 获得ST8Sia1 cDNA片段。
ST8Sia1PCR产物、pEGFP-C1载体双酶切及连接。ST8Sia1的PCR产物进行Bgl Ⅱ/Xba Ⅰ的双酶切, 体系(50 μL)为:ST8Sia1胶回收产物33 μL,Bgl Ⅱ 1 μL,Xba Ⅰ 1 μL,10×T buffer 10 μL,ddH2O 5 μL,37 ℃水浴消化过夜, 进行胶回收电泳及胶回收纯化, 得到带有Bgl Ⅱ/Xba Ⅰ黏性末端的ST8Sia1序列。pEGFP-C1载体双酶切,体系(50 μL)为:pEGFP-C1质粒3 μL (约1.5 μg),Bgl Ⅱ 1 μL,Xba Ⅰ 1 μL,10×T buffer 10 μL,ddH2O 35 μL,37 ℃水浴消化5 h, 进行胶回收电泳切胶并回收4 731 bp的条带, 得到带有Bgl Ⅱ/Xba Ⅰ黏性末端的线性化pEGFP-C1载体。连接目的基因ST8Sia1和载体pEGFP-C1, 连接体系(8 μL)为:胶回收的ST8Sia1 DNA 3 μL,胶回收的pEGFP-C1 plasmid 1 μL,DNA Ligation Kit Solution I 4 μL,16 ℃水浴5 h,获得连接产物。
连接产物转化及阳性克隆鉴定。取上述连接产物8 μL,加入30 μL DH5α感受态细胞,冰上放置30 min,42 ℃水浴中热激90 s, 然后迅速置于冰上冷却5 min。向管中加入1 mL LB液体培养基,混匀后,于37 ℃、220 r·min-1摇床振荡培养1 h。离心,去除900 μL上清, 余下培养基吸打混匀后,涂布于含卡那霉素的固体培养基平板。倒置于37 ℃生化培养箱中,培养过夜。挑取单个菌落接种于含卡那霉素的液体LB培养基中, 37 ℃培养。抽提质粒, PCR方法进行鉴定, 产生1 068 bp左右条带的为阳性, 对其进行DNA序列测定。
1.2.1.2 构建携带绿色荧光蛋白的ST8Sia1过表达慢病毒载体引物设计,从GenBank库中查找人ST8Sia1的mRNA序列,设计引物。h-ST8Sia1-Eco/Eco-forward primer: ggatctatttccggtGaattcgccaccATGAGCCCCTGCGGGCGG; h-ST8Sia1-Xho/Eco-reverse primer: tctagaactagtctcgagGGAAGTGGGCTGG AGTGAGGTATCT。
ST8Sia1片段PCR回收:同“1.2.1.1”。
pHBLV-CMV-MCS-3flag-EF1-ZsGreen-T2A-Puro载体酶切后,与ST8Sia1目的片段重组。用pHBLV-CMV-MCS-3flag-EF1-ZsGreen-T2A-Puro作为载体,目的片段插入MCS区, 由CMV启动子调控表达。载体用EcoRI酶切,体系(40 μL)为:载体(400 ng·μL-1) 2 μL,EcoRI 2 μL,10× Buffer 4 μL,H2O 32 μL。将以上反应物缓慢混合后,置于37 ℃恒温水浴锅中2 h,获得酶切后的pHBLV-CMV-MCS-3flag-EF1-ZsGreen-T2A-Puro载体。将“1.2.1.1”中处理好的ST8Sia1基因片段与载体连接,反应体系(20 μL)为:片段50 ng, 酶切后载体20 ng, HB-infusion Master Mix (2×) 10 μL, 超纯H2O加至总体系为20 μL。以上反应体系置于50 ℃水浴20 min,获得连接产物。
连接产物转化及阳性克隆鉴定。取上述连接产物10 μL到30 μL DH5α感受态细胞中, 涂布含氨苄西林的固体培养基平板, 37 ℃培养过夜, 挑取单个菌落接种于含氨苄西林的液体LB培养基中, 37 ℃培养。菌液进行PCR鉴定,将阳性克隆菌液送测序公司测序。
重组慢病毒的包装及滴度检测。对阳性克隆菌液进行高纯度无内毒素质粒抽提,得到慢病毒载体质粒,将重组质粒载体和两个包装质粒(pMD2.G和psPAX2)混合后,共转染293T细胞,培养72 h后,收集细胞上清液,0.45 μm滤器过滤,离心浓缩,得到高滴度的病毒浓缩液。采用稀释计数法测定各组病毒滴度。将293T细胞按2×103每孔接种于96孔板中。培养24 h后,将慢病毒原液以3倍稀释成6个梯度,加入对应的96孔板中。24 h后更换培养基,定期观察。48 h后在荧光显微镜下观察结果,荧光百分比在10%~30%的孔计算病毒滴度。
1.2.2 不同ST8Sia1基因过表达载体转染黑色素瘤WM451细胞用ST8Sia1低表达的黑色素瘤WM451细胞作为转染细胞株,分别用ST8Sia1-pEGFP-C1重组质粒和ST8Sia1过表达慢病毒载体对细胞进行转染,并用荧光显微镜观察转染效率。
1.2.2.1 ST8Sia1-pEGFP-C1重组质粒转染WM451细胞实验分为2组:①阴性对照组(NC):WM451细胞转染pEGFP-C1空载体对照质粒;② ST8Sia1-pEGFP-C1重组质粒组:WM451细胞转染ST8Sia1-pEGFP-C1重组质粒。细胞铺6孔板24 h后,按照Lipofectamine 3000说明书对其进行转染。转染48 h后,荧光显微镜下观察其绿色荧光的表达情况。
1.2.2.2 ST8Sia1过表达慢病毒载体感染WM451细胞实验分为3组:①空白对照组:WM451细胞正常培养;②阴性对照组(NC):WM451细胞感染空慢病毒载体;③ ST8Sia1过表达慢病毒载体组:WM451细胞感染ST8Sia1过表达慢病毒载体。细胞铺6孔板24 h后,吸去细胞原有培养基,加入1.5 mL含有5 mg·L-1聚凝胺的新鲜培养基,再分别吸取病毒原液加入相应的组中,4 h后补齐培养基至正常体积。感染24 h后,吸去含病毒的培养液,换上新鲜的完全培养液,继续37 ℃培养。48 h后,荧光显微镜下观察其绿色荧光的表达情况。加入嘌呤霉素进行筛选, 每48 h更换含嘌呤霉素的培养基, 至未被感染的细胞被嘌呤霉素杀光。继续加嘌呤霉素进行维持性筛选培养,连续筛选并传3代后,得到稳转细胞株WM451-NC、WM451- ST8Sia1。
1.2.3 实时荧光定量PCR(qRT-PCR)检测ST8Sia1 mRNA的表达水平将稳转细胞株WM451-NC、WM451- ST8Sia1分别接种于6 cm中皿培养24 h后,用TRIzol法提取总RNA,并测定RNA浓度和纯度。用逆转录试剂盒将RNA逆转录成cDNA,qRT-PCR检测细胞内ST8Sia1 mRNA表达水平,内参为GAPDH。反应体系(25 μL)为:2×SYBR Premix Ex Taq Ⅱ 12.5 μL, 正向引物1 μL (10 μmol·L-1),反向引物1 μL (10 μmol·L-1),模板DNA 2 μL,超纯H2O 8.5 μL。将以上反应物轻轻混匀后进入扩增程序,采用两步法qRT-PCR反应程序: 95 ℃ 30 s; 然后反复95 ℃ 5 s, 60 ℃ 30 s循环40次。熔解曲线分析为95 ℃ 15 s, 60 ℃ 1 min, 95 ℃ 15 s, 60 ℃ 15 s。采用相对定量法分析ST8Sia1的相对表达量, 以Folds=2-ΔΔCT表示待测组与对照组目的基因表达量的倍比关系。
1.2.4 Western blot检测ST8Sia1蛋白的表达水平将稳转细胞株WM451-NC(normal control)、WM451-ST8Sia1分别接种于6 cm中皿培养24 h后,提取总蛋白,用BCA法检测蛋白浓度。取等量蛋白(20 μg)通过聚丙烯酰胺凝胶电泳分离蛋白后,湿法转膜,10%脱脂牛奶摇床封闭1 h,剪膜。分别将含有目的蛋白ST8Sia1(47 ku)和内参蛋白GAPDH(36 ku)的PVDF膜放于相应的抗体中,4 ℃孵育过夜。TBST漂洗后,加入辣根过氧化物酶标记的IgG二抗室温孵育1 h。TBST漂洗,化学发光显影并拍照。
1.2.5 CCK-8法检测ST8Sia1过表达后细胞增殖分别将WM451-NC、WM451- ST8Sia1细胞以3×103每孔的密度种于96孔板中,待细胞贴壁后作为0 h,每孔加入含有10 μL CCK-8的培养液100 μL,培养箱孵育1 h后,检测每孔在450 nm波长处的吸光度, 连续检测4 d(24、48、72、96 h), 并绘制细胞生长曲线。
1.2.6 软琼脂糖法检测ST8Sia1过表达后细胞克隆形成能力配制0.7%软琼脂, 以每孔2 mL的量铺于6孔板,静置5 min,待其凝固。配制含有相应细胞悬液(3 000个左右)的0.35%软琼脂,以每孔1.5 mL的量铺于6孔板。4 ℃冰箱静置1~2 h凝固后,放入37 ℃培养箱,3~4周观察细胞克隆。
1.2.7 统计学方法实验数据用GraphPad Prism 7软件进行分析。实验数据用x±s表示, 组间比较采用单因素方差分析。研究数据均来自3次或3次以上独立实验。
2 结果 2.1 不同ST8Sia1过表达载体的构建及鉴定构建ST8Sia1-pEGFP-C1重组质粒,进行PCR鉴定(Fig 1A),并送测序公司测序(Fig 1B),结果表明ST8Sia1-pEGFP-C1重组质粒构建成功。构建ST8Sia1过表达慢病毒,进行PCR鉴定(Fig 2A),并送测序公司测序(Fig 2B),结果表明ST8Sia1过表达慢病毒构建成功。

|
| Fig 1 Identification results of ST8Sia1-pEGFP-C1 A: The PCR identification results of ST8Sia1-pEGFP-C1; B: The monoclonal sequencing results of ST8Sia1-pEGFP-C1 recombinant vector. |

|
| Fig 2 Identification results of ST8Sia1 over-expression lentiviral vector A: The PCR identification results of ST8Sia1 over-expression lentiviral vector; B: The monoclonal sequencing results of ST8Sia1 over-expression lentiviral vector. |
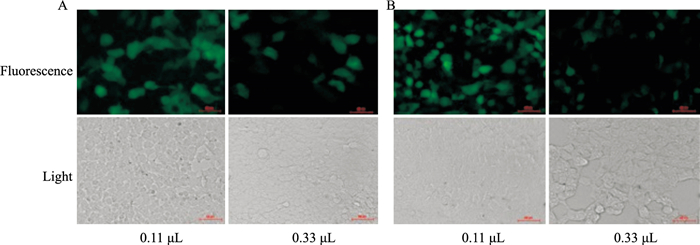
重组质粒载体和包装质粒共转染293T细胞,48 h后细胞出现融合现象,用荧光显微镜可观察到较强的绿色荧光,说明病毒包装成功。将病毒浓缩液梯度稀释后加入293T细胞,48 h后荧光显微镜下观察(Fig 3),荧光百分比在10%~30%的孔计算病毒滴度。滴度计算:对照组滴度=4×104×10%×感染复数(1)×病毒稀释倍数(30)×103=1×1011 TU·L-1;ST8Sia1滴度=4×104×10%×感染复数(1)×病毒稀释倍数(30) ×103=1×1011 TU·L-1。
|
| Fig 3 Calculation of ST8Sia1 over-expression lentivirus titer A: Expression of green fluorescent protein in 293T cells infected with different gradient dilution of empty lentivirus for 48 h; B: Expression of green fluorescent protein in 293T cells infected with different gradient dilution of ST8Sia1 overexpressed lentivirus for 48 h. |
不同ST8Sia1过表达载体转染WM451细胞48 h,在荧光显微镜下观察细胞内绿色荧光蛋白的表达。结果显示,ST8Sia1-pEGFP-C1过表达质粒组的绿色荧光蛋白表达水平远远低于慢病毒载体组(Fig 4),说明慢病毒载体的转染效率远高于ST8Sia1-pEGFP-C1过表达质粒。因此,选择ST8Sia1过表达慢病毒载体进行细胞转染实验。转染48 h后,加入嘌呤霉素进行筛选,得到稳定细胞株WM451-NC、WM451- ST8Sia1。

|
| Fig 4 Different ST8Sia1 over-expression vectors transfected into WM451 cells |
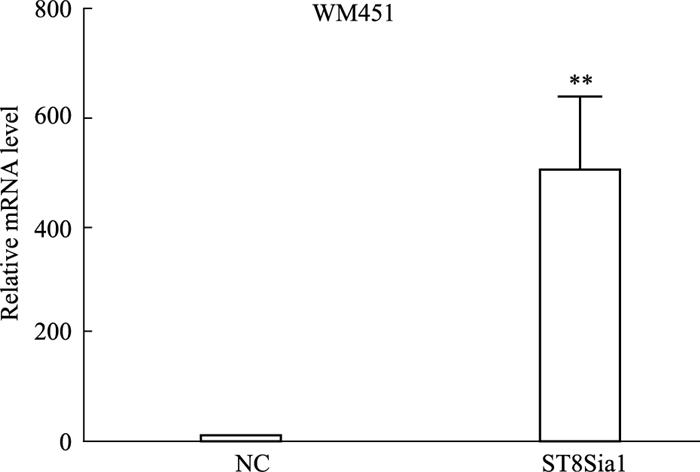
Fig 5的qRT-PCR结果显示,与空慢病毒载体组(NC)相比,ST8Sia1过表达慢病毒感染后,ST8Sia1 mRNA表达量明显提高(P<0.01)。另外, qRT-PCR的熔解曲线分析结果显示, ST8Sia1扩增产物的特异性良好, 40个扩增循环中没有引物二聚体的产生。
|
| Fig 5 Relative level of ST8Sia1 mRNA in WM451- NC cells and WM451- ST8Sia1 cells (x±s, n=3) **P < 0.01 vs NC group |
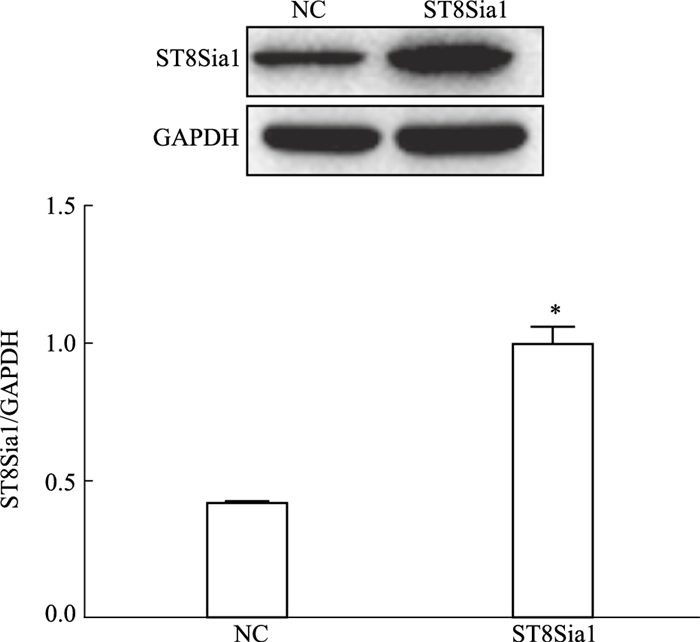
Fig 6的Western blot结果显示,与空慢病毒载体组(NC)相比,ST8Sia1过表达慢病毒感染后,ST8Sia1蛋白表达量明显提高(P<0.05)。
|
| Fig 6 Expression level ST8Sia1 protein in WM451- NC cells and WM451- ST8Sia1 cells (x±s, n=3) *P < 0.05 vs NC group |
CCK-8法检测ST8Sia1过表达后细胞增殖水平。结果表明,稳定过表达ST8Sia1的WM451细胞增殖速度明显高于正常对照(Fig 7)。说明ST8Sia1过表达可促进WM451细胞的增殖。

|
| Fig 7 Proliferation curve of WM451-NC cells and WM451- ST8Sia1 cells (x±s, n=3) *P < 0.05 vs NC group |
软琼脂糖法检测ST8Sia1过表达后细胞克隆形成能力。结果表明,与空白载体相比,稳定过表达ST8Sia1的WM451细胞克隆形成能力明显增加(Fig 8),说明ST8Sia1过表达可促进WM451细胞的克隆形成能力。

|
| Fig 8 Clony formation of WM451-NC cells and WM451- ST8Sia1 cells in soft agar |
目前,在细胞中基因过表达的载体包括非病毒载体和病毒载体, 病毒载体又包括慢病毒、腺病毒、逆转录病毒等。在此研究中,我们成功构建了两个新的普通质粒载体和慢病毒载体,并对它们的转染效率进行对比,发现慢病毒载体的转染效率远远高于普通质粒。因此,本研究选择ST8Sia1过表达慢病毒载体,进一步建立稳定转染ST8Sia1基因的细胞系。在20世纪90年代中期,各种病毒载体开始被应用于细胞转染。其中,慢病毒是以人类免疫缺陷型病毒(human immunodeficiency virus,HIV)为基础发展的基因治疗载体,与其他类型的病毒相比,慢病毒能够感染并整合到一些不分裂的细胞中,如巨噬细胞[8]。慢病毒载体可以将外源基因有效地整合到宿主染色体上,从而达到持久性表达。同时,慢病毒载体还具有安全性高的特点,并且能够有效感染多种细胞[9-10]。因此,利用慢病毒载体建立稳定高表达ST8Sia1的细胞株,为进一步研究ST8Sia1基因在肿瘤中的生物学功能奠定了基础。
ST8Sia1也被称为GD3s[5-6]。已有文献报道,GD3s在肿瘤中高表达。Yamashiro等[7]研究了GD3s在不同肿瘤细胞株的表达水平,发现GD3s在黑色素瘤细胞、成神经细胞瘤和胶质瘤中高表达。GD3s在雌激素受体阴性乳腺癌和三阴性乳腺癌中也高表达[11]。研究表明,GD3s不仅可以通过调节GD3和GD2,促进肿瘤的发展, 还可以通过多种机制,直接促进肿瘤的发生、发展、侵袭和迁移。Battula等[12]研究发现,GD3s能够调节上皮-间质转化, 从而促进乳腺癌细胞的侵袭和转移。抑制GD3s的表达可以降低乳腺癌干细胞的增殖,同时抑制其干细胞特性。Cazet等[13]发现,GD3s过表达可以诱导GD2和GD3在乳腺癌细胞MDA-MB-231细胞表面的累积,并且通过激活c-Met,进一步激活下游的MEK/ERK和PI3K/Akt信号通路,促进肿瘤细胞的增殖。GD3s还可以刺激黑色素瘤细胞增殖[14]。在黑色素瘤细胞SK-MEL-2中,NF-κB可以调控GD3s的转录活性,进而影响GD3的表达,起到肿瘤抑制的作用[15]。尽管对GD3s的功能和机制研究有一定的进展,但确切的机制仍不清楚。
本研究成功构建过表达ST8Sia1基因的两个不同载体,并对比不同载体在人黑色素瘤细胞WM451中的转染效率,挑选转染效率较高的慢病毒载体,建立了稳定高表达ST8Sia1的WM451细胞株,并在mRNA和蛋白质水平检测ST8Sia1的表达。结果显示,ST8Sia1过表达慢病毒感染后,WM451细胞的ST8Sia1 mRNA表达水平明显提高,约为对照组的500倍,而在蛋白水平仅为对照组的2倍。我们认为造成该现象的原因可能是因为基因转录和mRNA翻译是两个不同水平的过程。mRNA翻译为蛋白质是一个更为复杂的过程,受到了多种因素影响,例如mRNA的选择性剪接、翻译后修饰和蛋白质降解等,所以导致与基因mRNA表达水平发生不一致。随后,我们用获得的稳转细胞株检测了ST8Sia1过表达对黑色素瘤细胞增殖的影响,发现ST8Sia1过表达可以促进WM451细胞增殖和克隆形成。本研究为课题组进一步开展ST8Sia1基因在黑色素瘤中的功能和作用机制的研究,以及动物水平研究奠定了重要基础。
| [1] |
Bishop J M. Molecular themes in oncogenesis[J]. Cell, 1991, 64(2): 235-48. doi:10.1016/0092-8674(91)90636-D |
| [2] |
Weinberg R A. How cancer arises[J]. Sci Am, 1996, 275(3): 62-70. doi:10.1038/scientificamerican0996-62 |
| [3] |
纪玉婷, 杨燕, 郑荣生, 等. 慢病毒介导稳定高表达Cx32的Huh7细胞系建立及其对细胞增殖的影响[J]. 中国药理学通报, 2018, 34(2): 284-9. Ji Y T, Yang Y, Zheng R S, et al. Construction of lentiviral vector-mediated Cx32 stably over-expressed Huh7 cell line and its effect on cell proliferation[J]. Chin Pharmacol Bull, 2018, 34(2): 284-9. doi:10.3969/j.issn.1001-1978.2018.02.026 |
| [4] |
Azoury S C, Lange J R. Epidemiology, risk factors, prevention, and early detection of melanoma[J]. Surg Clin North Am, 2014, 94(5): 945-62. doi:10.1016/j.suc.2014.07.013 |
| [5] |
Takashima S, Matsumoto T, Tsujimoto M, et al. Effects of amino acid substitutions in the sialylmotifs on molecular expression and enzymatic activities of alpha2, 8-sialyltransferases ST8Sia-Ⅰ and ST8Sia-Ⅵ[J]. Glycobiology, 2013, 23: 603-12. doi:10.1093/glycob/cwt002 |
| [6] |
Rimoldi S, Papis E, Bernardini G, et al. Molecular cloning and expression of alpha2, 8-sialyltransferase (ST8Sia Ⅰ, GD3 synthase) in Xenopus[J]. Mol Cell Biochem, 2007, 301(1-2): 143-53. doi:10.1007/s11010-006-9406-1 |
| [7] |
Yamashiro S, Okada M, Haraguchi M, et al. Expression of alpha 2, 8-sialyltransferase (GD3 synthase) gene in human cancer cell lines: high level expression in melanomas and up-regulation in activated T lymphocytes[J]. Glycoconj J, 1995, 12(6): 894-900. doi:10.1007/BF00731251 |
| [8] |
Naldini L, Trono D, Verma I. Lentiviral vectors, two decades later[J]. Science, 2016, 353(6304): 1101-2. doi:10.1126/science.aah6192 |
| [9] |
de Bruyns A, Geiling B, Dankort D. Construction of modular lentiviral vectors for effective gene expression and knockdown[J]. Methods Mol Biol, 2016, 1448: 3-21. doi:10.1007/978-1-4939-3753-0 |
| [10] |
Tiscornia G, Singer O, Verma I. Design and cloning of lentiviral vectors expressing small interfering RNAs[J]. Nat Protoc, 2006, 1(1): 234-40. doi:10.1038/nprot.2006.36 |
| [11] |
Sarkar T, Battula V, Werden S, et al. GD3 synthase regulates epithelial-mesenchymal transition and metastasis in breast cancer[J]. Oncogene, 2015, 34(23): 2958-67. doi:10.1038/onc.2014.245 |
| [12] |
Battula V L, Shi Y, Evans K W, et al. Ganglioside GD2 identifies breast cancer stem cells and promotes tumorigenesis[J]. J Clin Invest, 2012, 122(6): 2066-78. doi:10.1172/JCI59735 |
| [13] |
Cazet A, Lefebvre J, Adriaenssens E, et al. GD3 synthase expression enhances proliferation and tumor growth of MDA-MB-231 breast cancer cells through c-Met activation[J]. Mol Cancer Res, 2010, 8(11): 1526-35. doi:10.1158/1541-7786.MCR-10-0302 |
| [14] |
Birkle S, Gao L, Zeng G, et al. Down-regulation of GD3 ganglioside and its O-acetylated derivative by stable transfection with antisense vector against GD3-synthase gene expression in hamster melanoma cells: effects on cellular growth, melanogenesis, and dendricity[J]. J Neurochem, 2000, 74(2): 547-54. |
| [15] |
Kang N Y, Kim C H, Kim K S, et al. Expression of the human CMP-NeuAc:GM3 alpha2, 8-sialyltransferase (GD3 synthase) gene through the NF-kappaB activation in human melanoma SK-MEL-2 cells[J]. Biochim Biophys Acta, 2007, 1769(11-12): 622-30. doi:10.1016/j.bbaexp.2007.08.001 |

