

2. 安徽省医学科学研究院药理毒理研究所,安徽 合肥 230061
2. Anhui Academy of Medical Sciences, Hefei 230061, China
糖尿病肾病(diabetic nephropathy, DN)是糖尿病患者最为易发的并发症之一,发病率为20%~40%,病程中伴随着复杂病理变化,细胞肥大、细胞外基质(extracellular matrix,ECM)的聚集引起肾小球基底膜与肾小管基底膜增厚,导致肾脏细胞的炎性和纤维化,进而导致肾脏组织整体的纤维化, 最终发展为终末期肾病,已成为糖尿病患者死亡的主要原因[1]。转化生长因子β1(transforming growth factor β1, TGF-β1)在慢性肾病中起着重要作用,并作为重要生物学标志物和主要治疗靶标逐渐被临床认可[2]。TGF-β1/Smads信号通路作为TGF-β1介导的重要信号通路,参与了DN众多进程,足细胞损伤、基底膜增厚、系膜细胞增生、肾细胞凋亡、上皮细胞间质转化等都有TGF-β1/Smads参与。除此之外,ECM中许多成分可以被TGF-β1/Smads信号通路刺激,进而发生ECM进行性积聚,最终导致肾脏组织纤维化[3]。
丹蛭降糖胶囊(Danzhijiangtang capsule,DZJT)是根据安徽中医药大学第一附属医院国家中医临床研究基地重点病种——糖尿病研究的经验方研制而成的院内制剂(皖药制字Z20090006),获得国家发明专利(专利号ZL200310112845.1),由太子参、地黄、丹皮、泽泻、菟丝子、水蛭等六味中药制成,具有益气、养阴、活血之功效,主治2型糖尿病及其慢性并发症之气虚阴亏血瘀症。前期研究表明,DZJT对糖尿病大鼠肾病有明显的防治作用[4],本研究观察DZJT对糖尿病大鼠肾脏TGF-β1/Smads信号通路的调控作用,并以此探讨DZJT对DN的防治作用和可能机制。
1 材料与方法 1.1 材料 1.1.1 实验动物清洁级3月龄健康♂SD大鼠,体质量(200±20)g,购自安徽省医学实验动物中心,合格证号:Scxk(皖)2013-002。大鼠分笼喂养,自由饮食,保持良好的通风环境,温度及湿度保持在适宜状态。
1.1.2 药物丹蛭降糖胶囊,安徽中医药大学第一附属医院制剂中心所制,太子参、地黄、牡丹皮、泽泻、菟丝子、水蛭六味中药重量比为5:4:4:3:2:5,干燥水蛭研细粉过100-120目筛灭菌备用,其余五味中药加水煎煮2~3次,每次1~2 h,合并煎液,滤过,浓缩,喷雾制粒,加入水蛭粉,混匀,装入胶囊,批号20131216;盐酸吡格列酮片,杭州中美华东制药有限公司,批号20130827。
1.1.3 试剂与仪器链脲佐菌素(streptozocin,STZ)(Sigma公司,批号:20130805427);尿素氮试剂盒(批号:0214041)、血肌酐试剂盒(批号:1114071)、尿蛋白检测试剂盒(批号:1114031),均购自四川Maccura生物科技股份有限公司;尿微量白蛋白放射免疫试剂盒(潍坊市三维诊断技术有限公司,批号:20140605);TGF-β1、Smad3、结缔组织生长因子(connective tissue growth factor,CTGF)抗体(美国Abcam公司);Smad2、Smad7抗体(美国Santa Cruz公司);β-actin抗体(Bioworld公司)。BX51型显微镜(日本Olympus公司);3K15型离心机(美国Sigma公司);FCM凝胶成像仪(美国Protein Simple公司)。
1.2 方法 1.2.1 模型的制备大鼠适应性喂养1周,100只SD♂大鼠中随机选取12只作为正常组,普通饲料喂养;其余大鼠给予高脂饲料(蛋白质14%、脂肪35%、碳水化合物51%)喂养,4周后,禁食12 h,参照本课题组的方法造模[5],以空腹血糖≥7.0 mmol·L-1并剔除血糖过高者(血糖测定仪显示为high)为糖尿病成模标准。
1.2.2 分组与给药成模大鼠65只,随机分为模型组、DZJT高、中、低剂量组(1 080、540、270 mg·kg-1)、吡格列酮(10 mg·kg-1)组,每天1次灌胃给药,连续给药8周,正常组与模型组给予等量溶媒。给药期间,由于打斗、灌胃等原因,大鼠死亡5只,其中模型组2只,DZJT高、中、低剂量组各1只。
1.2.3 血糖检测给药前及给药后第4周、8周,大鼠剪尾取血,测定随机血糖。末次给药后,腹主动脉取血,测定HbAlc。
1.2.4 肾功能检测末次给药后,收集大鼠24 h尿液,测定尿微量白蛋白(mAlb)、尿蛋白。取血测定血清血肌酐(serum creatinine,Scr)、尿素氮(blood urea nitrogen,BUN)、TGF-β1。
1.2.5 病理学检查取肾组织包埋切片,HE染色。200倍显微镜下,随机10个不重叠视野,根据发生病变肾小管(如肾小管的扩张或萎缩、间质扩张、炎细胞浸润或水肿等)所占总肾小管的比例进行评分:未发生病变为0分,<25%为1分,25%~50%为2分,>50%为3分,>75%为4分[4]。
1.2.6 TGF-β1/Smads信号通路蛋白检测采用Western blot法和免疫组织化学法对TGF-β1、Smad2、Smad3、Smad7、CTGF蛋白进行测定。免疫组化法:制片后200倍显微镜下观察,每组随机观察6个不重叠视野,采用Image-Pro Plus Version 6.0图像分析系统对图片进行半定量分析,各视野下阳性目标光密度和阳性面积百分比,即平均光密度(average optical density,AOD)代表蛋白的表达量。Western blot法:凝胶成像仪中曝光,采用Image-Pro Plus Version 6.0图像分析系统吸光度分析,以所测得的各指标的吸光度与内参照β-actin吸光度的比值代表定量值。
1.2.7 统计学分析采用SPSS 22.0统计学软件进行分析,数据以x±s表示,组间采用单因素方差分析ANOVA,两两比较采用LSD法。
2 结果 2.1 DZJT对大鼠血糖的影响Tab 1结果显示,模型组大鼠血糖(blood glucose,BG)、HbA1c明显高于正常组;给药第4周、8周,吡格列酮组、DZJT高、中、低剂量组大鼠BG、HbA1c明显下降(P<0.01,P<0.05)。
| Group | Dose/mg·kg-1 | BG/mmol·L-1 | HbA1c/% 8 weeks |
||
| 0 week | 4 weeks | 8 weeks | |||
| Normal | - | 5.33±0.54 | 4.97±0.63 | 5.62±0.57 | 5.73±1.03 |
| Model | - | 18.79±4.84** | 20.91±5.03** | 21.73±4.04** | 15.28±2.81** |
| DZJT | 1 080 | 18.82±4.59 | 15.54±2.31## | 14.92±2.42## | 10.23±2.21## |
| 540 | 18.31±3.89 | 17.01±2.51# | 16.96±2.71## | 13.02±2.19# | |
| 270 | 17.82±4.25 | 17.68±2.27# | 16.72±2.61## | 12.51±2.33# | |
| Pioglitazone | 10 | 18.87±4.24 | 13.70±2.54## | 12.72±1.93## | 9.13±2.21## |
| **P < 0.01 vs normal; #P < 0.05, ##P < 0.01 vs model | |||||
Tab 2结果显示,与正常组相比,给药8周后,模型组尿蛋白量、BUN、Scr、mAlb、TGF-β1水平明显升高(P<0.01);各给药组相较于模型组,尿蛋白量、BUN、Scr、mAlb、TGF-β1水平明显改善(P<0.01,P<0.05)。
| Group | Dose/mg·kg-1 | n | BUN/mmol·L-1 | Scr/μmol·L-1 | TGF-β1/ng·L-1 | mAlb/mg·24 h-1 | Protein/mg·24 h-1 |
| Normal | - | 12 | 5.8±1.9 | 66.9±9.2 | 11.6±1.2 | 0.06±0.02 | 4.1±2.9 |
| Model | - | 11 | 10.8±2.7** | 113.5±17.9** | 21.8±5.6** | 1.89±0.56** | 31.9±8.9** |
| DZJT | 1 080 | 12 | 7.9±1.9## | 92.7±14.6## | 15.9±4.0## | 0.59±0.20## | 14.4±5.7## |
| 540 | 12 | 8.2±2.1# | 89.6±11.7## | 18.3±3.0## | 0.63±0.20## | 16.1±7.9## | |
| 270 | 12 | 8.5±2.2# | 95.5±13.2# | 17.9±2.2## | 0.69±0.22## | 15.8±7.2## | |
| Pioglitazone | 10 | 13 | 8.0±1.8## | 87.3±11.6## | 15.2±1.7## | 0.52±0.17## | 10.5±6.5## |
| **P < 0.01 vs normal; #P < 0.05, ##P < 0.01 vs model | |||||||
如Fig 1所示,正常组大鼠未见肾损伤,其肾小球、肾小管结构完整,鲍曼氏囊结构完整,外缘清晰,未见炎性细胞浸润。模型组大鼠肾小球体积增大,细胞数增多,系膜区增宽,系膜细胞和系膜基质增多,肾小管上皮细胞出现坏死脱落、水肿、空泡变性,小管腔中有透明管型,病理评分明显上升(P<0.01)。与模型组相比,各给药组损伤均出现不同程度改善,病理评分值明显下降(P<0.05,P<0.01)。

|
| Fig 1 Effect of Danzhijiangtang capsule on pathology in renal tissues of rats (HE, ×200) A: Normal group; B: Model group; C: DZJT 1 080 mg·kg-1 group; D: DZJT 540 mg·kg-1 group; E: DZJT 270 mg·kg-1 group; F: Pioglitazone group; G: Pathological score of HE(x±s, n=10).**P < 0.01 vs normal; #P < 0.05, ##P < 0.01 vs model. |
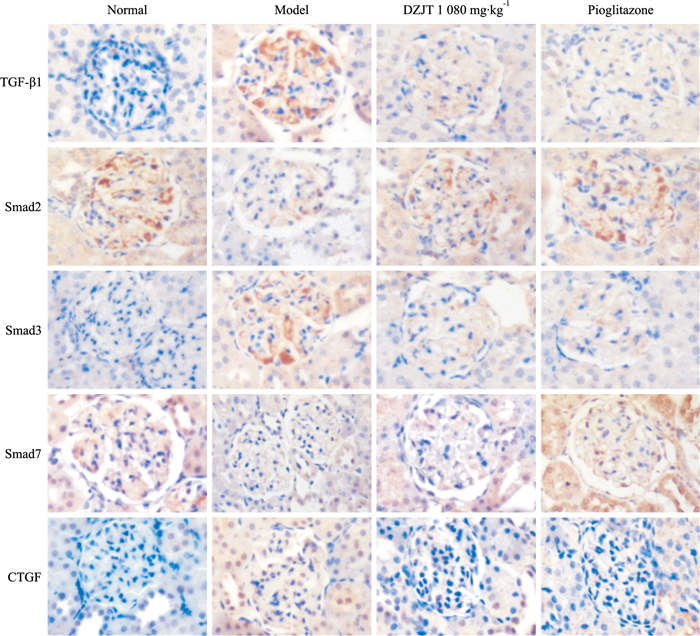
Tab 3、Fig 2结果表明,TGF-β1、Smad3、Smad2及Smad7在肾组织细胞胞质中表达,呈棕黄色块状或颗粒,CTGF在肾组织细胞核内表达,呈粒状。与正常组相比,模型组大鼠TGF-β1、Smad3、CTGF表达呈强阳性(P<0.01),而Smad2、Smad7表达减弱(P<0.01);与模型组相比,各给药组TGF-β1、Smad3、CTGF蛋白表达明显下降(P<0.01),Smad2、Smad7表达明显增加(P<0.01, P<0.05)。
| Group | Dose/mg·kg-1 | TGF-β1 | Smad2 | Smad3 | Smad7 | CTGF |
| Normal | - | 0.50±0.14 | 0.81±0.21 | 0.37±0.18 | 1.25±0.34 | 0.47±0.13 |
| Model | - | 1.82±0.61** | 0.24±0.09** | 0.93±0.37** | 0.25±0.11** | 1.93±0.52** |
| DZJT | 1 080 | 0.94±0.27## | 0.67±0.14## | 0.58±0.14## | 0.91±0.23## | 0.63±0.19## |
| 540 | 1.17±0.31## | 0.52±0.21## | 0.72±0.21## | 0.76±0.26## | 0.92±0.23## | |
| 270 | 1.42±0.33## | 0.33±0.11# | 0.79±0.28## | 0.48±0.21## | 1.32±0.47## | |
| Pioglitazone | 10 | 0.86±0.23## | 0.71±0.18## | 0.49±0.16## | 1.02±0.32## | 0.59±0.27## |
| **P < 0.01 vs normal; #P < 0.05, ##P < 0.01 vs model | ||||||
|
| Fig 2 Immunohistochemical expression of TGF-β1/Smads signaling pathway in renal tissues of rats (×200) |
由Fig 3可见,TGF-β1、Smad3、CTGF蛋白在模型组中表达明显高于正常组(P<0.01),Smad2、Smad7蛋白则与之相反(P<0.01)。各给药组TGF-β1、Smad3、CTGF蛋白表达相较于模型组则出现不同程度降低(P<0.01),Smad2、Smad7蛋白相较于模型组出现不同程度升高(P<0.01)。

|
| Fig 3 Western blot expression of TGF-β1/Smads signaling pathway in renal tissues of rats (x±s, n=5) 1:Normal group; 2: Model group; 3: DZJT 1 080 mg·kg-1 group; 4: DZJT 540 mg·kg-1 group; 5: DZJT 270 mg·kg-1 group; 6: Pioglitazone group.**P < 0.01 vs normal; ##P < 0.01 vs model. |
本实验采用造模方法为课题组多次实验摸索[4],以空腹血糖≥7.0 mmol·L-1并剔除血糖过高者(血糖测定仪显示为high)为成模标准,避免大鼠进食时间不统一造成的随机血糖值不稳定,无法真实反映其血糖水平的情况,并通过剔除过高血糖大鼠,避免胰岛过度损伤造成的大鼠实验中死亡。高脂喂养4周联合多次小剂量STZ(34 mg·kg-1)腹腔注射,既有较高的成模率,又避免了一次性大剂量STZ注射造成的高死亡率[6]。造模后,大鼠BG、HbAlc明显升高,且模型组在8周内一直维持较高水平,说明实验所用模型成功且稳定。治疗8周后,给药组大鼠较模型组大鼠BG、HbAlc明显降低,显示DZJT能有效改善模型大鼠的糖代谢。给药8周后,各给药组大鼠肾功能指标明显改善,肾脏病理也出现不同的改善,病理评分明显上升,显示DZJT能有效地改善STZ对大鼠造成的肾损伤。
TGF-β1在DN病程发展中参与多个环节,可调控多个影响DN病程的信号通路,在肾脏纤维化发展的进程中处于关键位置, 可指示慢性肾病病程,为主要治疗靶标[2]。无论是体内还是体外实验均显示,DN早期TGF-β1 mRNA及TGF-β1表达已有明显升高[7],而下调TGF-β1水平对四氧嘧啶或STZ诱导的DN模型均表现出一定的肾保护作用[8]。与文献报道相符,本次实验中,给药8周后模型组TGF-β1蛋白无论是在血清中,还是在肾组织中均明显升高,给药组较模型组则出现不同程度下降。
TGF-β1/Smads信号通路作为TGF-β1介导的重要信号通路,在肾脏纤维化中发挥着重要作用。当TGF-β1与其Ⅰ、Ⅱ型受体相结合形成三聚体后,会被下游Smad2和Smad3蛋白所识别[9],再将信号传递给Smad4,从而上调核内CTGF蛋白的表达,并刺激Smad7启动子转录增加[10]。单侧输尿管闭塞诱导的肾纤维化小鼠模型中,分别采用免疫组织化学法、Western blot法检测Smad3蛋白表达水平,均显示升高[11]。Smad3调节着肾脏纤维化,在体外,多种致纤维化因子均可以激活Smad3,基因敲除Smad3可以抑制小鼠和细胞纤维化[12]。本实验结果发现,模型组大鼠Smad3水平明显升高,给药8周后, 各给药组Smad3水平较模型组均有不同程度降低。CTGF作为TGF-β1/Smads信号通路下游蛋白,被认为可能是最终导致组织器官纤维化的关键因子,CTGF可介导细胞迁移、侵袭、血管发生和细胞凋亡的发生,并促进胶原及纤维连接蛋白等ECM的产生和沉积[13]。本实验中,两种检测手段均显示模型组CTGF表达明显升高,给药8周后, 各给药组CTGF水平较模型组均有不同程度降低,DZJT对肾脏的保护作用可能与其调节CTGF水平有关。Smad7蛋白启动子转录增加,表达上调,会竞争性地与TβR-Ⅰ结合,反馈性抑制Smad3磷酸化,并通过诱导NF-κB抑制剂α的表达,抑制NF-κB驱动的炎症反应[14]。本实验STZ诱导模型大鼠肾脏组织中,Smad7蛋白表达明显低于正常组,给药8周后, 各给药组Smad7水平较模型组均有不同程度升高,与文献报道一致。Smad2调控肾纤维化作用存在争议,文献报道,并非是Smad2调节着肾脏纤维化。虽然在体外多种致纤维化因子均可以激活Smad2,但基因敲除Smad2并未能有效抑制小鼠或细胞纤维化[15]。但亦有学者认为,肾脏损伤伴随着磷酸化Smad2表达的升高,磷酸化Smad2是肾脏损伤的指标性蛋白。本实验中,模型大鼠肾脏组织中Smad2蛋白表达明显低于正常组,给药8周后, 各给药组Smad2水平较模型组均有不同程度升高。Smad2在肾脏纤维化、肾脏损伤中究竟扮演着什么样的角色,还不能下结论,在以后的工作中,我们会继续对其研究。但不论Smad2起着什么样的作用,TGF-β1/Smads信号通路在肾脏纤维化中起着十分重要的作用是毋庸置疑的,DZJT对肾脏体现出的良好保护作用,其机制可能与影响TGF-β1/Smads信号通路及其下游CTGF表达有关。
( 致谢: 本研究在安徽中医药大学中西医结合临床学院药理学实验室完成,衷心感谢本课题组所有老师和同学的指导和帮助。)
| [1] |
贾会玉, 李中南, 陈光亮. 糖尿病肾病中转化生长因子β1/Sma和Mad相关蛋白信号通路的作用及其相关药物研究进展[J]. 中国药理学与毒理学杂志, 2016, 30(3): 266-71. Jia H Y, Li Z N, Chen G L. Effect of transforming growth factor beta 1/Sma-and Mad-related protein signal pathway in diabetic nephropathy and related drugs :a review[J]. Chin J Pharmacol Toxic, 2016, 30(3): 266-71. doi:10.3867/j.issn.1000-3002.2016.03.013 |
| [2] |
Hills C E, Squires P E. The role of TGF-β and epithelial-to mesenchymal transition in diabetic nephropathy[J]. Cytokine Growth Factor Rev, 2011, 22(3): 131-9. |
| [3] |
贾会玉, 李中南, 陈光亮, 等. 转化生长因子-β1介导的Smads和MAPKs信号通路在糖尿病肾病中的作用及其抑制剂研究进展[J]. 中国临床药理学与治疗学, 2015, 20(10): 1171-6. Jia H Y, Li Z N, Chen G L, et al. Role of Smads and MAPKs signaling pathway mediated by transforming growth factor beta 1 in diabetic nephropathy and its inhibitors[J]. Chin J Clin Pharmacol Ther, 2015, 20(10): 1171-6. |
| [4] |
贾会玉, 那莎, 李莉, 等. 丹蛭降糖胶囊对大鼠糖尿病肾病防治作用的研究[J]. 中华中医药杂志, 2016, 31(12): 5244-7. Jia H Y, Na S, Li L, et al. Study on preventive and therapeutic effect of Danzhi Jiangtang Capsule on rats with diabetic nephropathy[J]. Chin J Tradit Chin Med Pharm, 2016, 31(12): 5244-7. |
| [5] |
李莉, 陈光亮, 韩茹, 等. 多次低剂量链脲佐菌素诱导大鼠糖尿病模型的方法学研究[J]. 安徽医药, 2012, 16(7): 888-90. Li L, Chen G L, Han R, et al. Methodology research of rat diabetic model induced by streptozotocin several times[J]. Anhui Med Pharm J, 2012, 16(7): 888-90. doi:10.3969/j.issn.1009-6469.2012.07.006 |
| [6] |
左龙泉, 王欢, 汪应红, 等. 糖尿病高糖高脂对四氯化碳诱导的大鼠肝纤维化的作用研究[J]. 中国药理学通报, 2018, 34(4): 479-84. Zuo L Q, Wang H, Wang Y H, et al. Effect of diabetes on CCl4-induced rats liver fibrosis[J]. Chin Pharmacol Bull, 2018, 34(4): 479-84. doi:10.3969/j.issn.1001-1978.2018.04.009 |
| [7] |
Rawal S, Munasinghe P E, Nagesh P T, et al. Down-regulation of miR-15a/b accelerates fibrotic remodelling in the type 2 diabetic human and mouse heart[J]. Clin Sci(Lond), 2017, 131(9): 847-63. doi:10.1042/CS20160916 |
| [8] |
Abdel Aziz M A, Badary D M, Hussein M R A. Renal damage following Alloxan-induced diabetes is associated with generation of reactive oxygen species, alterations of p53, TGF-β1, and extracellular matrix metalloproteinases in rats[J]. Cell Biol Int, 2017, 41(5): 525-33. doi:10.1002/cbin.v41.5 |
| [9] |
Meng X M, Tang P M, Li J, et al. TGF-β/Smad signaling in renal fibrosis[J]. Front Physiol, 2015, 6(5): 82-9. |
| [10] |
Ying Q, Wu G. Molecular mechanisms involved in podocyte EMT and concomitant diabetic kidney diseases: an update[J]. Ren Fail, 2017, 39(1): 474-83. doi:10.1080/0886022X.2017.1313164 |
| [11] |
Bae K H, Seo J B, Jung Y A, et al. Lobeglitazone, a novel peroxisome proliferator-activated receptor γ agonist, attenuates renal fibrosis caused by unilateral ureteral obstruction in mice[J]. Endocrinol Metab, 2017, 32(1): 115-23. doi:10.3803/EnM.2017.32.1.115 |
| [12] |
Dai H Y, Zheng M, Lv L L, et al. The roles of connective tissue growth factor and integrin-linked kinase in high glucose-induced phenotypic alterations of podocytes[J]. J Cell Biochem, 2012, 113(1): 293-301. |
| [13] |
Sun L N, Chen Z X, Liu X C, et al. Curcumin ameliorates epithelial-to-mesenchymal transition of podocytes in vivo and in vitro via regulating caveolin-1[J]. Biomed Pharmacother, 2014, 68(8): 1079-88. doi:10.1016/j.biopha.2014.10.005 |
| [14] |
Bae E, Kim S J, Hong S, et al. Smad3 linker phosphorylation attenuates Smad3 transcriptional activity and TGF-β1/Smad3-induced epithelial-mesenchymal transition in renal epithelial cells[J]. Biochem Biophys Res Commun, 2012, 427(3): 593-9. doi:10.1016/j.bbrc.2012.09.103 |
| [15] |
沈豪, 郭霜, 刘秀芬, 等. TGF-β/Smads信号通路在姜黄素改善糖尿病大鼠心肌纤维化中的作用[J]. 中国药理学通报, 2018, 34(4): 522-7. Shen H, Guo S, Liu X F, et al. Curcumin ameliorates myocardial fibrosis via TGF-β/Smads signaling pathway in diabetic rats[J]. Chin Pharmacol Bull, 2018, 34(4): 522-7. doi:10.3969/j.issn.1001-1978.2018.04.017 |

