

吴成柱(1979-),男,博士,副教授,研究方向:药物化学,通讯作者,E-mail: wuchengzhu0611@foxmail.com
非小细胞性肺癌(non-small cell lung cancer,NSCLC)约占肺癌患者的80%,大多数患者发现时已处于晚期或中晚期,5年生存率不足10%,严重危害着人类健康和生命[1]。在过去较长时间内,以小分子靶向药物吉非替尼为代表的表皮生长因子受体酪氨酸激酶抑制剂(epidermal growth factor receptor tyrosine kinase inhibitor,EGFR-TKI),在NSCLC治疗中发挥重要作用。然而,随着化疗的推进,EGFR-TKI在表皮生长因子受体(epidermal growth factor receptor,EGFR)突变的NSCLC类型中不能发挥出很好的疗效,不可避免地出现获得性耐药,导致化疗失败[2]。因此,寻找更为低毒有效的化疗药物,成为当前NSCLC治疗研究的热点。
PI3K/Akt信号通路在肿瘤的发生、发展中发挥重要作用[3]。Akt作为该信号通路的关键蛋白,能够调节下游相关基因和分子,从而影响肿瘤细胞增殖、转移、凋亡等过程。大量研究表明,PI3K/Akt信号通路在许多肿瘤组织中持续活化,严重影响化疗的进行。因此,针对该信号通路的靶向抑制剂的研究已经成为了关注焦点,为抗肿瘤药物的研发提供新的思路。
从中草药中获得的天然产物,由于其结构复杂多样、毒性低,且具有多靶点、多途径的抗肿瘤活性,已经成为肿瘤药物研发的重要来源之一[4]。小白菊内酯(parthenolide,PTL)是从中草药小白菊(Chrysanthemum parthenium)中提取分离到的一种倍半萜内脂类化合物(结构见Fig 1A),可用于治疗头痛、风湿等疾病。近年来发现,PTL具有很强的抗肿瘤活性,能够抑制肿瘤细胞增殖,诱导肿瘤细胞凋亡等[5]。而关于PTL对EGFR突变型的NSCLC细胞株H1975的作用却未见报道。本研究以H1975细胞作为研究对象,观察PTL对其增殖、凋亡、侵袭、迁移等的影响,并探讨其相关的作用机制。
|
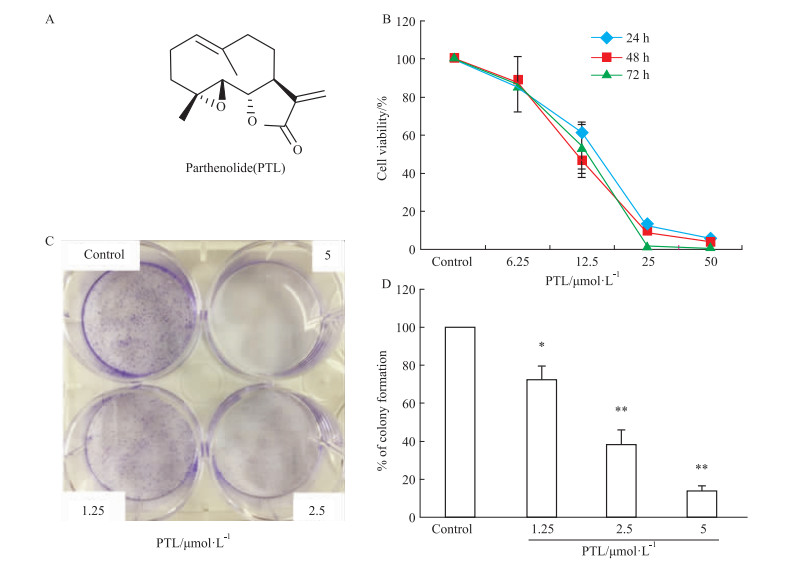
| Fig 1 Effects of PTL on proliferation of H1975 cells (x±s, n=3) A: The structure of PTL; B: Cytotoxic effect of PTL on H1975 cells for 24 h, 48 h, 72 h by MTT assay; C: Cell colonies significantly decreased with the increase of PTL concentration; D: Data analysis of C. *P < 0.05, **P < 0.01 vs control. |
PTL,由蚌埠医学院药物化学实验室提供,纯度为99.5%。RPMI 1640,购自HyClone公司;胎牛血清,购自浙江天杭生物科技有限公司;四甲基偶氮唑蓝(methyl thiazolyl tetrazolium,MTT),购自美国Sigma公司;结晶紫染液为碧云天公司产品;Transwell小室和基质胶(Matrigel),购自BD公司;Annexin V-FITC/PI试剂盒,购自贝博生物;β-actin、Bcl-2、Bax抗体,购自Proteintech公司;缺氧诱导因子1α(hypoxia inducible factor 1α,HIF-1α)、基质金属蛋白酶9(matrix metalloproteinase 9,MMP-9)抗体,购自Abcam公司;caspase-3、Akt、p-Akt(Ser473)抗体,购自CST公司。
1.1.2 细胞株EGFR突变型NSCLC细胞株H1975,购自上海细胞库。培养于含15%胎牛血清的RPMI 1640培养液中,在5% CO2、37 ℃以及饱和湿度的无菌培养箱中传代培养,取处于对数生长期的细胞进行实验。
1.1.3 仪器细胞培养箱(Thermo Scientific公司);倒置显微镜(OLYMPUS公司);流式细胞仪(BD公司);微量高速冷冻离心机(BECKMAN COULTER公司);酶标仪(BioTek公司);电泳仪、电泳槽及转移槽(Tanon公司);凝胶成像仪(Bio-Rad公司)。
1.2 MTT法检测PTL对细胞增殖的影响取处于对数生长期的H1975细胞,接种于96孔细胞培养板中,每孔1×104个细胞,培养24 h细胞贴壁后,更换含不同浓度PTL(6.25、12.5、25、50 μmol·L-1)的培养液,同时设阴性对照组和空白对照组,每组设3个复孔,分别培养24、48、72 h。待培养结束后,加入10 μL MTT(5 g·L-1),在37 ℃培养箱继续孵育4 h,弃上清,每孔加入100 μL DMSO,于37 ℃培养箱中孵育30 min,酶标仪上振荡20 s,以酶标仪检测波长490 nm处吸光度(A)值,计算细胞存活率。细胞存活率=(实验组A值-调零组A值)/(对照组A值-调零组A值)×100%。以上实验重复3次。
1.3 集落克隆形成实验将H1975细胞接种于6孔细胞培养板中,每孔1×104个细胞。培养24 h后,更换含不同浓度PTL(1.25、2.5、5 μmol·L-1)或等体积DMSO的新鲜培养液。置细胞培养箱中培养96 h后,预冷PBS洗2次,4%多聚甲醛固定15 min,弃固定液,然后加入结晶紫染液染色15 min,再用双蒸水洗去染液,室温下晾干,拍照。实验重复3次。
1.4 Annexin V-FITC/PI染色流式细胞仪检测细胞凋亡取生长良好的H1975细胞,接种于6孔板中,每孔3×105个细胞,继续培养24 h至细胞贴壁。然后更换含PTL(浓度为7.5、15、30 μmol·L-1)或等体积DMSO的新鲜培养液,置培养箱中作用24 h。作用结束后,收集细胞,1 500 r·min-1离心10 min,弃上清,加入预冷的Annexin V结合液重悬细胞,置冰浴,每管分别加入5 μL Annexin V-FITC染液和5 μL PI染液,避光染色20 min,上流式细胞仪检测分析。实验重复3次。
1.5 Transwell法检测细胞迁移取处于对数生长期的H1975细胞,胰酶消化收集细胞,再用PBS重悬细胞,洗去含血清的细胞培养液,接着用不含血清的RPMI 1640培养基重悬细胞,调整细胞浓度为2.5×108·L-1。小室上室为200 μL细胞悬液,即5×104个细胞,并加入不同浓度的PTL(0、1.25、2.5、5 μmol·L-1),将小室放置12孔板中。下室为800 μL含15%胎牛血清的RPMI 1640培养液。培养箱中继续培养24 h。作用结束后,小心吸去上室的细胞悬液,用4%多聚甲醛固定15 min,再用结晶紫染液染色15 min,然后将小室用PBS清洗2遍,棉棒小心擦去上室未迁移的细胞。倒置显微镜下随机选取3个视野,拍照(×200)保存,统计穿过微孔膜的细胞。以上实验重复3次。
1.6 Transwell法检测细胞侵袭取基质胶放于冰上融化,并用预冷的RPMI 1640培养基4 :1稀释。每个小室中加入45 μL基质胶,铺匀,放置培养箱中1~2 h。同迁移实验中处理细胞,调整细胞浓度为5×108·L-1,每个小室加入200 μL细胞悬液,即1×105个细胞。并加入不同浓度的PTL(终浓度0、1.25、2.5、5 μmol·L-1),作用时间为48 h。其余步骤同“1.5”。以上实验重复3次。
1.7 Western blot检测相关蛋白表达取处于对数生长期的H1975细胞,接种于6孔板中,每孔3×105个细胞,继续培养24 h至贴壁。按实验设计,更换含PTL(7.5、15、30 μmol·L-1)或等体积DMSO的新鲜培养液,继续作用24 h。作用结束后,收集细胞,2 500 r·min-1离心10 min,弃上清,每孔加入50 μL含蛋白酶抑制剂的RIPA裂解液,置冰上裂解30 min。4 ℃、12 000 r·min-1离心30 min,取上清,用BCA试剂盒进行蛋白定量。每组取50 μg蛋白进行SDS-PAGE电泳,转膜,封闭2 h,1×TBST洗3次,每次5 min,Bcl-2、Bax、caspase-3、Akt、p-Akt(Ser473)、HIF-1α、MMP-9一抗4 ℃孵育过夜,1×TBST洗3次,每次5 min,二抗室温孵育2 h,1×TBST洗3次,每次5 min,加入显影液,凝胶成像仪获取图像。实验重复3次。
1.8 统计学处理实验结果以x±s表示,采用SPSS 16.0统计软件进行方差分析及两样本均数t检验。
2 结果 2.1 PTL对H1975细胞的增殖抑制作用MTT结果显示,随着给药浓度的增加,PTL对H1975细胞的增殖抑制作用明显增加,其中PTL处理H1975细胞24、48、72 h的半数抑制浓度(IC50)分别为(15.83±0.35)μmol·L-1、(14.04±0.11)μmol·L-1、(14.05±0.21)μmol·L-1(Fig 1B)。同时,根据MTT实验结果,选取了低浓度的PTL(1.25、2.5、5 μmol·L-1)处理H1975细胞,观察到PTL能在低浓度明显抑制H1975细胞集落的形成(P < 0.05),见Fig 1C、1D。以上结果表明,天然产物PTL对NSCLC细胞系H1975具有较强的抑制增殖作用,且呈现浓度和时间依赖性。
2.2 PTL对H1975细胞凋亡的影响采用Annexin V-FITC/PI双染,流式细胞仪检测PTL对H1975细胞凋亡的影响。Fig 2结果显示,PTL(7.5、15、30 μmol·L-1)能明显诱导H1975细胞凋亡,凋亡率分别为(26.91±4.11)%、(41.43±6.36)%、(84.60±3.51)%,随着给药浓度的增加,凋亡比例逐渐升高,与对照组相比,差异具有统计学意义(P < 0.01)。

|
| Fig 2 Effect of PTL on apoptosis of H1975 cells (x±s, n=3) A: PTL induced apoptosis in H1975 cells by flow cytometry; B: With the increase of PTL concentration, cell apoptosis rate gradually increased. **P < 0.01 vs control. |
不同浓度的PTL处理H1975细胞24 h后,采用Western blot法检测Bcl-2、Bax、caspase-3蛋白表达的变化。Fig 3结果显示,PTL可促进H1975细胞中促凋亡蛋白Bax表达,而减少抑凋亡蛋白Bcl-2的表达,从而使Bax/Bcl-2的比例明显升高。caspase家族蛋白为凋亡的执行者,PTL能明显使caspase-3蛋白发生裂解,从而诱导细胞发生凋亡。

|
| Fig 3 Effects of PTL on expression level of Bcl-2, Bax, caspase-3 in H1975 cells by Western blot (x±s, n=3) *P < 0.05, **P < 0.01 vs control |
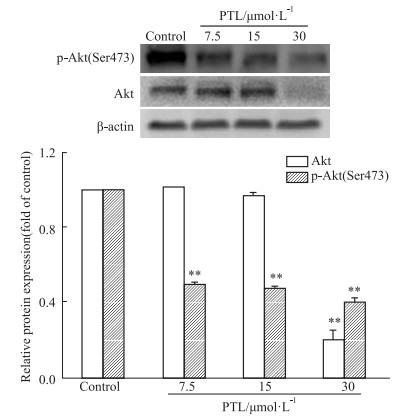
Akt作为肿瘤细胞内PI3K/Akt信号通路的关键蛋白,对肿瘤的生长、发展具有重要作用。Fig 4的Western blot结果显示,PTL能明显降低H1975细胞内Akt蛋白及p-Akt(Ser473)的表达(P < 0.01),从而抑制其信号通路的传导。
|
| Fig 4 Effects of PTL on expression levels of Akt, p-Akt (Ser473) in H1975 cells by Western blot (x±s, n=3) **P < 0.01 vs control |
采用Transwell小室法检测PTL对H1975细胞侵袭和迁移能力的影响,通过统计穿透到小室下方的相对细胞数目,可以反映出细胞侵袭和迁移能力的改变。Fig 5结果表明,PTL(1.25、2.5、5 μmol·L-1)能明显抑制H1975细胞向下侵袭浸润生长,其48 h抑制率分别为(57.62±7.40)%、(71.77±5.54)%、(82.26±1.50)%,相比于对照组,差异均具有统计学意义(P < 0.01)。迁移实验结果表明,PTL能有效降低H1975细胞迁移能力,PTL(1.25、2.5、5μmol·L-1)作用H1975细胞24 h后,抑制率分别为(47.87±2.33)%、(57.65±6.84)%、(74.28±4.02)%,与对照组相比差异有统计学意义(P < 0.01)。

|
| Fig 5 Effects of PTL on invasion and migration of H1975 cells by Transwell assay (×200) A: PTL significantly inhibited cell invasion and migration; B: Data analysis of A (x±s, n=3). **P < 0.01 vs control. |
Fig 6的Western blot结果显示,随着浓度的增加,PTL能明显降低H1975细胞中MMP-9及HIF-1α的表达(P < 0.05)。

|
| Fig 6 Effects of PTL on expression levels of HIF-1α, MMP-9 in H1975 cells by Western blot (x±s, n=3) *P < 0.05, **P < 0.01 vs control |
EGFR的激活与异常表达在肿瘤的发生、发展中有着重要作用。在过去较长的一段时间内,针对EGFR为特定靶点的小分子抑制剂成为了晚期NSCLC患者的首选。EGFR-TKI能特异性地抑制EGFR及其下游的信号通路,如PI3K/Akt,从而抑制肿瘤细胞生长增殖,诱导凋亡。但随着治疗的推进,患者大多会出现EGFR突变,继而产生耐药。其中,EGFR的20号外显子790位甲硫氨酸置换苏氨酸密码子的突变,即T790M突变,约占EGFR突变类型的50%~60%,是肿瘤对EGFR-TKI产生获得性耐药的重要原因[6]。本研究中,H1975细胞是T790M突变型NSCLC细胞株,因此,我们以其为研究对象,希望为NSCLC的治疗提供一定的研究基础。
我国中草药资源丰富,且几千年来形成了完整的中医理论,来指导中药的临床使用。对于肿瘤的治疗,中药有其独特的作用。中药中富含多种化学成分,已经成为抗肿瘤药物研发中发现先导化合物的重要来源。其中,以和厚朴酚、姜黄素、雷公藤甲素等为代表的天然产物,具有良好的抗肿瘤活性,包括抑制肿瘤细胞增殖,诱导肿瘤细胞凋亡,逆转肿瘤细胞耐药等[7-9],都已成为极具潜力的抗肿瘤新药。事实上,目前已上市的抗肿瘤药物大多也都来自天然产物,包括紫杉醇、喜树碱、长春新碱等。PTL作为一种天然产物,对多种肿瘤细胞具有很好的杀伤作用,但对于耐药NSCLC的研究未见报道,仍有较好的潜力,值得挖掘。
诱导肿瘤细胞发生凋亡是目前抗肿瘤药物研发的靶点之一。凋亡是细胞程序性死亡,在维持细胞增殖与死亡的平衡中发挥重要作用,Bcl-2家族蛋白具有调控细胞凋亡的功能,Bax/Bcl-2比值变化能够反映出细胞存活和凋亡的平衡关系。细胞发生凋亡也需要一些酶的作用,其中caspase扮演着重要角色,一直成为人们的研究热点,而caspase-3的激活更是被认为是细胞发生凋亡的早期标志[10]。本研究中,PTL能明显上调H1975细胞中促凋亡蛋白Bax水平,同时下调抑凋亡蛋白Bcl-2水平,Bax/Bcl-2比例明显升高,使caspase-3蛋白被激活,发生裂解,从而诱导H1975细胞发生凋亡。
Akt是肿瘤细胞重要信号通路PI3K/Akt中的关键分子,是整个PI3K/Akt信号通路转导的核心。Akt是一种丝氨酸/苏氨酸蛋白激酶,多种生长因子、信号蛋白等,均可通过磷酸化Thr308和Ser473位点激活Akt,磷酸化的Akt通过调节下游相关分子,对肿瘤细胞的增殖、凋亡等过程具有重要作用。研究表明,活化的Akt可以磷酸化Bcl-2家族中促凋亡蛋白Bad,引起Bad与其伴侣蛋白(chaperone 14-3-3)结合,阻断Bad蛋白的促凋亡功能,并激活下游分子Bcl-2释放,从而抑制肿瘤细胞凋亡,也可直接磷酸化Bax蛋白,阻断其促凋亡作用[11]。另外,caspase级联反应是凋亡发生的主要原因,其中,caspase-3作为凋亡的执行者,具有不可替代的作用,同样,Akt可磷酸化下游caspase-3、caspase-9等家族蛋白,使其失活,抑制其促凋亡作用[12]。本研究Western blot结果表明,PTL能明显降低H1975细胞内Akt、p-Akt(Ser473)蛋白水平,有效抑制Akt蛋白的活化,从而抑制其下游信号通路的转导,发挥促凋亡作用。
同时,大量研究表明,PI3K/Akt信号通路在肿瘤细胞转移过程中也有着重要的作用。通过PI3K/Akt信号通路激活Akt,活化的Akt可通过下游的雷帕霉素靶蛋白(mammalian target of rapamycin,mTOR),直接激活下游的HIF-1α,启动血管内皮生长因子(vascular endothelial growth factor,VEGF)基因的转录,促进VEGF蛋白生成,增加肿瘤组织血供,促进肿瘤细胞转移[13]。此外,活化的Akt能上调基质金属蛋白酶(matrix metalloproteinases,MMPs)的表达,特别是上调MMP-2、MMP-9 mRNA和蛋白水平,参与细胞外基质的降解,促进肿瘤细胞侵袭和迁移[14]。本研究Transwell实验结果显示,PTL能明显抑制H1975细胞侵袭和迁移,同时Western blot实验结果表明,PTL能明显下调H1975细胞HIF-1α和MMP-9的表达,从而抑制H1975细胞发生转移。
综上所述,天然产物PTL能明显诱导NSCLC细胞株H1975发生凋亡,同时抑制其侵袭和迁移,机制可能与PI3K/Akt信号通路中关键分子Akt被抑制有关,从而调节下游靶蛋白Bcl-2、Bax、caspase-3、HIF-1α及MMP-9的表达,发挥抗肿瘤作用。本研究为天然产物PTL的临床使用提供了一定的实验基础,但是作为有潜力的抗肿瘤新药,其体内的抗肿瘤作用及相应的毒副作用仍需要进一步研究。
| [1] |
Jemal A, Siegel R, Xu J, et al. Cancer statistics, 2010[J]. CA Cancer J Clin, 2010, 60(5): 277-300. doi:10.3322/caac.20073 |
| [2] |
Lu X, Yu L, Zhang Z, et al. Targeting EGFR (L858R/T790M) and EGFR (L858R/T790M/C797S) resistance mutations in NSCLC: current developments in medicinal chemistry[J]. Med Res Rev, 2018, 38(5): 1550-81. doi:10.1002/med.2018.38.issue-5 |
| [3] |
Hanahan D, Weinberg R A. Hallmarks of cancer: the next generation[J]. Cell, 2011, 144(5): 646-74. doi:10.1016/j.cell.2011.02.013 |
| [4] |
Stone R. Biochemistry. Lifting the veil on traditional Chinese medicine [J]. Science, 2008, 319(5864): 709-10.
|
| [5] |
Liu Y C, Kim S L, Park Y R, et al. Parthenolide promotes apoptotic cell death and inhibits the migration and invasion of SW620 cells[J]. Intest Res, 2017, 15(2): 174-81. doi:10.5217/ir.2017.15.2.174 |
| [6] |
于芹, 姜达, 李颖. T790M突变的非小细胞肺癌研究现状与前景[J]. 中国肺癌杂志, 2017, 20(3): 199-204. Yu Q, Jiang D, Li Y. Current status and prospect of T790M mutation in non-small cell lung cancer[J]. Chin J Lung Cancer, 2017, 20(3): 199-204. |
| [7] |
Dai X, Li R Z, Jiang Z B, et al. Honokiol inhibits proliferation, invasion and induces apoptosis through targeting Lyn kinase in human lung adenocarcinoma cells[J]. Front Pharmacol, 2018, 9: 558. doi:10.3389/fphar.2018.00558 |
| [8] |
任海玉, 孙剑经, 李多, 等. 姜黄素通过Wnt2/β-catenin通路逆转食管癌Eca-109/VCR细胞多药耐药性研究[J]. 中国药理学通报, 2018, 34(10): 1455-60. Ren H Y, Sun J J, Li D, et al. Curcumin reversed multi-drug resistance of esophageal carcinoma in Eca-109/VCR cell line through Wnt2/β-catenin pathway[J]. Chin Pharmacol Bull, 2018, 34(10): 1455-60. doi:10.3969/j.issn.1001-1978.2018.10.025 |
| [9] |
赵林, 吴鹏, 章平贵, 等. 雷公藤甲素对人结肠癌HCT116细胞增殖、自噬和凋亡的影响[J]. 中国药理学通报, 2016, 32(10): 1399-404. Zhao L, Wu P, Zhang P G, et al. Effect of triptolide on human colorectal cancer HCT116 cell proliferation, autophagy and apoptosis[J]. Chin Pharmacol Bull, 2016, 32(10): 1399-404. doi:10.3969/j.issn.1001-1978.2016.10.014 |
| [10] |
Ye Y T, Zhong W, Sun P, et al. Apoptosis induced by the methanol extract of Salvia miltiorrhiza Bunge in non-small cell lung cancer through PTEN-mediated inhibition of PI3K/Akt pathway[J]. J Ethnopharmacol, 2017, 200: 107-16. doi:10.1016/j.jep.2016.12.051 |
| [11] |
Yang J, Zou Y, Jiang D. Honokiol suppresses proliferation and induces apoptosis via regulation of the miR21/PTEN/PI3K/AKT signaling pathway in human osteosarcoma cells[J]. Int J Mol Med, 2018, 41(4): 1845-54. |
| [12] |
Kumar D, Haldar S, Gorain M, et al. Epoxyazadiradione suppresses breast tumor growth through mitochondrial depolarization and caspase-dependent apoptosis by targeting PI3K/Akt pathway[J]. BMC Cancer, 2018, 18(1): 52. doi:10.1186/s12885-017-3876-2 |
| [13] |
Kitajima Y, Miyazaki K. The critical impact of HIF-1α on gastric cancer biology[J]. Cancers (Basel), 2013, 5(1): 15-26. |
| [14] |
Cheng T C, Din Z H, Su J H, et al. Sinulariolide suppresses cell migration and invasion by inhibiting matrix metalloproteinase-2/-9 and urokinase through the PI3K/AKT/mTOR signaling pathway in human bladder cancer cells[J]. Mar Drugs, 2017, 15(8): E238. doi:10.3390/md15080238 |

