

2. 中国医学科学院神经科学中心,中国医学科学院北京协和医学院药物研究所,天然药物活性物质与功能国家重点实验室,北京 100050;
3. 湖南省中药饮片标准化与功能工程技术中心,湖南 长沙 410208
2. State Key Lab of Bioactive Substances and Functions of Natural Medicines, Institute of Materia Medica, Neuroscience Center, Chinese Academy of Medical Sciences and Peking Union Medical College, Beijing 100050, China;
3. Hunan Engineering Technology Center of Standardization and Function of Chinese Herbal Decoction Pieces, Changsha 410208, China
帕金森病(Parkinson's disease,PD)是常见的神经退行性疾病,据统计,我国65岁以上PD患病率高达1.7%,PD患者约为300万。随着社会的发展,人口老龄化现象越来越严重,PD患者人数可能还会持续增多。PD的主要病理改变是中脑黑质多巴胺(dopamine, DA)能神经元的变性死亡、纹状体中DA含量的明显减少,以及黑质残存神经元的胞质内出现嗜酸性包涵体。目前,临床上治疗PD疗效最好、最常用的治疗手段是服用左旋多巴作为DA的补充剂。但是左旋多巴治疗并不能从PD的发病机制上逆转PD的发生,也不能有效延缓PD的病程。长时间服用左旋多巴会引发恶心、厌食、药效波动等一系列的副作用,甚至在疾病的晚期,由于药物抵抗,会加剧和恶化患者的运动障碍,严重影响了病人顺从性和生活质量, 且服用时间越长,则毒副反应越明显、越重[1]。
瓜子金(Polygala japonica Houtt)是远志科远志属植物, 别名瓜子草、小远志、银不换,为多年生草本,主要生长在我国的南方各省。瓜子金常作为民间用药,药用其根或全草, 具有散郁助眠、益智安神、解毒消肿等功效,常用作治疗咽喉肿痛、失眠心悸、毒蛇咬伤等。瓜子金皂苷己(polygalasaponin F,PS-F)是从瓜子金中提取的齐墩果烷型三萜皂苷类化合物。前期实验室研究发现,PS-F可以通过维持线粒体功能及抑制caspase-3的激活,对MPP+诱导的PC12细胞凋亡起保护作用[2];还能通过抑制NF-κB通路的激活及减少p38的磷酸化水平,减少炎性因子肿瘤坏死因子α(tumor necrosis factor α,TNF-α)、诱导型一氧化氮合酶(inducible nitric oxide synthase, iNOS)、NO的表达量,缓解神经炎症的发生[3]。本实验在前期研究基础上,重点探究PS-F对脂多糖(lipopolysaccharide, LPS)神经炎症模型中IL-1β释放的影响及其作用机制,为瓜子金用于临床治疗PD提供一定的理论基础。
1 材料与方法 1.1 细胞株与试剂BV2细胞为永生化小鼠小胶质细胞系,购自中国医学科学院基础医学细胞中心,由本实验室传代并保存。DMEM/F12培养基、胎牛血清,均购自Gibco公司;LPS、多聚赖氨酸、DMSO、β-actin抗体,购自Sigma公司;BCA蛋白定量试剂盒、ECL超敏发光液,购自北京普利莱生物技术有限公司;caspase-1抗体、ASC抗体,购自Santa Cruz公司;caspase-11抗体、IL-1β抗体、NLRP3抗体,购自Abcam公司;ELISA试剂盒由R & D公司提供。
1.2 仪器ThermoForma 3110型二氧化碳培养箱(美国Thermo公司);Spectra Max 190酶标仪(美国BD公司);LAS-3000型化学发光成像分析系统(日本Fujifilm公司);蛋白电泳仪(北京六一仪器厂);PCR反应仪(Eppendorf公司)。
1.3 细胞培养与实验分组BV2细胞用含10%胎牛血清和链霉素100 mg·L-1的DMEM/F12培养基,置于5% CO2、37 ℃恒温培养箱中常规培养,每隔2~3 d进行传代,选取对数生长期、状态优良的细胞进行实验。实验分为对照组(加DMEM/F12)、LPS模型组(1 μg·L-1 LPS孵育12 h)、LPS+低、中、高剂量PS-F组[1 μg·L-1 LPS+PS-F(0.10、1.00、10.00 μmol·L-1)]。
1.4 Western blot检测蛋白表达选取对数生长期、状态优良的BV2细胞,按1×109·L-1接种于用多聚赖氨酸预处理的6孔板中,每孔2 mL,分组同“1.3”。当细胞贴壁长满70%~80%时,弃掉旧培养基,各组加入混有相应试剂的培养基之后继续培养12 h。待处理结束后,收集细胞,用预冷的PBS洗3遍,加入细胞裂解液,冰浴中裂解30 min后,4 ℃、12 000 r·min-1离心30 min。BCA蛋白定量,蛋白样品加相应体积的4×Loading buffer煮沸变性。蛋白经10% SDS-PAGE电泳分离后,湿法转至PVDF膜,3% BSA室温封闭2 h,分别加入IL-1β、NLRP3、caspase-1、ASC、caspase-11的抗体,4 ℃过夜,TBS洗膜后,加入辣根过氧化物酶标记的二抗,室温孵育2 h,洗膜后,加入ECL液,进行检测。
1.5 qPCR检测mRNA的表达分别收集上述各组细胞,用TRIzol提取细胞的总RNA,采用分光光度仪对提取的RNA进行定量,按照逆转录试剂盒说明书加入相应的试剂,逆转录合成cDNA,以cDNA为模板进行实时定量PCR检测。在NCBI GenBank数据库中查询IL-1β,利用Premier 5.0设计荧光PCR引物,引物序列为F:5′-GTGGCAGCTACCTGTGTCTT-3′,R:5′-GGAGCCTGTAGTGCAGTTGT-3′。反应条件为:95 ℃预变性2 min,95 ℃变性10 s、59 ℃退火30 s, 72 ℃延长30 s, 扩增40个循环。待反应结束后,结合扩增曲线及熔解曲线分析,选择符合要求的原始数据,用GAPDH为内参校正,根据循环次数,计算2-ΔΔCT值。
1.6 ELISA法检测炎性因子IL-1β的释放情况收集各组经12 h刺激后的培养液上清,根据ELISA试剂盒说明书的具体操作步骤,检测各组IL-1β释放的情况。在酶标仪450 nm波长处检测吸光度值,由标准品的吸光度值与相对应的浓度得到直线回归方程,并由此计算出各组细胞培养液上清中IL-1β的浓度。
1.7 统计学方法所有数据均以x±s表示, 实验结果至少重复3次。采用Graphpad Prism 5软件对数据进行单因素方差分析与t检验。
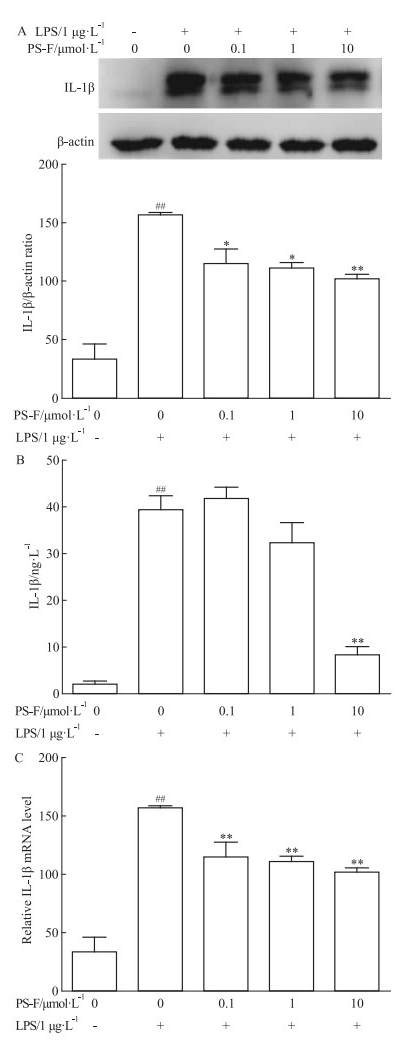
2 结果 2.1 PS-F对IL-1β蛋白表达、释放及mRNA水平的影响Western blot结果显示(Fig 1A),与对照组相比,LPS模型组IL-1β的表达量明显升高(P < 0.05);与模型组相比,PS-F低、中、高剂量组中IL-1β表达量呈浓度依赖性降低(P < 0.05, P < 0.01)。PS-F对释放到培养基中IL-1β的影响如Fig 1B所示,与对照组相比,LPS模型组释放到培养基上清的IL-1β含量升高(P < 0.01);与模型组相比,PS-F中、高剂量组的IL-1β释放量降低,且高剂量组差异有统计学意义(P < 0.01)。IL-1β mRNA的检测结果如Fig 1C所示,与Western blot结果基本一致,与对照组相比,LPS模型组IL-1β mRNA的表达明显升高(P < 0.01);与模型组相比,PS-F低、中、高剂量组呈浓度依赖性降低IL-1β mRNA(P < 0.01)。
|
| Fig 1 Effects of PS-F on IL-1β expression by Westernblot(A), ELISA(B) and qPCR(C)(x±s, n=3) ##P < 0.01 vs control group; *P < 0.05, **P < 0.01 vs LPS model group |
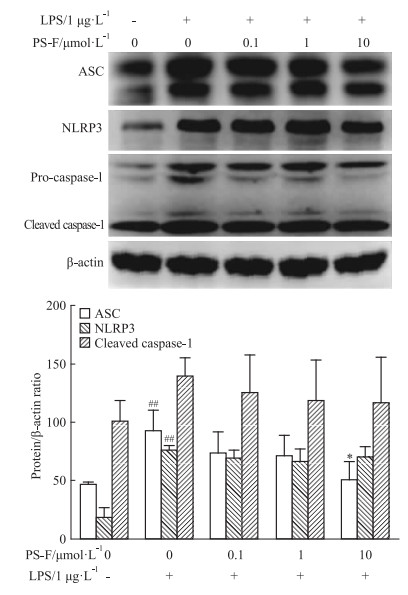
Fig 2的Western blot结果显示,与对照组相比,LPS模型组中NLRP3、caspase-1和ASC的表达量升高,其中ASC、NLRP3的差异有显著性(P < 0.01);与模型组相比,其表达量在PS-F低、中、高剂量组有一定的降低,且ASC的表达量在高剂量组中差异有显著性(P < 0.05)。
|
| Fig 2 Effects of PS-F on expressions of NLRP3, ASC, caspase-1 proteins(x±s, n=3) ##P < 0.01 vs control group; *P < 0.05 vs LPS model group |
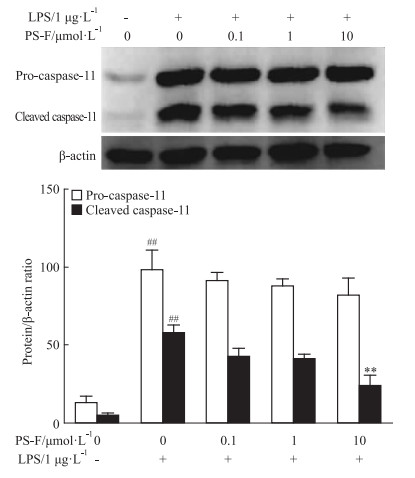
如Fig 3所示,与对照组相比,LPS模型组caspase-11的表达量明显升高(P < 0.01);与模型组相比,PS-F高剂量组明显降低caspase-11的表达(P < 0.01)。
|
| Fig 3 Effects of PS-F on expressionof caspase-11 proteins(x±s, n=3) ##P < 0.01 vs control group; **P < 0.01 vs LPS model group |
炎症是机体对外界刺激的一种防御反应,炎症的发生与多种疾病的发生、发展关系密切,与神经系统疾患关系最为密切的炎症反应为神经炎症。炎症反应是机体抵御感染与损伤复杂的级联过程,脑内发生的神经炎症与多种急慢性神经退行性疾病的发生发展有着密切关联。近年来,研究表明,神经炎症与PD的病程发展有着重要的联系[4]。小胶质细胞是脑内的固有免疫细胞,当脑部受到损伤与感染时,小胶质细胞被迅速激活,并伴随着大量炎性因子的释放,其中包括IL-1β[5]。PD是仅次于阿尔茨海默症(Alzheimer's disease,AD)的第2大神经退行性疾病,多发于老年人,男性发病率高于女性。随着人口老龄化的加剧,PD患者数量持续增加,严重影响了人们的生活质量,也加重了社会的经济负担。近年来,以神经炎症作为切入点,阐明PD病程的具体机制与开发神经保护作用的药物成为了研究的热点,希望通过控制PD发生、发展过程中的炎症反应,实现预防与治疗PD的效果。神经炎症是中枢神经系统的固有免疫应答反应,具有吞噬作用的小胶质细胞充当着外周巨噬细胞样的功能,是中枢神经系统中的第一道,也是最主要的免疫防线。在正常成年大脑中,小胶质细胞处于静息状态,当脑组织受到各种病理因素的损伤与刺激时,小胶质细胞转化为激活状态,迅速迁移到损伤部位,对死亡的细胞与组织碎片进行吞噬,释放出生长因子,促进组织修复。因此,对小胶质细胞的适度激活,能够促进神经损伤的恢复,起到神经保护作用,但神经炎症的过量发生,会导致大量炎性因子TNF-α、IL-1β等的释放,进而加重神经元的损伤甚至死亡[6-7]。
LPS也称内毒素,是革兰阴性菌细胞外壁的成分之一,是常用的小胶质细胞激活剂,本实验用LPS刺激小胶质细胞构建神经炎症模型。我们前期研究发现[8],PS-F能够明显减少LPS诱导的小胶质细胞中TNF-α、NO、iNOS表达量的增加,那么PS-F对炎性因子IL-1β的释放是否也有一定的影响呢?本研究围绕PS-F对神经炎症模型中IL-1β释放的影响及其具体作用机制展开。首先,检测了LPS模型与PS-F高、中、低3个剂量组中IL-1β的蛋白表达量及mRNA的水平,Western blot、ELISA、qPCR 3种不同的实验方法得出一致结果,其中Western blot、qPCR结果表明,在LPS神经炎症模型中,IL-1β的释放量较对照组明显增多,这与相关文献报道所得结果一致[9-10],PS-F高、中、低剂量组IL-1β较模型组明显减少。由此证实,PS-F通过抑制炎性因子IL-1β的释放,降低炎症反应,从而发挥神经保护作用。接下来,对PS-F抑制IL-1β释放的具体机制展开研究。
炎性因子IL-1β的释放是细胞内信号的级联反应过程,与多种促炎信号转导途径有着密切关联,在细胞内,有一种“炎性体”的多分子复合物调控IL-1β的分泌与合成。在探究PS-F减少LPS神经炎症模型中IL-1β合成与分泌,发挥抗神经炎症的具体作用机制实验中,我们针对“炎性小体”展开了一系列的检测。“炎性体”复合物主要存在于激活的免疫细胞中,介导含半胱氨酸的天冬氨酸蛋白水解酶caspase的激活,进而引起促炎因子IL-18、IL-1β的释放与宿主细胞的焦亡。炎性体可分为经典的炎性体与非经典的炎性体两大类。经典的炎性体由胞质内的模式识别受体(PRR)、caspase和衔接蛋白(apoptosis-associated specklike protein, ASC)三部分组成,它们由模式识别受体直接识别信号[11]。识别受体大致分为NLR家族与PYHIN家族,其中NLRP3炎性小体与PD的发生与发展有着重要关系。NLRP3炎性体由NLRP3识别受体、效应蛋白caspase-1以及接头蛋白ASC三部分组成。当NLRP3被激活时,首先发生NLRP3的寡聚化,接下来寡聚化的NLRP3会招募接头蛋白ASC,再之后,与NLRP3结合的ASC会招募半胱天冬酶原(pro-caspase-1), 完成炎性小体的组装。炎性小体组装完成之后,会引起pro-caspase-1蛋白的裂解,生成活化的caspase-1,caspase-1又会切割IL-1β前体(pro-interleukin-1 beta, pro-IL-1β),使其转变为成熟的IL-1β[12]。本研究发现,LPS神经炎症模型中,NLRP3、caspase-1、ASC蛋白的表达量较空白组均增加,其表达量在PS-F给药组均有所下调,特别是接头蛋白ASC的表达量在高剂量PS-F的干预下,较模型组明显减少。提示PS-F可能通过抑制NLRP3炎性复合体的激活,进而减少炎性因子IL-1β的释放。
除了经典的炎性体,还有一类非经典的炎性体,非经典的炎性体由含半胱氨酸的天冬氨酸蛋白水解酶11(caspase-11)对信号进行识别并介导,不依赖于传统的炎性体激活剂[13]。本研究除了检测经典的NLRP3炎性小体在PS-F干预下的变化情况,还检测了非经典炎性体中caspase-11的蛋白含量在各组中的表达。非经典的炎性体是由前体caspase-11(pro-caspase-11)与LPS结合组成的复合物。pro-caspase-11可以与LPS直接结合,当细胞受到胞内LPS的刺激时,迅速发生寡聚化,产生有活性的caspase-11,之后调节炎性因子IL-1β的释放[14]。这一具体过程尚未完全明确,现有的研究还表明,caspase-11可以影响经典的NLRP3炎性体的激活,由此可以明确caspase-11对炎症发生的整个过程至关重要。本实验结果显示,LPS诱导的BV2炎症模型中,pro-caspase-11和caspase-11的表达量较空白组均增多,PS-F干预组的表达均有所下降,特别是caspase-11在高剂量PS-F的干预下,表达量明显减少。由此得出结论,PS-F抑制神经炎症,减少LPS诱导的IL-1β分泌增加,也通过非经典的炎性体caspase-11途径发挥作用。
综上所述,本实验证实了PS-F能够有效减少LPS刺激BV2小胶质细胞引发的炎症因子IL-1β的释放,并证实这一过程是通过下调经典的炎性体NLRP3与抑制非经典的炎性体caspase-11的激活而实现的。
| [1] |
闫文芬, 衡洋, 邵千航, 等. 建立以α-突触核蛋白损伤为靶点的细胞筛选模型[J]. 中国药理学通报, 2015, 31(4): 586-90. Yan W F, Heng Y, Shao Q H, et al. Construction of cell model targeted on the damage by α-synuclein[J]. Chin Pharmacol Bull, 2015, 31(4): 586-90. doi:10.3969/j.issn.1001-1978.2015.04.029 |
| [2] |
吴苗苗, 苑玉和, 胡金凤, 等. 瓜子金皂苷己对MPP+诱导PC12细胞凋亡的保护作用[J]. 中国药理学通报, 2012, 28(4): 473-7. Wu M M, Yuan Y H, Hu J F, et al. The protective effect of polygalasaponin F against MPP+ induced PC12 cellular apoptosis[J]. Chin Pharmacol Bull, 2012, 28(4): 473-7. doi:10.3969/j.issn.1001-1978.2012.04.008 |
| [3] |
Wei W, Yuan Y H, Gao Y N, et al. Polygalasaponin F inhibits secretion of inflammatory cytokines via NF-κB pathway regulation[J]. J Asian Nat Prod Res, 2014, 16(8): 865-75. doi:10.1080/10286020.2014.918962 |
| [4] |
Anderson F L, Coffey M M, Berwin B L, et al. Inflammasomes: an emerging mechanism translating environmental toxicant exposure into neuroinflammation in Parkinson's disease[J]. Toxicol Sci, 2018, 166(1): 3-15. |
| [5] |
Wang Q, Liu Y, Zhou J. Neuroinflammation in Parkinson's disease and its potential as therapeutic target[J]. Transl Neurodegener, 2015, 4: 19. doi:10.1186/s40035-015-0042-0 |
| [6] |
Maiti P, Manna J, Dunbar G L. Current understanding of the molecular mechanisms in Parkinson's disease: targets for potential treatments[J]. Transl Neurodegener, 2017, 6: 28. doi:10.1186/s40035-017-0099-z |
| [7] |
Skaper S D, Facci L, Zusso M, et al. An inflammation-centric view of neurological disease: beyond the neuron[J]. Front Cell Neurosci, 2018, 12: 72. |
| [8] |
Yan W F, Shao Q H, Zhang D M, et al. The molecular mechanism of polygalasaponin F-mediated decreases in TNF-α: emphasizing the role of the TLR4-PI3K/AKT-NF-κB pathway[J]. Asian Nat Prod Res, 2015, 17(6): 662-70. doi:10.1080/10286020.2015.1056166 |
| [9] |
Sun X, Zeng H, Wang Q, et al. Glycyrrhizin ameliorates inflammatory pain by inhibiting microglial activation-mediated inflammatory response via blockage of the HMGB1-TLR4-NF-κB pathway[J]. Exp Cell Res, 2018, 369(1): 112-9. doi:10.1016/j.yexcr.2018.05.012 |
| [10] |
Zhu M D, Zhao L X, Wang X T, et al. Ligustilide inhibits microglia-mediated proinflammatory cytokines production and inflammatory pain[J]. Brain Res Bull, 2014, 109: 54-60. doi:10.1016/j.brainresbull.2014.10.002 |
| [11] |
Bae J Y, Lee S W, Shin Y H, et al. P2X7 receptor and NLRP3 inflammasome activation in head and neck cancer[J]. Oncotarget, 2017, 8(30): 48972-82. |
| [12] |
Jo E K, Kim J K, Shin D M, et al. Molecular mechanisms regulating NLRP3 inflammasome activation[J]. Cell Mol Immunol, 2016, 13(2): 148-59. doi:10.1038/cmi.2015.95 |
| [13] |
Yang J, Zhao Y, Shao F. Non-canonical activation of inflammatory caspases by cytosolic LPS in innate immunity[J]. Curr Opin Immunol, 2015, 32: 78-83. doi:10.1016/j.coi.2015.01.007 |
| [14] |
Lacey C A, Mitchell W J, Dadelahi A S, Skyberg J A. Caspases-1 and caspase-11 mediate pyroptosis, inflammation, and control of Brucella joint infection[J]. Infect Immun, 2018, 86(9): e00361-18. |

