

阿片类药物是一类强效镇痛剂,对手术或创伤后急性中重度疼痛尤其有效。除此之外,很多遭受难治性疼痛、长期疼痛的患者,最后只能使用阿片类药物来减轻疼痛[1],但是阿片类药物也带来很多问题,如耐受、痛觉过敏、呼吸抑制、成瘾等。其中阿片类药物成瘾发生率高,对个人、家庭及社会的危害极大。本文综述了中脑边缘奖赏系统参与阿片类药物成瘾的神经环路,以期为深入探索阿片类药物成瘾本质提供新的思路。
1 阿片类药物成瘾与中脑边缘奖赏系统概述 1.1 阿片类药物成瘾定义阿片类物质包括吗啡、海洛因、二氢埃托啡、哌替啶、美沙酮等。根据美国成瘾医学协会对成瘾的定义,成瘾具有以下特征:①难以中断;②行为自制障碍;③对药物的渴求;④人际关系淡化;⑤情绪失常[2]。但是,目前成瘾的定义仍不明确,与“依赖”“戒断”等词的界限不清。“成瘾”侧重强调对于阿片类药物的渴求,其基础是阿片类药物引起的脑内与精神动机有关的适应性改变。“依赖”强调对于阿片类药物的需求难以抑制。“戒断”指的是成瘾后停止药物使用,机体出现的激烈的躯体和精神戒断症状。
1.2 阿片成瘾在动物实验中的行为学评估在动物实验中,成瘾行为的评估通常采用条件性位置偏爱、自身给药、自发或催促的戒断反应、行为敏化等行为学指标。条件性位置偏爱实验将药物与环境线索配对,对动物进行训练。当动物被给予阿片药物时,动物将被放到特定环境中;当动物被给予空载剂时,动物将被放到另一个环境中,反复训练多次。最后通过观察动物对两种环境的偏好来反映动物对阿片类药物摄取的需要程度。自身给药实验是让动物学习完成一定的动作或任务,当动物完成动作后,动物可以获得由装置提供的阿片类药物;如动物未完成动作,则不会获得药物。实验通过记录动物完成规定动作的次数和频率,反映动物对阿片药物的需要程度。戒断实验是先给动物阿片类药物,后终止给药,观察动物的戒断反应。行为敏化实验是记录给予多次阿片类药物后,动物出现的自发活动的增强,将其作为反映动物成瘾状态的一项指标[7, 9, 13]。
1.3 中脑边缘奖赏系统的发现关于阿片类药物成瘾的机制,目前已经有了大量的研究,其中,中脑边缘奖赏系统在阿片类药物成瘾中发挥重要作用。1954年,詹姆斯·奥尔兹和皮特·米尔纳最先认识到脑内存在奖赏系统[3]。他们设计了与自身给药实验类似的装置,当大鼠按压按钮时,大鼠会接受大脑中的特定部位短暂的电刺激。他们发现大鼠会反复按压按钮,这种现象被称为颅内自我刺激或脑刺激奖励。对于动物出现这样行为的解释是,这样的刺激正在激活奖励系统。后来,人们逐渐认识到,大脑内存在多个区域,相互联系,构成一个复杂的系统,介导奖赏相关的行为和情绪反应。主要包括中脑腹侧被盖区(ventral tegmental area, VTA)、伏隔核(nucleus accumbens, NAc)、纹状体、黑质、海马、前额叶皮质、下丘脑、丘脑底核、腹侧苍白球、杏仁核等。
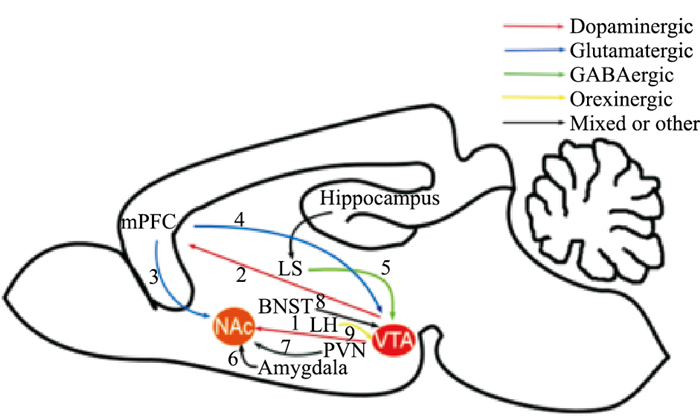
1.4 中脑边缘奖赏系统参与阿片成瘾阿片类药物成瘾后,中脑边缘奖赏系统的多个脑区发生了明显的细胞分子改变[4]。而通过多种方法调控这些区域的分子活动可以改变阿片类药物成瘾的表型,如吗啡成瘾状态下,VTA多巴胺代谢活动增强,与多巴胺代谢及转运相关的生化指标,如酪氨酸羟化酶、多巴胺、多巴胺转运体表达增加。NAc注射N-甲基-D-天冬氨酸(N-methyl-D-aspartic acid, NMDA)受体阻断剂能够抑制吗啡成瘾形成[5]。然而,这些广泛但孤立的神经生物学变化使得我们对阿片类药物成瘾机制的认识趋于复杂化。因此,从环路水平研究阿片类物质引起的生物学变化,用相互联系的观点审视阿片类物质成瘾的发生发展规律,将更有助于深入了解阿片类药物成瘾机制。以下综述了近年来通过药理学、神经示踪、电生理、光遗传学等技术揭示的中脑边缘奖赏系统参与阿片类药物成瘾的神经环路(Fig 1)。
|
| Fig 1 Schematic diagram of neurocircuitry inmesolimbic reward system involved in opioid addiction VTA: ventral tegmental area; NAc: nucleus accumbens; mPFC: medial prefrontal cortex; LS: lateral septum; PVN: paraventricular nucleus; BNST: bed nucleus of the striaterminalis; LH: lateral hypothalamus. |
VTA是一个异质性的脑结构,其细胞构成由65%多巴胺能神经元,30% γ-氨基丁酸(γ-aminobutyric acid, GABA)能神经元和5%谷氨酸能神经元组成。VTA向NAc投射密集的多巴胺能纤维。酪氨酸羟化酶是多巴胺生物合成中的一种关键酶,长期使用吗啡后,VTA区酪氨酸羟化酶表达上调,NAc多巴胺含量增加,表明VTA-NAc通路中多巴胺的上调可能在吗啡和其他阿片类药物奖赏中起重要作用[6]。此外,戒断状态大鼠给予急性吗啡,VTA多巴胺能神经元呈现爆发性放电,这被认为在编码奖赏信息中起作用[7]。小鼠在体电生理记录表明,慢性吗啡增加了VTA多巴胺能神经元的基础放电频率和爆发性放电概率[8]。Stuber等[9]通过光遗传技术,进一步证实了VTA多巴胺能神经元在阿片类药物成瘾中的作用,利用病毒注射方法将蓝光敏感的光敏感蛋白选择性表达在VTA区多巴胺能神经元。非连续、高频激活VTA区多巴胺能神经元可以导致对配对环境的条件性位置偏爱,而且这样的刺激可以引起NAc中多巴胺的含量明显增加,提示可能只有引起NAc区多巴胺增加的VTA多巴胺能神经元激活才能引起奖赏行为。NAc中神经元根据表达的多巴胺受体不同,分为两种神经元,主要表达多巴胺1型受体的神经元被称为D1神经元,而主要表达多巴胺2型受体的神经元被称为D2神经元。这两种神经元都接受VTA的多巴胺能投射,但是两种神经元介导的信号转导过程却有着明显差异,在阿片类药物成瘾中发挥的作用也有明显差别,甚至截然相反。
2.2 VTA-内侧前额叶皮质(medial prefrontal cortex, mPFC)通路与阿片成瘾mPFC参与多种认知功能,包括注意力、习惯形成、学习记忆等。mPFC主要分为前扣带皮质、前皮质和下皮质。电刺激VTA神经元或VTA微量注射选择性μ受体激动剂DAMGO,前扣带皮质中多巴胺和主要代谢产物增加。化学损伤前扣带皮质中多巴胺能纤维末梢,能够明显减弱VTA注射DAMGO引起的条件性位置偏爱。这些结果提示,VTA-前扣带皮质的信息传递可能在阿片诱导的位置偏爱的获得和维持中起着至关重要的作用[10]。
2.3 mPFC-NAc通路与阿片成瘾mPFC通过其与皮层下区域(如丘脑、纹状体、杏仁核和海马)的紧密互连,在厌恶和奖赏性刺激的处理中发挥重要作用。mPFC-NAc通路一直被认为介导奖赏相关的行为。生理状态下,电刺激VTA引起的NAc多巴胺电流可以时间依赖性调节电刺激mPFC引起的伏隔核兴奋性反应。在mPFC刺激前100 ms给予VTA刺激,mPFC-NAc传递抑制。在mPFC刺激的同时给予VTA刺激,mPFC-NAc传递增强。而在成瘾药物戒断状态下,这种调制作用减弱。因此,从mPFC到NAc的谷氨酸能投射可能在介导成瘾行为中起着至关重要的作用[11]。早期研究表明,调控mPFC-NAc通路可使酒精成瘾行为发生改变[12]。近期有光遗传学研究发现,尽管以20 Hz的频率激活mPFC-NAc通路,能够使NAc产生兴奋性突触后电位,但是不能增强小鼠的操作性自身光刺激行为。当以30 Hz频率进行刺激时,小鼠的自身刺激行为增加,提示mPFC-NAc通路激活需要达到一定强度,才能对奖赏和成瘾行为产生影响[13]。
2.4 mPFC-VTA通路与阿片成瘾前皮质内注射NMDA受体阻断剂AP-5,可以增强吗啡引起的条件性位置偏爱,VTA内多巴胺能神经元放电活动明显增加,同时抑制非多巴胺能的GABA能神经元放电[14]。前皮质内大麻素1型受体(cannabinoid type 1 receptor, CB1 receptor)激活可使吗啡奖励信号变成厌恶刺激,阻断CB1受体的正常传递,增强了亚奖赏阈值剂量吗啡的奖励效应。前皮质内CB1受体介导的吗啡奖赏减弱由VTA中κ阿片受体介导,而前皮质内CB1受体介导的吗啡奖赏增强由VTA中μ阿片受体介导[15]。此外,mPFC还投射到脚脑桥被盖核和侧向被盖核,它们又分别向VTA投射谷氨酸能和胆碱能传出纤维。mPFC注射多巴胺受体激动剂SKF-81297, 使成瘾行为增加。此外,脚脑桥被盖核/侧向被盖核注射离子型谷氨酸受体拮抗剂CNQX,可减轻成瘾行为。VTA注射CNQX、烟碱受体拮抗剂美加霉胺或毒蕈碱受体拮抗剂东莨菪碱,也可以抑制成瘾行为。这些结果表明,包括mPFC、脚脑桥被盖核/侧向被盖核和VTA的多突触环路介导了成瘾行为的发生[16]。
2.5 CA3-外侧隔(lateral septum, LS)-VTA通路与阿片成瘾Lisman等[17]提出了海马-VTA环的概念。新接收的信息首先到达海马,所产生的信号通过海马下托、NAc和腹侧苍白球等结构传递给VTA。反过来,多巴胺在海马内释放,产生长时程增强(long-term potentiation, LTP)和学习记忆的增强。海马-VTA环路参与短时记忆向长时记忆转换这一过程。而阿片类药物成瘾过程包含了对阿片药物的效应、服药所处环境的学习记忆过程。Luo等[18]确定了CA3-LS-VTA通路参与阿片药物成瘾。CA3给予θ频率的电刺激,VTA多巴胺神经元兴奋,而非多巴胺能神经元受到抑制。多巴胺能神经元兴奋可能是通过去抑制介导的,因为局部拮抗GABA受体阻断了对CA3刺激的反应。抑制CA3-LS-VTA通路中的任意环节,都可以阻断电刺激诱发的VTA反应。海马和VTA之间的这种跨突触连接似乎是环境线索调节目标导向行为的重要基础。有研究支持这一观点,当大鼠再次暴露于吗啡配对环境时,海马CA3区神经元活性增强,外侧隔中GABA能神经元兴奋性增加,进而使VTA中GABA能神经元抑制,导致多巴胺能神经元的去抑制激活[19]。这在吗啡配对环境暴露引起的位置偏爱中发挥重要作用。
2.6 基底外侧杏仁核(basolateral amygdala, BLA)-NAc通路与阿片成瘾另有研究发现,在线索诱发奖赏行为的过程中,BLA神经元对线索的应答反应先于NAc神经元,并且NAc神经元的反应依赖于BLA传入。这些结果表明,BLA输入是NAc神经元对线索的应答所必需的,并且是环境线索促进奖励寻求行为的基础[20]。BLA接收来源于VTA的多巴胺能神经支配,D1和D2受体在BLA都有表达。在正常大鼠,BLA给予D1受体阻断剂或激动剂,阻断或者增强联想性阿片奖励记忆的获取[21]。而在阿片依赖和戒断状态大鼠,BLA给予D1受体阻断剂或激动剂不起作用,给予D2受体阻断剂或激动剂阻断或增强阿片奖励记忆。体内单细胞记录证实了BLA多巴胺受体调控可以调节NAc神经元对吗啡的应答模式[22]。
2.7 下丘脑室旁核(paraventricular nucleus, PVN)-NAc通路与阿片成瘾有研究证明,PVN-NAc通路活动增强对于引起戒断行为是必要的,选择性沉默该通路可以消除小鼠阿片戒断症状。慢性吗啡暴露选择性地增强PVN和NAc中D2型中型棘突神经元之间的兴奋性传递,通过光遗传技术抑制这条通路,可以恢复突触间的正常传递,并明显减轻吗啡戒断症状[23]。
2.8 终纹床核(bed nucleus of the striaterminalis, BNST)-VTA通路与阿片成瘾厌恶性环境暴露使投射到VTA的BNST不同类型神经元产生不同的放电模式改变,谷氨酸能神经元活性增强,而GABA能神经元放电频率被抑制。BNST谷氨酸能和GABA能投射纤维优先支配VTA区非多巴胺能神经元,光激活BNST投射至VTA的谷氨酸能神经元导致厌恶和焦虑行为表型。相反,激活BNST投射至VTA的GABA能神经元产生奖赏和焦虑消退表型[24]。
2.9 外侧下丘脑(lateral hypothalamus, LH)-VTA通路与阿片成瘾下丘脑是产生食欲素的中枢区域,其到VTA的投射在奖赏和成瘾行为中起着重要的作用。有研究将逆行示踪剂WGA注射到VTA或蓝斑,结果发现投射到VTA的下丘脑食欲素神经元Fos激活的百分比在吗啡依赖大鼠中明显增加,并且Fos激活集中在外侧下丘脑,而不在背侧区或穹窿周区。并且Fos激活的百分比与条件性位置偏爱评分呈正相关,而投射到蓝斑的下丘脑食欲素神经元Fos激活与条件性位置偏爱评分无相关性。这些结果表明,VTA是下丘脑食欲素神经元介导吗啡依赖的一个特异靶区[25]。有研究发现,LH联合给药卡巴胆碱和亚成瘾剂量的吗啡,可以明显诱导条件性位置偏爱。此外,VTA注射选择性食欲素受体拮抗剂SB334867,可以减弱条件性位置偏爱评分。这表明VTA中食欲素-食欲素受体系统在大鼠吗啡成瘾中的重要作用[26]。
3 结语与展望综上所述,VTA-NAc通路可能是介导阿片类药物成瘾的最终通路,其他脑区如海马、杏仁核、下丘脑、前额叶皮质等,可向VTA和NAc投射不同类型的神经纤维,调节VTA-NAc的活动,从而在阿片类药物成瘾中发挥作用。目前,关于阿片类药物成瘾环路机制方面的研究大多数还是通过药理学方法,缺乏位点和时间特异性。光遗传学、化学遗传学技术可以实现对特定投射环路的精确调控,帮助我们探索不同神经环路在阿片类药物成瘾中的作用。本文对中脑边缘奖赏系统中参与阿片类药物成瘾的神经环路进行了综述,有助于从环路角度了解阿片类药物成瘾机制,同时也为临床阿片类药物成瘾问题的管理提供了新的思路。
| [1] |
边佳明, 吴宁, 李锦. 吗啡诱导的大鼠条件性位置偏爱模型中关键脑区PEBP及ERK活性的变化[J]. 中国药理学通报, 2017, 33(4): 542-6. Bian J M, Wu N, Li J. Analysis of brain PEBP and ERK in morphine-induced CPP model in rats[J]. Chin Pharmacol Bull, 2017, 33(4): 542-6. doi:10.3969/j.issn.1001-1978.2017.04.018 |
| [2] |
Caraci F, Drago F. New definition of addiction proposed by the American Society of Addiction Medicine: which implications for the treatment of tobacco dependence?[J]. Eur Neuropsychopharmacol, 2014, 24(1): 1-4. doi:10.1016/j.euroneuro.2013.05.003 |
| [3] |
Tzschentke T M. The medial prefrontal cortex as a part of the brain reward system[J]. Amino Acids, 2000, 19(1): 211-9. doi:10.1007/s007260070051 |
| [4] |
姚红月, 宋斐然, 刘春娜, 等. 神经肽Urocortin2对吗啡成瘾大鼠VTA神经元放电及DA能神经传递的影响[J]. 中国药理学通报, 2015, 31(7): 979-83. Yao H Y, Song F R, Liu C N, et al. Effects of neuroactive peptide urocortin 2 on VTA neuron's spontaneous discharge and DA-ergic neurotransmission in morphine addiction[J]. Chin Pharmacol Bull, 2015, 31(7): 979-83. doi:10.3969/j.issn.1001-1978.2015.07.018 |
| [5] |
Mazeirobison M S, Nestler E J. Opiate-induced molecular and cellular plasticity of ventral tegmental area and locus coeruleus catecholamine neurons[J]. Cold Spring Harb Perspect Med, 2012, 2(7): a012070. |
| [6] |
Liang J, Ma S S, Li Y J, et al. Dynamic changes of tyrosine hydroxylase and dopamine concentrations in the ventral tegmental area-nucleus accumbens projection during the expression of morphine-induced conditioned place preference in rats[J]. Neurochem Res, 2012, 37(7): 1482-9. doi:10.1007/s11064-012-0739-8 |
| [7] |
Howard L, Margolis, Elyssa B. Understanding opioid reward[J]. Trends Neurosci, 2015, 38(4): 217-25. doi:10.1016/j.tins.2015.01.002 |
| [8] |
Koo J W, Mazeirobison M S, Chaudhury D, et al. BDNF is a negative modulator of morphine action[J]. Science, 2012, 338(6103): 124-8. doi:10.1126/science.1222265 |
| [9] |
Stuber G D, Britt J P, Bonci A. Optogenetic modulation of neural circuits that underlie reward seeking[J]. Biol Psychiatry, 2012, 71(12): 1061-7. doi:10.1016/j.biopsych.2011.11.010 |
| [10] |
Narita M, Matsushima Y, Niikura K, et al. Implication of dopaminergic projection from the ventral tegmental area to the anterior cingulate cortex in μ-opioid-induced place preference[J]. Addict Biol, 2010, 15(4): 434-47. doi:10.1111/adb.2010.15.issue-4 |
| [11] |
Wang X, Liu L, Adams W, et al. Cocaine exposure alters dopaminergic modulation of prefrontal-accumbens transmission[J]. Physiol Behav, 2015, 145: 112-7. doi:10.1016/j.physbeh.2015.03.042 |
| [12] |
Keistler C R, Hammarlund E, Barker J M, et al. Regulation of alcohol extinction and cue-induced reinstatement by specific projections between medial prefrontal cortex, nucleus accumbens and basolateral amygdala[J]. J Neurosci, 2017, 37(17): 4462-71. doi:10.1523/JNEUROSCI.3383-16.2017 |
| [13] |
Riga D, Matos M R, Glas A, et al. Optogenetic dissection of medial prefrontal cortex circuitry[J]. Front Syst Neurosci, 2014, 8: 230. |
| [14] |
Tan H, Rosen L G, Ng G A, et al. NMDA receptor blockade in the prelimbic cortex activates the mesolimbic system and dopamine-dependent opiate reward signaling[J]. Psychopharmacology, 2014, 231(24): 4669-79. doi:10.1007/s00213-014-3616-0 |
| [15] |
Ahmad T, Lauzon N M, De J X, et al. Cannabinoid transmission in the prelimbic cortex bidirectionally controls opiate reward and aversion signaling through dissociable kappa versus μ-opiate receptor dependent mechanisms[J]. J Neurosci, 2013, 33(39): 15642-51. doi:10.1523/JNEUROSCI.1686-13.2013 |
| [16] |
Schmidt H D, Famous K R, Pierce R C. The limbic circuitry underlying cocaine seeking encompasses the PPTg/LDT[J]. Eur J Neurosci, 2010, 30(7): 1358-69. |
| [17] |
Lisman J E, Grace A A. The hippocampal-VTA loop: controlling the entry of information into long-term memory[J]. Neuron, 2005, 46(5): 703-13. doi:10.1016/j.neuron.2005.05.002 |
| [18] |
Luo A H, Tahsilifahadan P, Wise R A, et al. Linking context with reward: a functional circuit from hippocampal CA3 to ventral tegmental area[J]. Science, 2011, 333(6040): 353-7. doi:10.1126/science.1204622 |
| [19] |
Jiang J, Liu H, Huang Z, et al. The role of CA3-LS-VTA loop in the formation of conditioned place preference induced by context-associated reward memory for morphine[J]. Addict Biol, 2016, 23(1): 41-54. |
| [20] |
Ambroggi F, Ishikawa A H, Nicola S. Basolateral amygdala neurons facilitate reward-seeking behavior by exciting nucleus accumbens neurons[J]. Neuron, 2008, 59(4): 648-61. doi:10.1016/j.neuron.2008.07.004 |
| [21] |
Lintas A, Chi N, Lauzon N M, et al. Inputs from the basolateral amygdala to the nucleus accumbens shell control opiate reward magnitude via differential dopamine D1 or D2 receptor transmission[J]. Eur J Neurosci, 2012, 35(2): 279-90. doi:10.1111/j.1460-9568.2011.07943.x |
| [22] |
Lintas A, Chi N, Lauzon N M, et al. Identification of a dopamine receptor-mediated opiate reward memory switch in the basolateral amygdala-nucleus accumbens circuit[J]. J Neurosci, 2011, 31(31): 11172-83. doi:10.1523/JNEUROSCI.1781-11.2011 |
| [23] |
Zhu Y, Wienecke C F, Nachtrab G, et al. A thalamic input to the nucleus accumbens mediates opiate dependence[J]. Nature, 2016, 530(7589): 219-22. doi:10.1038/nature16954 |
| [24] |
Jennings J H, Sparta D R, Stamatakis A M, et al. Distinct extended amygdala circuits for divergent motivational states[J]. Nature, 2013, 496(7444): 224-8. doi:10.1038/nature12041 |
| [25] |
Richardson K A, Aston-Jones G. Lateral hypothalamic orexin/hypocretin neurons that project to ventral tegmental area are differentially activated with morphine preference[J]. J Neurosci, 2012, 32(11): 3809-17. doi:10.1523/JNEUROSCI.3917-11.2012 |
| [26] |
Razavi Y, Karimi S, Baniardalan M, et al. Chemical stimulation of the lateral hypothalamus potentiated the sensitization to morphine in rats: involvement of orexin-1 receptor in the ventral tegmental area[J]. EXCLI J, 2014, 13: 1120-30. |

