

2. 南京中医药大学医学与生命科学学院药理系,江苏 南京 210023;
3. 南京中医药大学附属苏州市中医医院苏州市吴门医派研究院,江苏 苏州 215003
江国荣(1963-),男,博士,主任中药师,研究方向:中药药理学,通讯作者,E-mail: guorongjiang@hotmail.com
 ,
BAO Kai-fan1,
JIA Zhi-rong1,
WANG Xiao-yu1,
ZHENG Jie2,
HONG Min1
,
BAO Kai-fan1,
JIA Zhi-rong1,
WANG Xiao-yu1,
ZHENG Jie2,
HONG Min1
 ,
JIANG Guo-rong3
,
JIANG Guo-rong3

2. Dept of Pharmacology, School of Medicine and Life Sciences, Nanjing University of Chinese Medicine, Nanjing 210023, China;
3. Suzhou Wu Men Yi Pai Research Institute, the Affiliated Suzhou Hospital of TCM of Nanjing University of Chinese Medicine, Suzhou Jiangsu 215003, China
过敏性反应是机体受到过敏原,如花粉、屋尘螨(house dust mite, HDM)等诱导后,引起的病理性组织损伤或者功能紊乱的一种免疫反应。过敏性疾病主要包括过敏性哮喘、过敏性皮炎、过敏性鼻炎等,其中患病率及复发率最高的为过敏性哮喘。据Global Burden of Disease Study资料显示,全球约有2.4亿过敏性哮喘患者,预计到2025年将达到3亿,并且有研究显示,该数值近年内将持续上升[1]。过敏性哮喘是一种变应原或其他因素引起的肺功能失常[2],以适应性的2型辅助性T细胞(type 2 T helper cell, Th2)功能异常为主要特征的2型免疫反应。发病时,主要伴随着Th2型细胞因子白介素(interleukin, IL)-4、IL-5、IL-13的产生,表现为嗜酸性粒细胞(eosinophils, EOS)增多、黏液分泌旺盛、气道高反应性,以及E型免疫球蛋白(immunoglobulin E, IgE)的表达增加。过敏性哮喘的病因及发病机制十分复杂[3],目前尚未被完全了解,因此,进一步研究过敏性哮喘的发病机制,并建立有效的干预或治疗手段,对于降低其发病率、复发率尤为重要。
20世纪末,美国学者Dixit等[4]通过实验,首次发现了锌指蛋白A20,因其最初是由肿瘤坏死因子α(tumor necrosis factor α, TNF-α)诱导内皮细胞产生的,所以又被称为肿瘤坏死因子α诱导蛋白3(tumor necrosis factor alpha-induced protein 3, TNFAIP3)。随着对于A20的深入研究,目前它被认为是炎症信号通路的关键调控因子,主要是核转录因子κB(nuclear factor κB, NF-κB)的一种负调控因子,可以通过多种途径抑制NF-κB的活化。目前已有若干报道证实,A20参与了过敏性疾病的发生和发展[5-6],其在过敏性哮喘的发病机制中的重要作用也越来越被重视。因此,对A20与过敏性哮喘的最新研究进展进行综述,有利于为过敏性哮喘的预防和治疗提供新思路。
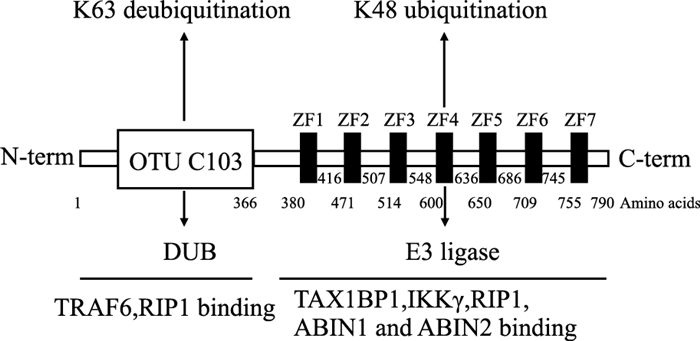
1 A20的起源与结构锌指蛋白A20,根据其cDNA克隆数而命名,是一种具有高度生物活性的胞质蛋白质。研究发现,人类的A20基因序列定位于染色体中6q23.3位,其cDNA全长为4 426 bp,发挥转录活性作用的可读区域框为2 370 bp(67~2 436 bp)。人的A20蛋白总共由790个氨基酸组成,蛋白分子质量为90 ku。进一步对其蛋白结构分析可知,A20属于去泛素化酶(deubiquitinating enzymes, DUBS)卵巢肿瘤(ovarian tumor, OTU)家族的一种,其N末端区(1~385)含有的半胱氨酸蛋白酶类OTU是A20蛋白的特征性结构区域之一[7]。同时,A20蛋白也具有泛素化功能,A20蛋白的锌指结构区在其C末端(386~775),该锌指区域由7个Cys2-Cys2结构组成[8],其中第4个结构区具有E3泛素连接酶活性,可特异性地与底物结合,招募26S蛋白酶体,将靶蛋白降解。正是因为这两种特殊的蛋白结构(Fig 1),A20蛋白具有了泛素化和去泛素化双重功能,在炎症调节中起着重要作用。
|
| Fig 1 Biochemical characteristics of A20 protein |
A20是一种具有高度保守性的、胞质诱导表达性蛋白,其在上皮细胞、T淋巴细胞、B淋巴细胞、树突状细胞等中均有表达。已有研究表明,A20作为NF-κB的负调控因子,在多种炎症性反应中扮演着重要的角色。A20蛋白可在多种促炎因子,如细菌脂多糖(lipopolysaccharides, LPS)、TNF-α、IL-1等刺激细胞后大量表达,其中,A20基因3’端非翻译区含有的4个“ATTTA”序列,是A20蛋白快速表达的基础。尽管目前广泛认为A20是一种存在于细胞质中的抗炎蛋白,但最初研究发现其是一种能够保护由TNF-α诱导细胞毒性的蛋白质。进一步研究发现,A20可以通过不同途径,抑制TNF-α诱导的NF-κB的活化,除此之外,还可以抑制由CD40、IL-1,以及包括模式识别受体(pattern recognition receptor, PRR)等在内诱导的NF-κB的活化,并且还可以抑制T细胞和B细胞抗原受体的激活[8]。A20在多种炎症反应中起着重要作用,特异性敲除小鼠体内A20基因不久后,小鼠体内多种器官即可产生炎症反应,并且缺失A20蛋白的细胞无法阻断由刺激因子诱导的NF-κB的活化。除此之外,近年来A20还被报道能调节其他细胞信号转导通路,如Wnt通路、干扰素调节因子(interferon regulatory factor, IRF)、自噬应答等途径。研究发现,A20还可以通过直接结合白细胞介素17受体A(interleukin-17 receptor type A, IL-17RA)的C末端结构域,来抑制IL-17信号转导,并且A20可以抑制TNFR、IL-1R和NOD样受体(NOD like receptors, NLR)信号通路,但是A20是否直接与这些受体结合,尚待考证。
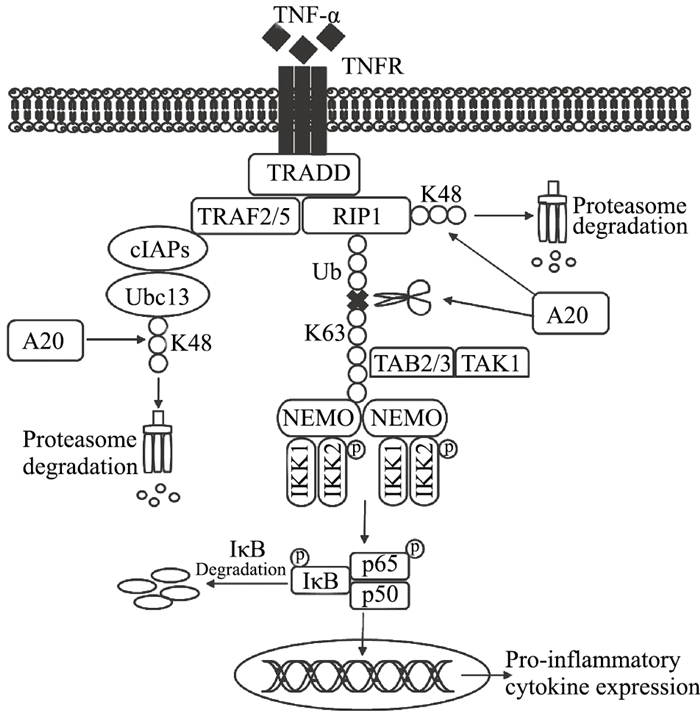
TNF受体1(TNF receptor 1, TNFR1)能够激活NF-κB活化的信号转导途径,A20被认为能通过调节该通路而成为炎症性疾病的潜在治疗靶点(Fig 2)。众所周知,蛋白质泛素化是生物体内的一种重要调节方式。该过程通过对靶蛋白进行一系列的特异性修饰后,即可招募26S蛋白酶体,将靶蛋白降解,其中起蛋白质降解标签作用的为K48多聚泛素蛋白链。除此之外,蛋白质的泛素化也可以进行信号转导,这主要依赖于K63多聚泛素蛋白链的作用,其可以被特异性的调控因子识别,启动相应信号[9]。A20被普遍认为是一种NF-κB信号的经典负调控因子,且已有文献证明,A20是一种泛素编辑酶复合体,同时具有E3泛素连接酶和DUB去泛素化酶活性。目前认为,A20抑制NF-κB信号的机制一方面是因其蛋白N末端的OTU结构域[7],而受体相互作用蛋白激酶1(receptor interacts with the protein kinase 1, RIP1)、肿瘤坏死因子受体相关因子6(tumor necrosis factor receptor- associated factor 6, TRAF6)和NF-κB必需调节蛋白(NF-κB- essential modulator, NEMO)等为OTU结构域的结合底物[10-12],并且RIP1、TRAF6、NEMO等被激活后,均能募集泛素蛋白聚合,形成K63多聚泛素化链。因此,A20能够特异性地趋向K63链,破坏其多聚泛素化链完整性,从而阻断相关信号的转导[10]。除了去泛素化活性之外,A20蛋白第4个锌指结构区域ZF4所具有的泛素连接酶功能,也参与NF-κB的抑制作用。A20的E3泛素连接酶活性能促进RIP1募集以lys48位点连接为主的泛素蛋白的多聚化,也就是可以促进靶蛋白附着K48多聚泛素化链,从而招募26S蛋白酶体降解RIP1,阻断下游的信号转导。除此之外,研究还发现,A20可以通过去泛素化黏膜相关淋巴组织淋巴瘤易位蛋白1(mucosa-associated lymphoid tissue lymphoma translocation protein 1, MALT1),负调控由T细胞受体(T cell receptor, TCR)诱导的NF-κB的活化。在淋巴细胞中,TRAF6对MALT1的泛素化也是NF-κB活化所必需的[13]。A20的生物学功能依赖于其蛋白结构基础,随着研究的发展,A20蛋白的更多功能也将会被发现。
|
| Fig 2 A20 protein function in tumor necrosis factor receptor (TNFR)- induced NF-κB inhibition |
过敏性哮喘是儿童和成人中最常见的慢性非传染性疾病之一,其特征是以呼吸道症状多变、气流受限为主。过敏性哮喘异质性强,是由环境和基因相互作用的结果,发病后出现严重的气道炎症和气道重塑[3]。目前,过敏性哮喘的治疗目标主要是实现对其良好的控制,尽量缓解过敏性哮喘症状,以及降低疾病复发几率。抗炎以及支气管扩张药物的使用是治疗过敏性哮喘的主要手段,尽管这些手段广泛应用于临床,但仍难以缓解恶性哮喘的发病症状,也无法防止哮喘的复发。目前,全球有很多机构都在研究过敏性哮喘,但其发病机制仍不明确。A20作为NF-κB的负调控因子,能够有效调节炎症反应,在过敏性哮喘中的研究也逐渐受到了重视。
目前,主要用于治疗过敏性哮喘的为糖皮质激素(glucocorticoid, GC)类药物,可以有效缓解气道炎症以及哮喘症状。GC既可以促进抗炎因子分泌,又可抑制许多促炎因子的表达[14]。糖皮质激素受体(glucocorticoid receptor, GR)是一种存在于细胞质中的转录因子,通过与GC特异性结合后转入到细胞核,参与相关基因调控。GC的治疗作用与A20的表达有关,Altonsy等[5]研究发现,特异性敲除A20后能明显增加人支气管上皮细胞分泌TNF-α,并且长效β2受体激动剂(longacting β2-adrenoceptor agonists, LABAs)能通过增加A20的表达,负调控NF-κB的活化,进而提高吸入性GC的抗炎作用。GC的抗炎作用还可通过与GR结合,促进抗炎因子A20和NFBIA基因、蛋白的表达[15]。
A20功能紊乱能够引起包括哮喘等多种免疫性疾病,但也有研究证明,A20可以限制过敏性气道炎症和耐受反应[6]。研究发现,A20参与了低剂量LPS诱导的免疫耐受。持续给予小鼠低剂量LPS,能够增强HDM诱导的哮喘小鼠的耐受性,支气管肺泡灌洗液(bronchoalveolar lavage fluid, BALF)和肺组织匀浆中IL-4、IL-5、IL-13的表达明显减少。而特异性敲除小鼠上皮细胞A20基因(Tnfaip3EC-KO)后,可明显影响LPS诱导的免疫耐受、过敏性哮喘模型外周血中嗜酸性粒细胞数目,以及BALF和肺组织匀浆中IL-4、IL-5、IL-13表达均明显增加[6]。Tan等[16]发现,灭活的铜绿假单胞菌药剂能够通过降低Act1,以及增加TLR4、A20的表达,来抑制卵清蛋白(ovalbumin, OVA)引起的过敏性气道炎症。此外,A20也参与了锌对哮喘的调控机制。Morgan等[17]发现,短期锌处理组并未改变A20和TRAF6水平,但是导致了RIP1(IKK上游一种重要的激活因子)的降解。为进一步确定锌作为哮喘治疗剂的应用效果,随后建立过敏性气道炎症模型,给予锌治疗,结果表明锌补充剂能够通过调节A20活性而抑制NF-κB的表达,同时,补锌后可以降低气道高反应性和血清中IgE水平,但对Th2型细胞因子表达无影响。因此,补充锌可能是治疗哮喘的一种潜在方法,并且主要是通过调控A20的表达而实现的。
过敏性哮喘的发生伴随着大量Th2型细胞因子IL-4、IL-5、IL13的表达,在哮喘发病的初始阶段,2型固有淋巴细胞(type 2 innate lymphoid cell, ILC2)是经典的,除了2型辅助性T细胞以外的Th2型细胞因子的主要来源之一。哮喘患者BALF和唾液中能够检测到大量ILC2的存在[18],并且ILC2已被报道在炎症反应、组织修复以及代谢平衡中十分重要,因此,ILC2与过敏性哮喘关系密切。与此同时,miRNAs作为调控基因表达的重要因子,在过敏性哮喘的研究中也逐渐受到重视[19]。研究发现,miR-19a能够通过抑制ILC2中A20和SOCS1蛋白、基因的表达,从而促进IL-4、IL-5、IL-13的分泌[20]。在外源OVA诱导产生的小鼠过敏性肺部炎症模型中,当体内转染入含有A20 cDNA(Ad-A20)的腺病毒后,能够明显减少气道炎症性细胞的募集,减轻气道高反应性及支气管炎症的发生,并且Ad-A20的保护性作用是通过抑制NF-κB信号转导途径实现的。HDM诱导的过敏性哮喘小鼠肺匀浆中A20(通过调节关键信号蛋白TRAF6的泛素化来抑制TLR反应)、IRAKM(结合MyD88和TRAF6,可以阻断TLR作用,稳定信号复合物)、Tollip(与IL-1R、TLR2和TLR4相互作用以防止细胞激活,并抑制IRAK自磷酸化)均有明显增加[21]。且有报道表明,哮喘组中肺组织TGF-β1和CTCF mRNA水平与正常组相比明显上升,而体内给予外源性A20重组蛋白后明显下降,提示外源性A20对于气道上皮增生、平滑肌增殖的抑制作用与降低TGF-β1、CTCF的表达有关。
总之,目前A20均被视为一种抗炎蛋白,可以有效抑制各种炎症信号通路转导。除了传统的一些炎症信号外,近年来也发现了A20的一些新的调控因素。NLRP3作为一种炎症小体,参与了多种疾病的发生,哮喘患者体内能够检测到NLRP3的高表达,并且HDM诱导的小鼠过敏性哮喘模型中能够激活NLRP3炎症小体的组装。A20是TNF-α诱导的NF-κB信号激活通路的有效抑制剂,A20的缺失能够导致IL-1β的表达增加[22],并且A20可以抑制NLRP3炎症小体的激活[23],说明A20可以通过调控NLRP3的表达,缓解过敏性哮喘的炎症状态。此外,A20还可以调控一些转录因子的表达。JAK-STAT是一种经典的信号通路,膜受体活化后,能够引起JAKs的磷酸化,随后募集STATs,通过Src同源体2(Src homology 2, SH2)结构域与受体结合,经过JAKs信号传递引起STATs的磷酸化,进一步形成STATs二聚体,进入核内与DNA启动子结合,启动靶基因转录。JAK-STAT通路参与了Th2细胞的分化,并且IL-4、IL-13与其受体IL-4Rα、IL-13Rα结合后,也可激活JAK-STAT通路。De Wilde等[24]发现,小鼠体内特异性敲除A20基因后,IRF4、STAT1的表达明显增加。Lee等[25]研究表明,小鼠体内过表达A20蛋白后,可以明显改善小鼠溃疡性结肠炎的炎症表现,并且过表达A20后,转录因子p-p65和p-STAT3的表达均明显减少。因此,A20可通过多种途径调控哮喘的发生。随着研究的进一步发展,A20更多的调控功能也将会被发现,其可能成为治疗过敏性哮喘的一个潜在新靶点。
4 小结越来越多的结果显示,A20在过敏性哮喘中扮演着重要的作用,参与了多种过敏性疾病的发生、发展。目前普遍认为A20主要是NF-κB的一种负调控因子,在参与过敏性哮喘发生的支气管上皮细胞及免疫细胞(如Th2细胞、ILC2等)中的研究较为广泛,但其具体调控机制仍不清楚。体内特异性敲除A20后,能够加重过敏性哮喘发病症状,给予重组A20能够明显缓解炎症反应,这些反应主要是依赖于A20蛋白与RIP1、NEMO、TRAF6等特异性结合后,发挥泛素化和去泛素化双重功能,起到信号抑制作用。除此之外,也有最新研究发现,A20可以调控IRF4、STAT3、STAT6等转录因子的表达,以及NLRP3炎症小体的组装,但是具体方式仍不清楚,提示A20可能存在多种负调控机制,并且其可能是治疗哮喘的潜在靶点。过敏性哮喘发病机制复杂,其多复发性成为世界性的难题,因此,对A20进行基因解析、蛋白质结构分析及调控机制探讨,对于过敏性哮喘的预防和治疗具有重大意义。
| [1] |
Fehrenbach H, Wagner C, Wegmann M. Airway remodeling in asthma: what really matters[J]. Cell Tissue Res, 2017, 367(3): 551-69. doi:10.1007/s00441-016-2566-8 |
| [2] |
魏盼, 李恋曲, 吴鹏, 等. 上皮间质转化与哮喘气道重塑的研究进展[J]. 中国药理学通报, 2018, 34(5): 600-3. Wei P, Li L Q, Wu P, et al. Advances in epithelial-mesenchymal transition and airway remodeling in asthma[J]. Chin Pharmacol Bull, 2018, 34(5): 600-3. doi:10.3969/j.issn.1001-1978.2018.05.003 |
| [3] |
Papi A, Brightling C, Pedersen S E, et al. Asthma[J]. Lancet, 2018, 391(10122): 783-800. doi:10.1016/S0140-6736(17)33311-1 |
| [4] |
Dixit V M, Green S, Sarma V, et al. Tumor necrosis factor-alpha induction of novel gene products in human endothelial cells including a macrophage-specific chemotaxin[J]. J Biol Chem, 1990, 265(5): 2973-8. |
| [5] |
Altonsy M O, Mostafa M M, Gerber A N, et al. Long-acting beta2-agonists promote glucocorticoid-mediated repression of NF-kappaB by enhancing expression of the feedback regulator TNFAIP3[J]. Am J Physiol Lung Cell Mol Physiol, 2017, 312(3): L358-70. doi:10.1152/ajplung.00426.2016 |
| [6] |
Schuijs M J, Willart M A, Vergote K, et al. Farm dust and endotoxin protect against allergy through A20 induction in lung epithelial cells[J]. Science, 2015, 349(6252): 1106-10. doi:10.1126/science.aac6623 |
| [7] |
Evans P C, Ovaa H, Hamon M, et al. Zinc-finger protein A20, a regulator of inflammation and cell survival, has de-ubiquitinating activity[J]. Biochem J, 2004, 378(Pt 3): 727-34. |
| [8] |
Beyaert R, Heyninck K, Van Huffel S. A20 and A20-binding proteins as cellular inhibitors of nuclear factor-kappa B-dependent gene expression and apoptosis[J]. Biochem Pharmacol, 2000, 60(8): 1143-51. doi:10.1016/S0006-2952(00)00404-4 |
| [9] |
Li S, Zhao J, Shang D, et al. Ubiquitination and deubiquitination emerge as players in idiopathic pulmonary fibrosis pathogenesis and treatment[J]. JCI Insight, 2018, 3(10): e120362. doi:10.1172/jci.insight.120362 |
| [10] |
Boone D L, Turer E E, Lee E G, et al. The ubiquitin-modifying enzyme A20 is required for termination of Toll-like receptor responses[J]. Nat Immunol, 2004, 5(10): 1052-60. doi:10.1038/ni1110 |
| [11] |
Wertz I E, Dixit V M. Signaling to NF-kappaB: regulation by ubiquitination[J]. Cold Spring Harb Perspect Biol, 2010, 2(3): a003350. |
| [12] |
Mauro C, Pacifico F, Lavorgna A, et al. ABIN-1 binds to NEMO/IKKgamma and co-operates with A20 in inhibiting NF-kappaB[J]. J Biol Chem, 2006, 281(27): 18482-8. doi:10.1074/jbc.M601502200 |
| [13] |
Abbasi A, Forsberg K, Bischof F. The role of the ubiquitin-editing enzyme A20 in diseases of the central nervous system and other pathological processes[J]. Front Mol Neurosci, 2015, 8: 21. |
| [14] |
Gerber A N. Glucocorticoids and the lung[J]. Adv Exp Med Biol, 2015, 872: 279-98. doi:10.1007/978-1-4939-2895-8 |
| [15] |
Kadiyala V, Sasse S K, Altonsy M O, et al. Cistrome-based cooperation between airway epithelial glucocorticoid receptor and NF-kappaB orchestrates anti-inflammatory effects[J]. J Biol Chem, 2016, 291(24): 12673-87. doi:10.1074/jbc.M116.721217 |
| [16] |
Tan Y, Liu H, Yang H, et al. An inactivated Pseudomonas aeruginosa medicament inhibits airway allergic inflammation and improves epithelial functions[J]. J Physiol Sci, 2013, 63(1): 63-9. doi:10.1007/s12576-012-0231-x |
| [17] |
Morgan C I, Ledford J R, Zhou P, et al. Zinc supplementation alters airway inflammation and airway hyperresponsiveness to a common allergen[J]. J Inflammation, 2011, 8(1): 36. |
| [18] |
Klose C S, Artis D. Innate lymphoid cells as regulators of immunity, inflammation and tissue homeostasis[J]. Nat Immunol, 2016, 17(7): 765-74. doi:10.1038/ni.3489 |
| [19] |
王晓钰, 于曦, 王燕, 等. MicroRNAs:过敏性疾病的潜在新靶点[J]. 中国药理学通报, 2016, 32(5): 616-9. Wang X Y, Yu X, Wang Y, et al. MicroRNAs: potential new targets of allergic disease[J]. Chin Pharmacol Bull, 2016, 32(5): 616-9. doi:10.3969/j.issn.1001-1978.2016.05.006 |
| [20] |
Singh P B, Pua H H, Happ H C, et al. MicroRNA regulation of type 2 innate lymphoid cell homeostasis and function in allergic inflammation[J]. J Exp Med, 2017, 214(12): 3627-43. doi:10.1084/jem.20170545 |
| [21] |
Habibzay M, Saldana J I, Goulding J, et al. Altered regulation of Toll-like receptor responses impairs antibacterial immunity in the allergic lung[J]. Mucosal Immunol, 2012, 5(5): 524-34. doi:10.1038/mi.2012.28 |
| [22] |
Oda H, Kastner D L. Genomics, biology, and human illness: advances in the monogenic autoinflammatory diseases[J]. Rheum Dis Clin North Am, 2017, 43(3): 327-45. doi:10.1016/j.rdc.2017.04.011 |
| [23] |
Duong B H, Onizawa M, Oses-Prieto J A, et al. A20 restricts ubiquitination of pro-interleukin-1beta protein complexes and suppresses NLRP3 inflammasome activity[J]. Immunity, 2015, 42(1): 55-67. doi:10.1016/j.immuni.2014.12.031 |
| [24] |
De Wilde K, Martens A, Lambrecht S, et al. A20 inhibition of STAT1 expression in myeloid cells: a novel endogenous regulatory mechanism preventing development of enthesitis[J]. Ann Rheum Dis, 2017, 76(3): 585-92. doi:10.1136/annrheumdis-2016-209454 |
| [25] |
Lee S H, Lee H R, Kwon J Y, et al. A20 ameliorates inflammatory bowel disease in mice via inhibiting NF-kappaB and STAT3 activation[J]. Immunol Lett, 2018, 198: 44-51. doi:10.1016/j.imlet.2018.03.015 |