

梅俏(1971-),男,博士,主任医师,教授,博士生导师,研究方向:炎症性肠病,E-mail:meiqiaomq@aliyun.com。
炎症性肠病(inflammatory bowel disease, IBD)是一种病因尚不完全明确的慢性肠道炎症性疾病。IBD的发病机制可能与遗传、感染、环境、免疫等因素有关,其中,黏膜免疫异常在IBD的持续肠道炎症过程中具有重要作用[1]。
IBD治疗的主要方向是恢复促炎因子与抗炎因子之间的平衡[1],调节肠道黏膜免疫异常。在肠道免疫功能的调节过程中,炎症小体的活化发挥重要影响,其中NOD样受体家族3(NOD-like receptor protein 3, NLRP3)炎症小体是目前研究最广泛的炎症小体,参与了炎症性疾病的发生、发展。Zhang等[2]研究发现,NLRP3基因多态性与IBD风险增加有关。NLRP3炎症小体是一种多蛋白复合物,负责IL-1β和IL-18的蛋白水解成熟和分泌。NLRP3炎症小体由NLRP3、凋亡相关斑点样蛋白[apoptosis associated speck-like protein containing a caspase activation and recruitment domain(CARD),ASC]和胱天蛋白酶1(caspase-1)组成,被激活时,NLRP3受体通过ASC聚合并募集和活化pro-caspase-1,活化的caspase-1切割无活性的pro-IL-1β和pro-IL-18,并以成熟形式分泌,加重IBD中肠道炎症过程[3]。
炎症消退是炎症过程的重要调控机制,由一系列抗炎介质控制,其中消退素D1(resolvin D1,RvD1)是体内重要的促炎症消退因子。RvD1最早由小鼠腹腔炎性渗出物中分离,是由ω3-二十二碳六烯酸(DHA)衍生的内源性抗炎和促进炎症消退的脂质分子。RvD1发挥限制中性粒细胞黏附与浸润、限制炎症损伤等作用[4]。Bento等[5]、Norling等[6]在结肠炎、关节炎等方面研究均证明RvD1可以改善组织炎症,保护相关器官功能,但RvD1抗结肠炎的具体机制尚不十分清楚。因此,本研究通过探讨RvD1对结肠炎小鼠肠道炎症过程中NLRP3信号通路的影响,为RvD1抗结肠炎作用提供实验依据。
1 材料 1.1 实验动物C57BL/6小鼠32只,♂,6~8周龄,体质量(18~22) g,购自安徽省动物中心,No.34000200001280。实验前适应性饲养1周,温度(20~26) ℃,相对湿度40%~70%。
1.2 试剂葡聚糖硫酸钠(dextran sodium sulfate, DSS),美国Sigma公司|RvD1,美国Cayman公司|髓过氧化物酶(myeloperoxidase,MPO)试剂盒,南京建成生物工程研究所|IL-1、IL-6、IL-10、TNF-α试剂盒,均购自武汉新启迪生物科技有限公司|抗诱导型一氧化氮合酶(inducible nitric oxide synthase,iNOS)、NLRP3、ASC、caspase-1 p20、IL-1β、pro-IL-1β抗体,均购自Bioss生物科技有限公司|抗β-actin抗体,北京中杉生物科技有限公司|DNA合成试剂盒,美国Thermo Scientific公司|QuantiNova SYBR Green PCR试剂盒,德国Qiagen公司。
1.3 仪器EPS 300型电泳仪(上海天能科技有限公司)|TS-1000水平摇床(海门市其林贝尔仪器制造有限公司)|K960型PCR仪(杭州晶格科学仪器有限公司)|PikoReal 96型荧光定量PCR仪(Thermo Scientific公司)|高速台式冷冻离心机(安徽嘉文仪器装备有限公司)|Elx800型酶标仪(美国Bio-Tek公司)|752N型可见紫外分光光度计(上海精密科学仪器有限公司)。
2 方法 2.1 模型的制备与实验分组按Chu等[7]方法,使用DSS建立小鼠实验性结肠炎模型。实验分为4组:A组为正常组,小鼠自由饮水,并腹腔注射生理盐水|B组为RvD1对照组,小鼠自由饮水并腹腔注射RvD1|C组为DSS模型组,小鼠给予5% DSS溶液自由饮用,并腹腔注射生理盐水|D组为RvD1给药组,小鼠给予5% DSS溶液自由饮用,并腹腔注射RvD1。将RvD1溶于生理盐水,分别于d 2、4、6进行小鼠腹腔注射(50 μg·kg-1)。实验d 8处死所有小鼠,分离血清于-80 ℃保存,同时收集小鼠小肠和结肠组织,待测样品液氮储存。
2.2 结肠炎程度评估实验期间每天观察小鼠体质量、大便性状和便血情况,进行疾病活动指数(disease activity index,DAI)评分[8]。大便隐血检测采用潜血检测试纸进行。将取出的结肠组织用福尔马林固定并石蜡包埋,切片厚4 μm,HE染色,进行组织学指数(histological index,HI)评分[9]。用生理盐水制备10%结肠组织匀浆。按ELISA试剂盒说明,检测结肠组织匀浆中MPO活性。
2.3 小肠黏膜通透性检测按文献方法[10]制备小肠肠囊,注入伊文思蓝0.2 mL,置于20 mL Krebs液烧杯中,95% O2 37 ℃水浴,30 min后取出肠囊组织,生理盐水冲洗肠腔,37 ℃干燥,加入1 mL甲酰胺溶液,50 ℃孵育24 h,取出肠组织,溶液离心沉淀,取上清液进行紫外分光光度计检测,检测波长为655 nm。
2.4 透射电镜观察将小肠组织于2.5%戊二醛中4 ℃固定6 h,1%锇酸固定,梯度浓度乙醇脱水,环氧树脂包埋,70 nm切片,JEM-1230F电子显微镜观察小鼠小肠黏膜上皮细胞连接情况。
2.5 结肠组织中IL-1、IL-6、IL-10和TNF-α水平测定按ELISA试剂盒说明书,检测小鼠结肠组织中IL-1、IL-6、IL-10和TNF-α水平。
2.6 Western blot检测结肠组织中相关蛋白的表达从结肠组织中提取蛋白质,使用SDS-PAGE分离,并转移至PVDF膜。在室温下用封闭液(5%脱脂乳)封闭2 h。将膜与一抗在4 ℃孵育过夜,一抗包括ASC、NLRP3、caspase-1、IL-1β、pro-IL-1β、iNOS(1 :300)及β-actin(1 :1 000)。TBST洗涤,将HRP连接的二抗在室温下与膜孵育2 h。再次洗涤,使用ECL蛋白质印迹检测系统和ImageJ软件检测分析结果。
2.7 qPCR检测小鼠结肠组织IL-1β、iNOS mRNA表达使用TRIzol试剂从巨噬细胞和结肠组织中提取总RNA。用RevertAidTM M-MuLV逆转录酶进行逆转录,合成DNA第一链,并按DNA合成试剂盒的说明,将RNA逆转录成cDNA。使用QuantiNova SYBR Green PCR试剂盒扩增获得的cDNA用于定量PCR。以β-actin作为内参,测量目的基因相对表达。引物序列(正向和反向)为:β-actin:5′-AGTGTG ACGTTGACATCCGT-3′和5′-TGCTAGGAGCCAGAG CAGTA-3′; iNOS:5′-CCTTGTTCAGCTACGCCTTC-3′和5′-CTTCAGAGTCTGCCCATTGC-3′; IL-1β:5′-GA AGAAGAGCCCATCCTCTG-3′和5′-TCATCTCGGAGC CTGTAGTG-3′。
2.8 统计学方法所有数据均用SPSS 22软件进行统计分析,数据采用x±s表示,组间比较采用单因素方差分析。
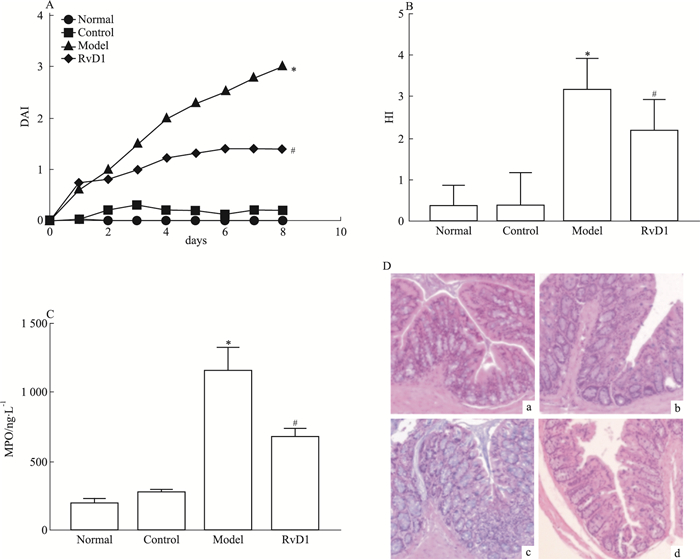
3 结果 3.1 RvD1对结肠炎小鼠肠道炎症的影响与正常组小鼠相比,模型组小鼠DAI评分、HI评分、MPO水平明显升高(Fig 1A、1B、1C),病理可见结肠中大量中性粒细胞浸润,隐窝明显减少,并累及部分上皮细胞(Fig 1D)|RvD1组小鼠DAI评分、HI评分及MPO水平明显降低,病理可见结肠中性粒细胞浸润减少,隐窝数量基本正常,表明RvD1可以改善DSS结肠炎小鼠中结肠炎症损伤程度。
|
| Fig 1 Effect of RvD1 on colonic inflammation in DSS-induced colitis mice(x±s, n=8) A:DAI scoring; B: HI scoring; C: MPO activity; D: Histopathologic features of the colon. a: Normal group; b: RvD1 control group; c: Model group; d: RvD1 group.*P < 0.05 vs normal group; #P < 0.05 vs model group. |
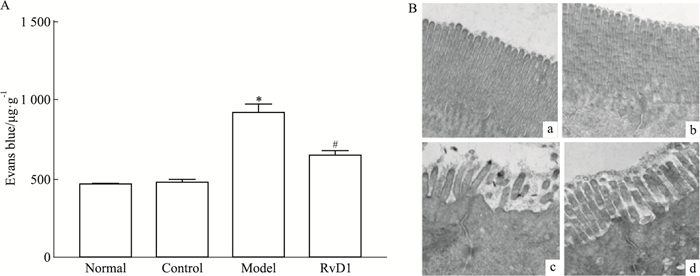
如Fig 2所示,与正常组小鼠相比,模型组小鼠小肠肠囊中伊文思蓝浓度明显上升,电镜可见小肠上皮细胞绒毛杂乱,密度不均,细胞间连接增宽|RvD1组小鼠小肠肠囊中伊文思蓝浓度降低,电镜可见上皮绒毛稍稀疏,但排列规整,细胞间隙基本正常,表明RvD1可改善DSS引起的小鼠小肠结构和功能破坏。
|
| Fig 2 Effect of RvD1 on intestinal barrier function and structure in DSS-induced colitis mice A: Evans blue test(±s, n=8).*P < 0.05 vs normal group; #P < 0.05 vs model group. B: Electron microscopy. a: Normal group; b: RvD1 control group; c: Model Group; d: RvD1 group. |
Tab 1结果显示,与正常组小鼠相比,模型组小鼠结肠组织中IL-1、IL-6、TNF-α水平增高,IL-10水平降低|与模型组小鼠相比,RvD1组小鼠结肠组织中IL-1、IL-6、TNF-α水平降低,IL-10水平增加。提示RvD1可调节DSS结肠炎小鼠肠黏膜中细胞因子水平,发挥抗结肠损伤作用。
| Group | IL-1 | IL-6 | IL-10 | TNF-α |
| Normal | 150.06±18.14 | 71.63±7.71 | 112.87±8.57 | 119.41±16.92 |
| RvD1 control | 157.21±14.81 | 70.8±10.26 | 110.13±13.64 | 113.04±13.52 |
| Model | 594.16±34.21* | 389.98±31.95* | 59.42±3.44* | 516.46±48.48* |
| RvD1 | 293.65±72.78# | 245.68±34.21# | 78.69±4.48# | 208.64±16.16# |
| *P < 0.05 vs normal; #P < 0.05 vs model | ||||
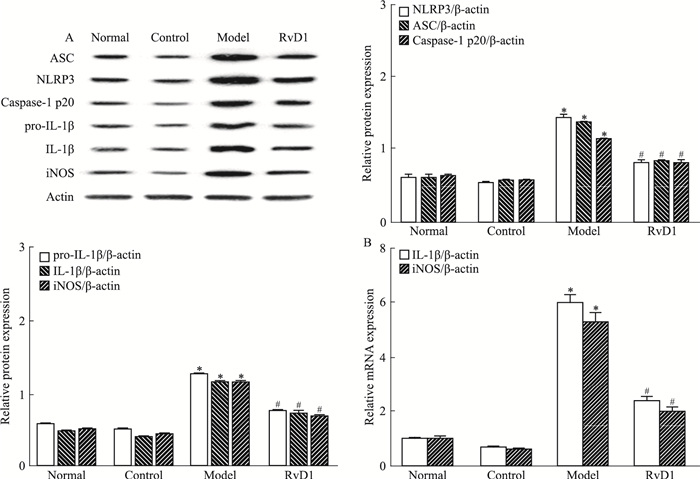
通过Western blot及qPCR检测结肠炎小鼠结肠NLRP3炎症小体相关标志物,包括ASC、NLRP3、IL-1β、pro-IL-1β、iNOS、caspase-1 p20。如Fig 3所示,与正常组小鼠比较,模型组小鼠结肠中ASC、NLRP3、IL-1β、pro-IL-1β、iNOS、caspase-1p20水平升高|与模型组小鼠比较,RvD1组小鼠结肠中ASC、NLRP3、IL-1β、pro-IL-1β、iNOS、caspase-1 p20水平降低。表明RvD1可降低NLRP3炎症小体信号通路中主要标志物的表达水平,改善结肠炎小鼠肠道炎症程度。
|
| Fig 3 Effect of RvD1 on expressions of NPRP3 pathway-related proteins(A) and mRNA(B) in DSS-induced colitis mice(±s, n=8) *P < 0.05 vs normal group, #P<0.05 vs model group |
IBD治疗药物包括氨基水杨酸制剂、糖皮质类激素、免疫抑制剂和各种生物制剂(如TNF-α单抗等),这些药物长期使用会引起明显的副作用,如激素依赖、骨髓抑制和严重感染。因此,探讨更为安全有效的抗结肠炎药物是目前IBD研究的热点之一。
RvD1作为消退素家族中的一员,在体内起到重要的抗炎作用,其机制与限制中性粒细胞黏附与浸润有关[4]。相关研究证实RvD1具有改善组织炎症,保护器官功能的作用[5-6],但RvD1抗结肠炎的具体机制尚不十分清楚。本研究结果显示,腹腔注射RvD1可明显降低实验性结肠炎小鼠的DAI和HI评分,降低结肠组织中MPO水平。同时发现RvD1具有维持肠上皮完整性和通透性的作用。表明RvD1可以有效改善实验性小鼠结肠炎的炎症损伤。另外,RvD1可以降低结肠组织中IL-1、IL-6、TNF-α水平,升高IL-10水平,发挥调节细胞因子水平的作用。
IL-1β在结肠炎症的促炎因子释放中起重要作用,可以上调IL-6、TNF-α等促炎因子的表达,扩大和加重结肠炎症损伤。NLRP3炎症小体作为IL-1β成熟释放的关键信号通路[11],在肠道内稳态和炎症中起重要作用,有研究显示DSS可以激活巨噬细胞NLRP3炎症小体,用DSS或TNBS处理的NLRP3-/-小鼠结肠炎症减轻,结肠组织中促炎细胞因子水平较低[12-13]。本研究发现,DSS模型组中NLRP3、ASC、caspase-1 p20表达量均明显增加,IL-1β、iNOS水平增加|RvD1可以降低结肠炎小鼠结肠组织中NLRP3、ASC、caspase-1 p20、IL-1β、iNOS表达,表明RvD1具有通过抑制NLRP3炎症小体的活化,抑制促炎因子合成,改善小鼠结肠炎症的作用。目前,有关NLRP3炎症小体在实验性结肠炎中的作用存在一定争论。有研究显示,NLRP3-/-小鼠对实验性结肠炎更敏感[14-15],原因可能为NLRP3作为先天性免疫的的重要组成部分,起到维持肠内稳态的关键作用,当NLRP3功能缺失,造成肠道微生物紊乱引起的黏膜损伤,是IBD可能的致病机制之一,经过抗生素处理的NLRP3-/-小鼠结肠炎症减轻[15]。
综上所述,本研究发现RvD1可以减轻DSS结肠炎小鼠结肠炎症的严重程度,保护肠道屏障功能,其机制可能与抑制NLRP3炎症小体活化,调控促炎细胞因子表达有关,提示RvD1可作为治疗IBD治疗的潜在候选药物。
| [1] |
Powell N, Lo J W, Biancheri P, et al. Interleukin 6 increases production of cytokines by colonic innate lymphoid cells in mice and patients with chronic intestinal inflammation[J]. Gastroenterology, 2015, 149(2): 456-67. doi:10.1053/j.gastro.2015.04.017 |
| [2] |
Zhang Q, Fan H W, Zhang J Z, et al. NLRP3 rs35829419 polymorphism is associated with increased susceptibility to multiple diseases in humans[J]. Genet Mol Res, 2015, 14(4): 13968-80. doi:10.4238/2015.October.29.17 |
| [3] |
Song-Zhao G X, Srinivasan N, Pott J, et al. Nlrp3 activation in the intestinal epithelium protects against a mucosal pathogen[J]. Mucosal Immunol, 2014, 7(4): 763-74. doi:10.1038/mi.2013.94 |
| [4] |
Hsiao H M, Sapinoro R E, Thatcher T H, et al. A novel anti-inflammatory and pro-resolving role for resolvin D1 in acute cigarette smoke-induced lung inflammation[J]. PLoS One, 2013, 8(3): e58258. doi:10.1371/journal.pone.0058258 |
| [5] |
Bento A F, Claudino R F, Dutra R C, et al. Omega-3 fatty acid-derived mediators 17(R)-hydroxy docosahexaenoic acid, aspirin-triggered resolvin D1 and resolvin D2 prevent experimental colitis in mice[J]. J Immunol, 2011, 187(4): 1957-69. doi:10.4049/jimmunol.1101305 |
| [6] |
Norling L V, Headland S E, Dalli J, et al. Proresolving and cartilage-protective actions of resolvin D1 in inflammatory arthritis[J]. JCI Insight, 2016, 1(5): e85922. |
| [7] |
Chu C C, Hou Y C, Pai M H, et al. Pretreatment with alanyl-glutamine suppresses T-helper-cell-associated cytokine expression and reduces inflammatory responses in mice with acute DSS-induced colitis[J]. J Nutr Biochem, 2012, 23(9): 1092-9. doi:10.1016/j.jnutbio.2011.06.002 |
| [8] |
Okayasu I, Hatakeyama S, Yamada M, et al. A novel method in the induction of reliable experimental acute and chronic ulcerative colitis in mice[J]. Gastroenterology, 1990, 98(3): 694-702. doi:10.1016/0016-5085(90)90290-H |
| [9] |
Murano M, Maemura K, Hirata I, et al. Therapeutic effect of intracolonically administered nuclear factor kappa B(p65) antisense oligonucleotide on mouse dextran sulphate sodium(DSS)-induced colitis[J]. Clin Exp Immunol, 2000, 120(1): 51-8. doi:10.1046/j.1365-2249.2000.01183.x |
| [10] |
Laharie D, Ménard S, Asencio C, et al. Effect of rebamipide on the colonic barrier in interleukin-10-deficient mice[J]. Dig Dis Sci, 2007, 52(1): 84-92. doi:10.1007/s10620-006-9183-4 |
| [11] |
卞芳, 金 肆.. NLRP3炎症小体在动脉粥样硬化相关细胞中作用的研究进展[J]. 中国药理学通报, 2016, 32(2): 163-9. Bian F, Jin S. Research progress of NLRP3 inflammasome in atherosclerosis-related cells[J]. Chin Pharmacol Bull, 2016, 32(2): 163-9. doi:10.3969/j.issn.1001-1978.2016.02.004 |
| [12] |
Bauer C, Duewell P, Mayer C, et al. Colitis induced in mice with dextran sulfate sodium (DSS) is mediated by the NLRP3 inflammasome[J]. Gut, 2010, 59(9): 1192-9. doi:10.1136/gut.2009.197822 |
| [13] |
Wang Y, Wang H, Qian C, et al. 3-(2-Oxo-2-phenylethylidene)-2, 3, 6, 7-tetrahydro-1H-pyrazino[2, 1-a]isoquinolin-4(11bH)-one(compound 1), a novel potent Nrf2/ARE inducer, protects against DSS-induced colitis via inhibiting NLRP3 inflammasome[J]. Biochem Pharmacol, 2016, 101: 71-86. doi:10.1016/j.bcp.2015.11.015 |
| [14] |
Hirota S A, Ng J, Lueng A, et al. NLRP3 inflammasome plays a key role in the regulation of intestinal homeostasis[J]. Inflamm Bowel Dis, 2011, 17(6): 1359-72. doi:10.1002/ibd.21478 |
| [15] |
Zaki M H, Boyd K L, Vogel P, et al. The NLRP3 inflammasome protects against loss of epithelial integrity and mortality during experimental colitis[J]. Immunity, 2010, 32(3): 379-91. doi:10.1016/j.immuni.2010.03.003 |
