

2. 石河子大学 新疆农垦科学院畜牧兽医研究所,新疆 石河子 832000
张云生(1976-),男,博士,副研究员,研究方向:基因检测,通讯作者,E-mail:xmszys@163.com
2. the Research Institute of Animal Husbandry and Veterinary, Xinjiang Agricultural Reclamation Academy, Shihezi Xinjiang 832000, China
菊苣(Cichorium intybus L.)为药食同源的菊科菊苣属植物,是我国维吾尔医习用药材。维名“卡申纳”(kasina),其性味微苦、咸、凉,有清肝利胆、健胃消食、利尿消肿之功效,用于治疗湿热黄疸、胃痛食少、水肿尿少等病症[1]。菊苣含有倍半萜类、黄酮类、香豆素类、有机酸类、糖类等多种活性成分[2],其根部含菊粉高达15%~20%,可做为食品添加成份[3]。另外,还含有山莴苣素、山莴苣苦素、绿原酸等成分,均具有抗菌消炎作用[4]。
有些药用植物,多个部位可以同时入药的,大多数存在药效相似性,但入药部位的疗效却不尽相同。菊苣的根、茎做为植物的不同器官,含有的活性成分亦有所不同,但均具有一定的抑菌作用[5-6]。目前,已报道的菊苣抑菌药效研究仅针对其中的单一部位,而对两者之间抑菌效果差异性却并不清楚,使药用部位的选择缺乏有效参考依据。本文从抑菌圈、最小抑菌浓度(minimum inhibitory concentration,MIC)、生长曲线等方面,对菊苣根、菊苣茎提取物的抑菌效果进行比较分析,为明确菊苣更有效的抑菌部位提供参考。
1 材料 1.1 药物与试剂菊苣根、茎(批号:20151013、20151101),均购自新疆麦迪森维药有限公司饮片厂;营养琼脂(批号:20170818)、营养肉汤(nutrient broth, NB,批号:20160112),均购自青岛高科园海博生物技术有限公司;2,3,5-三苯基氯化四氮唑(TTC)(批号:717J032),购自北京索莱宝科技有限公司;碱性磷酸酶(alkaline phosphatase, AKP)测试盒(批号:20180614),购自南京建成生物工程研究所。
1.2 仪器恒温培养箱(Sheldon Manufacturing); SKY-100B型恒温摇床(上海天呈实验仪器制造有限公司);Vs-840-1超净工作台(上海博讯实业有限公司医疗设备厂);3001型全波长扫描多功能读数仪(美国Thermo Fisher);5426XG型离心机(德国Eppendorf)。
1.3 菌种金黄色葡萄球菌、粪肠球菌,均由新疆医科大学微生物实验室赠予。
2 方法 2.1 菊苣根、茎乙醇提取液的制备分别称取干燥的菊苣根、茎各100 g,粉碎后放入圆底烧瓶,加95%乙醇1000 mL,浸泡24 h后,在80 ℃水浴锅中回流浸提,每次2 h,回流3次。收集3次滤液,用旋转蒸发仪旋转浓缩至10 g,得供试品浸膏(1 g相当于10 g生药量)备用。
2.2 供试液的制备称取一定量的供试品浸膏,用DMSO溶解后,配制成不同浓度的供试液[7]。
2.3 菌悬液的制备在超净台中,用接种环将冻存的供试菌种接种至营养琼脂平板上,在恒温培养箱中37 ℃培养24 h。再挑取单个菌落接种于NB培养基内,37 ℃、180 r·min-1振荡培养24 h,得所需菌悬液。
2.4 抑菌活性研究 2.4.1 牛津杯法测定抑菌圈直径[8]将0.1 mL菌悬液加入到营养琼脂平板上均匀涂布,再用无菌镊子将灭菌的牛津杯(内径6 mm,外径8 mm,高10 mm的不锈钢杯)放在含菌培养基上,往杯中加入0.1 mL供试药液,使用DMSO作阴性对照,青霉素(6 g·L-1)作阳性对照,放入恒温培养箱中37 ℃培养24 h后,测量抑菌圈直径。
2.4.2 二倍稀释法测定MIC[9]取无菌96孔板,每孔加入营养肉汤培养基(含1% TTC)0.1 mL,在第1孔加入已知浓度的供试药液0.1 mL,充分混匀后,吸取0.1 mL加入第2孔充分混匀,照此重复至第7孔,吸取0.1 mL弃去,再在1~7孔各加入0.02 mL的菌液。第8孔只加菌液,作细菌对照,第9孔只加供试药液,作为供试药液对照。然后将96孔板放入恒温培养箱中37 ℃培养24 h,观察培养基的颜色变化。
2.5 菊苣根、茎95%乙醇提取物对供试菌生长动力学影响依据文献[10]采用生长曲线法观察细菌生长状况。将金黄色葡萄球菌菌悬液分别转接到含浓度为12.5、25、50 g·L-1的菊苣根、茎提取物的营养肉汤培养基中(粪肠球菌时药物浓度为16、32、64 g·L-1),调整初始菌量为106 CFU·L-1,未处理的菌悬液作为空白对照,6 g·L-1青霉素作为阳性对照。37 ℃、180 r·min-1振荡培养。每2 h用酶标仪测量样品在600 nm处的光密度值(OD值),以绘制生长曲线。
2.6 菊苣根、茎95%乙醇提取物对供试菌细胞壁的影响按照“2.4.3”的方法对细菌进行前处理,按照文献[10]方法,37 ℃、180 r·min-1振荡孵育,每隔1 h取样0.5 mL,4 500 r·min-1离心10 min,取上清,用AKP试剂盒测定上清液中AKP浓度。
2.7 菊苣根不同溶剂萃取物的制备干燥的菊苣根500 g粉碎,95%乙醇50 ℃浸泡5次,每次3 d,真空浓缩得到浸膏(1 g相当于10 g生药量),再将浸膏用25 ℃蒸馏水混匀,依次用石油醚、乙酸乙酯、正丁醇与水1 :1萃取,常温挥发溶剂后得到石油醚部位、乙酸乙酯部位、正丁醇部位及水层萃取物[11]。
2.8 统计学分析采用GraphPad Prism 6.0软件对实验数据进行绘图及分析,每组数值经过3次独立实验取平均值,数据表示为x±s,并用单向ANOVA分析。
3 结果 3.1 菊苣根、茎对抑菌圈直径的影响菊苣根、茎提取物对金黄色葡萄球菌、粪肠球菌均有较强的抑菌作用,见Tab 1。
| Group | Average diameter of inhibition zone | |
| Staphylococcus aureus | Enterococcus faecalis | |
| 95% ethanol extract of chicory roots | 11.67±0.33 | 12.00±0.58 |
| 95% ethanol extract of chicory stems | 12.33±0.33 | 12.00±1.00 |
| DMSO | - | - |
| Penicillin | 26.67±0.47 | 22.67±0.94 |
| “-” is no inhibition zone. Extract concentration is 500 g·L -1, penicillin concentration is 6 g·L -1. | ||
菊苣茎95%乙醇提取物对金黄色葡萄球菌、粪肠球菌的MIC值分别为50 g·L-1、64 g·L-1;菊苣根95%乙醇提取物对金黄色葡萄球菌、粪肠球菌的MIC值均为64 g·L-1。
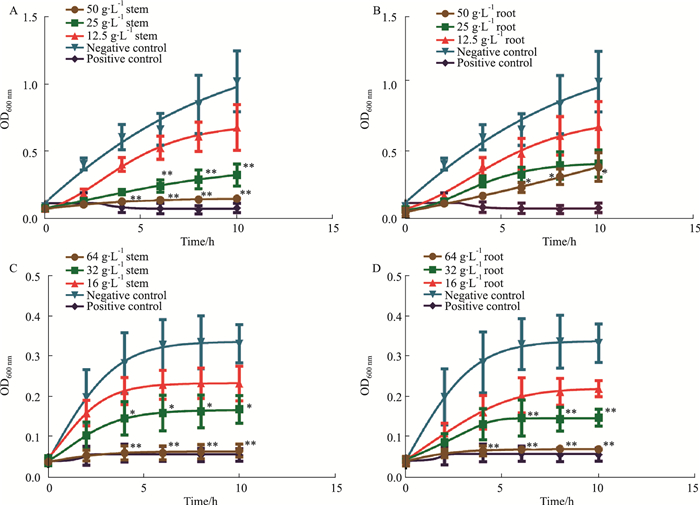
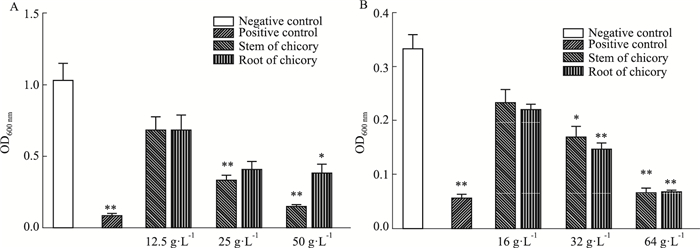
3.3 菊苣根、茎对金黄色葡萄球菌和粪肠球菌生长动力学的影响与空白对照组相比,菊苣茎提取物浓度为25、50 g·L-1时,对金黄色葡萄球菌增殖具有明显的抑制作用(P < 0.01,Fig 1A);菊苣根提取物浓度为50 g·L-1时,对金黄色葡萄球菌增殖也具有明显的抑制作用(P < 0.05,Fig 1B)。菊苣茎提取物浓度为64 g·L-1时,对粪肠球菌增殖具有明显抑制作用(P < 0.01),浓度为32 g·L-1时,对粪肠球菌增殖也有明显的抑制作用(P < 0.05),见Fig 1C);菊苣根提取物浓度为64、32 g·L-1时,对粪肠球菌皆具有明显抑制增殖作用(P < 0.01,Fig 1D)。为了更直观地对比根、茎对金黄色葡萄球菌和粪肠球菌的抑制效果,本研究比较了提取物处理10 h后的菌液OD值,Fig 2结果表明,菊苣茎提取物对金黄色葡萄球菌抑制效果较好,而菊苣根提取物则对粪肠球菌抑制作用较好。
|
| Fig 1 Growth curve (x±s, n = 3) A: Staphylococcus aureus; B: Staphylococcus aureus; C: Enterococcus faecalis; D: Enterococcus faecalis. *P < 0.05, **P < 0.01 vs negative control. |
|
| Fig 2 Optical density value of bacterial suspension (x±s, n = 3) A: Staphylococcus aureus; B: Enterococcus faecalis. *P < 0.05, **P < 0.01 vs negative control. |
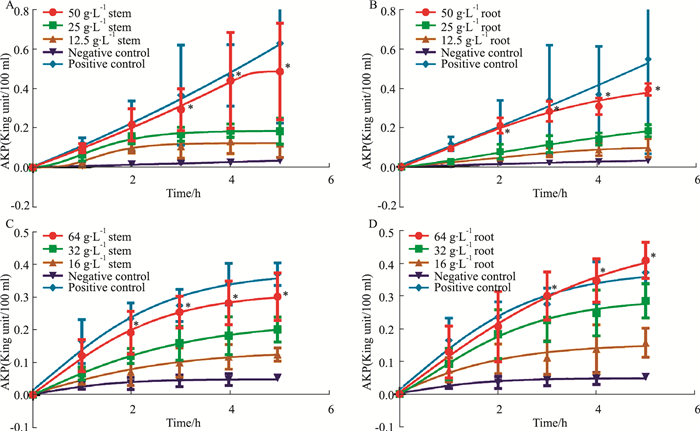
菊苣根、茎提取物对金黄色葡萄球菌和粪肠球菌的胞外AKP浓度均有明显的影响。如Fig 3所示,在50 g·L-1的菊苣根、茎提取物处理下,金黄色葡萄球菌、粪肠球菌胞外溶液AKP含量明显增加(P < 0.05)。结果表明,菊苣根、茎提取物对两种菌的细胞壁均有破坏作用,造成金黄色葡萄球菌和粪肠球菌细胞壁通透性增加,细胞内AKP渗出。
|
| Fig 3 Changes of concentration of AKP in bacterial suspension (x±s, n = 3) A: Staphylococcus aureus; B: Staphylococcus aureus; C: Enterococcus faecalis; D: Enterococcus faecalis. *P < 0.05 vs negative control. |
Tab 2结果显示,与菊苣根95%乙醇提取物相比,正丁醇萃取物、乙酸乙酯萃取物在浓度为200 g·L-1时,对金黄色葡萄球菌抑制作用均明显增强(P < 0.01);乙酸乙酯部位对粪肠球菌抑制作用也明显增强(P < 0.01),正丁醇萃取物抑菌效果与95%乙醇提取物抑菌效果没有差异;石油醚萃取物对上述两种菌均没有抑制作用。
| Group | Average diameter of inhibition zone | |
| Staphylococcus aureus | Enterococcus faecalis | |
| 95% ethanol extract of chicory roots | 10.67±0.33 | 9.00±0.47 |
| Petroleum ether extract of chicory roots | - | - |
| Ethyl acetate extract of chicory roots | 14.67±0.33** | 11.33±0.33** |
| N-butanol Extracts of chicory roots | 13.33±0.33** | 10.00±0.00 |
| DMSO | - | - |
| Penicillin | 23.87±0.47 | 22.67±0.94 |
| “-” is no inhibition zone. Test sample concentration is 200 g·L-1, penicillin concentration is 6 g·L-1. **P < 0.01 vs 95% ethanol extract of chicory roots. | ||
据报道,菊苣根比菊苣茎部位含有更多的山莴苣素和山莴苣苦素,而菊苣茎中则含有较多的秦皮乙素和绿原酸[3],另外,菊苣茎中总黄酮含量超过菊苣根中的含量[12-13],药物活性成分的差异,导致两者药效的天然差别。本实验从绘制的生长曲线可以看出,金黄色葡萄球菌对菊苣茎的处理较为敏感,粪肠球菌对菊苣根的处理更为敏感。当细菌受到药物处理后,细胞外部完整性被破坏,会造成菌体内AKP渗出[10]。细胞外溶液AKP浓度的变化表明,菊苣根、菊苣茎提取物会破坏细胞膜结构的完整性,造成细菌内容物渗出,导致了细菌的死亡。
为了进一步明确菊苣根的有效抑菌成分,本研究用不同溶剂对菊苣根95%乙醇提取物再进行萃取,分析不同极性萃取物的抑菌活性,结果显示,菊苣根乙酸乙酯萃取物对金黄色葡萄球菌和粪肠球菌的抑菌圈直径最大,抑菌效果最为明显。乙酸乙酯属于中等极性萃取溶剂,推测其萃取物中可能含有游离生物碱、萜类、有机酸、黄酮、香豆素苷元等,而萜类化合物正是具有杀菌、消炎、抗肿瘤的生物活性物质[14]。山莴苣苦素是菊苣根中的主要成分之一,为萜类化合物,因此,推测菊苣根、菊苣茎含有的主要有效抑菌成分可能为山莴苣苦素。
( 致谢: 本实验中菊苣提取实验在石河子大学新疆特种植物药资源省部共建教育部重点实验室完成,抑菌实验在新疆农垦科学院畜牧兽医研究所完成。感谢各位老师和同学对实验的帮助!)
| [1] |
国家药典委员会. 中华人民共和国药典:一部[M]. 北京: 中国医药科技出版社, 2015. National Parmacopoeia Commission. Chinese Pharmacopoeia One[M]. Beijing: China Medical Science Press, 2015: 310. |
| [2] |
再娜布·吐合达洪, 仲婕, 信学蕾, 等. 毛菊苣药材不同部位主要活性成分含量[J]. 中国中药杂志, 2010, 35(8): 1018-21. Zai N P, Zhong J, Xin X L, et al. Comparative studies in content of majoractive compositions in different parts of Cichorium glandulosum[J]. China J Chin Mater Med, 2010, 35(8): 1018-21. |
| [3] |
张泽生, 卢亚莉, 张云轩, 等. 菊苣中苦味物质的研究进展[J]. 中国食品添加剂专论综述, 2015, 26(5): 174-8. Zhang Z S, Gao Y F, Zhang Y X, et al. Advances in research on bitter substances in chicory[J]. China Food Additives, 2015, 26(5): 174-8. |
| [4] |
Ahmed B, alhowiriny T A, Siddiqui A B, et al. Antihepatotoxic activity of seeds of Cichorium lntybus[J]. J Ethnopharmacol, 2003, 7(2): 237-40. |
| [5] |
徐雅梅, 呼天明, 杨亚丽, 等. 菊苣根提取物的抑菌活性研究[J]. 西北植物学报, 2006, 26(3): 615-9. Xu Y M, Hu T M, Yang Y L, et al. Study on antibacterial activity of chicory root extract[J]. Acta Botanica Boreali-Occidentalia Sin, 2006, 26(3): 615-9. doi:10.3321/j.issn:1000-4025.2006.03.031 |
| [6] |
吐尔逊娜依·迪力夏提, 穆拉丁·库热西, 阿不都拉·阿巴斯.菊苣茎乙醇提取物抑菌活性研究[J].食品科学, 2009, 30(11): 80-2.
|
| [7] |
胡君茹, 姜华, 李喜香. 三种非水溶性供试品溶剂对抑菌试验效果的影响[J]. 西部中医药, 2013, 26(11): 30-1. Hu J R, Jiang H, Li X X. Study on three non-water-soluble solvents influencing of inhibitory activity in antibacterial test[J]. Western J Tradit Chin Med, 2013, 26(11): 30-1. |
| [8] |
黄德斌, 胡泽华, 余昭芬, 等. 马桑水提取物对烧伤创面感染常见3种耐药菌的抑制作用[J]. 中国药理学通报, 2016, 32(10): 1388-94. Huang D B, Hu Z H, Yu Z F, et al. Inhibition of Coriaria Sinica Maxim's extract on burn wound infections with common three kinds of resistant bacteria[J]. Chin Pharmacol Bull, 2016, 32(10): 1388-94. doi:10.3969/j.issn.1001-1978.2016.10.012 |
| [9] |
王倩, 谢明杰. 木犀草素对金黄色葡萄球菌的抑菌活性及其机制[J]. 微生物学报, 2010, 50(9): 1180-4. Wang Q, Xie M J. Antibacterial activity and mechanism of Luteolin on Staphylococcus aureus[J]. Acta Microbiol Sin, 2010, 50(9): 1180-4. |
| [10] |
李婷, 杨舒然, 何聪芬, 等. 姜厚朴水提物对大肠杆菌和金黄色葡萄球菌的抑菌机理研究[J]. 现代食品科技, 2016, 32(2): 84-92. Li T, Yang S R, He C F, et al. Antibacterial mechanism of Ginger Mix-fried Magnolia Bark extract against Escherichia coli and Staphylococcus aureus[J]. Mod Food Sci Technol, 2016, 32(2): 84-92. |
| [11] |
李广胜, 鲁光华, 陈宁, 等. 胡颓子叶不同提取物药理活性的比较研究[J]. 中国药理学通报, 2014, 30(8): 1181-2. Li G S, Lu G H, Chen N, et al. A comparative study on the pharmacological effects of different extract from Elaeagnus pungens Thunb[J]. Chin Pharmacol Bull, 2014, 30(8): 1181-2. doi:10.3969/j.issn.1001-1978.2014.08.030 |
| [12] |
热阳古·阿布拉, 热比古丽·依敏, 木尼热·阿不都克里木. 维吾尔医药材菊苣不同器官总黄酮含量的对比研究[J]. 喀什大学学报, 2017, 38(3): 48-50. ReYangGu·Abula, ReBiGuLi·Yimin, MuNiRe·Abudukelimu. Comparative study on total flavonoids content in different organs of chicory of Uyghur medicinal[J]. J Kashgar Univ, 2017, 38(3): 48-50. |
| [13] |
阿布力米提, 艾来提, 迪丽努尔, 等. 菊苣基生叶中总黄酮提取工艺的研究[J]. 生物技术, 2008, 18(6): 63-5. Ablimit, Ayrat, Dilnur, et al. Study on flavonoid extraction from Cichorium intybus[J]. Biotechnology, 2008, 18(6): 63-5. |
| [14] |
牟玉兰, 闫浩, 龚黎黎. 萜类化合物的研究概况[J]. 化工管理, 2018, 30(11): 12-3. Mou Y L, Yan H, Gong L L. Overview of research on terpenoids[J]. Chem Enterprise Management, 2018, 30(11): 12-3. doi:10.3969/j.issn.1008-4800.2018.11.009 |

