

2. 上海市生物物质成药性评价专业技术服务平台;
3. 上海医药工业研究院创新药物与制药工艺国家重点实验室,上海 200437
2. State Key Lab of New Drug &Pharmaceutical Process, Shanghai Institute of Pharmaceutical Industry;
3. Shanghai Professional and Technical Service Center for Biological Material Druggability Evaluation, Shanghai 200437, China
蛹虫草俗称北虫草,主要含有虫草素、虫草多糖、虫草酸等物质,具有抗肿瘤、抗病毒、抗炎、治疗肾损伤、增强机体免疫力、降血糖等功效[1-4]。Cunningham等[5]首次从蛹虫草中提取到虫草素,并确定其结构为3-脱氧腺苷。研究表明,虫草素能够促进淋巴细胞分泌干扰素-γ,激活自然杀伤细胞和巨噬细胞,增强其杀伤吞噬活性,从而提高机体非特异性免疫功能[6]。
蛹虫草提取精制过程中,提取温度和提取次数均会影响虫草素的得率。因此,本研究中将不同人工培植方法得到的两种虫草子实体——超Ⅴ星虫草和Ⅰ星虫草,直接经粉碎机制备成虫草子实体菌粉,经HPLC(NYT/2116-2012)分析测试发现,超Ⅴ星虫草和Ⅰ星虫草子实体菌粉的虫草素含量分别为1.07×104 mg·kg-1和1.41×103 mg·kg-1,超Ⅴ星虫草子实体菌粉中虫草素的含量为Ⅰ星虫草含量的7.6倍。本文通过检测免疫低下小鼠的巨噬细胞吞噬、自然杀伤细胞杀伤活性、细胞因子分泌水平等,分析比较了超Ⅴ星虫草和Ⅰ星虫草子实体菌粉对机体非特异性免疫功能的调节作用。
1 材料与方法 1.1 实验动物与细胞株SPF级♂BALB/c小鼠50只,体质量(18~20) g,购自上海西普尔-必凯实验动物有限公司,生产许可证号:SCXK(沪)2013-0016。小鼠淋巴瘤细胞YAC-1,由本实验室传代保存。
1.2 药物与试剂蛹虫草子实体-超Ⅴ星(批号S160321P-0,深褐色粉末)、蛹虫草子实体菌粉-Ⅰ星(批号S170603,浅黄色粉末),均由常德炎帝生物工程有限公司提供;蛹虫草菌粉胶囊(吉林省中晟制药有限公司,批号20160101);地塞米松磷酸钠注射液(辰欣药业股份有限公司,批号1705252111)。刀豆球蛋白A(ConA,Sigma,批号SLBM9735V);脂多糖(LPS,Sigma,批号011M4001V);乳酸脱氢酶(lactate dehydrogenase,LDH)试剂盒(南京建成生物工程研究所,批号20180113);小鼠白介素2(interleukin 2,IL-2)ELISA试剂盒(批号K25031872)、肿瘤坏死因子α(tumor necrosis factor α,TNF-α)ELISA试剂盒(批号Q15031805),均购自武汉华美生物工程有限公司;小鼠IL-6 ELISA试剂盒(上海酶联,批号01/2018)。
1.3 仪器Varioskan Flash全波长扫描式多功能读数仪、Legend Micro 21R离心机、370 Series二氧化碳培养箱(Thermo Scientific公司);GI54DWS(50L)全自动高压灭菌锅(Zealway公司);5810R高速离心机(Eppendorf公司);NIB-100普通倒置显微镜(宁波永新光学股份有限公司)。
1.4 模型的制备及分组给药50只BALB/c小鼠随机分为对照组、模型组、超Ⅴ星虫草(1 g·kg-1)组、Ⅰ星虫草(1 g·kg-1)组和虫草胶囊(阳性药,1 g·kg-1)组。动物分组后,持续给药28 d,给药体积为10 mL·kg-1体质量,对照组和模型组灌胃给予等体积的饮用水。除对照组外,其余各组于实验d 22、23腹腔注射地塞米松20 mg·kg-1,期间每周称量动物体质量。末次给药后24 h称重,以各组解剖当日体质量减去地塞米松造模前体质量计算体质量变化值;取血,测血常规;颈椎脱臼处死动物后解剖,取胸腺、脾脏称重,计算胸腺指数和脾脏指数。
1.5 巨噬细胞吞噬中性红实验用DMEM完全培养液将腹腔巨噬细胞调节至1×109·L-1,接种于96孔板,每孔100 μL,置于37 ℃、5% CO2培养箱中培养3 h。弃上清,每孔加DMEM完全培养液100 μL,再加1 g·L-1的中性红水溶液100 μL,置于37 ℃、5% CO2培养箱中培养3 h。弃上清,用PBS冲洗3次,加细胞裂解液过夜,酶标仪于540 nm波长下测OD值。
1.6 自然杀伤(natural killer,NK)细胞杀伤活性测定用含5 g·L-1牛血清蛋白(bull serum albumin,BSA)的RPMI 1640完全培养液,将脾淋巴细胞调至2.5×1010·L-1作为效应细胞,用含5 g·L-1BSA的RPMI 1640培养液将YAC-1细胞调节至5×108·L-1作为靶细胞;向96孔板中分别加入100 μL效应细胞和靶细胞(效应细胞:靶细胞 = 50 :1)悬液,自然释放孔加100 μL的靶细胞和100 μL含5 g·L-1 BSA的RPMI 1640培养液,最大释放孔加100 μL的靶细胞和100 μL 0.2%的NP-40裂解液,置于37 ℃、5% CO2培养箱中培养4 h;低温离心取上清;按照LDH测定试剂盒说明书测定细胞上清液的LDH活性。
NK细胞杀伤活力 = (实验孔OD-自然释放孔OD)/(最大释放孔OD-自然释放孔OD)×100%
1.7 脾淋巴细胞分泌IL-2水平检测用RPMI 1640完全培养液将脾淋巴细胞调节至1×109·L-1,取24孔培养板,每孔加入0.5 mL含ConA(终浓度5 mg·L-1)的小鼠脾淋巴细胞悬液,置37 ℃、5% CO2培养箱中培养24 h,离心取上清,用ELISA法测定上清中IL-2的含量。
1.8 腹腔巨噬细胞分泌TNF-α及IL-6水平的检测用DMEM完全培养液将腹腔巨噬细胞调节至1×109·L-1,在24孔培养板中,每孔加入0.5 mL小鼠腹腔巨噬细胞悬液,2 h后弃上清,每孔加入0.5 mL含LPS(终浓度10 mg·L-1)的培养液,置37 ℃、5% CO2培养箱中培养24 h,取上清,用ELISA法测定上清中TNF-α、IL-6的含量。
1.9 统计学处理采用SPSS 16.0统计学软件进行统计学处理,计量资料均以x±s表示,组间比较采用单因素方差分析。
2 结果 2.1 超Ⅴ星虫草和Ⅰ星虫草子实体菌粉对免疫低下小鼠体质量变化的影响Tab 1结果显示,d 22造模后,各组小鼠体质量均降低,模型组小鼠体质量明显下降,毛色无华,精神萎靡。与模型组比较,Ⅰ星虫草、超Ⅴ星虫草与虫草胶囊均可明显拮抗地塞米松造成的体质量下降,Ⅰ星虫草和超Ⅴ星虫草比较差异无显著性。但在体质量恢复的趋势上,超Ⅴ星虫草略好于Ⅰ星虫草。
| Group | Changes of body mass/g | Thymus index/mg·g-1 | Spleen index/mg·g-1 |
| Control | 0.60±.60 | 1.07±0.30 | 4.17±1.12 |
| Dexamethasone | -1.02±1.02** | 0.67±0.16** | 2.95±0.41** |
| I star CM | -0.39±0.39## | 0.85±0.20## | 3.43±0.61# |
| Super V CM | -0.26±0.26## | 0.84±0.16## | 3.99±0.47##△▲ |
| Cordyceps capsule | -0.50±0.50## | 0.87±0.25## | 3.45±0.55# |
| **P < 0.01 vs control;#P < 0.05,##P < 0.01 vs dexamethasone;△P < 0.05 vs Ⅰ star CM;▲P<0.05 vs cordyceps capsule | |||
胸腺和脾脏都是机体质量要的免疫器官,前者是T细胞分化、发育、成熟的场所,后者是机体细胞免疫和体液免疫的中心,两者的脏器指数可在一定程度上反映机体免疫功能的强弱。由Tab 1可见,采用地塞米松造模后,模型小鼠胸腺指数和脾脏指数明显下降,与模型组相比,Ⅰ星虫草、超Ⅴ星虫草与虫草胶囊均明显拮抗地塞米松造成的胸腺指数和脾脏指数下降。在拮抗由地塞米松所导致的胸腺指数下降方面,超Ⅴ星虫与Ⅰ星虫草相比差异无显著性,但在胸腺指数恢复的趋势上,超Ⅴ星虫草略好于Ⅰ星虫草。在拮抗由地塞米松所导致的脾脏指数下降方面,超Ⅴ星虫草明显强于Ⅰ星虫草。
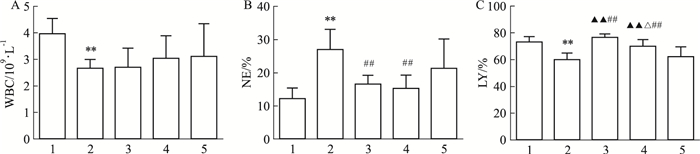
2.3 超Ⅴ星虫草和Ⅰ星虫草子实体菌粉对免疫低下小鼠血常规指标的影响如Fig 1所示,采用地塞米松造模后,模型小鼠白细胞计数明显降低,中性粒细胞百分率明显升高,淋巴细胞百分率明显降低。超Ⅴ星虫草和Ⅰ星虫草可明显拮抗由地塞米松所导致的中性粒细胞百分率升高,超Ⅴ星虫草与Ⅰ星虫草相比差异无显著性;超Ⅴ星虫草和Ⅰ星虫草可明显拮抗由地塞米松所导致的淋巴细胞百分率降低,超Ⅴ星虫草与Ⅰ星虫草相比有显著性差异。
|
| Fig 1 Effects of different levels of Cordyceps militaris on blood routine in mice after 28 days of administration(x±s, n = 10) A:White blood cell(WBC) count. B:Percentage of neutrophilic granulocytes(NE%), C:Percentage of lymphocytes (LY%), 1: Control; 2: Dexamethasone; 3: Ⅰ star CM; 4: Super Ⅴ CM; 5: Cordyceps capsule. **P < 0.01 vs control; ##P < 0.01 vs dexamethasone; △P < 0.05 vs I star CM; ▲▲P < 0.01 vs cordyceps capsule. |
由Fig 2可知,用地塞米松造模的小鼠巨噬细胞吞噬能力明显降低,而超Ⅴ星虫草和Ⅰ星虫草可明显拮抗该变化,超Ⅴ星虫与Ⅰ星虫草相比差异无显著性,但增强巨噬细胞吞噬活性的趋势方面,超Ⅴ星虫草略好于Ⅰ星虫草。超Ⅴ星虫草、Ⅰ星虫草与虫草胶囊比较差异均无显著性。

|
| Fig 2 Effects of different levels of Cordyceps militaris on phagocytic activity of mice abdominal macrophages after 28 days of administration(x±s, n = 10) 1: Control; 2: Dexamethasone; 3: Ⅰ star CM; 4: Super Ⅴ CM; 5: Cordyceps capsule. *P < 0.05 vs control; #P < 0.05 vs dexamethasone |
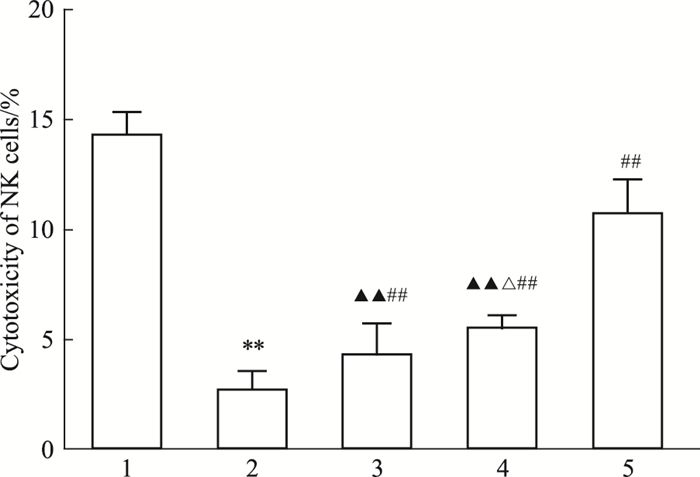
由Fig 3可知,用地塞米松造模可明显降低NK细胞活性,而超Ⅴ星虫草和Ⅰ星虫草、虫草胶囊均可明显拮抗该变化,且超Ⅴ星虫草与Ⅰ星虫草相比具有显著性差异。
|
| Fig 3 Effect of different levels of Cordyceps militaris on NK cell killing activity in mice after 28 days of administration(x±s, n = 10) 1: Control; 2: Dexamethasone; 3: Ⅰ star CM; 4: Super Ⅴ CM; 5: Cordyceps capsule.**P < 0.01 vs control; ##P < 0.01 vs dexamethasone; △P < 0.05 vs I star CM; ▲▲P < 0.01 vs cordyceps capsule |
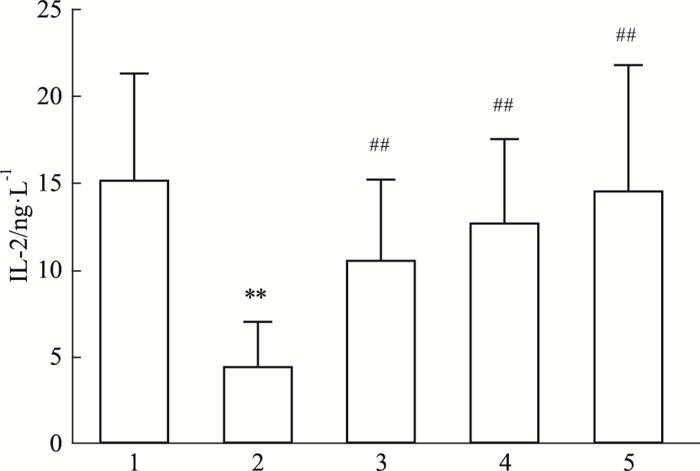
本实验选择测定IL-2水平,来观察不同级别虫草子实体菌粉对免疫低下小鼠T淋巴细分泌细胞因子的影响。Fig 4结果显示,与正常对照组相比,给予地塞米松后,IL-2的生成量明显降低,而超Ⅴ星虫草和Ⅰ星虫草、虫草胶囊都可以明显拮抗地塞米松引起的IL-2分泌降低,超Ⅴ星虫草和Ⅰ星虫草相比差异无显著性,趋势上超Ⅴ星虫草略好于Ⅰ星虫草。
|
| Fig 4 Effect of different levels of Cordyceps militaris on IL-2 level secreted by mouse spleen lymphocytes after 28 days of administration(x±s, n = 10) 1: Control; 2: Dexamethasone; 3: Ⅰ star CM; 4: Super Ⅴ CM; 5: Cordyceps capsule. **P < 0.01 vs control; ##P < 0.01 vs dexamethasone |
本实验选择测定TNF-α和IL-6,观察不同级别虫草子实体菌粉对巨噬细胞分泌细胞因子的影响。由Fig 5可知,与正常对照组相比,给予地塞米松后,TNF-α和IL-6分泌量均明显降低,而超Ⅴ星虫草和Ⅰ星虫草、阳性药都可以拮抗地塞米松引起的TNF-α和IL-6分泌量降低;在拮抗地塞米松诱导的TNF-α分泌量降低方面,超Ⅴ星虫草和Ⅰ星虫草相比具有显著性差异。

|
| Fig 5 Effects of different levels of Cordyceps militaris on TNF-α secretion and IL-6 secretion of mice abdominal macrophages after 28 days of administration(x±s, n = 10) 1: Control; 2: Dexamethasone; 3: Ⅰ star CM; 4: Super Ⅴ CM; 5: Cordyceps capsule.**P < 0.01 vs control; ##P < 0.01 vs dexamethasone; △P < 0.05 vs I star CM |
本实验从体质量、脏器指数、血常规、巨噬细胞功能测定、NK细胞活性和细胞因子分泌等多个方面,对超Ⅴ星虫草和Ⅰ星虫草的免疫调节功效进行了比较。对于体质量,超Ⅴ星虫草和Ⅰ星虫草均可明显拮抗地塞米松造成的体质量降低,Ⅰ星虫草和超Ⅴ星虫草比较差异无显著。但体质量恢复的趋势方面,超Ⅴ星虫草略好于Ⅰ星虫草。对于血常规,超Ⅴ星虫草和Ⅰ星虫草可明显拮抗地塞米松导致的白细胞计数和淋巴细胞降低,以及中性粒细胞升高,对地塞米松造成的淋巴细胞百分率降低的拮抗作用,超Ⅴ星虫草与Ⅰ星虫草比较具有显著性差异。
影响非特异性免疫功能的研究方法较多,免疫药理实验常以药物对实验动物免疫器官重量的影响,作为初步观察药物对免疫功能影响的指标,当机体的整体免疫功能增强时,其质量有所增加,脏器系数增加[7-8]。对于脏器指数,超Ⅴ星虫草和Ⅰ星虫草均明显拮抗地塞米松造成的胸腺指数和脾脏指数下降,对地塞米松造成的胸腺指数下降的拮抗作用,超Ⅴ星虫与Ⅰ星虫草比较差异无显著,但胸腺指数恢复的趋势方面,超Ⅴ星虫草略好于Ⅰ星虫草。对地塞米松造成的脾脏指数下降的拮抗作用,超Ⅴ星虫草明显强于Ⅰ星虫草。
在机体内,巨噬细胞是其免疫系统的一种重要免疫细胞,具有很强的吞噬功能及抗原递呈作用,对特异性免疫应答的诱导和调节起关键作用。巨噬细胞通过释放NO、IL-6、TNF-α等细胞因子,诱导细胞免疫,杀灭病原微生物[9-10]。巨噬细胞吞噬力的高低,反映了机体免疫水平的高低。巨噬细胞活性强、吞噬力高,机体的免疫力就高。对于单核-巨噬细胞功能,腹腔巨噬细胞吞噬中性红实验中,超Ⅴ星虫草和Ⅰ星虫草可明显拮抗地塞米松造成的小鼠巨噬细胞吞噬能力的降低,超Ⅴ星虫与Ⅰ星虫草比较差异无显著,但增强巨噬细胞吞噬活性的趋势方面,超Ⅴ星虫草略好于Ⅰ星虫草。
NK细胞是生物体内天然存在的非特异的免疫杀伤细胞。NK细胞对T细胞、B细胞、骨髓干细胞等细胞的功能均有一定的调节作用,还能够分泌多种细胞因子,它在宿主的免疫监视功能中起重要作用。对于NK细胞活性,超Ⅴ星虫草和Ⅰ星虫草可明显增加NK细胞活性,超Ⅴ星虫草与Ⅰ星虫草比较具有显著性差异。
综上所述,超Ⅴ星虫草和Ⅰ星虫草对地塞米松诱导的免疫功能低下的各个环节均具有明显的改善作用,在提高脾脏指数、增强NK细胞杀伤能力、提高巨噬细胞分泌TNF-α分泌水平方面,超Ⅴ星虫草作用明显优于Ⅰ星虫草。
| [1] |
Lee H H, Jeong J W, Lee J H, et al. Cordycepin increases sensitivity of Hep3B human hepatocellular carcinoma cells to TRAIL-mediated apoptosis by inactivating the JNK signaling pathway[J]. Oncol Rep, 2013, 30(3): 1257-64. doi:10.3892/or.2013.2589 |
| [2] |
袁明霞, 唐荣, 周巧玲, 等. 冬虫夏草对糖尿病肾病大鼠肾组织HIF-1α及VEGF表达的影响[J]. 中南大学学报:医学版, 2013, 38(5): 448-57. Yuan M X, Tang R, Zhou Q L, et al. Effect of Cordyceps sinensis on expressions of HIF-1α and VEGF in the kidney of rats with diabetic nephropathy[J]. J Central South Univ (Med Sci), 2013, 38(5): 448-57. |
| [3] |
Kwon H K, Jo W R, Park H J. Immune-enhancing activity of C. militaris fermented with Pediococcus pentosaceus (GRC-ON89A) in CY-induced immunosuppressed model[J]. BMC Complement Altern Med, 2018, 18(1): 75. doi:10.1186/s12906-018-2133-9 |
| [4] |
徐雷雷, 王静凤, 唐筱, 等. 蛹虫草降血糖作用及其机制研究[J]. 中国药理学报, 2011, 27(9): 1331-2. Xu L L, Wang J F, Tang X, et al. Hypoglycemia effect and the mechanism of Cordyceps militaris[J]. Chin Pharmacol Bull, 2011, 27(9): 1331-2. |
| [5] |
Cunningham K G, Manson W, Spring F S, et al. Cordycepin, a metabolic product isolated from cultures of Cordyceps militaris (Linn.) Link[J]. Nature, 1950, 166(4231): 949. |
| [6] |
王静凤, 李晓林, 滕来宾, 等. 海参虫草复剂对免疫功能低下小鼠的免疫调节作用[J]. 卫生研究, 2011, 40(2): 215-8. Wang J F, Li X L, Teng L B, et al. Immunomodulatory effects of a mixture of Apostichopus japonicus and Cordyceps militaris on immunocompromized mice[J]. J Hygiene Res, 2011, 40(20): 215-8. |
| [7] |
刘小敏, 梁毅. 加味愈白丸对小鼠免疫功能的影响[J]. 医药导报, 2013, 32(11): 1425-7. Liu X M, Liang Y. Effect of Jiawei Yubai pills on immunological function of mice[J]. Herald Med, 2013, 32(1): 1425-7. |
| [8] |
王峰, 王玲, 张才军, 等. 云南虫草菌粉免疫调节作用的实验动物研究[J]. 昆明医科大学学报, 2012(7): 45-8. Wang F, Wang L, Zhang C J, et al. Immunoregulation effect of Yunnan Cordyceps Sinensison in animal experiment[J]. J Kunming Med Univ, 2012(7): 45-8. doi:10.3969/j.issn.1003-4706.2012.07.012 |
| [9] |
王米, 张丽芳, 费陈忠, 等. 蛹虫草多糖对小鼠腹腔巨噬细胞免疫功能的影响[J]. 中国生化药物杂志, 2015, 35(4): 10-2. Wang M, Zhang L F, Fei C Z, et al. Effects of Cordyceps militaris polysaccharides on immune function of mouse peritoneal macrophage[J]. Chin J Biochem Pharm, 2015, 35(4): 10-2. |
| [10] |
Ellermann-Eriksen S. Macrophages and cytokines in the early defence against herpes simplex virus[J]. Virol J, 2005, 2: 59. doi:10.1186/1743-422X-2-59 |

