

BRAFV600E突变,即BRAF蛋白产物第600位的缬氨酸(V)被谷氨酸(E)替代,持续性激活下游MAPK信号通路,使细胞增殖异常,进而引发肿瘤[1]。该突变首先在黑色素瘤中被发现,且呈高频率突变的状态,目前已经成为黑色素瘤的治疗靶标[2]。然而,约10%结肠癌也存在BRAFV600E突变[3],但由于我国结肠癌的发病率远远高于黑色素瘤,因而开发治疗结肠癌BRAFV600E突变的靶向药物更具有临床价值和经济效益。
目前,临床上常用的威罗菲尼、达拉菲尼等BRAFV600E抑制剂,能够有效治疗80%以上BRAFV600E突变型黑色素瘤[4],但是对BRAFV600E突变型结肠癌的抑制效果却不足5%[5]。近年来,BRAFV600E突变型结肠癌作为一种独特的生物样本,因其难以进行标准的化疗治疗和严重的不良预后[6],已成为目前结肠癌治疗的重点。本研究通过慢病毒载体感染构建BRAFV600E稳定表达的CT26细胞稳转株,用于评价中药化学成分库中筛选所得的BRAFV600E高亲和小分子抑制剂的体外抑癌活性,为中药治疗结肠癌的作用机制研究提供新的思路和方法,同时也为开发高效抑制BRAFV600E突变型结肠癌的药物提供实验依据。
1 材料与方法 1.1 细胞株与试剂小鼠结肠癌CT26细胞株,浙江省医学科学院实验动物中心保存。RPMI 1640培养基(BBI);胎牛血清(Hyclone);BRAFV600E慢病毒(PPL);中药单体化合物库(TargetMol);MTT(Sigma);抗体BRAFV600E(26039,NewEast Biosciences);MEK(4694S)、p-MEK(9154S)、p-ERK(4370S)抗体,均购自CST公司;ERK(16443-1-AP)、β-actin一抗(60008-1-Ig),均购自Proteintech公司;蛋白marker(上海翊圣)。
1.2 仪器CO2培养箱(Eppendorf);荧光倒置显微镜(ZEISS);多功能酶标仪(MD);流式细胞仪(BD公司);电泳仪及转膜仪(Bio-Rad);化学发光分析仪(Linex)。
1.3 细胞培养及分组CT26细胞置于含10%胎牛血清的RPMI 1640培养基中,在37 ℃、5% CO2培养箱培养,2~3 d传代1次。设计引物扩增含CT26细胞对应人BRAFV600位点的序列,并进行测序。
1.4 BRAFV600E慢病毒感染CT26细胞取对数生长期CT26细胞,接种于6孔板,待细胞生长到汇合度为50%时,更换为1 mL新鲜培养基,将60 μL病毒滴度> 1011 PFU·L-1的BRAFV600E慢病毒与4 μL聚凝胺(Polybrene)预混后加到培养基,37 ℃、5% CO2培养条件下继续培养48 h,加入4 mg·L-1嘌呤霉素筛选1周,获得BRAFV600E CT26稳转株。
1.5 细胞增殖检测细胞接种于96孔板,每孔5 000个,每组处理6个复孔,分别在d 1、2、3每孔加入5 g·L-1 MTT 20 μL,继续培养4 h。弃旧液,每孔加入150 μL二甲基亚砜,避光放置30 min,至紫色结晶完全溶解。多功能酶标仪在490 nm处测量吸光值。
1.6 细胞划痕实验取两组对数生长期细胞接种于6孔板,待细胞汇合度为90%,用灭菌枪头在孔板底部单层细胞的中央划出一划痕,PBS洗去死细胞后,显微镜下拍照,并于24 h后观察细胞生长状态并拍照。ImageJ软件计算各组0 h和24 h划痕面积,计算划痕愈合率,愈合率 = (0 h划痕面积-24 h划痕面积)/0 h划痕面积×100%。
1.7 Western blot检测BRAFV600E细胞MEK/ERK通路蛋白分别收集BRAF野生型组、BRAFV600E突变型组对数生长期细胞,RIPA裂解,蛋白定量后,取等量进行SDS-PAGE,转移到PVDF膜上,孵育一抗、二抗,化学发光分析仪检测各组BRAFV600E、MEK、p-MEK、ERK、p-ERK的蛋白变化,以β-actin为内参。MTT确定特异性抑制BRAFV600E CT26细胞的药物组,药物处理48 h以同上的方法检测BRAFV600E表达。
1.8 中药单体化合物筛选利用Discovery Studio 4.0软件(DS),将Targetmol中药单体化合物数据库中的3万个天然产物与BRAFV600E蛋白对接,进行计算机虚拟筛选,总能量越低,亲和度越高,以此确定候选化合物,并将排分靠前的10个化合物分别进行体外活性验证,观察其对BRAF野生型和BRAFV600E突变型细胞的抑制作用。将细胞分为CT26野生型对照组、BRAFV600E组,接种对数生长期细胞于96孔板,每孔5000个细胞,12 h后加入高、中、低浓度候选化合物,继续培养48 h后,进行MTT检测。药物抑制率 = (1-药物处理组OD/未加药物对照组平均OD)×100%。
1.9 统计学分析应用SPSS 16.0统计软件分析,计量资料以x±s表示,各组间差异采用t检验。
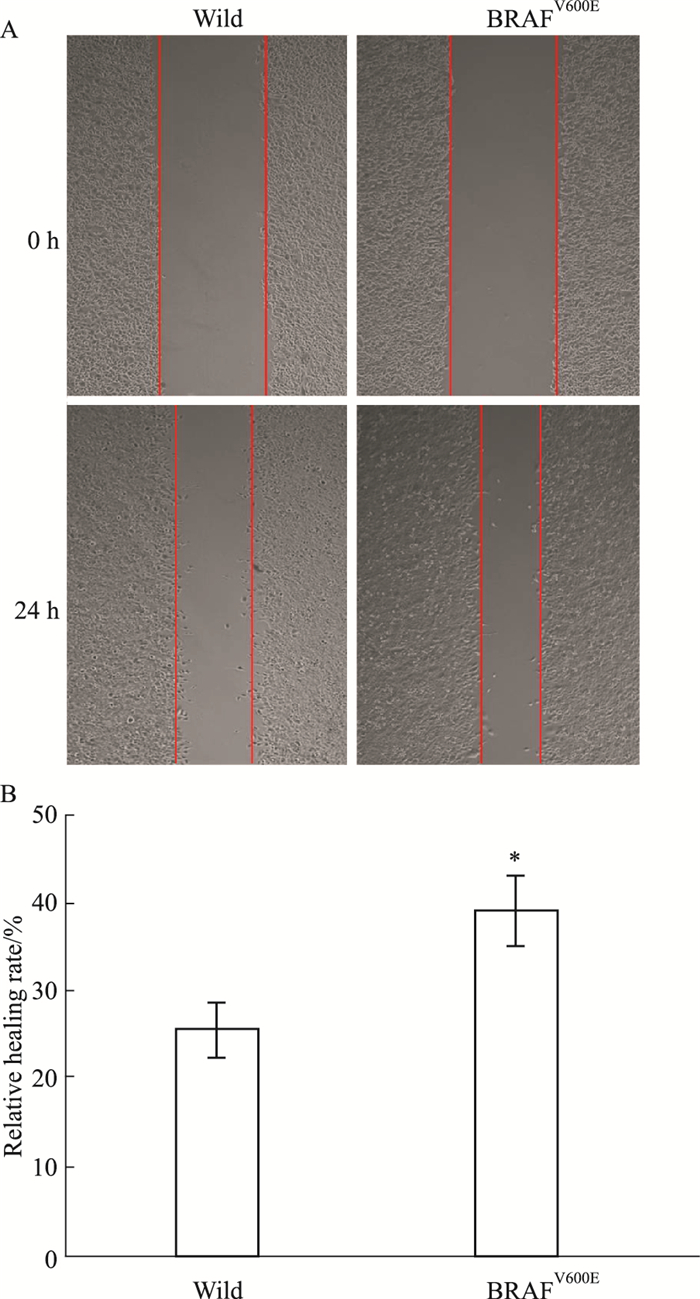
2 结果 2.1 BRAFV600E 对CT26细胞增殖和迁移的影响前期测序结果显示,CT26细胞的BRAF基因为野生型(数据未给出)。BRAFV600E慢病毒感染CT26细胞,并经嘌呤霉素1周筛选,获得BRAFV600E CT26稳转株。Fig 1的MTT检测结果显示,在d 2、3,细胞处于对数生长期,BRAFV600E CT26细胞相比野生型CT26细胞增殖速度更快,差异具有显著性(P < 0.05)。Fig 2的划痕实验结果表明,BRAFV600E CT26组24 h后划痕愈合能力明显强于野生型CT26组,量化愈合率有显著差异。以上结果说明,BRAFV600E能够促进CT26细胞增殖和迁移。

|
| Fig 1 Effect of BRAFV600E on CT26 cell proliferation(x±s, n = 6) *P < 0.05 vs wild group |
|
| Fig 2 Effect of BRAFV600E on CT26 cell migration (x±s, n = 3) A: The result of wound healing(×50); B: Quantization of wound healing rate. *P < 0.05 vs wild group. |
Fig 3的Western blot结果显示,BRAFV600E CT26组高表达BRAFV600E蛋白,而野生型CT26组则无表达;与野生型CT26组相比,BRAFV600E CT26组p-MEK蛋白表达上调,但总MEK和ERK蛋白表达差异无显著性。

|
| Fig 3 Effect of BRAFV600E on MEK/ERK pathway in CT26 cells |
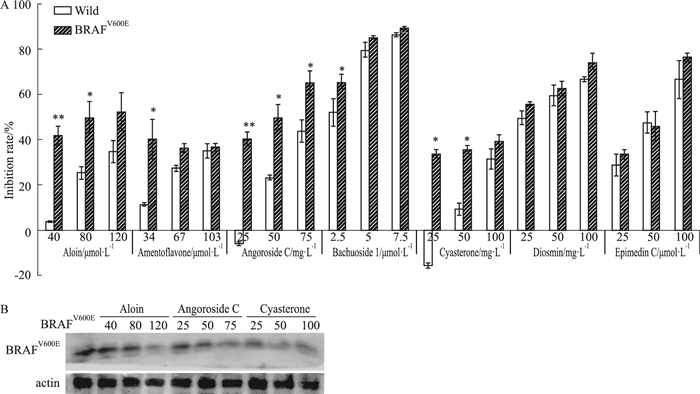
如Tab 1所示,DS初筛得到18种与BRAFV600E具有高亲和性的候选中药单体化合物。采用MTT法,分别检测18种化合物对BRAFV600E CT26组和野生型CT26组细胞增殖的抑制效果。Fig 4结果显示,给药48 h后,低、中剂量芦荟素、安格洛苷C和杯苋甾酮对BRAFV600E组细胞增殖抑制效果优于对照组,差异具有显著性(P < 0.05);但在高剂量给药浓度下,两组间差异无显著性。宝藿苷I(baohuoside I)、地奥司明(diosmin)和朝霍定C(epimedin C)对两组细胞增殖均有抑制效果,并随药物浓度升高,抑制率逐渐增加,但两组细胞的抑制率差异无显著性。其他药物对两组细胞均无明显抑制效果(数据未给出)。同时,Western blot结果显示(Fig 4),药物作用48 h后,随着芦荟素、安格洛苷C和杯苋甾酮浓度的增加,细胞中BRAFV600E蛋白表达逐渐降低。
| Monomer | Total energy | VDW | HBond | Elec |
| Epimedin C | -159.387 | -125.413 | -33.9739 | 0 |
| Forsythoside B | -156.176 | -125.443 | -30.7329 | 0 |
| Forsythoside A | -145.13 | -117.761 | -27.3691 | 0 |
| Aloin | -138.643 | -99.2013 | -39.4413 | 0 |
| Eleutheroside E | -137.454 | -110.041 | -27.4136 | 0 |
| Naringin dihydrochalcone | -136.838 | -116.916 | -19.9217 | 0 |
| Cyasterone | -135.808 | -117.606 | -18.2022 | 0 |
| Neohesperidin | -134.356 | -101.969 | -32.3869 | 0 |
| Isoacteoside | -130.678 | -108.466 | -22.2121 | 0 |
| Hesperidin | -130.514 | -104.981 | -25.5321 | 0 |
| Amentoflavone | -130.472 | -97.7077 | -32.7642 | 0 |
| Diosmin | -130.332 | -112.119 | -18.2135 | 0 |
| Baohuoside I | -129.805 | -112.13 | -17.6758 | 0 |
| Glucosylvitexin | -129.589 | -106.157 | -23.4319 | 0 |
| Angoroside C | -128.991 | -116.849 | -12.1422 | 0 |
| Nuezhenide | -127.887 | -95.4114 | -32.4757 | 0 |
| Rhoifolin | -126.906 | -99.8704 | -27.0355 | 0 |
| Icariin | -126.716 | -105.191 | -21.525 | 0 |
| VDW: Van der Waals force; Hbond: Hydrogen bonds; Elec: Electric charge. | ||||
|
| Fig 4 Inhibitory effect of compounds from traditional Chinese medicine on BRAFV600E CT26 cells A:The result of MTT (x±s, n=3). *P < 0.05, **P < 0.01 vs wild group; B: The result of Western blot, unit of measurement as the same as in A. |
BRAFV600E突变型结肠癌常见于近端结肠,分化较差,且与微卫星不稳定性(Microsatellite Instability,MSI)相关,原发肿瘤体积较大,化疗的缓解率和临床获益都较低[7]。研究表明,BRAFV600E突变能够持续激活MEK/ERK通路,并使癌细胞具有较高的增殖和迁移能力。此外,相对于黑色素瘤细胞,结肠癌细胞中表皮生长因子受体(Epidermal Growth Factor Receptor,EGFR)活化水平更高;接受BRAF抑制剂处理后,可导致MAPK通路的再度激活,进而使其对BRAF抑制剂产生耐药[8]。因此,针对BRAFV600E突变型结肠癌,常采用联合用药的策略,抑制EGFR-RAS-BRAF-MEK-ERK通路的激活[9],如采用双药联用,同时抑制EGFR/BRAF或者BRAF/MEK;或三药联用,抑制EGFR/BRAF/MEK[10]。但是这些靶向药物常常毒副作用较强,成分较高,且疗效甚微[11],因此,研发新型的抗结肠癌BRAFV600E抑制剂已成为目前国内外研究的热点。
中药及天然药物中的小分子化合物因其毒副作用小、作用广泛等特点,是寻找治疗结肠癌药物的重要来源[12-14]。已有报道证实,某些中药成分能调控结肠癌细胞增殖[15],但针对BRAFV600E突变型结肠癌的中药单体化合物的研究,尚未见报道。本研究通过计算机虚拟筛选并结合体外细胞实验发现,与野生型CT26组相比,芦荟素、安格洛苷C和杯苋甾酮对BRAFV600E CT26细胞具有明显的抑制作用,尤其在低、中剂量给药浓度下,对BRAFV600E CT26细胞抑制率在40%左右;且对野生型CT26细胞几乎没有抑制效果,提示这3种中药单体化合物可能是结肠癌BRAFV600E的特异性抑制剂;而宝藿苷I、地奥司明和朝霍定C对野生型和突变型CT26细胞均有抑制作用,且两组间抑制率差异无显著性,提示其存在着其他机制发挥抑癌作用。同时,Western blot结果也显示,药物作用48 h后,随着芦荟素、安格洛苷C和杯苋甾酮浓度的增加,细胞中BRAFV600E蛋白表达逐渐降低,进一步证明了3种化合物对BRAFV600E突变型CT26结肠癌细胞具有特异性抑制效果,但其药效机制及成药性仍需进一步通过体内、外实验证明。
| [1] |
Davies H, Bignell G R. Mutations of the BRAF gene in human cancer[J]. Nature, 2002, 417(6892): 949-54. doi:10.1038/nature00766 |
| [2] |
Tsai J, Lee J T, Wang W, et al. Discovery of a selective inhibitor of oncogenic B-Raf kinase with potent antimelanoma activity[J]. Proc Natl Acad Sci USA, 2008, 105: 3041-6. doi:10.1073/pnas.0711741105 |
| [3] |
Stewart B W, Wild C P. World Cancer Report 2014 [webpage on the Internet]. Available from: http://publications.iarc.fr/Non-Series-Publications/World-Cancer-Reports/World-Cancer-Report-2014.
|
| [4] |
Flaherty K T, Puzanov I, Kim K B, et al. Inhibition of mutated, activated BRAF in metastatic melanoma[J]. N Engl J Med, 2010, 363(9): 809-19. doi:10.1056/NEJMoa1002011 |
| [5] |
Kopetz S, Desai J, Chan E, et al. Phase II pilot study of vemurafenib in patients with metastatic BRAF-mutated colorectal cancer[J]. J Clin Oncol, 2015, 33(34): 4032-8. doi:10.1200/JCO.2015.63.2497 |
| [6] |
Ursem C, Atreya C E, Van Loon K. Emerging treatment options for BRAF-mutant colorectal cancer[J]. Gastrointest Cancer, 2018, 8: 13-23. |
| [7] |
Sanz-Garcia E, Argiles G, Elez E, et al. BRAF mutant colorectal cancer: prognosis, treatment, and new perspectives[J]. Ann Oncol, 2017, 28(11): 2648-57. doi:10.1093/annonc/mdx401 |
| [8] |
Prahallad A, Sun C, Huang S, et al. Unresponsiveness of colon cancer to BRAF(V600E) inhibition through feedback activation of EGFR[J]. Nature, 2012, 483(7387): 100-3. |
| [9] |
Lam M, Pant S, Yap T A. Combination drug development in BRAF mutant colorectal cancer[J]. Oncoscience, 2018, 5(3-4): 51-3. |
| [10] |
Pan J H, Zhou H, Zhu S B, et al. Development of small-molecule therapeutics and strategies for targeting RAF kinase in BRAF-mutant colorectal cancer[J]. Cancer Manag Res, 2018, 10: 2289-301. doi:10.2147/CMAR |
| [11] |
Sundar R, Hong D S, Kopetz S, et al. Targeting BRAF-mutant colorectal cancer: progress in combination strategies[J]. Cancer Discov, 2017, 7(6): 558-60. doi:10.1158/2159-8290.CD-17-0087 |
| [12] |
赵林, 吴鹏, 章平贵, 等. 雷公藤甲素对人结肠癌HCT116细胞增殖、自噬和凋亡的影响[J]. 中国药理学通报, 2016, 32(10): 1399-404. Zhao L, Wu P, Zhang P G, et al. Effect of triptolide on human colorectal cancer HCT116 cell proliferation, autophagy and apoptosis[J]. Chin Pharmacol Bull, 2016, 32(10): 1399-404. doi:10.3969/j.issn.1001-1978.2016.10.014 |
| [13] |
高干, 周艺, 刘杰, 等. 单酚类抗氧化剂及其衍生物的抗肿瘤作用及机制[J]. 中国现代应用药学, 2017, 34(4): 613-7. Gao G, Zhou Y, Liu J, et al. Antineoplastic activities and its possible mechanisms of the monophenolic antioxidants[J]. Chin J Mod Applied Pharm, 2017, 34(4): 613-7. |
| [14] |
肖晓慧, 宫瑞松, 张相强, 等. 重楼活性单体PP-22对人结肠癌SW620细胞增殖和凋亡的影响[J]. 中国现代应用药学, 2015, 32(10): 1175-80. Xiao X H, Gong R S, Zhang X Q, et al. Effects of active monomer PP-22 purified from Paridis Rhizoma on proliferation and apoptosis of human colorectal cancer SW620 cells[J]. Chin J Mod Applied Pharm, 2015, 32(10): 1175-80. |
| [15] |
马瑞, 徐玲, 曲秀娟, 等. 结直肠癌的中药治疗进展[J]. 辽宁中医杂志, 2017, 44(10): 2217-9. Ma R, Xu L, Qu X J, et al. Advances in treatment of colorectal cancer with traditional Chinese medicine[J]. Liaoning J Tradit Chin Med, 2017, 44(10): 2217-9. |

