

2. 齐齐哈尔医学院 组织学与胚胎学教研室,黑龙江 齐齐哈尔 161006
2. Dept of Histology and Embryology, Qiqihar Medical University, Qiqihar Heilongjiang 161006, China
糖尿病心肌病(diabetic cardiomypathy,DCM)为2型糖尿病(type 2 diabetic melitus,T2DM)患者常见的心脏并发症,主要病理表现为微血管病变导致的心肌肥大、局灶性心肌坏死、心肌纤维化,易并发心力衰竭及心律失常,是糖尿病患者死亡的主要原因之一[1-2]。近年来发现,糖尿病患者高血糖状态、心肌细胞内质网功能紊乱,均可引发内质网应激(endoplasmic reticulum stress,ERS),ERS在DCM发生、发展中发挥重要作用[3]。
多胺包括腐胺、精脒和精胺,是广泛存在于生物体各种组织细胞内的小分子脂肪族化合物。鸟氨酸脱羧酶(ornithine decarboxylase,ODC)是多胺合成途径中的关键限速酶。二氟甲基鸟氨酸(DL-α-difluoromethylornithine,DFMO)同鸟氨酸的结构类似,被公认为最有效的ODC特异性抑制剂,可作为ODC的底物进行脱羧反应,导致ODC发生不可逆的结构改变,降低细胞内多胺含量[4]。前期研究发现,DFMO通过抑制ERS,具有抑制心肌肥大及心肌细胞凋亡的作用[5-6],但是其对T2DM引发的心肌肥厚及ERS的影响尚不清楚。本实验以T2DM大鼠为研究对象,探讨DFMO对T2DM大鼠心肌肥厚的影响,并从ERS角度探讨其机制。
1 材料 1.1 实验动物Wistar大鼠,♂,SPF级,体质量(200~250) g。由齐齐哈尔医学院动物研究所提供,动物合格证编号:SYXK(黑) 2008004。
1.2 药物与试剂高糖高脂饲料(20%蔗糖、10%猪油、2.5%胆固醇、1%胆盐和66.5%基础饲料),北京科澳协力饲料有限公司提供;链脲佐菌素(steptozotocin,STZ)、DFMO,均购自美国Sigma公司;丙二醛(malondialdehyde,MDA)、超氧化物歧化酶(superoxide dismutase,SOD)、总抗氧化能力(total antioxidant capacity,T-AOC)测定试剂盒,购自南京建成生物工程研究所。
1.3 仪器光学显微镜、病理切片机(德国徕卡公司);离心机(德国Eppendorf公司);血糖仪(美国强生公司);电泳仪、电泳槽(上海天能科技有限公司)电泳成像系统(美国Bio-Rad公司)。
2 方法 2.1 实验动物分组与处理实验动物分笼饲养,自由进食、饮水,12 h昼夜交替人工照明。将大鼠随机分为正常对照组10只、模型组40只。对照组大鼠给予普通饲料饲养,模型组大鼠给予高脂饲料喂养4周,4周后禁食不禁水,一次性腹腔注射STZ 55 mg·kg-1(溶于0.1 mmol·L-1柠檬酸缓冲液中,pH 4.4,冰浴,现配现用,5 min内用完),72 h后尾静脉采血测量血糖浓度,血糖≥16.7 mmol·L-1为T2DM大鼠造模成功,正常对照组大鼠单次腹腔注射相同剂量的枸橼酸缓冲液。将成模的T2DM大鼠随机分为2组,模型组12只、治疗组14只,治疗组进行DFMO干预,T2DM大鼠给予2% DFMO水溶液连续饮用12周。实验过程中,除正常对照组外,其余各组大鼠均给予高糖高脂饲料。
2.2 取材干预治疗12周后,大鼠禁食10 h,取大鼠尾静脉血测定血糖。处死前,称量大鼠体质量(body weight, BW),3%戊巴比妥钠腹腔注射麻醉,迅速开胸取出心脏,剪去心脏周围组织和血管,滤纸吸干后,称全心重(heart weight, HW),沿室间隔剪去右心室组织,称量左室重(left ventricular weight,LVW)。计算心脏参数HW/BW和LVW/BW。4%多聚甲醛固定心肌组织,石蜡包埋,常规HE染色,光镜下观察心肌细胞及心肌间质的变化,将心肌组织置于液氮中保存备用。
2.3 生化指标检测各组大鼠取左心室组织,匀浆后,严格按照试剂盒说明书操作,分别测定MDA含量、SOD和T-AOC活性。
2.4 Masson染色石蜡切片脱蜡至水,自来水和蒸馏水冲洗,苏木精染液染核5~10 min,充分水洗后,用Masson丽春红酸性复红液染色5~10 min,浸洗分化后,苯胺蓝液染5 min,二甲苯透明、中性树胶封固。胶原纤维被苯胺蓝所染呈蓝色,肌纤维被丽春红所染呈红色。
2.5 Western blot检测各组取心肌组织约50 mg,裂解液充分作用,4 ℃离心后取上清液,Bradford法测定蛋白质浓度后,蛋白定量,蛋白变性。各组蛋白上样量为30 μg,SDS-PAGE电泳,蛋白转至PVDF膜,封闭液室温封闭1 h后,分别加入一抗GRP78、CHOP、β-actin(1 :500),4 ℃孵育过夜,相应二抗(1 :5 000)室温孵育1.5 h。ECL化学发光显色,电泳成像系统定量扫描分析,结果以β-actin校正。
2.6 统计学处理实验数据均经SPSS 15.0统计软件处理,结果以x±s表示,两组之间均数比较采用t检验。
3 结果 3.1 DFMO对T2DM大鼠空腹血糖和心脏参数的影响心脏参数HW/BW和LVW/BW能够反映大鼠的心肌肥厚程度。Tab 1结果表明,与对照组比较,T2DM组大鼠空腹血糖及心脏参数HW/BW、LVW/BW均增高,差异有统计学意义(P < 0.05,P < 0.01),治疗组大鼠空腹血糖和心脏参数HW/BW、LVW/BW均低于糖尿病组(P < 0.05)。
| Group | Fasting bloodglucose/mmol·L-1 | HW/BW/mg·g-1 | LVW/BW/mg·g-1 |
| Control | 5.87±0.37 | 3.34±0.09 | 2.07±0.05 |
| T2DM | 17.05±0.66** | 3.66±0.07* | 2.53±0.04* |
| DFMO | 15.26±0.59# | 3.42±0.06# | 2.35±0.05# |
| *P < 0.05, **P < 0.01 vs control; #P < 0.05 vs T2DM | |||
Tab 2结果显示,T2DM模型组大鼠与对照组比较,心肌组织MDA含量明显增高(P < 0.01),SOD活性和T-AOC明显下降(P < 0.01);与T2DM模型组比较,DFMO治疗组MDA含量明显下降(P < 0.01),SOD和T-AOC活性升高(P < 0.05,P < 0.01)。
| Group | MDA/μmol·g-1 Pro | SOD/kU·g-1 Pro | T-AOC/kU·L-1 |
| Control | 11.73±0.42 | 151.32±4.72 | 132.21±3.05 |
| T2DM | 20.41±0.56** | 121.53±5.71** | 105.03±2.39** |
| DFMO | 14.63±0.40## | 138.79±4.97# | 124.87 ±3.11## |
| *P < 0.05, **P < 0.01 vs control; #P < 0.05, ##P < 0.01 vs T2DM | |||
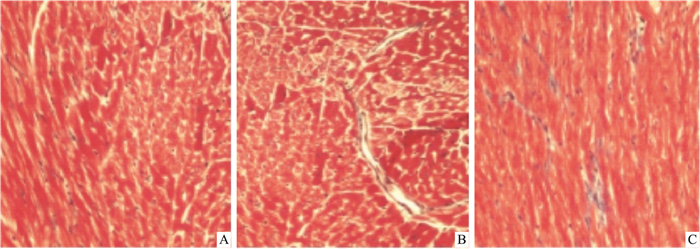
Masson染色是经典胶原纤维染色方法,染色后胶原纤维呈蓝色,肌纤维呈红色。Fig 1结果表明,正常对照组心肌细胞间隙清晰可见,间质胶原纤维极少。与对照组相比,T2DM组大鼠心肌细胞间质和血管旁有较多明显蓝色深染;治疗组与T2DM组比较,心肌细胞间质和血管旁的蓝色深染逐渐减少,胶原沉积逐渐减轻,表明DFMO可以一定程度抑制T2DM大鼠心肌胶原纤维的沉积。
|
| Fig 1 Masson staining of myocardium in rats(×400) A:Control group; B:T2DM group; C:DFMO group. |
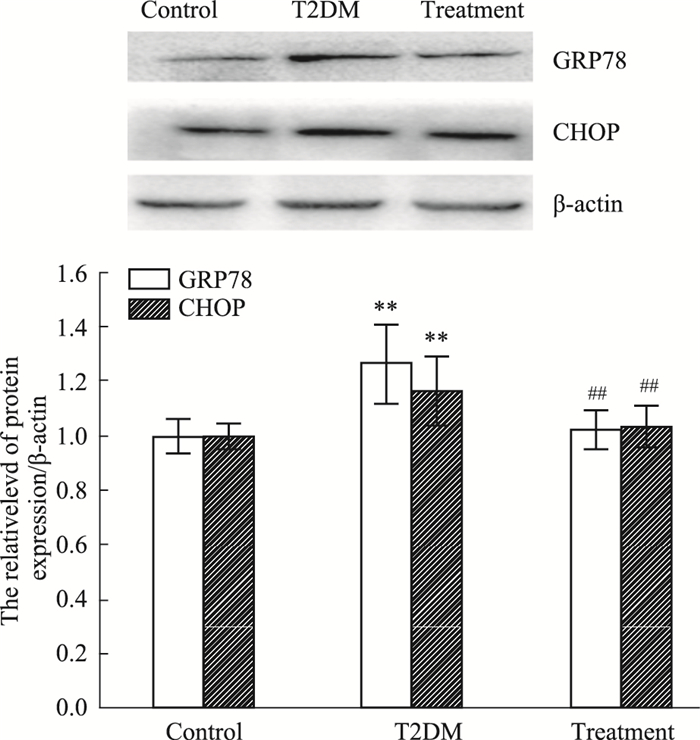
如Fig 2所示,T2DM组与对照组比较,GRP78和CHOP蛋白表达量明显增加(P < 0.01);DFMO治疗组与T2DM组比较,GRP78和CHOP蛋白表达量明显下降(P < 0.01)。
|
| Fig 2 Effect of DFMO on protein expression of GRP78 and CHOP(x±s, n = 3~5) **P < 0.01 vs control group; ##P < 0.01 vs T2DM group |
DCM是由高血糖、心肌代谢紊乱引起的心肌细胞原发性损伤,是T2DM患者常见并发症,典型表现为心脏微血管病变及心肌纤维化,最终引发左心室肥厚,心肌功能障碍及心力衰竭。DCM发病机制复杂,氧化应激、炎症、心肌细胞凋亡、糖脂代谢紊乱、线粒体损伤、心肌纤维化,都被认为是DCM发生、发展的机制[7-8],目前临床对DCM尚缺乏有效的治疗措施。
多胺生理作用广泛,能与细胞内核酸、蛋白质等生物大分子相互作用,从而影响和调节细胞生理功能。DFMO为多胺合成代谢限速酶的特异性抑制剂,通过抑制鸟氨酸脱羧酶活性,明显降低细胞内多胺水平,从而减弱胃肠道组织、心肌组织等增生反应。前期研究表明,DFMO通过抑制鸟氨酸脱羧酶活性,减少细胞内多胺含量,对老年性心肌病、心肌肥厚、心肌缺血/再灌注损伤等具有保护作用,但对糖尿病引起的心肌肥大尚无明确报道。本研究动物实验显示,DFMO能够明显降低T2DM大鼠空腹血糖和心脏参数,改善T2DM大鼠的心肌肥厚。
高糖血症和胰岛素抵抗是T2DM的主要特征,二者均使葡萄糖和脂肪酸的氧化作用增加,而引起氧化应激反应,线粒体内部活性氧大量聚集,进一步加重T2DM患者的代谢紊乱,导致恶性循环[9]。生化指标检测发现,DFMO干预后,心肌组织MDA含量明显降低,SOD活性和T-AOC明显升高,提示DFMO可通过抑制心肌脂质过氧化物生成,增强总抗氧化能力,减轻氧化应激损伤,进而对T2DM发挥保护作用。
氧化应激、缺氧、脂质积聚等病理刺激都会影响内质网的正常生理功能,引起未折叠蛋白或错误折叠蛋白在内质网的聚集,从而引发ERS[10]。ERS通过上调GRP78的表达,有助于蛋白质折叠修复,但若ERS长时间持续,通过促进CHOP的转录诱导,启动细胞凋亡过程[11-12]。本研究中,T2DM大鼠心肌组织GRP78和CHOP表达水平增加,DFMO治疗组GRP78和CHOP蛋白表达水平降低,提示ERS参与了T2DM的发生、发展,表明DFMO对T2DM的心肌保护作用与ERS具有相关性。
综上所述,本实验结果初步显示,DFMO可降低大鼠心肌组织GRP78和CHOP蛋白表达,该结果可能与其心肌保护作用有关。
( 致谢: 感谢齐齐哈尔医学院基础医学院分子生物学研究室为本课题研究提供仪器设备和技术支持。)
| [1] |
Battiprolu P K, Lopez-Crisosto C, Wang Z V, et al. Diabetic cardiomyopathy and metabolic remodeling of the heart[J]. Life Sci, 2013, 92(11): 609-15. doi:10.1016/j.lfs.2012.10.011 |
| [2] |
Isfort M, Stevens S C, Schaffer S, et al. Metabolic dysfunction in diabetic cardiomyopathy[J]. Heart Fail Rev, 2014, 19(1): 35-48. doi:10.1007/s10741-013-9377-8 |
| [3] |
丁文龙, 潘大彬. 内质网应激在糖尿病心肌病发病机制中的作用[J]. 承德医学院学报, 2016, 33(4): 336-9. Ding W L, Pan D B. The role of endoplasmic reticulum stress in the pathogenesis of diabetic cardiomyopathy[J]. J Chengde Med Coll, 2016, 33(4): 336-9. |
| [4] |
Alexiou G A, Lianos G D, Ragos V, et al. Difluoromethylornithine in cancer: new advances[J]. Future Oncol, 2017, 13(9): 809-19. doi:10.2217/fon-2016-0266 |
| [5] |
Lin Y, Zhang X J, Xiao W, et al. Endoplasmic reticulum stress is involved in DFMO attenuating isoproterenol-induced cardiac hypertrophy in rats[J]. Cell Physiol Biochem, 2016, 38(4): 1553-62. doi:10.1159/000443096 |
| [6] |
Lin Y, Zhang X J, Lina W, et al. Polyamine depletion attenuates isoproterenol induced hypertrophy and endoplasmic reticulum stress in cardiomyocytes[J]. Cell Physiol Biochem, 2014, 34(5): 1455-65. doi:10.1159/000366350 |
| [7] |
刘涛, 李晶, 鲍翠玉, 等. 线粒体损伤与糖尿病心肌病发病关系的研究进展[J]. 中国药理学通报, 2018, 34(4): 456-8. Liu T, Li J, Bao C Y, et al. Research progress of mitochondria in diabetic cardiomyopathy[J]. Chin Pharmacol Bull, 2018, 34(4): 456-8. doi:10.3969/j.issn.1001-1978.2018.04.004 |
| [8] |
徐天娇, 刘勇, 李萍, 等. 泛素连接酶Cbl-b调控p38MAPK在胰岛素与硒协同抑制糖尿病心肌病大鼠心肌细胞凋亡中的作用[J]. 中国药理学通报, 2016, 32(8): 1170-4. Xu T J, Liu Y, Li P, et al. Role of ubiquitin ligase Cbl-b regulated p38MAPK in insulin and selenium synergistic anti-myocardial apoptosis in diabetic cardiomyopathy[J]. Chin Pharmacol Bull, 2016, 32(8): 1170-4. doi:10.3969/j.issn.1001-1978.2016.08.027 |
| [9] |
Zhang N, Yang Z, Xiang S Z, et al. Nobiletin attenuates cardiac dysfunction, oxidative stress and inflammatory in streptozotocin:induced diabetic cardiomyopathy[J]. Mol Cell Biochem, 2016, 417(1-2): 87-96. doi:10.1007/s11010-016-2716-z |
| [10] |
周宇, 李晶, 鲍翠玉. 内质网应激在糖尿病心肌病中的研究进展[J]. 中国药理学通报, 2017, 33(9): 1200-3. Zhou Y, Li J, Bao C Y. Research progress of endoplasmic reticulum stress in diabetic cardiomyopathy[J]. Chin Pharmacol Bull, 2017, 33(9): 1200-3. |
| [11] |
陈丹, 吴基良, 李晶. 内质网应激信号通路在高脂诱导的心肌细胞损伤中的作用[J]. 中国药理学通, 2017, 33(7): 966-71. Cheng D, Wu J L, Li J. Role of endoplasmic reticulum stress in high fatty acid induced injury in cardiomyocytes[J]. Chin Pharmacol Bull, 2017, 33(7): 966-71. |
| [12] |
Yu H, Zhen J, Yang Y, et al. Ginsenoside Rg1 ameliorates diabetic cardiomyopathy by inhibiting endoplasmic reticulum stress-induced apoptosis in a streptozotocin-induced diabetes rat model[J]. J Cell Mol Med, 2016, 20(4): 623-31. |
