


2. 西双版纳傣药南药重点实验室, 云南 景洪 666100;
3. 黑龙江中医药大学药学院,黑龙江 哈尔滨 150040;
4. 中国医学科学院药用植物研究所,北京 100093
2. Key Lab of Dai and Southern Medicine of Xishuangbanna Dai Autonomous Prefecture, Jinghong, Yunnan 666100, China;
3. College of Pharmacy, Heilongjiang University of Chinese Medicine, Haerbin 150040, China;
4. Institute of Medicinal Plant, Chinese Academy of Medical Sciences, Peking Union Medical College, Beijing 100093, China
H9c2心肌细胞是上世纪70年代由Kimes等[1]从胚胎期BDIX大鼠心脏组织中分离得到的一种具有骨骼肌特性的心肌细胞株, 常用于心血管疾病体外药效及作用靶点筛选。目前, 心肌缺血/再灌注损伤(myocardial ischemia/reperfusion injury, MIRI)已成为临床上影响冠心病患者获得再灌注最佳疗效的主要障碍[2]。H9c2心肌细胞是当前研究MIRI的最常用细胞株, 用于其作用机制通路的研究[3-4]。研究者常加入H2O2或缺氧/复氧(hypoxia/reoxygenation, H/R)两种处理方式, 模拟MIRI[4-6], 与加入H2O2相比, H/R处理后H9c2心肌细胞更能够真实反映心肌缺血/再灌注的损伤过程, 故为更多的研究者使用。但实验过程中, 由于使用试剂及仪器的不同, H/R的条件也不尽相同[7-8]。同时, 大多数研究者通过检测H9c2心肌细胞存活率, 作为模型成功的衡量标准, 缺乏在H/R过程中对细胞的生长状态的检测, "终点"检测很难真实反映H/R的损伤过程。
实时阻抗细胞分析(real time cellular analysis, RTCA)技术是近年来新兴的细胞活性检测方法。该方法是把微电子细胞传感器芯片整合到表面适于细胞贴附生长的细胞检测板的底部, 细胞在检测板上的贴壁程度及生长可引起各个电极阵列的电极结构的阻抗变化, 该系统可以实时并自动获取其电阻模拟电信号, 并可以转换成数字信号以进行分析。因此, 电阻抗即反映为细胞指数(cell index, CI)的值, 用于指示细胞生长、伸展、形态变化、死亡、贴壁程度等生理状态。该方法具有实时监控、无需标记、全自动化、高灵敏度、高准确性等优点, 更多应用于肿瘤药物筛选、免疫、药物毒性检测等方面[9-10]。本研究基于RTCA技术, 评价在H/R过程中H9c2心肌细胞的损伤过程, 以期寻找最佳H/R条件, 真实反映H9c2心肌细胞H/R过程中的损伤状态, 并使用目前研究较多的三七皂苷R1(notoginsenoside R1, NGR1)进行评价, 从而建立规范、标准的造模方法, 为MIRI的药物作用靶点筛选及作用机制研究提供参考。
1 材料 1.1 细胞与试剂H9c2心肌细胞, 购自中国科学院昆明细胞库。胎牛血清(货号:20151206, 武汉普诺赛生命科技有限公司); DMEM高糖培养基(货号:AB217802, HyClone公司); 无糖的DMEM (货号:1810192, Gibco公司); NGR1(货号:110745-201619, 中国食品药品检定研究院); 细胞凋亡检测试剂盒(货号:1758909, Thermo公司)。
1.2 仪器RTCA S16多功能实时无标记细胞分析仪(ACEA Biosciences Inc); SW-CJ-1F型超净工作台(苏州净化设备有限公司); Spectramax i3多功能读板仪(美谷分子仪器有限公司); NU-4950三气培养箱(美国Nuaire公司); C6流式细胞仪(美国BD公司)。
2 方法 2.1 细胞培养大鼠H9c2胚胎心肌细胞株置于37℃、5% CO2培养箱中, 含10%胎牛血清的DMEM高糖培养液培养。细胞贴壁80%~90%时, 用0.25%胰酶消化, 计数, 以1:3的比例传代, 每2~3 d传代1次。
2.2 MTT实验用0.25%胰蛋白酶消化细胞, 收集到离心管中混匀。按每孔8 000个细胞接种于96孔培养板, 置于37℃、5% CO2培养箱中孵育。细胞处理后, 每孔加MTT溶液(5 g·L-1)20 μL, 置于37℃、5% CO2培养箱中孵育4 h后, 离心弃上清, 每孔加入100 μL DMSO, 震荡, 酶标仪测定490 nm处的吸光度。
2.3 RTCA实验首先在E-Plate板中加入50 μL培养基, 测定基线CI值, 再加入100 μL细胞悬液, 放入RTCA多功能实时无标记细胞分析仪, 动态监测细胞黏附伸展及增殖状况。
2.4 H/R实验取对数生长期H9c2心肌细胞, 接种于96孔板或E-Plate板中, 37℃、5% CO2培养箱中孵育35 h后, 在三气培养箱中H/R处理, 检测细胞生长状况。
2.5 统计学方法具体时间点CI值、细胞凋亡率及细胞存活率结果以x±s表示, 用统计学软件SPSS 13.0对组间数据进行t检验及单因素方差分析。
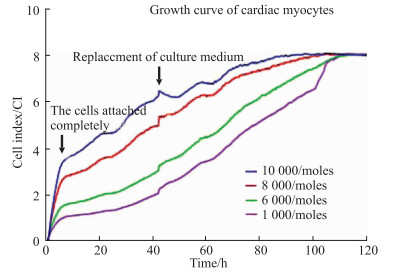
3 结果 3.1 RTCA检测H9c2心肌细胞增殖状况分别将4 000、6 000、8 000、10 000个/孔的H9c2心肌细胞接种于E-Plate板中, 设3个复孔, RTCA检测细胞增殖状况。如Fig 1所示, 分别接种4 000~10 000个/孔细胞数, 经过培养后, 大约经过100 h可达到平台期, 且更换培养基后, 对H9c2心肌细胞的CI值有影响。
|
| Fig 1 Growth curve of H9c2 cardiomyocytes |
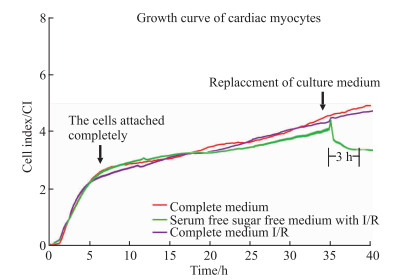
将8 000个/孔的H9c2心肌细胞接种于E-Plate板中, 3个复孔, 37℃、5% CO2培养箱中孵育35 h后, 将三气培养箱中氧气浓度调整为2%, 进行缺氧处理, 实时记录细胞状况。如Fig 2、Tab 1所示, 使用完全培养基建模, 缺氧后与正常细胞的CI值无差异, 随时间延长(3~5 h)差异明显(P < 0.05), 而无血清、无糖培养基造模后, CI值明显降低, 且缺氧3 h后, CI值下降趋势不明显, 达到平台期。因此, 可选取3~5 h作为缺氧时间。
|
| Fig 2 Effect of different hypoxia time on CI value of H9c2 cardiomyocytes (x±s, n=3) |
| Group | Hypoxia time | ||
| 3 h | 4 h | 5 h | |
| Control | 4.78±0.22 | 4.85±0.26 | 4.91±0.26 |
| Complete medium | 3.44±0.67* | 3.48±0.68* | 3.53±0.67* |
| H/R | 1.69±0.30** | 1.69±0.32** | 1.67±0.32** |
| *P < 0.05, **P < 0.01 vs control | |||
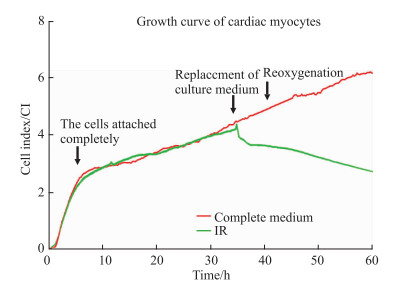
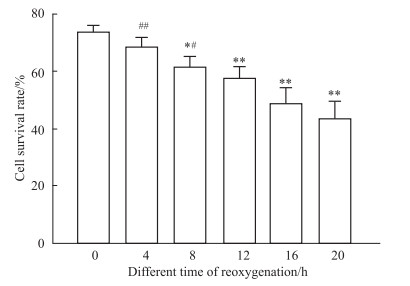
将8 000个/孔的H9c2心肌细胞接种于E-Plate板中, 3个复孔, 37℃、5% CO2培养箱中孵育35 h后, 将三气培养箱中氧气浓度调整为2%, 缺氧4 h后, 进行复氧, 实时记录细胞状况。如Fig 3所示, 当进行复氧处理后, H9c2心肌细胞CI值出现下降趋势。根据正常细胞和H/R处理后H9c2心肌细胞中CI值, 按公式细胞存活率=CI缺氧/复氧处理细胞/CI正常细胞, 计算经H/R处理后H9c2心肌细胞的凋亡率。根据文献[11-12], H/R损伤后细胞活力大概控制在50%左右, 由Fig 4可知, 经过缺氧4 h/复氧16 h后, H9c2心肌细胞的存活率为(48.82±5.32)%, 且细胞凋亡率与复氧时间存在时间依赖关系, 从而确定H/R模型条件为缺氧4 h, 复氧16 h。
|
| Fig 3 Effect of different reoxygenation time on CI value of H9c2 cardiomyocytes after 4 h hypoxia (x±s, n=3) |
|
| Fig 4 Effect of different reoxygenation time on apoptotic rate of H9c2 cardiomyocytes (x±s, n=3) *P < 0.05, **P < 0.01 vs reoxygenation for 0 h; #P < 0.05, ##P < 0.01 vs reoxygenation for 16 h |
将8 000个/孔的H9c2心肌细胞接种于96孔板中, 37℃、5% CO2培养箱中孵育35 h后, 将三气培养箱中氧气浓度调整为2%, 缺氧4 h后, 复氧16 h, H/R结束后, MTT法测定细胞活力。如Fig 5所示, 使用96孔板测定H/R处理后细胞存活率为(50.72±6.38)%, 与RTCA分析结果差异无显著性, 说明使用RTCA分析H9c2心肌细胞H/R模型的方法比较可靠。

|
| Fig 5 Survival rate of H9c2 cardiomyocytes determined by MTT (x±s, n=3) **P < 0.01 vs control |
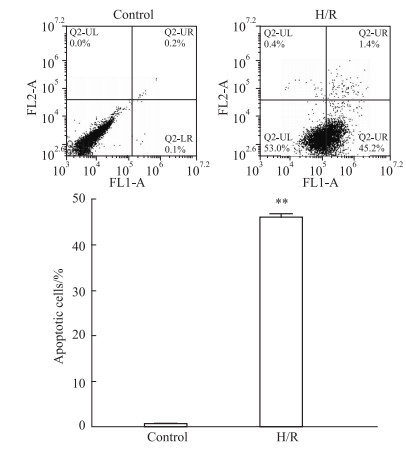
将105个/孔的H9c2心肌细胞接种于6孔板中, 37℃、5% CO2培养箱中孵育35 h后, 将三气培养箱中氧气浓度调整为2%, 缺氧4 h后, 复氧16 h, H/R结束后, 流式细胞术测定细胞活力。如Fig 6所示, 利用本实验方法将H9c2心肌细胞进行缺氧4 h/复氧16 h处理后, 细胞凋亡率(46.17±0.72)%, 与RTCA及MTT法测定结果差异无显著性, 说明RTCA方法可替代MTT及流式细胞术, 评价H9c2心肌细胞H/R模型。
|
| Fig 6 Effect of apoptosis of H9c2 cardiomyocytes after hypoxia reoxygenation (x±s, n=3) **P < 0.01 vs control |
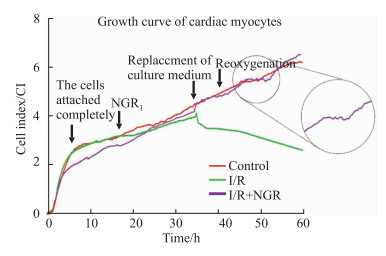
将8 000个/孔的H9c2心肌细胞接种于E-Plate板中, 37℃、5% CO2培养箱中孵育后, 加入25 mg·L-1 NGR1处理24 h, 使用三气培养箱进行H/R处理, 实时记录细胞状况。如Fig 7所示, NGR1预处理H9c2心肌细胞后, H/R处理后, 能够明显增加细胞CI值, 在复氧8~12 h期间, 经NGR1处理后, H9c2心肌细胞增殖出现短暂平台期, 随后以较大斜率进行增殖, 表明NGR1促进H/R后H9c2心肌细胞的增殖并非时间依赖性。
|
| Fig 7 Effect of NGR1 on CI value of H9c2 cardiomyocytes after H/R |
RTCA技术是一种基于电阻值, 实时反映细胞贴壁状态的新型观测细胞增殖的技术, 对于测定细胞毒性, 观察细胞增殖状况具有明显的优越性。在本研究中, 通过RTCA能够实时观察H/R过程中H9c2心肌细胞状态, 从而明确H/R条件对H9c2心肌细胞的损伤作用。研究结果发现, 造模过程中培养基对于模型影响较大, H/R过程中, 完全培养基基本不会引起细胞损伤, 使用无血清、无糖培养基才是成模的关键。
目前研究建立H9c2心肌细胞H/R模型一般使用MTT终点法[13-14], 不能够真实反映H/R细胞损伤的过程, 因此出现了H/R条件不同的情况。本研究使用三气培养箱做为造模工具, 尽量减少人为因素干扰, 对建立规范、标准的造模方法具有一定的指导意义, 并且具有快速、准确、易操作等优点。通过本研究最终确定的成模条件为H9c2心肌细胞培养35 h后, 更换无血清、无糖DMEM培养基, 在2%氧气、5% CO2、37℃条件下培养4 h进行缺氧处理, 然后调整氧气浓度为21%, 相同条件培养16 h, 作为复氧处理。
NGR1对H/R处理后H9c2心肌细胞具有保护作用, 相关研究较多[9, 15]。通过该技术我们发现, NGR1促进H/R处理后H9c2心肌细胞增殖并不存在时间依赖性, 而是存在一定的平台期, 然后快速增殖, 这有可能是给药后通过一定的时间积累, 激活H9c2心肌细胞中的某些关键因素而促进细胞增殖, 其深入机制还有待进一步证实, 这也为发现新药物靶点和作用机制提供了参考。
| [1] |
Kimes B W, Brandt B L. Properties of a clonal muscle cell line from rat heart[J]. Exp Cell Res, 1976, 98(2): 367-81. doi:10.1016/0014-4827(76)90447-X |
| [2] |
李光, 邢小燕, 张美双, 等. 基于表观遗传学调控的中医药防治心肌缺血/再灌注损伤的研究进展[J]. 药学学报, 2016, 51(7): 1047-53. Li G, Xing X Y, Zhang M S, et al. Research progress in epigenetic regulation of myocardial ischemia/reperfusion injury by traditional Chinese medicine[J]. Acta Pham Sin, 2016, 51(7): 1047-53. |
| [3] |
Soumya R S, Prathapan A, Raj P S, et al. Selenium incorporated guar gum nanoparticles safeguard mitochondrial bioenergetics during ischemia reperfusion injury in H9c2 cardiac cells[J]. Int J Biol Macromol, 2017, 107: 254-60. |
| [4] |
Sheng M, Huang Z, Pan L, et al. SOCS2 exacerbates myocardial injury induced by ischemia/reperfusion in diabetic mice and H9c2 cells through inhibiting the JAK-STAT-IGF-1 pathway[J]. Life Sci, 2017, 188(Supplement C): 101-9. |
| [5] |
Brand M D, Goncalves R L S, Orr A L, et al. Suppressors of superoxide-H2O2 production at site IQ of mitochondrial complex I protect against stem cell hyperplasia and ischemia-reperfusion injury[J]. Cell Metab, 2016, 24(4): 582-92. doi:10.1016/j.cmet.2016.08.012 |
| [6] |
Ai Q D, Sun G B, Luo Y, et al. Ginsenoside Rb1 prevents hypoxia-reoxygenation-induced apoptosis in H9c2 cardiomyocytes via an estrogen receptor-dependent crosstalk among the Akt, JNK, and ERK 1/2 pathways using a label-free quantitative proteomics analysis[J]. Rsc Adv, 2015, 5(33): 26346-63. doi:10.1039/C5RA02432C |
| [7] |
Li X L, Yang R, Yang X H, et al. Original article paeonol protects H9c2 cardiomyocytes from ischemia/reperfusion injury by activating Notch1 signaling pathway in vitro[J]. Int J Clin Exp Med, 2017, 10(2): 2866-73. |
| [8] |
Yu Y L, Sun G B, Luo Y, et al. Cardioprotective effects of notoginsenoside R1 against ischemia/reperfusion injuries by regulating oxidative stress- and endoplasmic reticulum stress- related signaling pathways[J]. Sci Eep-UK, 2016, 6(5): 21730. |
| [9] |
Chen H B, Zheng H T. MicroRNA-200c represses migration and invasion of gastric cancer SGC-7901 cells by inhibiting expression of fibronectin 1[J]. Eur Rev Med Pharma Co, 2017, 21(8): 1753-8. |
| [10] |
Liu N C, Hsieh P F, Hsieh M K, et al. Capsaicin-mediated tNOX(ENOX2) up-regulation enhances cell proliferation and migration in vitro and in vivo[J]. J Agr Food Chem, 2012, 60(10): 2758-65. doi:10.1021/jf204869w |
| [11] |
俞辰斌, 赵国龙, 于立明, 等. JAK2/STAT3信号通路介导原花青素抗H9c2细胞缺氧/复氧损伤[J]. 生理学报, 2016, 68(5): 568-74. Yu C B, Zhao G L, Yu L M, et al. Proanthocyanidin protects H9c2 cells against hypoxia/reoxygenation injury via JAK2/STAT3 signaling pathway[J]. Acta Physiol Sin, 2016, 68(5): 568-74. |
| [12] |
刘善新.羟基红花黄素A对缺氧/复氧诱导的H9c2心肌细胞凋亡的影响及机制研究[D].杭州: 浙江大学, 2011. Liu S X. The study of effect and mechanisms of hydroxysafflor yellow A on anoxia/reoxygenation-induced apoptosis of H9c2 cardiomyocytes[D]. Hangzhou: Zhejiang University, 2011. |
| [13] |
董曦, 孙桂波, 罗云, 等. 异鼠李素对H2O2引起的H9c2细胞氧化应激损伤的保护作用研究[J]. 中国药理学通报, 2015, 31(6): 853-60. Dong X, Sun G B, Luo Y, et al. Protective effect of isorhamnetin on H9c2 cell line against oxidative stress[J]. Chin Pharmacol Bull, 2015, 31(6): 853-60. doi:10.3969/j.issn.1001-1978.2015.06.023 |
| [14] |
谢飞, 魏珂, 闵苏, 等. 神经生长因子对H9c2心肌细胞缺氧/复氧后凋亡的保护作用及其机制[J]. 中国药理学通报, 2014, 30(4): 506-10. Xie F, Wei K, Min S, et al. Anti-apoptotic effect of NGF on H9c2 cardiac myocytes in a hypoxia/reoxygenation injury model[J]. Chin Pharmacol Bull, 2014, 30(4): 506-10. doi:10.3969/j.issn.1001-1978.2014.04.014 |
| [15] |
Meng X, Wang M, Wang X, et al. Suppression of NADPH oxidase- and mitochondrion-derived superoxide by notoginsenoside R1 protects against cerebral ischemia-reperfusion injury through estrogen receptor-dependent activation of Akt/Nrf2 pathways[J]. Free Radical Res, 2014, 48(7): 823-38. doi:10.3109/10715762.2014.911853 |

