

2. 湖南中医药大学预防医学教研室,湖南 长沙 410208;
3. 湖南中医药大学生理学教研室,湖南 长沙 410208
2. Dept of Preventive Medicine, Hunan University of Chinese Medicine, Changsha 410208, China;
3. Dept of Physiology, Hunan University of Chinese Medicine, Changsha 410208, China
糖尿病肾病(diabetic nephropathy, DN)是糖尿病最常见、最严重的并发症之一。研究表明, 糖尿病发病10~20年后, 大约20%患者会发展为DN, 最终进展为终末期肾病[1]。目前, 我国DN已成为终末期肾功能衰竭的第2位病因, 造成沉重的家庭和社会负担[2]。
DN发生的标志性事件是肾小球微血管通透性增高, 形成微量蛋白尿。而足细胞损伤是导致蛋白尿持续发生和DN进展的重要原因。目前研究证实, 对于足细胞等终末分化细胞的生长和发育而言, 自噬具有重要意义。足细胞在生理状态下就具有较高的自噬水平, 自噬通过降解清除受损蛋白质和细胞器, 来维持足细胞功能[3]。在自然衰老及肾小球受损时, 足细胞的自噬功能受到抑制, 自噬抑制剂或敲除自噬相关基因的足细胞, 其滤过功能明显降低[4], 提示足细胞自噬在维持肾小球功能中发挥重要作用。研究发现, AMPK-mTOR途径是与营养密切相关的自噬调控的关键信号通路。
DN进展到肾功能衰竭的过程属阳气衰败, 水湿瘀浊内聚。因此, 当以温补肾阳、化气行水大法。金匮肾气汤是温补肾阳、化气行水的代表方。金匮肾气汤广泛应用于泌尿生殖系统、神经系统、免疫系统等疾病治疗。金匮肾气汤能够调节Bcl-2/Fas基因表达, 抑制肾小球细胞凋亡[5], 还能降低Ⅱ型糖尿病肾病血糖、尿白蛋白排泄率, 从而促进肾组织损伤修复、保护肾脏功能[6]。本研究旨在通过db/db糖尿病小鼠模型, 观察金匮肾气汤对足细胞自噬和AMPK-mTOR信号通路的影响, 探讨金匮肾气汤改善DN进展的分子机制, 为临床防治DN提供实验依据。
1 材料与方法 1.1 动物模型的建立4周龄♂ SPF级C57BL/KsJ-db/db小鼠20只, 作为II型糖尿病动物模型; 4周龄♂ C57BL/KsJ-db/m小鼠5只, 作为正常对照组(control)。小鼠均购自上海市斯莱克实验动物有限公司, 许可证号:SCXK (沪)2012-0002, 实验单位使用许可证号:SYXK (湘)2014-0012。6周龄时, 将20只db/db小鼠随机分为4组(每组5只), 并开始灌胃, 分别为:生理盐水组(db/db)、金匮肾气汤低剂量组(db/db+JG1, 1.3 g·kg-1)、金匮肾气汤高剂量组(db/db+JG2, 2.6 g·kg-1)、二甲双胍阳性对照组(db/db+MF, 0.2 g·kg-1)。于第18周龄处死动物。
1.2 药物制备金匮肾气汤各配方颗粒, 购自江阴天江药业有限公司。成人每日量10 g, 包括茯苓颗粒1 g (相当于饮片量为10 g, 以下括号内数值同)、牡丹皮颗粒1 g (6 g)、熟地黄4 g (10 g)、山药0.5 g (10 g)、泽泻1 g (10 g)、酒萸肉1.5 g (6 g)、桂枝0.5 g (6 g)、附片0.5 g (3 g)。将每10 g颗粒充分溶解于加热后的蒸馏水中。药物根据动物/人体表面积法折算, 结合前期预实验结果, 金匮肾气汤低、高剂量组剂量分别为1.3、2.6 g·kg-1。盐酸二甲双胍片, 中美上海施贵宝制药有限公司产品, 溶解于蒸馏水中, 剂量为0.2 g·kg-1。
1.3 血糖、肾功能检测18周时, 尾静脉取血, 用血糖仪检测血糖(三诺GA-3血糖试条, 三诺生物传感股份有限公司); 眼眶取血, 分别用尿素氮测定试剂盒、肌酐测定试剂盒(宁波医杰生物科技有限公司), 检测血清尿素氮和肌酐水平; 留24 h尿液, 分别用白蛋白测定试剂盒和肌酐测定试剂盒(宁波医杰生物科技有限公司), 测定24 h尿白蛋白排泄量和尿肌酐。
1.4 肾组织病理学检查18周龄处死动物后, 留取双侧肾皮质, 一部分肾皮质用4%多聚甲醛固定后, 制作成3 μm厚石蜡切片, 进行过碘酸希夫反应(PAS)染色, 用奥林巴斯BX-50显微镜观察肾小球内系膜区细胞外基质增生情况。一部分肾皮质用2.5%戊二醛固定后, 制作成50~100 nm切片, 用3%醋酸铀以及硝酸铅双染色, 透射电子显微镜(日立H7700)观察肾小球超微结构。
1.5 免疫组织化学染色采用SP法, 按照试剂盒的操作步骤, 检测足细胞Wilms肿瘤特异性基因(Wilms′ tumor protein 1, WT1)在肾小球的表达。兔抗小鼠WT1抗体(德国Abcam公司, 货号:ab89901)。光镜下胞核出现棕黄色颗粒为阳性表达, 400倍下随机采集20个不重叠视野, 计数每个视野下的阳性细胞数量, 并计算平均值。
1.6 Western blot检测采用2×SDS裂解液提取肾组织总蛋白, BCA法进行蛋白定量, 10% SDS-聚丙烯酰胺凝胶进行电泳分离, 转PVDF膜。牛奶室温封闭1 h后, 分别加入LC3Ⅱ/Ⅰ(货号12741S)、p62(货号5114S)、p-mTOR (货号5536S)、mTOR (货号2972S)、p-AMPK (货号2535S)、AMPK (货号5832S)一抗(抗体均购自美国CST公司), 4℃孵育过夜, TBST洗3次, 加入二抗(1:5 000), 室温孵育1 h, TBST洗3次, 用ECL显色并曝光, 采用ImageJ软件进行条带灰度扫描。
1.7 统计学分析实验数据以x±s表示, 运用SPSS 19.0统计软件进行分析。若数据符合正态分布及方差齐性, 采用多组间单因素方差分析方法(LSD); 若数据方差不齐或不符合正态分布, 进行秩转换后采用Kruskal-Wallis检验。
2 结果 2.1 金匮肾气汤对生化指标的影响为探讨金匮肾气汤对db/db小鼠的肾保护作用, 测定血糖、尿白蛋白、尿肌酐和血清肌酐水平。Tab 1结果显示, db/db小鼠血糖、血肌酐、24 h尿白蛋白、尿白蛋白/肌酐水平均明显高于db/m小鼠(P < 0.01), 提示db/db糖尿病小鼠肾功能受损。治疗12周后, 二甲双胍可使db/db小鼠血糖、血肌酐、24 h尿白蛋白、尿白蛋白/肌酐水平明显降低(P < 0.05);金匮肾气汤高剂量组可明显降低db/db小鼠血肌酐、24 h尿白蛋白、尿白蛋白/肌酐水平(P < 0.05);金匮肾气汤低剂量组可明显降低db/db小鼠24 h尿白蛋白、尿白蛋白/肌酐水平(P < 0.05)。提示金匮肾气汤可减轻db/db小鼠肾脏损伤, 改善肾功能, 但对血糖影响不明显。
| Group | Blood glucose/mmol·L-1 | Blood creatinine/μmol·L-1 | Urinary albumin/g·24 h-1 | Urinary albumin/creatinine/mg·g-1 |
| Control | 8.5±1.8 | 16.6±2.1 | 0.6±0.1 | 1.7±0.2 |
| db/db | 24.2±2.1** | 22.4±2.1** | 1.5±0.5** | 12.3±2.8** |
| db/db+JG1 | 23.5±8.9 | 20.8±1.9 | 1.0±0.2# | 10.7±2.2# |
| db/db+JG2 | 19.4±3.7 | 18.4±2.1# | 0.9±0.1# | 9.4±1.3# |
| db/db+MF | 17.7±4.7# | 16.8±2.1# | 1.1±0.1# | 9.7±1.3# |
| **P<0.01 vs control; #P<0.05 vs db/db | ||||
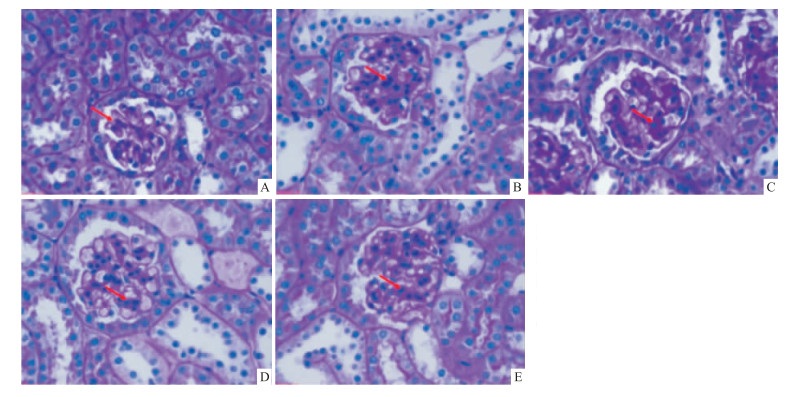
采用PAS染色观察db/db小鼠肾小球的病理变化。如Fig 1所示, 与正常对照组相比, db/db小鼠肾小球系膜区明显增宽, 金匮肾气汤低、高剂量组及二甲双胍组小鼠肾小球内系膜区增宽程度较生理盐水组减轻, 且金匮肾气汤高剂量组肾小球系膜区增宽程度较二甲双胍组轻, 表明金匮肾气汤延缓了DN肾小球病变的进展。
|
| Fig 1 Pathological changes of kidney in each group of mice (PAS, ×400) A:Control; B:db/db; C:db/db+JG1;D:db/db+JG2;E:db/db+MF.Red arrow showed mesangial region in glomerulus. |
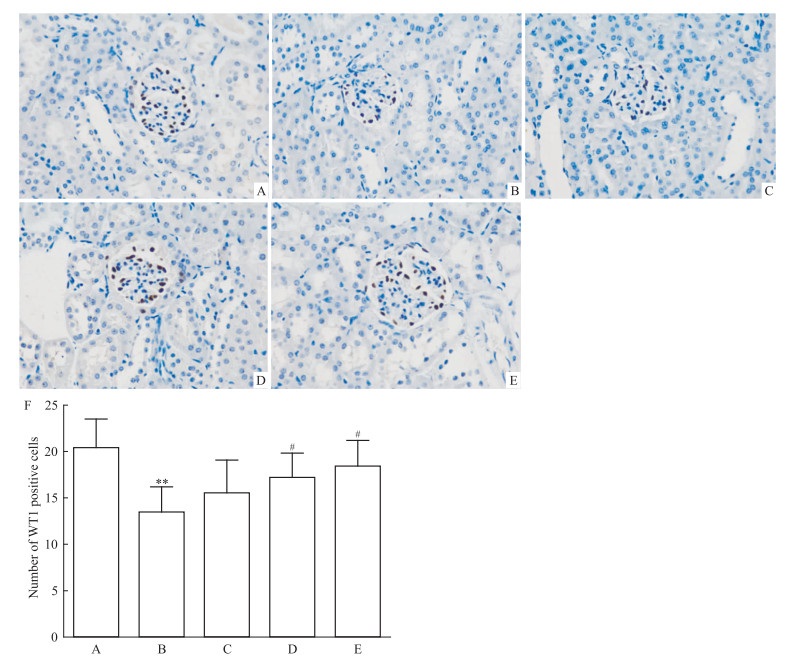
采用免疫组织化学方法标记肾小球足细胞WT1的表达。如Fig 2所示, 与正常对照组相比, db/db糖尿病小鼠生理盐水组肾小球内WT1阳性的细胞核数量明显减少; 金匮肾气汤治疗后, 低剂量组WT1阳性细胞核数量有所增加, 金匮肾气汤高剂量组和二甲双胍组阳性细胞核数量明显增加(P < 0.05)。提示金匮肾气汤可减轻db/db小鼠肾脏足细胞损伤。
|
| Fig 2 Number of WT1 positive cells in different groups (×400) A:Control; B:db/db; C:db/db+JG1;D:db/db+JG2;E:db/db+MF.F:Number fo WT1 possitive cells.**P < 0.01 vs control; #P < 0.05 vs db/db |
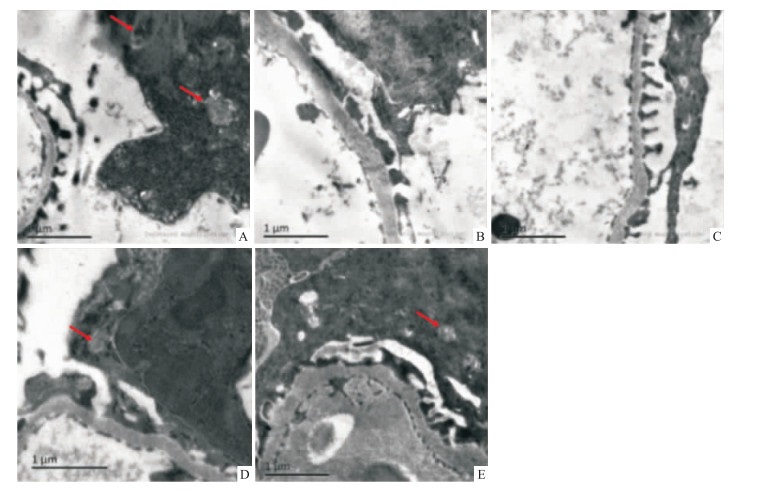
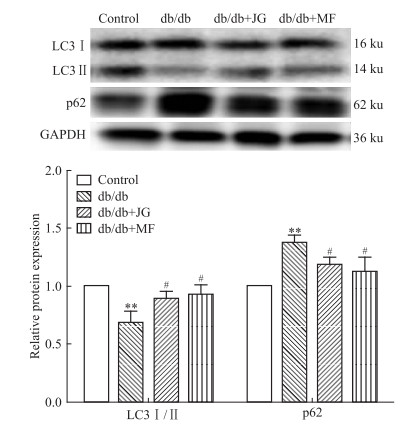
为了阐明自噬在金匮肾气汤肾脏保护中的作用, 采用透射电子显微镜检测肾小球足细胞内自噬体的情况。Fig 3结果显示, 正常组小鼠肾小球足细胞内可看到自噬体, db/db小鼠足细胞内自噬体缺失, 而金匮肾气汤高剂量组和二甲双胍组小鼠肾小球足细胞内也可见自噬体。采用Western blot检测肾组织中LC3和p62的蛋白表达, 如Fig 4所示, 生理盐水组db/db小鼠肾皮质LC3Ⅱ表达降低, p62表达增高; 金匮肾气汤高剂量组和二甲双胍组小鼠肾皮质内LC3Ⅱ表达明显增强, p62表达明显降低(P < 0.05)。结果表明, 金匮肾气汤的肾脏保护作用可能与改善糖尿病小鼠肾脏足细胞自噬不足有关。
|
| Fig 3 Transmission electron microscopy of kidneys in different groups (×2 000) A:Control; B:db/db; C:db/db+JG1;D:db/db+JG2;E:db/db+MF.Red arrow showed autophagosome in podocytes. |
|
| Fig 4 Expression of LC3I/II and p62 proteins in kidney tissues of each group (x±s, n=5) **P < 0.01 vs control; #P < 0.05 vs db/db |
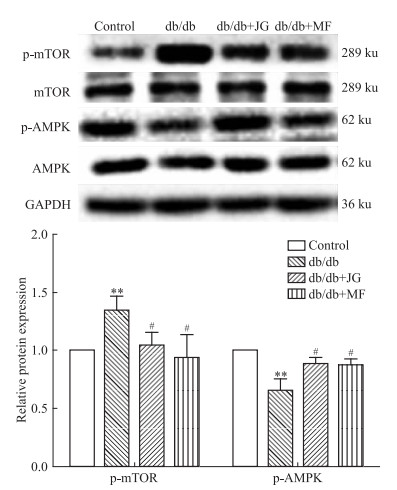
AMPK的激活和mTOR信号的衰减可促进自噬。如Fig 5所示, 与db/db糖尿病小鼠相比, 金匮肾气汤明显增强AMPK磷酸化, 抑制mTOR磷酸化(P < 0.05)。提示金匮肾气汤可能通过调节AMPK-mTOR信号通路, 促进足细胞自噬, 从而保护足细胞。
|
| Fig 5 Expression of p-mTOR/mTOR and p-AMPK/AMPK proteins in kidney tissues of each group (x±s, n=5) **P < 0.01 vs control; #P < 0.05 vs db/db |
金匮肾气汤方中重用地黄, 善滋补肾阴、益精填髓, 为君药。臣以山茱萸、山药, 补肝脾而益精血, 加以附子、肉桂之辛热, 助命门以温阳化气。君臣相伍, 补肾填精, 温肾助阳, 乃阴中求阳之治。佐以泽泻、茯苓利水渗湿泄浊, 丹皮清泄肝火, 三药于补中寓泻。诸药合用, 助阳之弱以化水, 滋阴之虚以生气, 使肾阳振奋, 气化复常, 则诸症自除。
前期研究发现, 金匮肾气汤可以减轻db/db糖尿病小鼠肾小球硬化, 减少24 h尿蛋白, 并激活足细胞自噬, 但具体的分子机制尚不清楚。本研究首先探讨金匮肾气汤对db/db糖尿病小鼠肾脏足细胞的保护作用。结果显示, 用金匮肾气汤治疗db/db
小鼠12周后, 24 h尿白蛋白、血清肌酐和尿白蛋白/肌酐水平降低, 系膜基质扩张减轻, 表明金匮肾气汤可以减缓DN的进展。但是, 本实验中金匮肾气汤并没有明显降低db/db小鼠的血糖水平, 这一发现与金匮肾气丸临床治疗2型DN患者[7]和干预STZ诱导的2型糖尿病大鼠后[8], 空腹血糖降低的结果不一致, 可能与动物和人体的差异或不同的实验模型有关。提示金匮肾气汤对db/db小鼠的肾保护作用可能与血糖控制无关。金匮肾气汤与二甲双胍皆可改善DN, 若能同时用药可能效果更佳, 有待进一步探讨。糖尿病足细胞损伤的形态学表现为足突消失、融合、肥大、脱离和死亡等[9]。蛋白尿的产生与足细胞密度降低和足细胞形态改变有关[10-11], 足细胞数量的减少可以预测蛋白尿的程度和肾功能的逐渐下降。WT1是肾脏发生过程中的一种重要蛋白, 对维持肾脏成熟足细胞的表型及功能状态起重要作用。本研究观察到, 与正常对照组相比, db/db糖尿病小鼠生理盐水组肾小球内WT1阳性的细胞核数量明显减少; 金匮肾气汤治疗后, 低剂量组WT1阳性细胞核数量有所增加, 金匮肾气汤高剂量组和二甲双胍组阳性细胞核数量明显增加。结果提示金匮肾气汤可减轻db/db小鼠肾脏足细胞损伤, 从而改善肾功能和蛋白尿。
足细胞具有活跃的自噬能力, 即使在非应激状态下也是如此, 这表明足细胞需要较高的基础自噬水平来维持细胞内稳态。Lenoir等[12]研究发现, 在特异性敲除足细胞自噬相关基因Atg5后, 随着小鼠年龄的增长, 足细胞内出现泛素化蛋白聚集、线粒体损伤、自噬活性减弱, 进而导致肾小球硬化, 表明自噬对维持足细胞的正常功能具有非常重要的作用。Ilatovskaya等[13]研究表明, DN患者出现明显的足细胞损伤, 如足细胞足突消失及足细胞数量减少, 且与蛋白尿产生和肾小球硬化呈正相关。本研究发现, 金匮肾气汤恢复了LC3II的表达, 降低了p62的表达。此外, 电镜检查也证实金匮肾气汤能增强足细胞的自噬活性。这些结果表明, 在db/db糖尿病小鼠中, 改善足细胞内的自噬不足在金匮肾气汤的肾保护作用中起着重要作用。
AMPK-mTOR途径是与营养密切相关的自噬调控的关键信号通路。Langer等[14]研究发现, 高糖能够降低足细胞AMPK磷酸化、激活mTOR, 从而抑制自噬, 二甲双胍(AMPK激活剂)可以剂量依赖性促进自噬、抗凋亡, 并且逆转高糖诱导的足细胞损伤。本研究发现, 与db/db糖尿病小鼠相比, 金匮肾气汤明显增强AMPK磷酸化, 抑制mTOR磷酸化。提示金匮肾气汤可能通过调节AMPK-mTOR信号通路来促进足细胞自噬, 从而保护足细胞。
综上所述, 金匮肾气汤通过AMPK-mTOR途径促进足细胞自噬, 保护足细胞, 延缓DN的进展。这些发现为进一步了解金匮肾气汤在DN中肾保护作用的分子机制提供了新的思路。
( 致谢: 本研究在湖南中医药大学医学院实验室和湘雅医院病理科完成, 在此致以由衷的感谢! )
| [1] |
Van Buren P N, Toto R. Current update in the management of diabetic nephropathy[J]. Curr Diabetes Rev, 2013, 9(1): 62-77. doi:10.2174/157339913804143207 |
| [2] |
Xu Y, Wang L, He J, et al. Prevalence and control of diabetes in Chinese adults[J]. JAMA, 2013, 310(9): 948-59. doi:10.1001/jama.2013.168118 |
| [3] |
Mizushima N, Komatsu M. Autophagy: renovation of cells and tissues[J]. Cell, 2011, 147(4): 728-41. doi:10.1016/j.cell.2011.10.026 |
| [4] |
Fang L, Zhou Y, Cao H, et al. Autophagy attenuates diabetic glomerular damage through protection of hyperglycemia-induced podocyte injury[J]. PLoS One, 2013, 8(4): e60546. doi:10.1371/journal.pone.0060546 |
| [5] |
展照双, 齐丽娟, 吕翠霞, 等. 肾气丸与右归丸对肾虚大鼠肾脏细胞凋亡及肾组织内Bcl-2、Fas表达的影响[J]. 山东中医杂志, 2011, 30(6): 412-4. Zhan Z S, Qi L J, Lyu C X, et al. Effects of Shenqi Pill and Yougui Pill on apoptosis of renal cells and expression of Bcl-2, Fas in renal tissue of kidney deficiency rats[J]. Shandong J Tradit Chin Med, 2011, 30(6): 412-4. |
| [6] |
李青, 韩宇博. 金匮肾气丸联合美卡素治疗Ⅲ期糖尿病肾病的临床研究[J]. 光明中医, 2014, 29(3): 576-7. Li Q, Han Y B. Clinical study of Jinguishenqi Pill combined with mekacin in the treatment of stage Ⅲ diabetic nephropathy[J]. Guangming J Chin Med, 2014, 29(3): 576-7. doi:10.3969/j.issn.1003-8914.2014.03.076 |
| [7] |
刘忠文. 金匮肾气丸治疗糖尿病肾病的疗效评价[J]. 中国中医基础医学杂志, 2014, 20(6): 118-9, 128. Liu Z W. Evaluation of curative effect of Jinkui Shenqi Pill on diabetic nephropathy[J]. Chin J Basic Med Tradit Chin Med, 2014, 20(6): 118-9, 128. |
| [8] |
金智生, 陈雪, 李甜. 金匮肾气丸对实验性2型糖尿病肾病大鼠肾脏组织NO、NOS的影响[J]. 中医药学报, 2012, 40(1): 60-3. Jin Z S, Chen X, Li T. Effect of Jinguishenqi Pill on NO, NOS in renal tissue of experimental type 2 diabetic nephropathy rats[J]. Acta Chin Med Pharmacol, 2012, 40(1): 60-3. |
| [9] |
Weil E J, Lemley K V, Mason C C, et al. Podocyte detachment and reduced glomerular capillary endothelial fenestration promote kidney disease in type 2 diabetic nephropathy[J]. Kidney Int, 2012, 82(9): 1010-7. doi:10.1038/ki.2012.234 |
| [10] |
Shankland S J. The podocyte's response to injury: role in proteinuria and glomerulosclerosis[J]. Kidney Int, 2006, 69(12): 2131-47. doi:10.1038/sj.ki.5000410 |
| [11] |
丁海华, 邱原野, 王盈盈, 等. 小檗碱对糖尿病肾病大鼠nephrin、podocin和α3β1整合素表达的影响[J]. 中国药理学通报, 2015, 31(10): 1414-20. Ding H H, Qiu Y Y, Wang Y Y, et al. Effect of berberine on the expression of nephrin, podocin and intergrin α3β1 in diabetic nephropathy rats[J]. Chin Pharmacol Bull, 2015, 31(10): 1414-20. doi:10.3969/j.issn.1001-1978.2015.10.018 |
| [12] |
Lenoir O, Jasiek M, Henique C, et al. Endothelial cell and podocyte autophagy synergistically protect from diabetes-induced glomerulosclerosis[J]. Autophagy, 2015, 11(7): 1130-45. doi:10.1080/15548627.2015.1049799 |
| [13] |
Ilatovskaya D V, Levchenko V, Lowing A, et al. Podocyte injury in diabetic nephropathy: implications of angiotensin Ⅱ-dependent activation of TRPC channels[J]. Sci Rep, 2015, 5: 17637. doi:10.1038/srep17637 |
| [14] |
Langer S, Kreutz R, Eisenreich A. Metformin modulates apoptosis and cell signaling of human podocytes under high glucose conditions[J]. J Nephrol, 2016, 29(6): 765-73. doi:10.1007/s40620-015-0258-1 |

