

2. 大理白族自治州人民医院体检中心,云南 大理 671000;
3. 云南省第一人民医院/昆明理工大学附属医院,云南 昆明 650032
肖怀(1973-),女,博士,教授,研究方向:天然药物化学、天然药物药理学,Tel:0872-2214251,通讯作者,E-mail:422022546@qq.com
 ,
ZOU Hong-qun2,
LI Qi-yan1,3,
GAO Yuan1,
ZHANG Zhi-xue1,
ZHAO Hai-rong1,
ZHANG Cheng-gui1
,
ZOU Hong-qun2,
LI Qi-yan1,3,
GAO Yuan1,
ZHANG Zhi-xue1,
ZHAO Hai-rong1,
ZHANG Cheng-gui1
 ,
XIAO Huai1
,
XIAO Huai1

2. Dept of Pathology, Dali Bai Autonomous Prefecture People's Hospital, Dali Yunnan 671000, China;
3. The First People's Hospital of Yunnan Province/The Affiliated Hospital of Kunming University of Science and Technology, Kunming 650032, China
脑缺血性疾病是严重危害人类健康的常见病和多发病。脑缺血损伤与细胞凋亡的关系非常密切, 在脑缺血后的几小时内, 缺血半暗带或梗死区周围的神经元死亡主要以凋亡性死亡为主。其中, 海马CA1区的锥体神经元对全脑缺血引起的损伤尤为敏感, 再灌注2~4 d后, 该部位出现锥体神经元迟发性死亡[1-2]。基于神经细胞凋亡与脑缺血损伤关系的深入研究, 神经保护源的研究成为抗脑缺血研究的主要焦点。缺血性脑血管病目前常规的治疗, 采用抗凝、抗血小板聚集、溶栓、针对卒中单元的改善等。替格瑞洛(ticagrelor)是一种新型抗血小板药物, 口服后无代谢激活, 可与血小板表面的P2Y12受体蛋白可逆结合, 拮抗血小板聚集[3], P2Y12受体蛋白属于G蛋白偶联受体家族, 是抗血小板聚集药物研发的常用靶点。临床上用于预防急性冠脉综合征(acute coronary syndrome, ACS)患者的血栓栓塞。相关报道还显示, 替格瑞洛除具有抗血小板作用, 还具有神经保护作用[4]。因此, 本实验以四血管阻塞法(four-vessel occlusion, 4-VO), 即双侧椎动脉、双侧颈总动脉阻塞15 min制备大鼠全脑缺血/再灌注损伤模型, 探讨替格瑞洛对大鼠海马组织CA1区神经元数目的影响, 以研究其对大鼠全脑缺血/再灌注损伤的神经保护作用, 为后续研究替格瑞洛神经保护机制及临床开发药物新用途提供一定的实验依据。
1 材料 1.1 实验动物SPF级健康♂Wistar大鼠, 体质量(250~300) g, 购于辽宁长生生物技术股份有限公司, 许可证号:SCXK (辽)2015-0001。实验动物在大理大学实验动物中心实验室适应性饲养1~2周后, 用于正式实验。饲养条件:清洁级, 室温(16~22)℃, 相对湿度70%, 12 h明暗交替照明, 自由进食、饮水。动物处置方法均符合中国伦理委员会有关动物研究指导原则要求。
1.2 药物与试剂替格瑞洛(批号:0868314002), 购自Astra Zeneca AB; 多聚甲醛(批号:20151115), 购自天津市光复精细化工研究所; 水合氯醛(批号:20170712), 购自国药集团化学试剂有限公司; 注射用青霉素钠(批号:F7032114), 购自华北制药股份有限公司; 薇婷脱毛膏(批号:J20170017), 购自利洁时家化(中国)有限公司。
1.3 仪器AggRAM血小板聚集仪(Helena Laboratories公司); TCL16M型台式高速冷冻离心机(湖南湘立科学仪器有限公司); Elektrisk kniv型电凝器(精益医疗器械有限公司); MOTIC倒置显微镜(日本SPEED FAIR公司)。
2 方法 2.1 模型的制备所有大鼠于实验前1 d, 用脱毛膏将枕骨部位毛发脱干净, 以便进行手术及防止手术后伤口感染。参考Pulsinelli等[5]和李兵等[6]的4-VO 15 min法复制模型, 主要分3个步骤:(1)大鼠以10%水合氯醛300 mg·kg-1腹腔注射麻醉后, 仰卧位固定于直流加热垫上(温度控制在37℃), 酒精消毒后备皮, 在颈部正中切口约1.5 cm, 暴露双侧颈总动脉, 并在两侧颈总动脉穿线套扣, 再缝合颈部伤口。(2)俯卧位固定, 在枕骨后切开皮肤, 暴露第1颈椎两侧的翼小孔, 用尖端直径为0.5 mm的电凝器, 插入翼孔, 烧灼双侧的椎动脉, 造成永久性闭塞, 再缝合颈部伤口, 注射青霉素。(3)待动物适应24 h后, 用异氟烷吸入式麻醉大鼠后, 剪开在颈部正中的切口, 用镊子轻轻拉出套扣, 暴露两侧颈总动脉, 再夹闭两侧颈总动脉, 夹闭时间为15 min, 此为全脑缺血期。15 min后松开动脉夹, 并除去套扣, 可恢复血流, 进行再灌注实验, 此为缺血后再灌注期。缺血达到以下标准, 即夹闭双侧颈总动脉10 s内, 大鼠出现意识丧失、角膜反射和翻正反射消失, 可见大鼠四肢上举, 双侧瞳孔散大, 眼球呈灰白色, 身体可呈角弓反张, 并在15 min缺血期内, 意识和上述反射均未恢复者, 视为手术成功, 方可实施再灌流及治疗给药。在缺血期死亡或仅出现昏睡, 以及在整个实验过程中出现抽搐的大鼠均被剔除。假手术组不进行双侧椎动脉电凝, 也不夹闭双侧颈总动脉, 其余操作相同。
2.2 动物分组及给药将造模成功大鼠分为模型组、替格瑞洛低、中、高剂量组(37.5、75、150 mg·kg-1), 每组10只。分别于造模后2、24、48 h给药, 替格瑞洛按照相应剂量灌胃0.08 mL·kg-1, 假手术组和模型组等体积灌胃生理盐水, 连续治疗给药3 d, 每天1次。
2.3 指标检测 2.3.1 大鼠卒中指数和神经病学评分大鼠再灌注2、24、48 h后, 分别进行卒中指数(apoplexy index)和神经病学症状(neurology symptom)评分。卒中指数评分标准[7]:毛发脏乱颤抖, 1分; 运动减少或迟钝, 1分; 耳触觉迟钝, 3分; 头翘起, 3分; 后肢外展呈"八"字, 3分; 上睑下垂, 1分; 转圈, 3分; 惊厥或爆发运动, 3分; 极度虚弱, 6分。总分25分, 0~3分为症状组, 3~9分为中间组, 可能有损伤, >10分明显有损伤。神经病学症状评分标准[8]:有自发探究, 0分; 刺激时能走动, 1分; 正常步态, 0分; 共济失调, 1分; 爬行, 2分; 无步态, 3分; 能进食, 0分; 不能进食, 1分; 能饮水, 0分; 不能饮水, 1分; 疼痛刺激可移动, 0分; 仅头或躯干运动, 1分; 肢体回缩或无反应, 2分。总分10分, 0分正常, 1~3分轻度损伤, 4~6分中度损伤, 7~10分严重损伤。
2.3.2 凝血功能检测末次给药2 h后, 各组大鼠以10%水合氯醛300 mg·kg-1腹腔注射麻醉, 腹主动脉取血, 采用3.8%枸橼酸钠溶液抗凝(枸橼酸钠与血液容积之比为1:9), 3 000 r·min-1离心10 min, 分离血浆, 用全自动凝血分析仪检测活化部分凝血活酶时间(activated partial thrombophastin time, APTT)、凝血酶原时间(prothrombin time, PT)、凝血酶时间(thrombin time, TT)和纤维蛋白原(fibrinogen, FIB)。
2.3.3 血小板聚集率的测定参考实验方法[9], 大鼠以10%水合氯醛300 mg·kg-1腹腔注射麻醉, 腹主动脉取血, 采用3.8%枸橼酸钠溶液抗凝(枸橼酸钠与血液容积之比为1:9), 充分混匀后, 25℃、1 022 r·min-1离心10 min, 取上层血浆即得富血小板血浆(platelet rich plasma, PRP)。将剩余的血浆, 25℃、4 571 r·min-1离心15 min后, 取上层血浆即得贫血小板血浆(platelet poor plasma, PPP)。参考文献方法[10], 按比浊法测定3 min血小板最大聚集率。
2.3.4 HE染色观察组织病理学形态所有大鼠腹主动脉取血后, 用预冷的生理盐水进行心脏灌流, 直至右心耳流出的液体无色清亮时停止, 再用4%多聚甲醛灌注固定。固定后立即取脑, 去除嗅球及小脑, 置10%中性福尔马林液中24 h, 于视交叉(左右两条视神经在下视丘下面的会合)处切开取材, 常规脱水, 石蜡包埋, 连续冠状切片(厚度4~5 μm), 置37℃温箱内烘烤1~2 h后, 二甲苯脱蜡, 进行HE染色, 在光学显微镜下观察脑组织病变。
2.3.5 Nissl染色检测脑组织海马CA1区神经元数目前期处理同HE染色, 切片、烘片、脱蜡后进行Nissl染色, 在光镜下观察海马CA1区的病理学变化, 以及在400倍镜下计数1 mm长度细胞条带内细胞膜和核膜完整的神经元数目, 取两侧海马区神经元数目之和的平均数为CA1区正常神经元数, 神经元密度(neuronal density, ND)[11]计算公式如下:

|
数据均用SPSS 21.0统计软件处理, 结果以表示, 采用单因素方差分析(One-way ANOVA)进行组间均数的显著性检验, 并以LSD-t检验进行多重比较。数据不符合正态性或方差不齐的采用非参数检验中的Mann-Whitney检验分析比较。
3 结果 3.1 替格瑞洛对大鼠全脑缺血/再灌注损伤卒中指数评分的影响Tab 1结果显示, 与假手术组比较, 模型组、替格瑞洛各组卒中指数在再灌注2、24、48 h均明显升高(P < 0.01);与模型组比较, 替格瑞洛(37.5、75、150 mg·kg-1)组卒中指数在再灌注24 h (P < 0.05)和48 h (P < 0.01)时均降低。
| Group | Dose/ mg·kg-1 | Stroke index | ||
| 2 h | 24 h | 48 h | ||
| Sham | - | 0.00±0.00 | 0.00±0.00 | 0.00±0.00 |
| Vehicle | - | 9.6±3.4** | 10.9±1.5** | 10.7±1.5** |
| Ticagrelor | 37.5 | 9.3±1.7** | 8.1±1.9**# | 7.6±1.4**## |
| 75 | 9.4±2.2** | 8.2±1.6**# | 6.9±1.6**## | |
| 150 | 9.1±2.8** | 8.0±1.9**# | 7.2±1.6**## | |
| **P < 0.01 vs sham; #P < 0.05, ##P < 0.01 vs vehicle | ||||
Tab 2结果显示, 与假手术组比较, 模型组、替格瑞洛各组神经病学评分在再灌注2、24、48 h均明显升高(P < 0.01);与模型组比较, 替格瑞洛(37.5、75、150 mg·kg-1)组神经病学评分在再灌注48 h明显降低(P < 0.01), 2 h和24 h均有降低的趋势。
| Group | Dose/ mg·kg-1 | Neurological functional score | ||
| 2 h | 24 h | 48 h | ||
| Sham | - | 0.00±0.00 | 0.00±0.00 | 0.00±0.00 |
| Vehicle | - | 4.8±1.8** | 4.6±2.3** | 4.8±1.2** |
| Ticagrelor | 37.5 | 3.4±0.9** | 3.0±1.1** | 2.5±0.9**## |
| 75 | 3.5±0.9** | 3.1±1.1** | 2.6±0.9**## | |
| 150 | 3.4±1.3** | 3.1±1.0** | 2.8±1.0**## | |
| **P < 0.01 vs sham; ##P < 0.01 vs vehicle | ||||
Tab 3结果显示, 与假手术组比较, 替格瑞洛(37.5、75、150 mg·kg-1)组PT和TT未见明显变化; APTT有延长的趋势; FIB含量呈升高的趋势, 差异均无统计学意义(P>0.05)。
| Group | n | Dose/mg·kg-1 | APTT/s | PT/s | TT/s | FIB/s |
| Sham | 7 | - | 23.54±4.60 | 15.36±3.42 | 32.50±6.31 | 2.46±1.29 |
| Vehicle | 10 | - | 24.14±2.73 | 15.51±1.46 | 29.87±1.93 | 2.86±0.59 |
| Ticagrelor | 9 | 37.5 | 25.39±2.75 | 16.16±0.99 | 29.83±0.89 | 2.74±0.57 |
| 8 | 75 | 24.44±1.88 | 15.53±0.65 | 30.01±0.73 | 3.16±0.54 | |
| 8 | 150 | 26.29±6.16 | 16.14±2.60 | 29.33±1.68 | 2.79±0.91 |
Tab 4结果显示, 与假手术组比较, 模型组血小板聚集率明显升高(P < 0.01);与模型组比较, 替格瑞洛(37.5、75、150 mg·kg-1)组血小板聚集率均明显降低(P < 0.01)。
| Group | Dose/mg·kg-1 | Platelet aggregation rate/% |
| Sham | - | 50.82±4.41 |
| Vehicle | - | 60.56±2.98** |
| Ticagrelor | 37.5 | 15.49±6.31**## |
| 75 | 14.69±4.60**## | |
| 150 | 11.52±0.75**## | |
| **P < 0.01 vs sham; ##P < 0.01 vs vehicle | ||
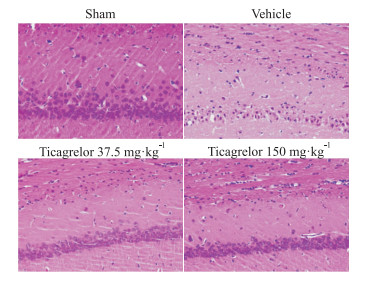
再灌注48 h, 大鼠石蜡脑切片HE染色结果显示(Fig 1), 假手术组海马CA1区锥体神经元排列整齐紧密, 有3~4层神经元, 细胞紫蓝色较深, 细胞形态完整, 边界清晰; 模型组海马CA1区神经元体积缩小, 有2~3层神经元, 细胞紫蓝色较浅, 细胞膜皱缩内陷, 形成泡状小体即凋亡小体; 替格瑞洛各剂量组海马CA1区锥体神经元排列疏松, 有2~3层神经元, 细胞紫蓝色较浅, 细胞形态完整, 边界清晰, 无小胶质细胞浸润。
|
| Fig 1 Hippocampal CA1 region of brain tissues (HE×400) |
再灌注48 h, 大鼠石蜡脑切片尼氏染色结果显示(Fig 2), 假手术组大鼠海马CA1区锥体细胞形态结构完整, 排列整齐紧密, 核膜核仁清晰, 胞核饱满, 大量神经元存在; 模型组大鼠海马CA1区神经元细胞大量丢失, 残存的神经元体积缩小呈现固缩破裂, 疏松变形, 排列紊乱, 胞体形状不规则, 核仁消失, 出现大量空泡样结构; 细胞膜皱缩内陷, 形成泡状小体即凋亡小体; 替格瑞洛各剂量组海马CA1区锥体神经元排列较为紧密, 细胞形态完整, 边界清晰。替格瑞洛治疗能保持神经元细胞的结构完整性, 并具有一定剂量依赖性, 其中替格瑞洛150 mg·kg-1组细胞结构和形态已基本和假手术组一致。

|
| Fig 2 Hippocampal CA1 region of brain tissues (Nissl, ×400) |
Tab 5结果显示, 与假手术组比较, 模型组大鼠海马神经元数目明显降低(P < 0.01);与模型组比较, 替格瑞洛(37.5、75、150 mg·kg-1)组大鼠海马神经元数目明显增加(P < 0.01), 且与假手术组已基本无差异(P>0.05)。
| Group | n | Dose/mg·kg-1 | Number of neurons |
| Sham | 7 | - | 174±20 |
| Vehicle | 8 | - | 76±60** |
| Ticagrelor | 7 | 37.5 | 172±63## |
| 6 | 75 | 205±48## | |
| 8 | 150 | 197±20## | |
| **P < 0.01 vs sham; ##P < 0.01 vs vehicle | |||
本实验采用的4-VO法是目前国际公认的全脑缺血动物模型制备方法之一, 电凝双侧椎动脉加结扎双侧颈总动脉, 达到全脑缺血目的, 该方法制备的动物模型病理与人脑急性缺血性病变接近, 且重复性强、成功率高。替格瑞洛是一种被批准用于治疗急性冠脉综合征的抗血小板药物, 其作为抗血小板聚集药物, 可拮抗P2Y12受体, 抑制血小板活化和聚集, 用于治疗脑梗死和心肌梗死[3]。有证据表明, 替格瑞洛在动物急性卒中模型中具有神经保护作用, 本实验旨在探讨替格瑞洛对大鼠全脑缺血/再灌注损伤的脑组织海马神经元的神经保护作用。缺血性脑卒中是全球最常见的死亡率和致残率均较高的脑血管疾病之一。脑组织在缺血/缺氧损伤作用下, 缺血半暗带神经元发生一系列神经功能缺损形态学变化[12]。除引起神经功能障碍外, 全脑缺血/再灌注损伤还有较强的区域敏感性, 还可选择性导致大鼠海马及皮层损伤, 其中海马CA1区锥体神经元最为敏感, 缺血时极易受损。因此, 以海马CAl区作为观察区域。缺血/再灌注3 d后, 明显看到大量CA1区锥体细胞破坏, 主要病变表现为神经细胞肿胀、核质空泡形成、核染色深, 甚至神经细胞结构消失。本实验结果表明, 替格瑞洛对大鼠全脑缺血/再灌注引起的海马神经元损伤有一定保护作用, 具体表现为抑制CA1区神经元细胞固缩、浓染, 减少神经元丢失, 改善神经元形态的病变。缺血/再灌注损伤引起的神经细胞死亡主要有坏死和凋亡2种方式。细胞凋亡是重要的神经细胞死亡方式。Bcl-2是重要的抗凋亡蛋白, 可通过抑制caspase-3的生成和活化, 发挥抑制凋亡的作用。本实验还存在不足之处, 未对神经细胞凋亡相关蛋白进行检测, 今后将对神经凋亡相关基因、蛋白进行检测, 以明确其神经保护作用机制。
抗血小板药物能够有效预防缺血性脑卒中的发病及复发, 综合国内外相关研究显示, 替格瑞洛是一个很有潜力的新型口服抗血小板聚集药物。出血是所有抗血小板药物首要的安全问题, 不仅导致并发症、死亡和医疗费用增加, 而且由于抑制了血小板的活性, 在受伤或手术等事件中给止血带来困难[13]。替格瑞洛也不例外, 但替格瑞洛与P2Y12受体的结合为可逆性结合, 当替格瑞洛在体内代谢消除之后, ADP可与血小板的受体结合, 使血小板重新恢复活性, 循环中的血小板功能均能够恢复, 长期使用不会导致血小板水平呈破坏性下降。替格瑞洛还具有撤药后药效消失较快的特点, 因此有益于降低出血可能性。林开敏等[14]研究结果显示, 替格瑞洛对临床患者治疗1个月后, 替格瑞洛组出血事件的发生率为4.16%。替格瑞洛对全脑缺血/再灌注损伤大鼠血小板聚集率影响实验结果显示, 替格瑞洛治疗组血小板聚集率比Sham组低。因此, 在临床应用中应对其出血风险加强监控, 以及使用可能增加出血风险药物的患者慎用替格瑞洛, 则可能降低替格瑞洛的使用风险, 使其用药安全、有效。
抗血栓形成的重要机制之一是抑制凝血系统的活化。凝血过程由于启动环节不同, 分为内源性与外源性凝血两条途径, 其中反映内源性凝血途径活性的是APTT, 反映外源性凝血途径活性的是PT, 而TT则反映了两种途径的共同影响因子凝血酶的活性。无论内源性, 还是外源性凝血途径, 最终都通过激活凝血因子Ⅱ(凝血酶)使纤维蛋白原变为纤维蛋白, 从而发生凝血[15]。本研究结果提示, 替格瑞洛各剂量均可延长APTT、PT时间, 表明替格瑞洛对凝血酶-纤维蛋白原反应有直接抑制作用, 即替格瑞洛有凝血活性。
综上所述, 本实验结果显示替格瑞洛能降低大鼠卒中指数和神经病学评分, 抑制大鼠血小板聚集, 保护神经元结构的完整性, 减少再灌注损伤海马神经元丢失, 对全脑缺血4-VO大鼠模型具有一定神经保护作用, 其神经保护机制还需进行进一步相关实验研究, 以期阐明其神经保护机制, 为替格瑞洛抗凋亡治疗脑血管疾病提供实验依据。
( 致谢: 本实验在大理大学昆虫生物医药研发重点实验室完成, 感谢实验室的老师和同学对实验的指导和帮助。)
| [1] |
Ouyang Y B, Stary C M, Yang G Y, et al. microRNAs: innovative targets for cerebral ischemia and stroke[J]. Curr Drug Targets, 2013, 14(1): 90-101. doi:10.2174/138945013804806424 |
| [2] |
周晓楠, 宋雪兰, 李艳, 等. 对羟基苯甲醛对脑缺血/再灌注损伤的保护作用研究[J]. 中国药理学通报, 2017, 33(12): 1733-5. Zhou X N, Song X L, Li Y, et al. The protective effects of 4-hydroxybenzaldehyde on cerebral ischemia/reperfusion injury[J]. Chin Pharmacol Bull, 2017, 33(12): 1733-5. |
| [3] |
李慕鹏, 熊艳, 陈小平. 抗血小板药物替格瑞洛药代药效动力学及遗传药理学研究进展[J]. 中国临床药理学与治疗学, 2014, 19(2): 214-22. Li M P, Xiong Y, Chen X P. Advances in pharmacodynamics and pharmacogenetics of anti-platelet drug ticagrelor[J]. Chin J Clin Pharmacol Ther, 2014, 19(2): 214-22. |
| [4] |
Gelosa P, Pignieri A, Fontana L, et al. Neuroprotective evidence for the P2Y 12 antagonist ticagrelor in an acute model of stroke in rodents[C]. Milan, 2012: 12-3.
|
| [5] |
Pulsinelli W A, Brierley J B. A new model of bilateral hemispheric ischemia in the unanesthetized rat[J]. Stroke, 1979, 10(3): 267. |
| [6] |
李兵, 章翔, 蒋晓帆, 等. 改良四血管阻塞法建立大鼠全脑缺血模型[J]. 中华神经外科疾病研究杂志, 2005, 4(2): 110-3. Li B, Zhang X, Jiang X F, et al. Modifying the four-vessel occlusion method to establish the globalbrain ischem icmodel of rat[J]. Chin J Neurosurg Dis Res, 2005, 4(2): 110-3. doi:10.3969/j.issn.1671-2897.2005.02.005 |
| [7] |
Ni J, Ohta H, Matsumoto K, Watanabe H. Progressive cognitive impairment following chronic cerebral hypoperfusion induced by permanent occlusion of bilateral carotid arteries in rats[J]. Brain Res, 1994, 653(1-2): 231-6. doi:10.1016/0006-8993(94)90394-8 |
| [8] |
张继东, 侯铁胜, 赵定麟. 大剂量甲基强的松龙对大鼠损伤脊髓中神经生长因子的影响[J]. 中华外科杂志, 1995, 33(12): 727-9. Zhang J D, Hou T S, Zhao D L. The effect of high dose methyl-prednisolone on tatal nerve growth factor with injured spinal cord in rat[J]. Chin J Surgery, 1995, 33(12): 727-9. doi:10.3760/j:issn:0529-5815.1995.12.009 |
| [9] |
Tyurenkov I N, Perfilova V N, Karamysheva V I, et al. Effect of GABA derivatives on the rate of thrombus formation, platelet aggregation, and plasma coagulation capacity in rats with experimental gestosis[J]. Bulletin of Experimental Biology and Medicine, 2014, 158(2): 219-221. doi:10.1007/s10517-014-2726-3 |
| [10] |
关杰, 任军伟, 朱远, 等. 光学比浊法与连续血小板计数法监测血小板聚集功能的比较[J]. 解放军医学院学报, 2013, 34(8): 838-41. Guan J, Ren J W, Zhu Y, et al. Platelet aggregation function monitored by light transmittance aggregometry and continuous platelet count[J]. Acad J Chin PLA Med Sch, 2013, 34(8): 838-41. doi:10.3969/j.issn.2095-5227.2013.08.016 |
| [11] |
蒋玉凤, 朱陵群, 黄启福, 等. 清开灵注射液对SHPsp出血性中风海马区兴奋性氨基酸含量的影响[J]. 中国中医急症, 1997, 6(5): 219-21. Jiang Y F, Zhu L Q, Huang Q F, et al. Effects of Qingkailing Injection on the content of excitatory amino acids in hippocampus of SHPsp hemorrhagic stroke[J]. JETCM, 1997, 6(5): 219-21. |
| [12] |
佘颜, 王宇红, 邵乐, 等. 补阳还五汤精简方对大鼠脑缺血后血管新生及Nrf2/HO-1信号途径的影响[J]. 中国药理学通报, 2016, 32(1): 126. Yu Y, Wang Y H, Shao L, et al. Effects of thin recipe of Buyang Huanwu Decoction on angiogenesis and signal pathway of Nrf2 / HO-1 after cerebral ischemic injury in rat[J]. Chin Pharmacol Bull, 2016, 32(1): 126. |
| [13] |
苏子云, 袁叶, 田溪, 等. 替格瑞洛相关不良反应的研究进展[J]. 中国新药杂志, 2016, 25(8): 878-82. Su Z Y, Yuan Y, Tian X, et al. Progress in research of the side effect of ticagrelor[J]. Chin J New Drugs, 2016, 25(8): 878-82. |
| [14] |
林开敏, 吴雅芳, 谢强. 比较替格瑞洛与氯吡格雷对老年患者支架术后出血的影响[J]. 中国生化药物杂志, 2015, 35(9): 152-4. Lin K M, Wu Y F, Xie Q. Comparison of ticagrelor versus clopidogrel in effect of bleeding in elderly patients after stenting[J]. Chin J Biochem Drugs, 2015, 35(9): 152-4. |
| [15] |
冯锐, 王音, 朱凤, 等. Ento-Ⅰ涂膜剂的镇痛及其抗凝抗血栓形成作用[J]. 国际药学研究杂志, 2016, 43(3): 512-3. Feng R, Wang Y, Zhu F, et al. Effects of Ento-Ⅰplastic on analgesia, anticoagulation and anti-thrombosis[J]. J Int Pharm Res, 2016, 43(3): 512-3. |