

2. 浙江大学城市学院药学系,浙江 杭州 310015
2. Dept of Pharmacy, City College, Zhejiang University, Hangzhou 310015, China
乳腺癌是严重威胁女性健康的恶性疾病之一,全球每年新发病患者超过100万。近年来,我国女性乳腺癌的发病率以每年3%的速度增长,且发病人群日趋年轻化。虽然最近肿瘤治疗在分子靶向治疗和生物治疗等方面突飞猛进,但与乳腺癌相关的研究进展较少,且由于乳腺癌是实体肿瘤中对化疗敏感的肿瘤,因此,化疗在乳腺癌的临床治疗中仍然占有重要地位[1-2]。然而,由于晚期乳腺癌患者复发率和转移率高,我国每年因乳腺癌的死亡人数高达4万人,加上药物的滥用以及肿瘤本身的异质性或其他原因,越来越多的晚期乳腺癌的化疗以失败告终,因此,寻找新型化疗药物对乳腺癌的治疗有重要意义。
7-氯4-氧代-喹啉(chloroxoquinoline),简称氯氧喹,是一种新型的口服喹啉类抗肿瘤药。氯氧喹主要通过损伤肿瘤细胞DNA合成来发挥抗肿瘤作用,其抗瘤谱较广,临床常作为晚期乳腺癌和非小细胞肺癌的化疗用药[3]。然而,氯氧喹对非小细胞肺癌和胃癌的治疗研究仅有零星报道,对乳腺癌细胞的研究更显缺失,且其对乳腺癌细胞凋亡、增殖、细胞周期的影响及确切机制尚不清楚[4-7]。本研究检测了氯氧喹对3种不同乳腺癌细胞系的抑制作用,并对其作用机制进行了初步探讨。
1 材料与方法 1.1 材料 1.1.1 细胞株正常乳腺上皮细胞MCF10A,以及乳腺癌细胞系Bcap37、MDA-MB-231、MDA-MB-453,均由浙江大学肿瘤研究所提供。
1.1.2 药物与试剂氯氧喹、紫杉醇,均购自通化茂祥制药有限公司,用10%的DMSO溶解后过滤,实验时用培养基稀释到所需终浓度。RPMI 1640培养基、胎牛血清,购自美国Gibco公司;MTT粉末、DMSO,购自美国Sigma公司;Annexin V/PI凋亡试剂盒,购自美国Life Technologies公司;抗体多聚ADP核糖聚合酶(poly ADP-ribose polymerase,PARP)、caspase-3、GAPDH、p21、CDC2,均购自美国Cell Signaling Technology公司。
1.1.3 仪器流式细胞仪FACSCaliber(美国BD公司);酶标仪SpectraMax 190(美国Molecular Devices公司)。
1.2 细胞培养Bcap37、MDA-MB-231和MDA-MB-453细胞用含10%胎牛血清、100 kU·L-1青霉素、100 mg·L-1链霉素的RPMI 1640培养基培养。将细胞置于37 ℃、5% CO2培养箱静置培养,待细胞长至80%~90%时进行传代,接种于培养瓶或培养板中,取对数生长期的细胞进行实验。
1.3 MTT法观察细胞增殖抑制率取对数生长期的细胞,以4×103每孔接种到96孔板中,培养24 h后,给予氯氧喹(50、100、150、200、300 mg·L-1),分别观察药物作用24、48、72 h后肿瘤细胞的存活率,每个浓度和时间设至少3个复孔,对照组给予相同浓度的等容量培养基。MTT法的检测按常规方式进行,并计算存活率,细胞存活率/%=(实验组OD-空白组OD)/(对照组OD-空白组OD)×100%。
1.4 Annexin V/PI双染法检测细胞凋亡率取对数生长期的细胞,以5×104每孔接种到12孔板中,培养24 h后,加入不同浓度的氯氧喹培养。基于前期实验结果及氯氧喹的溶解度,选取100、200 mg·L-1两个浓度。继续培养48 h后,加入100 μL预先配制的1×Annexin结合液,再加入5 μL Annexin V-FITC和1 μL碘化丙啶(PI),混匀后,冰上避光孵育15 min,加入400 μL预冷的结合液,轻柔混匀后,立即用流式细胞仪检测,记录并保存结果。
1.5 细胞周期的检测取对数生长期的细胞,以1×105每孔接种到6孔板中,培养24 h。加入氯氧喹(100、200 mg·L-1)培养48 h,消化后,将细胞轻轻吹打成单个细胞,离心后,加入预冷的PBS和3.5 mL无水乙醇,混匀后,于4 ℃固定30 min,离心除去无水乙醇,加入200 μL PBS和2 μL的RNA酶(0.25 g·L-1),于37 ℃孵育30 min。再加入0.5 mL浓度为50 mg·L-1的PI溶液室温避光孵育30 min,立即用流式细胞仪检测。
1.6 Western blot检测取生长状态良好的细胞,以1×105/孔接种到6孔板中,并置于37 ℃、5% CO2培养箱培养24 h。加入不同浓度的氯氧喹培养48 h。收集细胞,提取总蛋白,经SDS-PAGE凝胶电泳、转膜、封闭后,分别加入抗PARP、caspase-3、p21、CDC2抗体(1 : 1 000)或GADPH抗体(1 : 2 000),4 ℃孵育过夜,洗膜后,用辣根过氧化酶标记的相应二抗(1 : 5 000)孵育2 h。采用ECL化学发光剂获取蛋白表达信号,蛋白表达比值采用ImageJ软件进行灰度分析。
1.7 统计学分析采用SPSS 16.0软件进行统计学分析,数值以x±s表示。组间比较采用one-way ANOVA分析。
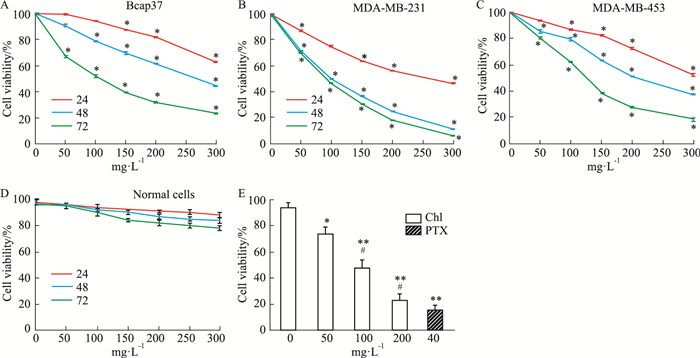
2 结果 2.1 氯氧喹对乳腺癌细胞生长的抑制作用氯氧喹对Bcap37、MDA-MB-231和MDA-MB-453三种乳腺癌细胞株增殖的影响见Fig 1A-1C。在作用24 h后,随着氯氧喹浓度的增加,在最低给药浓度50 mg·L-1时,对Bcap37和MDA-MB-453的抑制作用不明显,但当浓度增加到150 mg·L-1时,对3种细胞的增殖均有明显抑制作用,呈现浓度依赖关系。氯氧喹作用48、72 h后,各个浓度均可以明显抑制3种细胞系的增殖(P < 0.05), 且作用72 h的抑制作用较作用48 h的抑制作用更为明显。作用72 h后,氯氧喹对Bcap37、MDA-MB-231和MDA-MB-453的IC50值为别为97.9、81.3、105.23 mg·L-1。上述结果表明,氯氧喹对乳腺癌细胞的增殖具有明显抑制作用,其中对MDA-MB-231细胞更敏感。为验证氯氧喹是否具有毒性作用,采用同样处理方式,观察了氯氧喹对正常乳腺上皮细胞MCF10A的生长抑制作用。如Fig 1D所示,氯氧喹不同浓度作用24 h后,对正常细胞的生长抑制作用不明显,但在作用48、72 h后,氯氧喹浓度为100 mg·L-1时抑制率约为10%,在200 mg·L-1时约为18%,提示氯氧喹高剂量和长时间作用后具有一定的毒性作用。
|
| Fig 1 Chl inhibited growth of breast cancer cells (x±s, n=5) Cells were treated with different dose of Chl for 24, 48 and 72 h, and cell viability was assessed by MTT assay. A: Cell viability of Bcap37 cells; B: Cell viability of MDA-MB-231 cells; C: Cell viability of MDA-MB-453 cells; D: Cell viability of normal breast epithelial cells; E: MDA-MB-231 cells were treated with either 0, 50, 100 and 200 mg·L-1 of Chl or 40 mg·L-1 of PTX for 48 h, and subjected to MTT assay. *P < 0.05, **P < 0.01 vs control of the same time point; #P < 0.05 vs PTX. |
选取常用乳腺癌化疗药紫杉醇(paclitaxel,PTX)40 mg·L-1为阳性对照药,以MDA-MB-231为观察对象,不同浓度氯氧喹作用48 h后,抑制效果均较紫杉醇低,但200 mg·L-1氯氧喹与紫杉醇相比差异无显著性(Fig 1E)。
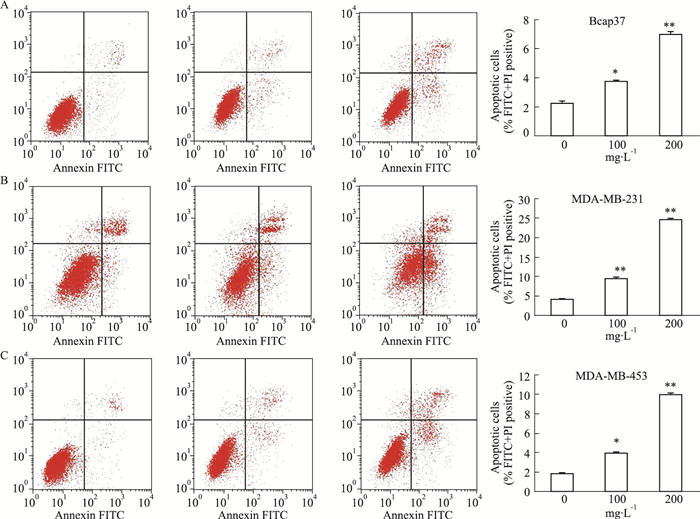
2.2 氯氧喹对乳腺癌细胞凋亡的影响基于生长抑制实验的结果,选取氯氧喹(100、200 mg·L-1)作用48 h后,用流式细胞术检测凋亡细胞比例。如Fig 2所示,氯氧喹(100、200 mg·L-1)均可明显增加3个细胞系的凋亡细胞数目(P < 0.05),且在200 mg·L-1时效果更明显,尤其在MDA-MB-231细胞,凋亡率增加更为明显。
|
| Fig 2 Chl promoted apoptosis in breast cancer cells (x±s, n=3) A: Representative image of flow cytometry and quantitative analysis of apoptotic cells in Bcap37 cells; B: Representative image of flow cytometry and quantitative analysis of apoptotic cells in MDA-MB-231 cells; C: Representative image of flow cytometry and quantitative analysis of apoptotic cells in MDA-MB-453 cells. *P < 0.05, **P < 0.01 vs control. |
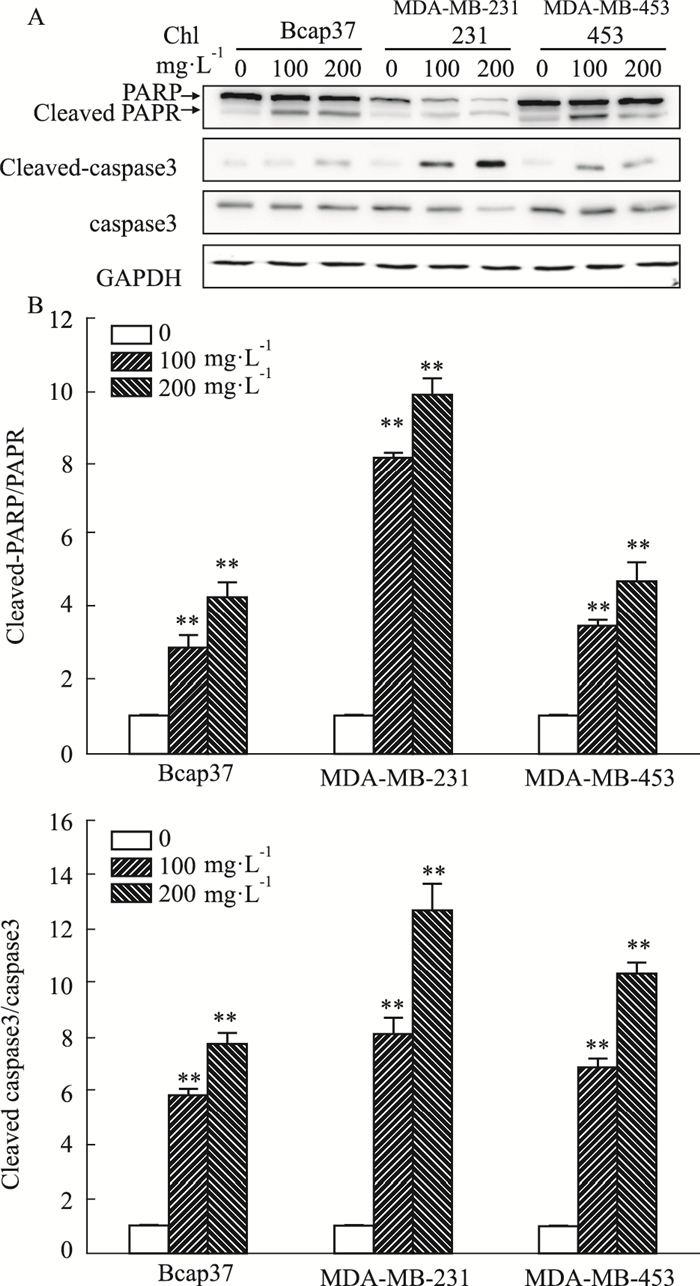
为了进一步验证氯氧喹对乳腺癌细胞凋亡的影响,检测了凋亡相关蛋白cleaved-PARP、cleaved-caspase-3的表达。Fig 3的Western blot结果显示,氯氧喹(100、200 mg·L-1)作用48 h后,3个细胞系中cleaved-PARP/PARP、cleaved-caspase-3/caspase-3的比值均较对照组明显增加(P < 0.05),尤其是在MDA-MB-231细胞更为明显,与流式细胞术检测的细胞凋亡结果一致。上述结果提示,氯氧喹对于乳腺癌细胞有很好的促凋亡作用。
|
| Fig 3 Chl promoted cleaved-PARP and cleaved-caspase-3 expression in breast cancer cell (x±s, n=3) A: Representative blots of cleaved-PARP, PARP, cleaved-caspase-3, caspase-3 expression in three breast cancer cells; B: Quantitative analysis of the ratio of cleaved-PARP/PARP expression; C: Quantitative analysis of the ratio of cleaved-caspase-3/caspapse-3 expression. The cleaved-PARP/PARP and cleaved-caspase-3/caspase-3 ratio were normalized to the control group. *P < 0.05, **P < 0.01 vs control. |
如Fig 4所示,虽然在高剂量下,氯氧喹对MDA-MB-231的细胞周期有一定阻滞作用(P < 0.05),但G2/M期占比仅为23.6%。而在Bcap37和MDA-MB-453细胞中,低浓度氯氧喹即导致G2/M期占比分别为21.7%、25.8%(P < 0.05),高浓度下占比更加明显,分别为64.8%和58.6%(P < 0.01)。提示氯氧喹可阻滞细胞周期,尤其在Bcap37和MDA-MB-453细胞中更为明显。

|
| Fig 4 Chl arrested breast cancer cells on G2/M stage (x±s, n=3) A: Representative image of flow cytometry and quantitative analysis of cell cycle in Bcap37 cells; B: Representative image of flow cytometry and quantitative analysis of cell cycle in MDA-MB-231 cells; C: Representative image of flow cytometry and quantitative analysis of cell cycle in MDA-MB-453 cells.*P < 0.05, **P < 0.01 vs control. |
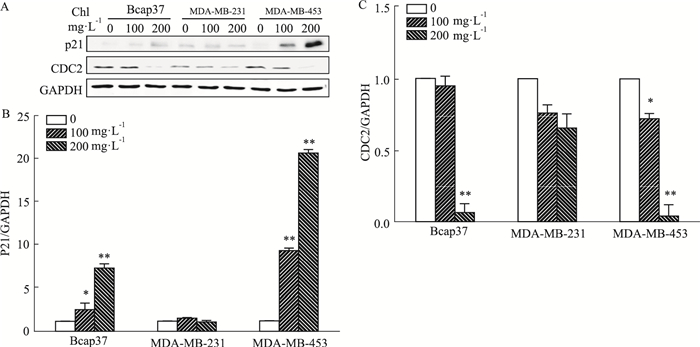
氯氧喹对细胞周期相关蛋白表达的影响见Fig 5。氯氧喹高、低剂量对MDA-MB-231细胞p21、CDC2蛋白表达的作用均不明显。但在Bcap37和MDA-MB-453细胞中,氯氧喹可上调p21、下调CDC2的表达(P < 0.05),且高剂量更为明显(P < 0.01)。以上结果进一步验证在Bcap37和MDA-MB-453细胞系,氯氧喹具有细胞周期调控作用。
|
| Fig 5 Chl increased p21 expression and decreased CDC2 expression in breast cancer cells (x±s, n=3) A: Representative blots of p21 and CDC2 expression in three breast cancer cells; B: Quantitative analysis of p21 protein expression; C: Quantitative analysis of CDC2 protein expression. *P < 0.05, **P < 0.01 vs control. |
氯氧喹作为新型抗肿瘤化疗药物,已经有较多的临床研究报道。国内临床研究通过比较氯氧喹单药与环磷酰胺-阿霉素-顺铂联合化疗方案治疗晚期非小细胞肺癌的疗效,发现两者的疗效无明显差异,但氯氧喹的毒副反应明显低于联合化疗组[4-6]。氯氧喹还能与其他抗癌药物合用,具有协同作用,如与表阿霉素、顺铂和5-氟尿嘧啶合用治疗晚期胃癌,可延长患者生存时间,减轻化疗的毒副作用,提高晚期癌症患者的生存质量[7]。氯氧喹还对肺癌细胞和裸鼠异体种植的肺癌有放射增敏作用[8]。本研究发现,氯氧喹可明显降低3种乳腺癌细胞的存活率,但其作用机制有差异。其中对于MDA-MB-231主要表现为促进肿瘤细胞凋亡,而在Bcap37和MDA-MB-453细胞主要以细胞周期阻滞作用为主。
诱导肿瘤细胞凋亡是许多化疗药物发挥抗肿瘤作用的途径。化疗药物诱导的肿瘤细胞的凋亡主要有两条途径,包括外源性途径和内源性途径。外源性途径是指化疗药物通过活化肿瘤细胞膜表面的死亡受体,如肿瘤坏死因子受体家族成员等,引起caspase-8的活化,从而导致肿瘤细胞的凋亡。内源性途径通过触发肿瘤细胞中间代谢途径,导致线粒体通透性的改变,也可以通过提高促凋亡第2信使Smac/DIABLO的浓度,导致线粒体渗透性的改变[9-10]。乳腺癌细胞的凋亡与乳腺癌易感基因1和2 (BRCA1、BRCA2)关系密切,BRCA1和BRCA2基因是抑癌基因,在DNA双链损伤的同源重组修复中发挥重要作用,并通过多种通路诱导细胞凋亡[11]。本研究发现,氯氧喹能促进3种乳腺癌细胞凋亡,尤其对于MDA-MB-231细胞株的促凋亡作用明显,Western blot的结果亦证实,断裂的PARP和caspase-3蛋白表达在MDA-MB-231细胞株明显增加。然而,即使在MDA-MB-231细胞系中,高剂量氯氧喹能使细胞凋亡率增加25%以上,但高剂量下细胞活性的下降高达80%左右,提示细胞活性减少不仅仅是来自于细胞凋亡,还有可能来自抑制细胞增殖。虽然文献中未能查阅Bcap37和MDA-MB-453是否存在BRCA1和BRCA2基因突变,但MDA-MB-231细胞株为非突变株,提示氯氧喹在BRCA1和BRCA2非突变株的促细胞凋亡效果更好,可能通过线粒体通路诱导细胞凋亡[12-13]。另外,由于MDA-MB-231细胞株为高转移性乳腺癌,上皮间质转化在其转移和浸润中发挥重要作用[14]。本研究发现,氯氧喹对MDA-MB-231细胞株的生长增殖尤其敏感,氯氧喹能否抑制其转移和浸润,将是非常有意义的研究。
细胞周期阻滞是抗肿瘤药物发挥作用的另一个常见途径。细胞周期的有序运行通过相关蛋白的严格监视和调控来保证,其中p21和CDC2蛋白均为重要的细胞周期调控蛋白。p21是p53的下游基因,通过阻断DNA聚合酶的活性,抑制DNA合成,从而阻滞细胞周期,抑制细胞分裂。CDC2与cyclin B组成的复合物正调控G2/M期检测点,促进细胞进入M期,是推动细胞优势分裂的重要蛋白,受p21的负调控。本研究发现,氯氧喹可将Bcap37和MDA-MB-453细胞明显阻滞于G2/M期,且p21蛋白表达明显上升,而CDC2蛋白明显下降,提示在这两个细胞系中,氯氧喹有很好的细胞周期阻滞作用,与他人研究报道一致[15]。
本研究中选取的3个细胞系均为雌激素受体(estrogen receptor, ER)阴性的细胞系,因此不能评价氯氧喹在ER阳性的乳腺癌细胞系的作用。今后将以ER阳性细胞系如MCF-7为实验对象,进一步探索氯氧喹的作用与ER的关系。另外,目前临床应用氯氧喹以单用为主,在将来的实验中我们将比较其单用与联合阿霉素和紫杉醇用药的作用及可能的机制。
综上所述,氯氧喹对Bcap37、MDA-MB-231和MDA-MB-453均有明显增殖抑制作用,其分别与细胞凋亡和细胞周期阻滞有关,为氯氧喹临床应用于乳腺癌奠定了理论基础,也为乳腺癌的化疗提供新的思路。
( 致谢:本实验在浙江大学城市学院药物研究所完成,感谢药理学研究室所有的老师和同学对本课题研究给予的悉心指导和帮助。)
| [1] |
Westphal T, Gampenrieder S P, Rinnerthaler G, et al. Cure in metastatic breast cancer[J]. Memo, 2018, 11(3): 172-9. doi:10.1007/s12254-018-0426-9 |
| [2] |
Allahverdiyev A M, Parlar E, Dinparvar S, et al. Current aspects in treatment of breast cancer based of nanodrug delivery systems and future prospects[J]. Artif Cells Nanomed Biotechnol, 2018, 9(27): 1-8. |
| [3] |
耿维凤. 抗癌新药——氯氧喹胶囊[J]. 中国医院药学杂志, 2005, 25(10): 100. Geng W F. Chloroxoquinoline capsule:the new anti-cancer drug[J]. Chin Hosp Pharm, 2005, 25(10): 100. |
| [4] |
要静妍. 氯氧喹治疗晚期非小细胞肺癌临床观察[J]. 山西医药杂志(下半月刊), 2012, 41(6): 619-20. Yao J Y. Clinical observation of chloroxoquinoline in the treatment of advanced non-small cell lung cancer[J]. Shanxi Med J, 2012, 41(6): 619-20. |
| [5] |
曲雅琴, 董丽华, 李宝英, 等. 氯氧喹对晚期非小细胞肺癌T细胞亚群的影响[J]. 中国肿瘤临床, 2001, 28(2): 155-7. Qu Y Q, Dong L H, Li B Y, et al. Effect of chloroxoquinoline on T cell subsets in advance non-small cell lung cancer[J]. Chin J Clin Oncol, 2001, 28(2): 155-7. doi:10.3969/j.issn.1000-8179.2001.02.031 |
| [6] |
孔玉莲, 李肇彦, 杨会燕, 等. 三种方法治疗晚期非小细胞肺癌疗效对比[J]. 中国误诊学杂志, 2012, 12(12): 2872. Kong Y L, Li Z Y, Yang H Y, et al. Comparison of the efficacy of three methods in the treatment of advanced non-small cell lung cancer[J]. Chin J Misdiagnostics, 2012, 12(12): 2872. |
| [7] |
Zhu X D, Hu X C, Zhang W, et al. Chloroxoquinoline in combination with epirubicin, cisplatin and 5-fluorouracil in metastatic gastric cancer[J]. Hepatogastroenterology, 2009, 56(90): 555-60. |
| [8] |
陈志明, 赵银龙, 潘兴喜, 等. 氯氧喹对Lewis肺癌细胞及荷瘤小鼠的辐射增敏作用[J]. 中华放射医学与防护杂志, 2011, 31(1): 33-7. Chen Z M, Zhao Y L, Pan X X. Radition sensitizing effect of chloroxoquinoline on Lewis lung cancer cells and xenograft tumors in mice[J]. Chin J Radiol Med Prot, 2011, 31(1): 33-7. |
| [9] |
Saelens X, Festjens N, Vande W L, et al. Toxic proteins released from mitochondria in cell death[J]. Oncogene, 2004, 23(16): 2861-74. doi:10.1038/sj.onc.1207523 |
| [10] |
Moll U M, Wolff S, Speidel D, et al. Transcription-independent pro-apoptotic functions of p53[J]. Currt Opin Cell Biol, 2005, 17(6): 631-6. doi:10.1016/j.ceb.2005.09.007 |
| [11] |
Feng Y, Spezia M, Huang S, et al. Breast cancer development and progression: Risk factors, cancer stem cells, signaling pathways, genomics, and molecular pathogenesis[J]. Genes Dis, 2018, 5(2): 77-106. doi:10.1016/j.gendis.2018.05.001 |
| [12] |
韦立群, 李婉婷, 李通, 等. 金雀异黄酮对三阴乳腺癌MDA-MB-231细胞凋亡及EGFR/PI3K/Akt通路的影响[J]. 中国药理学通报, 2017, 33(10): 1376-81. Wei L Q, Li W T, Li T, et al. Effects of genistein on apoptosis and EGFR/PI3K/Akt signal transduction pathway in triple-negative breast cancer MDA-MB-231 cells[J]. Chin Pharmacol Bull, 2017, 33(10): 1376-81. doi:10.3969/j.issn.1001-1978.2017.10.010 |
| [13] |
袁立明, 马楠, 曹交欢, 等. 顺铂加重乳腺癌MCF-7细胞DNA损伤促凋亡的研究[J]. 中国药理学通报, 2017, 33(3): 334-7. Yuan L M, Ma N, Cao J H, et al. Study of cisplatin aggravating DNA damage and causing a high apoptosis rate on breast cancer MCF-7 cells[J]. Chin Pharmacol Bull, 2017, 33(3): 334-7. doi:10.3969/j.issn.1001-1978.2017.03.009 |
| [14] |
Liang Q, Li L, Zhang J, et al. CDK5 is essential for TGF-β1-induced epithelial-mesenchymal transition and breast cancer progression[J]. Sci Rep, 2013, 3: 2932. doi:10.1038/srep02932 |
| [15] |
周慧, 周伟强. 组蛋白去乙酰化酶抑制剂调控p21(WAF1/CIP1)启动子乙酰化水平影响乳腺癌MCF-7细胞周期[J]. 中国药理学通报, 2017, 33(10): 1421-5. Zhou H, Zhou W Q. SAHA affects cell cycle of MCF-7 breast cancer cells by regulating acetylated levels of p21WAF1/CIP1 promoter[J]. Chin Pharmacol Bull, 2017, 33(10): 1421-5. doi:10.3969/j.issn.1001-1978.2017.10.018 |

