

补骨脂为豆科植物补骨脂(Psoralea corylifolia L.)的干燥成熟果实,具有温肾助阳、纳气和止泻的功效。补骨脂含有多种活性成分,主要成分为补骨脂素和异补骨脂素。补骨脂的应用十分广泛,常用中成药中含有补骨脂的有30余种。近年来,补骨脂的肝脏毒性引起了广泛关注,相继有临床和实验研究报道,其能导致肝脏毒性[1-2],韩国曾报道了与大量食用补骨脂有关的急性肝炎病例。另外,部分含有补骨脂的中成药,如壮骨关节丸、白蚀丸也偶见肝毒性报道[3-4]。补骨脂素与异补骨脂素在补骨脂所导致的肝损害中贡献较大[5-6],研究表明,异补骨脂素能导致HepG2细胞胆汁酸蓄积,进而产生细胞毒性;腹腔注射异补骨脂素可以引起C57BL/6J小鼠肝损伤[7-8]。以上研究显示,异补骨脂素在细胞水平及整体动物水平,均能引起肝损伤。基于此,本研究通过对SD大鼠连续灌胃异补骨脂素1、3、7 d,进一步验证异补骨脂素对肝脏的损伤作用,探讨异补骨脂素的毒性作用规律,并且基于胆汁酸转运体,初步探讨异补骨脂素肝脏毒性的作用机制。
1 材料与方法 1.1 实验动物SD大鼠,32只,♀♂各半,体质量170~200 g,购自北京华阜康生物科技股份有限公司,许可证号:SCXK(京)2014-0004。
1.2 药物与试剂异补骨脂素购自天津市月牙湖科技有限公司,批号201502,其纯度经HPLC检测大于98%。黄蓍树胶粉购自北京索莱宝科技有限公司;TRIzol购自塞默飞世尔科技公司;谷氨酸氨基转移酶(alanine transaminase, ALT)试剂盒、天冬氨酸氨基转移酶(aspartate transaminase, AST)试剂盒、碱性磷酸酶(alkaline phosphatase, ALP)试剂盒、总胆汁酸(total bile acid, TBA)试剂盒、总胆固醇(total cholesterol, TC)试剂盒、总甘油三脂(total triglyceride, TG)试剂盒、总胆红素(total bilirubin, TBIL)试剂盒,均由中生北控生物科技股份有限公司生产;实时定量聚合酶链式反应引物,由上海生工生物工程有限公司合成;反转录试剂盒、扩增试剂盒,购自北京全式金生物技术有限公司。
1.3 仪器Legend Micro17离心机(赛默飞世尔科技公司);7020全自动生化仪(日本Hitachi公司);CFX96型荧光定量PCR仪(美国Bio-Rad公司);超声破碎仪(Vibra-cell processors,美国Sonics公司)。
1.4 方法 1.4.1 异补骨脂素对大鼠的肝毒性大鼠适应性喂养5 d后,随机分为对照组(黄蓍树胶助溶剂组)、异补骨脂素60 mg·kg-1给药1 d组、3 d组以及7 d组,每组8只,♀♂各半。异补骨脂素用受试药5%量的黄蓍树胶助溶,溶解于生理盐水中。给药结束后,所有动物进行麻醉取血、取肝脏,全自动生化仪检测血清中ALT、AST、ALP、TBA、TC、TG及TBIL的含量,计算肝脏系数。肝脏系数=肝脏重量(g)/体质量(g)×100%。
1.4.2 实时定量PCR称取50~70 mg相同位置的肝脏组织,使用眼科剪将组织剪成约1 mm3大小的碎块,加入TRIzol试剂,运用超声破碎仪破碎组织后,按照常规方法提取总RNA。按反转录试剂盒要求进行反转录。实时定量PCR反应体系为20 μL,其中cDNA样本2 μL,上、下游引物各0.4 μL,Top/Tip Green qPCR SuperMix试剂10 μL,无RNA酶水7.2 μL。在94 ℃预变性4 min,每个循环94 ℃变性5 s,50~60 ℃退火15 s,72 ℃延伸10 s,共35~40个循环。取2-△△CT值进行数据统计。引物序列见Tab 1。
| Gene | Forward primer | Reverse primer |
| BSEP | 5’-CCTTGCTGATTGCCTTCT-3’ | 5’-TGTGCGGATATTGCTGAG-3’ |
| NTCP | 5’-CATTCTCTCTGCTCTCTTCCAACTCA-3’ | 5’-AGTTGAATGTTTTGGAATCCTGTTTC-3’ |
| MRP2 | 5’-GACTGCACGACCTTCGAGAGA-3’ | 5’-CCTCAGACTCCCCGAGAACAA-3’ |
| MRP4 | 5’-CAGCAGCTGGGTAAGGGCG-3’ | 5’-ATTCCGTCTGAAGTACACCTGTTTTG-3’ |
| MDR1 | 5’-GTGGATGAAGATGTGCCTATGG-3’ | 5’-TATCGGAGTCGCTTGGTGAG-3’ |
| ABCG5 | 5’-TCTCCTTGTACATCGAGAGTGGC-3’ | 5’-CGTCCAGCAGCGTGGTTT-3’ |
| ABCG8 | 5’-ACCAACTGTGGAACTGCTGCT-3’ | 5’-CCGGAAGTCATTGGAAATCTG-3’ |
| OSTα | 5’-GTGTCTGTGTTCTGCTGCTT-3’ | 5’-GGTGTCCTTCAGTGTCCTTAGT-3’ |
| GAPDH | 5’-ATGGGAAGCTGGTCATCAAC-3’ | 5’-GTGGTTCACACCCATCACAA-3’ |
实验数据以x±s表示,各给药组与对照组之间比较采用t检验。
2 结果 2.1 异补骨脂素对大鼠体质量的影响如Fig 1所示,给药前,各组动物体质量没有明显区别。给药后,与对照组相比较,异补骨脂素60 mg·kg-1给药3 d组的大鼠体质量明显下降。异补骨脂素60 mg·kg-1给药1 d后,大鼠肝脏重量没有明显变化,给药3 d和7 d后,大鼠肝脏重量明显增加。异补骨脂素给药1、3、7 d后,肝脏系数均明显升高。

|
| Fig 1 Effect of isopsoralen on body weight(A), liver weight(B) and liver/body weight ratio(C)after oral administration for 1, 3 or 7 days (x±s, n=8) *P < 0.05, **P < 0.01 vs control group |
如Tab 2所示,大鼠给予异补骨脂素3 d和7 d后,血清中的ALT均明显升高。给予异补骨脂素1、3、7 d后,血清中AST的含量明显增加,ALP的水平在3组中均没有明显变化。TBA在异补骨脂素给药7 d组的大鼠血清中明显升高,给药1 d和3 d组中的TC明显降低。各给药组中的TG均明显上升,给药7 d组的TBIL明显增加。
| Group | ALT/U·L-1 | AST/U·L-1 | ALP/U·L-1 | TBA/μmol·L-1 | TC/mmol·L-1 | TG/mmol·L-1 | TBIL/μmol·L-1 |
| Control | 31.4±5.7 | 94.9±13.0 | 183.5±40.0 | 137.64±79.43 | 1.73±0.19 | 0.24±0.04 | 0.23±0.08 |
| Isopsoralen 1 d | 32.0±7.7 | 130.8±16.5** | 182.8±68.6 | 144.46±102.77 | 1.40±0.37* | 0.49±0.16** | 0.23±0.06 |
| Isopsoralen 3 d | 54.8±11.4** | 151.0±25.0** | 186.5±72.1 | 229.34±155.18 | 1.30±0.34** | 0.44±0.18** | 0.31±0.12 |
| Isopsoralen 7 d | 46.5±7.6** | 139.4±16.1** | 148.1±58.4 | 262.38±137.43* | 1.54±0.29 | 0.34±0.07** | 0.32±0.08* |
| *P < 0.05, **P < 0.01 vs control group | |||||||
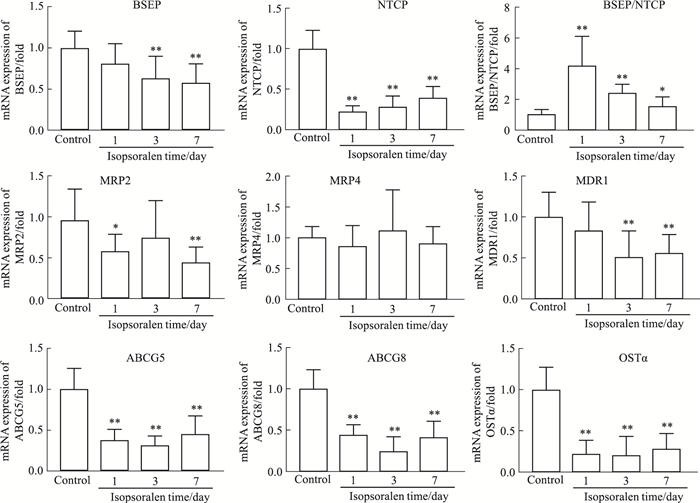
如Fig 2所示,大鼠给予异补骨脂素3 d和7 d后,肝脏中胆盐输出泵(bile salt export pump, BSEP)的mRNA水平明显下降,异补骨脂素1、3、7 d组中钠离子-牛磺胆酸共转运蛋白(sodium taurocholate cotransporting polypeptide, NTCP)的mRNA水平明显下降,BSEP、NTCP的mRNA之比也明显升高。异补骨脂素给药1 d和7 d后,多药耐药相关蛋白2(multidrug resistance associated protein 2, MRP2)的mRNA水平明显下降,异补骨脂素给药3 d组中MRP2的mRNA水平有下降趋势,但是差异无显著性。各组中多药耐药相关蛋白4(multidrug resistance associated protein 4, MRP4)的mRNA水平均没有明显变化。异补骨脂素给药3 d和7 d组中,多药耐药蛋白1(multidrug resistance 1, MDR1)的mRNA水平明显下降。异补骨脂素给药1、3、7 d后,三磷酸腺苷结合转运蛋白G超家族成员5(ATP-binding cassette subfamily G member 5, ABCG5)、ABCG8、有机溶质转运蛋白α(organic solute transporter alpha, OSTα)的mRNA水平均明显下降。
|
| Fig 2 The mRNA levels of BSEP, NTCP, MRP2, MRP4, MDR1, ABCG5, ABCG8 and OSTα in rat liver after oral administration for 1, 3 or 7 days(x±s, n=8) *P < 0.05, **P < 0.01 vs control group |
补骨脂应用十分广泛,历代中医用于治疗肾虚、冷泻、遗滑精、小便频数、腰膝冷痛等,外治用于皮肤病、白癜风等。现代药理学研究表明,补骨脂具有扩张冠脉、抗肿瘤、抗菌、抗抑郁、拟雌激素样等多种作用[9-12]。然而,补骨脂的肝毒性也被多个研究报道证实,且其毒性成分和致毒机制尚不清楚。异补骨脂素为补骨脂的主要活性成分,其可能与补骨脂引起的肝损害和胆汁淤积有关。
肝细胞坏死时,由于肝细胞膜破损,细胞内的一些酶溢出细胞外,如ALT、AST等。因此,胞外或血清中ALT和AST的含量能敏感地反映肝细胞损伤与否及损伤程度。在本实验中,给予异补骨脂素后,血清中ALT和AST的水平持续明显升高,尤其是AST,在给予异补骨脂素1 d之后即有明显的上升,提示异补骨脂素给药1~7 d均能引起肝损伤。异补骨脂素给药1 d和3 d后,TC的含量明显降低;异补骨脂素给药7 d后,TBA明显增加。由于胆固醇是合成胆汁酸的原料,该结果说明异补骨脂素作用后,可能引起了由胆固醇合成胆汁酸增多,从而造成TC含量的下降和TBA含量的升高。异补骨脂素给药1、3、7 d后,TG的含量均明显升高,表明异补骨脂素作用后引起肝功能的减退,可能加重机体的脂肪负荷。异补骨脂素给药7 d后,TBIL的水平也明显升高,表明异补骨脂素作用7 d,造成肝细胞的受损和肝功能的减退。另外,异补骨脂素作用1 d之后引起肝系数的明显升高,并且一直保持高水平。以上研究表明,异补骨脂素作用1 d即引起肝脏的损伤,表现出急性肝脏毒性;作用3 d后,肝脏的损伤进一步加重;作用7 d,肝脏的损伤持续存在,但是没有进一步加重的趋势。而引起肝脏损伤的因素有多种,在本研究中,异补骨脂素的作用能导致胆汁酸水平的升高,最终造成胆汁淤积,损伤肝脏,但是其确切机制还需进一步探讨。
研究表明,造成胆汁淤积和肝损伤的原因除与胆汁形成有关以外,还与胆汁酸的分泌和转运等过程紊乱有关[13]。胆汁酸在肝脏中合成,通过各级管道最终分泌到十二指肠,进行辅助消化脂肪。而胆汁酸在细胞内浓度过高,可导致线粒体介导的细胞凋亡,从而引起毒性的产生[14]。BSEP和NTCP是肝细胞膜上两个重要的胆汁酸转运蛋白,BSEP将胆汁酸由肝细胞转运至细胞间胆管,NTCP则将胆汁酸从血液转运至肝细胞。这两种转运蛋白的正常生理功能对于维持血液和肝细胞中的胆汁酸平衡至关重要。在本研究中,异补骨脂素可以抑制BSEP mRNA的水平,且随着给药时间的延长,抑制作用越明显,具有一定的时间依赖性。同时,异补骨脂素也能降低NTCP mRNA水平,并且该抑制作用呈现时间依赖性地减弱。该数据表明,异补骨脂素给药后,引起BSEP和NTCP转录水平的改变,可能对胆汁酸的转运造成影响。而NTCP mRNA水平的降低可能与肝细胞内胆汁淤积后,负反馈调节NTCP的转录,抑制其不断向肝细胞内运输胆汁酸有关,这也与之前的文献报道一致[15]。MRP2、MDR1、ABCG5及ABCG8与BSEP类似,位于肝细胞的顶侧,主要功能是把肝细胞中的胆汁酸转运到微胆管,从而排出肝细胞中过量的胆汁酸。异补骨脂素作用1、3、7 d能抑制MRP2、MDR1、ABCG5、ABCG8的mRNA水平,推测其可能抑制胆汁酸从肝细胞排向胆管。MRP4和OSTα主要功能是把肝细胞中的胆汁酸转运到血液中。异补骨脂素对MRP4 mRNA的水平没有影响,但是能够明显抑制OSTα mRNA的水平,从而抑制胆汁酸向血液排出。以上研究表明,异补骨脂素给药1、3、7 d能干扰胆汁酸转运体的转录,从而抑制胆汁酸转运体的功能,造成肝脏损伤。而胆汁酸转运体的水平主要受核受体的调控,法尼醇X受体(farnesoid X receptor, FXR)、孕烷X受体(pregnane X receptor, PXR)等核受体,通过调控胆汁酸的代谢、外排与转运,从而实现对胆汁酸稳态的调控[16]。因此,异补骨脂素是否通过核受体调控胆汁酸水平,导致肝损伤,将是我们下一步研究要解决的主要问题。
综上所述,异补骨脂素给药可造成肝脏的损伤,其机制可能是通过调控胆汁酸转运体,从而导致肝损伤。
| [1] |
辛丹, 颜冬梅, 王跃飞, 等. 补骨脂及其相关化学成分的药理与毒理研究进展[J]. 辽宁中医药大学学报, 2009, 11(7): 70-2. Xin D, Yan D M, Wang Y F, et al. Pharmacology and toxicology of Psoralea Corylifolia L. and its related chemical constituents[J]. J Liaoning Univ Tradit Chin Med, 2009, 11(7): 70-2. |
| [2] |
Cheung W I, Tse M L, Ngan T, et al. Liver injury associated with the use of Fructus Psoraleae (Bol-gol-zhee or Bu-gu-zhi) and its related proprietary medicine[J]. Clin Toxicol (Phila), 2009, 47(7): 683-5. doi:10.1080/15563650903059136 |
| [3] |
Nam S W, Baek J T, Lee D S, et al. A case of acute cholestatic hepatitis associated with the seeds of Psoralea corylifolia (Boh-Gol-Zhee)[J]. Clin Toxicol (Phila), 2005, 43(6): 589-91. doi:10.1081/CLT-200068863 |
| [4] |
唐进法, 王晓艳, 杨伟, 等. 基于统计建模的壮骨关节丸诱发特异质肝损伤相关易感性细胞因子分析[J]. 药学学报, 2018, 53(4): 574-84. Tang J F, Wang X Y, Yang W, et al. Cytokine analysis of Zhuangguguanjie wan-induced idiosyncratic liver injury based on mathematical modeling[J]. Acta Pharm Sin, 2018, 53(4): 574-84. |
| [5] |
周昆, 代志, 柳占彪, 等. 补骨脂水提物引起的大鼠肝损害[J]. 天津中医药大学学报, 2013, 32(4): 221-4. Zhou K, Dai Z, Liu Z B, et al. Aqueous extract of Psoralea corylifolia induced liver injury in rats[J]. J Tianjin Univ Tradit Chin Med, 2013, 32(4): 221-4. |
| [6] |
张玥, 毕亚男, 袁晓美, 等. 基于靶器官的补骨脂肝毒性成分探讨[J]. 时珍国医国药, 2017, 28(8): 1844-7. Zhang Y, Bi Y N, Yuan X M, et al. Study on the hepatotoxicity components of Psoralea corylifolia based on target organs[J]. Lishizhen Med Mater Med Res, 2017, 28(8): 1844-7. |
| [7] |
周昆, 毕亚男, 史红. 异补骨脂素抑制MRP2、MRP3所致的HepG2细胞内胆汁酸蓄积和毒性[J]. 中国药理学通报, 2015, 31(8): 1112-6. Zhou K, Bi Y N, Shi H. Psoralen induced bile acid accumulation and cytotoxicity by inhibiting MRP2 and MRP3 in HepG2 cells[J]. Chin Pharmacol Bull, 2015, 31(8): 1112-6. doi:10.3969/j.issn.1001-1978.2015.08.017 |
| [8] |
宋蕾, 毕亚男, 袁晓美, 等. 异补骨脂素腹腔注射9 d所致的C57小鼠肝损害[J]. 毒理学杂志, 2018, 32(1): 21-4. Song L, Bi Y N, Yuan X M, et al. Study on the influence of isopsoralen on C57 mice liver injury after intraperitoneal injection for 9 days[J]. J Toxicol, 2018, 32(1): 21-4. |
| [9] |
Lee S J, Nam K W, Mar W. Induction of quinone reductase activity by psoralidin isolated from Psoralea corylifolia in mouse hepa 1c1c7 cells[J]. Arch Pharm Res, 2009, 32(7): 1061-5. doi:10.1007/s12272-009-1712-1 |
| [10] |
Yadava R N, Verma V. A new biologically active flavonol glycoside from Psoralea corylifolia (Linn[J]. J Asian Nat Prod Res, 2005, 7(4): 671-5. doi:10.1080/10286020310001608921 |
| [11] |
Chen Y, Cheung Y T, Kong L D, et al. Transcriptional regulation of corticotrophin releasing factor gene by furocoumarins isolated from seeds of Psoralea corylifolia[J]. Life Sci, 2008, 82(21-22): 1117-21. doi:10.1016/j.lfs.2008.03.014 |
| [12] |
Lim S H, Ha T Y, Kim S R, et al. Ethanol extract of Psoralea corylifolia L. and its main constituent, bakuchiol, reduce bone loss in ovariectomised Sprague-Dawley rats[J]. Br J Nutr, 2009, 101(7): 1031-9. doi:10.1017/S0007114508066750 |
| [13] |
韩平, 田德安. 肝内胆汁淤积发病机制及药物治疗新进展[J]. 胃肠病学和肝病学杂志, 2016, 25(5): 584-8. Han P, Tian D A. New progress of pathogenesis and therapeutic agents of hepatic cholestasis[J]. Chin J Gastroenterol Hepatol, 2016, 25(5): 584-8. |
| [14] |
Palmeira C M, Rolo A P. Mitochondrially-mediated toxicity of bile acids[J]. Toxicology, 2004, 203(1-3): 1-15. doi:10.1016/j.tox.2004.06.001 |
| [15] |
Geier A, Dietrich C G, Gerloff T, et al. Regulation of basolateral organic anion transporters in ethinylestradiol-induced cholestasis in the rat[J]. Biochim Biophys Acta, 2003, 1609(1): 87-94. doi:10.1016/S0005-2736(02)00657-0 |
| [16] |
陈攀, 李晶洁, 陈杰. 以核受体为靶标的胆汁淤积治疗药物研究进展[J]. 中国药理学通报, 2015, 31(9): 1195-8. Chen P, Li J J, Chen J. Nuclear receptor as drug targets in cholestasis[J]. Chin Pharmacol Bull, 2015, 31(9): 1195-8. doi:10.3969/j.issn.1001-1978.2015.09.003 |

