

 、AUC0-t及MRT0-inf分别为槲皮素溶液的1.2、1.5、2.4倍。结论 槲皮素混合胶束包封率及载药量高,可改善体外释放行为,延长槲皮素在大鼠体内的时间,明显提高槲皮素的生物利用度。
、AUC0-t及MRT0-inf分别为槲皮素溶液的1.2、1.5、2.4倍。结论 槲皮素混合胶束包封率及载药量高,可改善体外释放行为,延长槲皮素在大鼠体内的时间,明显提高槲皮素的生物利用度。 , AUC0-t and MRT0-inf of quercetin mixed micelles were calculated to be 1.2, 1.5 and 2.4 times of free quercetin, respectively. Conclusions The quercetin-loaded mixed micelles have high entrapment efficiency and loading efficiency, which can improve the release behavior in vitro, prolong the time of quercetin, and significantly enhance the fraction of bioavailability of quercetin in rats.
, AUC0-t and MRT0-inf of quercetin mixed micelles were calculated to be 1.2, 1.5 and 2.4 times of free quercetin, respectively. Conclusions The quercetin-loaded mixed micelles have high entrapment efficiency and loading efficiency, which can improve the release behavior in vitro, prolong the time of quercetin, and significantly enhance the fraction of bioavailability of quercetin in rats.槲皮素(quercetin,3,3’,4’, 5,7-五羟基黄酮)是一种植物多元酚,所含的生物黄酮素广泛存在于各种蔬菜与水果中[1]。研究表明,槲皮素毒性低,具有抗病毒、抗氧化、抗炎、抗肿瘤、心血管系统和神经系统保护等多种药理作用[2-3]。但槲皮素水溶性差,在水中溶解度仅为0.166~7.7 mg·L-1[4],化学结构不稳定(尤其是在碱性溶液中极易分解),且大部分药物在到达体循环之前已基本代谢[5],限制了其临床应用。因此,提高槲皮素水溶性和增强化学稳定性,延长药物半衰期成为选择合适剂型的关键。聚合物胶束作为一种新型的纳米递药系统,是由两亲性嵌段共聚物在水溶液中通过疏水作用力自发形成的超分子有序聚集体[6],具有特殊的核-壳结构(疏水嵌段为内核,亲水嵌段为外壳)。其内核作为载药容器,能增溶难溶性药物;而外壳可避免胶束被体内网状内皮系统(reticulo-endothelial system,RES)识别和摄取,延长药物在体内的循环时间,并保持其稳定。本实验采用的泊洛沙姆(Poloxamer),商品名为普兰尼克(Pluronic),是一种非离子型三嵌段共聚物,由聚氧乙烯-聚氧丙烯-聚氧乙烯(PEO-PPO-PEO)组成,近年来在胶束载药研究中备受关注。其分子量小于15 000 u,具有良好的生物相容性。本研究制备了槲皮素Pluronic P123/Poloxamer 188混合胶束,并初步考察其体外释放特征及大鼠体内药物代谢动力学行为,为该药的新剂型研发提供新思路。
1 材料 1.1 仪器ACQUTIY超高效液相色谱仪、e2695高效液相色谱仪(美国Waters公司);UV-2100紫外可见分光光度计(北京莱伯泰科仪器有限公司);3K30高速冷冻离心仪、4-1S低速离心仪(德国Sigma公司);WH-2微型漩涡混合仪(上海沪西分析仪器厂);旋转蒸发仪(巩义市英峪高科仪器厂);H7650透射电镜(日本HITACHI公司);ZEN3690马尔文粒度仪(Malvern公司);RC8MD溶出试验仪、RZQ-8D取样收集系统(天津市天大天发科技有限公司)。
1.2 药物与试剂槲皮素(中国食品药品检定研究院);Pluronic P123、Poloxamer 188(美国Sigma公司);甲酸、乙腈(色谱纯),美国Fisher Scientific公司;吐温-80(国药集团化学试剂有限公司)。
1.3 实验动物10只健康SD大鼠,♂,体质量180~220 g,SPF级,购自北京华阜康生物科技股份有限公司,许可证号:SCXK(京)2014-0004。
2 方法 2.1 槲皮素混合胶束的制备采用薄膜分散法制备混合胶束,以包封率、载药量为指标,单因素分别考察投药量、P123质量分数、旋转蒸发温度、水浴温度、水相用量对处方的影响,经[L9(34)]正交实验优化,得制备方法为:称取1:1比例的Pluronic P123以及Poloxamer 188适量,槲皮素20 mg于圆底烧瓶中,加入丙酮混匀,磁力搅拌至完全溶解。50 ℃旋转蒸发将有机溶剂挥尽,得干燥薄膜,室温干燥过夜除去残留溶剂。水浴加热(40 ℃)药膜1 h使胶束骨架溶解,得透明凝胶样制剂,加入5 mL去离子水,继续磁力搅拌水化,最终经0.22 μm微孔滤膜过滤得澄清黄色胶束溶液。分别通过透射电镜、Malvern粒度分析仪测得胶束的外观、粒径及电位。
2.2 体外释放考察采用透析法考察胶束的体外释放行为。参考文献,释放介质选用含1%吐温-80的生理盐水[7],槲皮素在此介质中溶解度为(117.81±1.2)mg·L-1,满足漏槽条件。分别精密吸取3.0 mL槲皮素混合胶束溶液以及等量浓度的槲皮素溶液,置于已处理的透析袋(截留分子量为1 000 u)内,每组平行3份,将袋口扎紧后浸入释放介质中,37 ℃、100 r·min-1条件下搅拌,且隔一定时间取样2 mL,并补充等量新鲜介质。样品过0.22 μm微孔滤膜后高效液相进样,得药物浓度。计算药物累积释放率,结果经DD Solver软件进行模型拟合,并推测释药机制。
2.3 大鼠体内药物代谢动力学 2.3.1 给药方案健康♂SD大鼠10只,随机分成两个实验组(每组5只):槲皮素溶液组与槲皮素混合胶束组。自由饮水,禁食24 h后,分别尾静脉注射7.5 mg·kg-1的槲皮素溶液(精密称取槲皮素8 mg,加入0.8 mL无水乙醇混匀溶解,再次加入9.2 mL注射用水,并加入吐温-80适量,超声溶解后,过0.22 μm微孔滤膜得黄色透明槲皮素溶液)[8]以及槲皮素混合胶束。给药后,两组分别于5、10、15、30、45、60、90、120 min眼眶后静脉丛取血0.3 mL,置于肝素钠抗凝管中。3 000 r·min-1离心10 min后,取上层血浆,-80 ℃保存。
2.3.2 血浆样品处理取血浆样品100 μL,加入1倍体积乙腈,涡旋60 s沉淀蛋白,于10 000 r·min-1离心10 min后取上清液,经0.22 μm微孔滤膜过滤后,放入-80 ℃冰箱保存待测。
2.3.3 样品测定方法的建立色谱柱:ACQUITY UPLC BEH C18柱(2.1 mm×50 mm,1.7 μm,爱尔兰Waters);流动相A:100%乙腈;流动相B:0.1%甲酸溶液;梯度洗脱:0~2 min,68% B;2~6 min,68%~10% B;流速0.3 mL·min-1;柱温30 ℃;进样量4 μL;检测波长374 nm[9]。精密称取槲皮素5.0 mg于50 mL容量瓶中,乙腈溶解并稀释至刻度,配成浓度为100 mg·L-1储备液。分别吸取不同浓度槲皮素储备液加入大鼠空白血浆中混匀,得浓度为0.1、0.5、1、2、3、6、12、24 mg·L-1血浆样品。经“血浆样品处理”后,按色谱条件进样。以浓度(C)对峰面积(A)作图,进行线性回归,求得回归方程。
2.3.4 方法学考察配制含槲皮素0.3、3、12 mg·L-1的低、中、高浓度血浆样品,考察精密度,方法回收率及萃取回收率[10]。
2.3.5 数据分析数据经PK Solver药代动力学软件处理,通过比较Rsqr_adj与AIC值,选出合适的房室模型,并计算药动学参数,所有数据均需t检验进行两两比较。
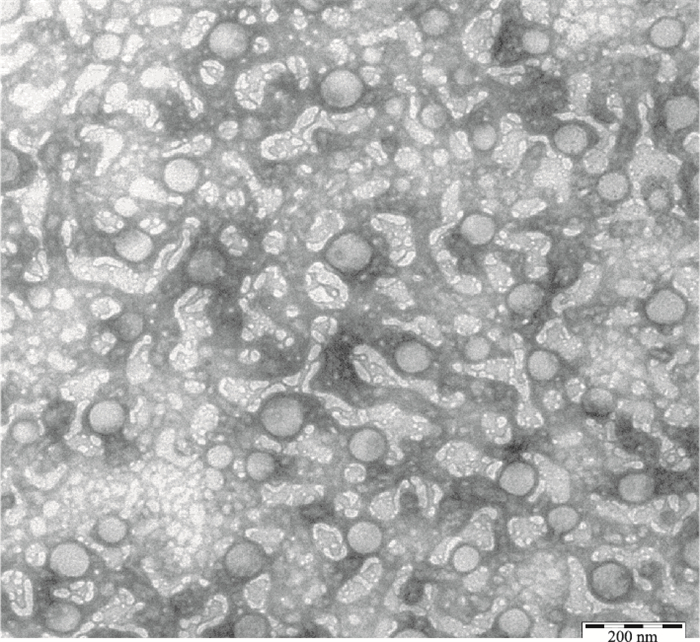
3 结果 3.1 体外测定方法经考察,混合胶束呈类圆形,药物包埋于其中,无聚集现象,见Fig 1。制备的槲皮素混合胶束平均粒径为(77.88±1.07)nm,电位为(-17.12±1.29)mV,包封率为(94.25±2.13)%,载药量为(8.61±0.18)%。体外溶出线性方程为y=1 339.3x-291.54,r=0.9995,说明槲皮素在0.8~16 mg·L-1浓度范围内线性关系良好。日内精密度RSD分别为1.45%、1.36%、0.95%,日间精密度RSD分别为1.80%、1.68%、1.37%,均满足要求。
|
| Fig 1 Transmission electronic microphotograph (TEM) image of mixed micelles (×20 000) |
槲皮素以及槲皮素混合胶束在释放介质中体外释放曲线见Fig 2。数据表明,槲皮素及胶束在含1%吐温-80介质中,累积释放量分别为(83.65±3.97)%和(52.90±1.08)%。槲皮素溶液在9 min内完全释放;而混合胶束则在72 h完全释放。结果显示,槲皮素混合胶束可延长药物的释放时间。

|
| Fig 2 Release profiles of free quercetin and mixed micelles (n=3) |
拟合结果见Tab 1。根据Rsqr_adj与AIC值对结果进行模型拟合(Rsqr_adj值越靠近1,AIC值越小则拟合度越高),经拟合,游离槲皮素释药行为符合First-order方程,拟合方程为:F= 100·[1-Exp(-0.379·t)](Rsqr_adj=0.955 5,AIC=46.796 9);槲皮素混合胶束释药行为符合Higuchi动力学方程,拟合方程为:F=6.735·t0.5(Rsqr_adj=0.960 4,AIC=75.584 0)。
| Mathematical model | Equation | Rsqr_adj | AIC |
| Free QUE | |||
| Zero-order | F=14.224·t | 0.431 1 | 67.440 6 |
| First-order | F=100·[1-Exp(-0.379·t)] | 0.955 5 | 46.796 9 |
| Higuchi | F=34.422·t0.5 | 0.900 9 | 53.352 5 |
| Korsmeyer-Peppas | F=36.727 ·t0.456 | 0.891 3 | 54.890 3 |
| QUE-Micelles | |||
| Zero-order | F=0.939·t | 0.714 9 | 102.265 2 |
| First-order | F=100·[1-Exp(-0.015·t)] | 0.867 7 | 91.441 9 |
| Higuchi | F=6.735·t0.5 | 0.960 4 | 75.584 0 |
| Korsmeyer-Peppas | F=6.151 ·t0.526 | 0.959 0 | 75.920 7 |
以血药浓度(C)对峰面积(A)作图,进行线性回归,求得回归方程,线性方程为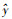
槲皮素及槲皮素混合胶束平均药-时曲线见Fig 3。经PK Solver药代动力学软件处理,主要药动学参数见Tab 2。由Fig 3可见,槲皮素溶液在60 min左右在体内基本代谢;槲皮素混合胶束在120 min左右基本代谢。由Tab 2可见,大鼠静脉注射槲皮素溶液以及混合胶束的体内过程均符合二室模型,混合胶束消除半衰期

|
| Fig 3 Mean plasma concentration-time curves after intravenous injection of quercetin solution and quercetin-loaded mixed micelles in rats (n=5) |
| Parameter | Quercetin solution | Quercetin micell |
| V/mL·μg-1 | 0.24±0.08 | 0.28±0.02 |
 /min /min |
3.10±1.01 | 3.61±0.32 |
 /min /min |
30.47±5.54 | 34.88±22.78 |
| K21/min-1 | 0.049±0.013 | 0.048±0.040 |
| K10/min-1 | 0.165±0.052 | 0.093±0.002* |
| K12/min-1 | 0.075±0.008 | 0.068±0.039 |
| AUC0-t/μg·min·mL-1 | 188. 70±28.21 | 279.13±23.81** |
| AUMC0-inf/μg·mL-1·min2 | 2 156.74±112.72 | 7 826.01±657.15** |
| CL/mL·μg-1·min-1 | 0.037±0.003 | 0.026±0.002** |
| MRT0-inf/min | 11.22±0.84 | 27.06±1.41** |
| *P < 0.05,**P < 0.01 vs quercetin solution | ||
槲皮素不溶于水,因此在体外释放实验中选用普通溶出介质(双蒸水、磷酸盐缓冲液、生理盐水等)时,几乎检测不到药物。然而,选用40%乙醇作为释放介质时,混合胶束溶解迅速,改变了槲皮素释药结果。因此,本文选用既满足漏槽条件,又保证胶束稳定性的1%吐温-80的生理盐水为释放介质。
释放数据显示,混合聚合物胶束能够延长药物的释放时间,拟合结果为游离槲皮素释药行为符合First-order方程,槲皮素胶束释药行为符合Higuchi动力学方程。除常用动力学方程,本文采用Korsmeyer-Peppas模型对剂型进行拟合。此方程中指数项n值代表不同的释药机制:n<0.45时,释放机制是扩散;0.45<n<0.89时,释药机制是溶蚀和扩散;n>0.89时,释药机制为骨架溶蚀[11-12]。混合胶束Korsmeyer-Peppas模型的n=0.526,在0.45<n<0.89范围中,因此,混合胶束的释放机制为溶蚀和扩散。与游离槲皮素相比,混合胶束累积释放量减少至少20%,这可能与胶束的二次聚集有关。胶束的二次聚集能够减小其表面积,导致药物不易扩散。
在建立超高效液相方法时,本实验根据以往文献选取不同的流动相比例,如乙腈-0.05%甲酸[13]、乙腈-0.1%甲酸[14]、乙腈-5%甲酸[15]。结果显示,乙腈-0.05%甲酸与乙腈-5%甲酸分离效果均不满意,药物峰有严重拖尾,而乙腈-0.05%甲酸能够很好分离药物峰与血浆内容物,经过梯度洗脱后药物峰峰型良好。因此,用此超高效液相方法分析样品有快速、精准、简便的优点。
用PK Solver软件对大鼠静脉注射两种溶剂后的血药浓度进行拟合,根据Rsqr_adj与AIC值判定房室模型种类。Rsqr_adj为校正的R2,Rsqr_adj值越靠近1,AIC值越小则拟合度越高。经拟合,两种溶剂均为二室房室模型,且大多数拟合参数在统计学上差异有显著性(P<0.05,P<0.01)。拟合结果充分说明混合胶束作为载药体系,能够增加槲皮素在体内时间,提高槲皮素的生物利用度。
本实验制备的Pluronic P123/Poloxamer 188槲皮素混合聚合物胶束粒径小、包封率与载药量高,延长了药物在体外释放时间,明显提高槲皮素在体内的利用度。本研究为进一步研究槲皮素的混合胶束制剂体内的分布以及代谢产物提供了基础。
| [1] |
Zhu Y, Teng T, Wang H, et al. Quercetin inhibits renal cyst growth in vitro and via parenteral injection in a polycystic kidney disease mouse model[J]. Foot Funct, 2018, 9(1): 389-96. doi:10.1039/C7FO01253E |
| [2] |
Khor C M, Ng W K, Chan K P, et al. Preparation and characterization of quercetin/diet-ary fiber nanoformulations[J]. Carbohydr Polym, 2017, 161: 109-17. doi:10.1016/j.carbpol.2016.12.059 |
| [3] |
侯晓敏, 秦小江. 槲皮素通过激活Kv1.5保护糖尿病大鼠冠脉损伤[J]. 中国药理学通报, 2017, 33(10): 1442-5. Hou X M, Qin X J. Quercetin protects coronary artery from injury induced by diabetes in rats by activating Kv1.5[J]. Chin Pharmacol Bull, 2017, 33(10): 1442-5. doi:10.3969/j.issn.1001-1978.2017.10.022 |
| [4] |
谭启.槲皮素磷脂—壳聚糖纳米粒制剂及其经皮给药的研究[D].济南: 山东大学, 2012. Tan Q. Preparation and evaluation of quercetin-loaded lecithin-chitosan nanoparticles for topical delivery[D]. Jinan: Shandong University, 2012. http://cdmd.cnki.com.cn/Article/CDMD-10422-1012463324.htm |
| [5] |
Mukhopadhyay P, Maity S, Mandal S, et al. Preparation, characterization and in vivo evaluation of pH sensitive, safe quercetin- succinylated chitosan-alginate core-shell-corona nanoparticle for diabetes treatment[J]. Carbohydr Polym, 2018, 182: 42-51. doi:10.1016/j.carbpol.2017.10.098 |
| [6] |
刘荣, 时政, 李红梅, 等. 嵌段聚合物胶束药物传递系统的稳定性综述[J]. 高分子材料科学与工程, 2016, 32(11): 173-7. Liu R, Shi Z, Li H M, et al. Progress in stability of block copolymer micelle as vehicles for drug delivery[J]. Polymer Mater Sci Eng, 2016, 32(11): 173-7. |
| [7] |
Yamamoto T, Yokoyama M, Maitani Y, et al. What are determining factors for stable drug incorporation into polymeric micelle carriers? Consideration on physical and chemical characters of the micelle inner core[J]. J Control Release, 2007, 123(1): 11-8. doi:10.1016/j.jconrel.2007.07.008 |
| [8] |
Khor C M, Ng W K, Chan K P, et al. Preparation and characterization of quercetin/dietary fiber nanoformulations[J]. Carbohydr Polym, 2017, 161: 109-17. |
| [9] |
陆苑, 潘洁, 杨淑婷, 等. UPLC-MS法研究艾迪注射液对大鼠体内阿霉素药代动力学的影响[J]. 中国药理学通报, 2018, 34(3): 423-7. Lu Y, Pan J, Yang S T, et al. Effect of Aidi injection on in vivo pharmacokinetics of doxorubicin in Sprague-Dawley rats by UPLC-MS method[J]. Chin Pharmacol Bull, 2018, 34(3): 423-7. doi:10.3969/j.issn.1001-1978.2018.03.024 |
| [10] |
李嫄, 赵静, 余忠姝, 等. 壳聚糖包覆姜黄素脂质体体外释放和药代动力学研究[J]. 中国药理学通报, 2018, 34(6): 810-4. Li Y, Zhao J, Yu Z S, et al. Release characteristics in vitro and pharmacokinetics of chitosan coated curcumin liposomes in rats[J]. Chin Pharmacol Bull, 2018, 34(6): 810-4. doi:10.3969/j.issn.1001-1978.2018.06.014 |
| [11] |
Plichta A, Kowalczk S, Oledzka E, et al. Effect of structural factors on release profiles of camptothecin from block copolymer conjugates with high load of drug[J]. Int J Pharm, 2018, 538(1-2): 231-42. doi:10.1016/j.ijpharm.2018.01.022 |
| [12] |
Costa P, Sousa Lobo J M. Modeling and comparison of dissolution profiles[J]. Eur J Pharm Sci, 2001, 13(2): 123-33. doi:10.1016/S0928-0987(01)00095-1 |
| [13] |
Luo Y, Wu S, Li X, et al. LC-ESI-MS-MS determination of rat plasma protein binding of major flavonoids of Flos Lonicerae Japonicae by centrifugal centuifugal ultrafiltration[J]. Chromatographia, 2010, 72(1-2): 71-7. doi:10.1365/s10337-010-1618-6 |
| [14] |
He J, Feng Y, Ouyang H Z, et al. A sensitive LC-MS/MS method for simultaneous determination of six flavonoids in rat plasma: application to a pharmacokinetic study of total flavonoids from mulberry leaves[J]. J Pharm Biomed Anal, 2013, 84(10): 189-95. |
| [15] |
Moon Y J, Wang L, Dicenzo R, et al. Quercetin pharmacokinetics in humans[J]. Biopharm Drug Dispos, 2008, 29(4): 205-17. doi:10.1002/(ISSN)1099-081X |

