

2. 遵义医学院基础药理学教育部重点实验室暨特色民族药教育部国际合作联合实验室,贵州 遵义 563003
2. Key Lab of Basic Pharmacology of Ministry of Education and Joint International Research Laboratory of Ethnomedicine of Ministry of Education, Zunyi Medical University, Zunyi Guizhou 563003, China
随着社会经济的不断发展,糖尿病的发病率也逐年增加,严重影响了人们的生活水平和生命质量。糖尿病并发症包括糖尿病心脏病、糖尿病肝病、糖尿病肾病(diabetic nephropathy,DN)、糖尿病脑病等,是糖尿病患者出现残疾,甚至死亡的主要原因。在我国,约65%的糖尿病患者出现严重的肾脏结构破坏和功能损伤,发生DN,进而发展为氮质血症、尿毒症,病人生活质量下降,经济负担加重。DN已成为终末期肾脏病的主要原因之一。国内外对DN的预防和治疗已进行了大量研究,但仍缺乏针对性治疗药物和有效手段。柚皮素(naringenin,NAR)是柚皮苷的苷元,主要存在于芸香科植物,如西红柿与柚、橙等柑橘类水果中,具有抗菌、抗炎、抗氧化、抗肿瘤、保护脑缺血/再灌注损伤等多种药理学活性[1]。在糖尿病大鼠模型,柚皮素具有降糖、抗炎、抗氧化、保护胰腺组织等作用[2],但对其在糖尿病肾损伤的研究较少。
有研究发现,花生四烯酸(arachidonic acid,AA)经细胞色素P450(cytochrome P450,CYP450)氧化酶途径代谢产物在代谢紊乱相关疾病中具有重要作用。20-羟-二十烷四烯酸(20-hydroxy eicosatetraenoic acid,20-HETE)是AA ω-羟化酶途径经CYP4A/CYP4F催化生成的重要代谢产物,在糖尿病、心血管疾病、肿瘤等疾病的发生、发展过程中具有重要的作用[3]。在DN大鼠模型中,CYP4A表达和20-HETE生成增加,抑制20-HETE的生成对DN有保护作用[4]。但Luo等[5]的研究结果与之相反,在DN大鼠的肾小球,CYP4A表达和20-HETE产生明显减少,氯贝特可上调CYP4A表达,增加20-HETE而产生肾保护作用。那么,20-HETE在糖尿病肾损伤中究竟具有怎样的调节作用?这是一个需要深入研究的问题。另有研究发现,在DOCA-盐诱导的高血压大鼠模型,另一个贝特类药物非洛贝特也可以上调CYP4A表达,增加20-HETE而产生降压作用[6]。众所周知,贝特类药物是过氧化物酶体增殖物激活受体α(peroxisome proliferator activated receptor α,PPARα)激动剂。有趣的是,大量研究证实,柚皮素的作用与其对PPARα受体的激活有关[7]。那么,在糖尿病引起的肾脏损伤中,柚皮素的作用是否与20-HETE的变化有关?目前国内外未见相关报道。本研究拟利用高糖高脂饮食联合链脲佐菌素(streptozocin,STZ)建立糖尿病模型,观察柚皮素对糖尿病肾损伤的保护作用,以及20-HETE的变化情况。
1 材料与方法 1.1 材料 1.1.1 实验动物6~8周龄清洁级♂昆明小鼠,重庆医科大学实验动物中心提供,许可证号:SCXK(渝)20120001。
1.1.2 试剂柚皮素,纯度98%,白色针状结晶,用0.5%羧甲基纤维素钠制成混悬液,购自成都德锐可生物科技有限公司,批号:drk-688-910714;STZ购自Sigma公司,批号:WXBC2544V;兔抗CYP4A多克隆抗体、鼠抗GAPDH单克隆抗体,购自美国Proteintech公司;小鼠20-HETE ELISA检测试剂盒,购自上海江莱生物科技有限公司;ECL化学发光试剂盒购自美国Thermo公司;其余试剂均为国产分析纯。
1.1.3 仪器AU5811全自动生化分析仪(美国贝克曼库尔特有限公司);ONETOUCH Ultra血糖仪(美国强生公司);DENLEY DRAGON Wellscan MK 3酶标仪(美国Thermo公司)。
1.2 方法 1.2.1 糖尿病模型的建立小鼠适应性喂养1周后,用高糖高脂饮食喂养4周,腹腔注射STZ(溶于pH 4.5的柠檬酸缓冲液中,现用现配)40 mg·kg-1·d-1,连续5 d。7 d后,用血糖仪测空腹血糖值(fasting blood glucose, FBG)。从40只小鼠中选取FBG≥11.1 mmol·L-1小鼠30只(继续给予高糖高脂饮食),随机分成3组(每组10只),分别为:模型组(DM):给予等剂量的羧甲基纤维素钠缓冲溶液;柚皮素低剂量组(NARL)、柚皮素高剂量组(NARH):分别灌胃柚皮素25、75 mg·kg-1·d-1,持续4周。正常组(NC,10只):给予正常饲料喂养4周,连续5 d腹腔注射等剂量的枸橼酸缓冲溶液,7 d后测血糖值,然后继续用正常饲料饲养,同时灌胃等剂量的羧甲基纤维素钠缓冲溶液4周。
每周检测小鼠的FBG和体质量,并用代谢笼收集尿液(检测尿液体积和尿白蛋白含量)。给药4周后,眼眶取血,处死小鼠。立即取出肾脏并称重,计算肾脏指数(肾质量/体质量)。分装标本,液氮速冻后,保存于-80 ℃冰箱备用。
1.2.2 肾功能指标检测将血液分装后,室温静置30 min,4 ℃、3 000 r·min-1离心15 min,取血清冻存于-80 ℃冰箱备用。尿液于4 ℃、3 000 r·min-1离心15 min,取上清冻存于-80 ℃冰箱备用。用自动生化分析仪检测血肌酐(serum creatinine, SCr)、尿素氮(urea nitrogen, BUN)和尿白蛋白的水平。
1.2.3 Masson染色肾脏组织置于4%的多聚甲醛中固定24 h,75%乙醇脱水,石蜡包埋,将其制作成切片。用Masson染色进行病理学检查。使用ImageJ 1.43软件测量肾小球横断面面积(glomerular cross-sectional area, GA),计算平均肾小球体积(glomerular volume, GV)。每只小鼠取20个肾小球的面积,计算GV:GV=β/κ×GA3/2,其中β=1.38,为球体形状系数;κ=1.1,为粒径分布系数。每组取5只小鼠。
1.2.4 透射电镜用冷刀片切取0.5 mm3肾组织,置于4%的戊二醛固定液中,4 ℃固定2 h,用PBS清洗3次,后经1%的四氧化锇固定2 h,常规乙醇和丙酮梯度脱水,环氧树脂浸透、包埋、聚合、切片,醋酸铀和枸橼酸铅双重染色,置于透射电镜下观察。
1.2.5 Western blot检测肾脏组织CYP4A蛋白的表达称取50 mg肾脏组织,加入0.5 mL RIPA裂解液,4 ℃匀浆。于4 ℃、12 000×g离心15 min,提取肾脏组织蛋白,BCA法测定蛋白浓度。SDS-聚丙烯酰胺凝胶电泳,转膜,封闭,加入一抗GAPDH (1:2 000)、CYP4A (1:1 000),4 ℃过夜;TBST洗膜,5 min×3次,二抗(1:3 000)室温孵育2 h,洗膜后加ECL发光试剂显影,采用Image Lab 4.1进行检测分析,蛋白相对表达量=目的蛋白条带灰度/GAPDH条带灰度,每组重复3次。
1.2.6 ELASA检测20-HETE含量取血清,按照试剂盒说明书操作,于450 nm波长下,用酶标仪检测20-HETE的水平。
1.2.7 数据处理实验数据均以x±s表示,采用SPSS 19.0软件对数据统计分析,两组间比较采用t检验,多组间比较采用单因素方差分析(one-way AVONA)。采用GraphPad Prism 5.01软件作图。
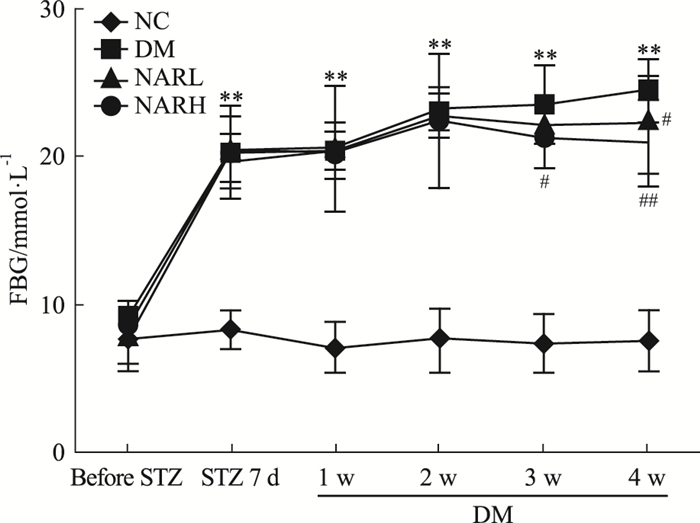
2 结果 2.1 柚皮素对糖尿病小鼠血糖的影响如Fig 1所示,给予STZ 7 d后,小鼠FBG升高至(20.51±2.23)mmol·L-1(P<0.01)。在整个实验期间,模型组FBG维持在较高的水平,NARL和NARH组血糖水平略有下降(P<0.05),但仍远高于11.1 mmol·L-1的糖尿病诊断标准。
|
| Fig 1 Effect of naringenin on FBG of mice (x±s, n=10) **P < 0.01 vs NC group; #P < 0.05, ##P < 0.01 vs DM group |
如Tab 1所示,糖尿病形成4周后,模型小鼠BUN、肌酐、尿白蛋白明显升高(P<0.01),且尿白蛋白比正常组高23.47倍,提示糖尿病小鼠出现了肾损伤。柚皮素给药剂量依赖地使糖尿病小鼠上述指标水平明显下降(P<0.05),NARL使尿白蛋白降低了48.45%,NARH组降低了56.81%。
| Group | BUN/mmol·L-1 | SCr/μmol·L-1 | Urinary albumin/ μg·24 h-1 |
| NC | 6.80±0.24 | 19.04±0.46 | 58.84±4.62 |
| DM | 8.53±0.30** | 33.00±4.38** | 1 380.98±256.13** |
| NARL | 7.90±0.08# | 29.07±1.11# | 711.88±132.36## |
| NARH | 7.47±0.10## | 24.33±0.79## | 596.48±139.12## |
| **P < 0.01 vs NC; #P < 0.05, ##P < 0.01 vs DM | |||
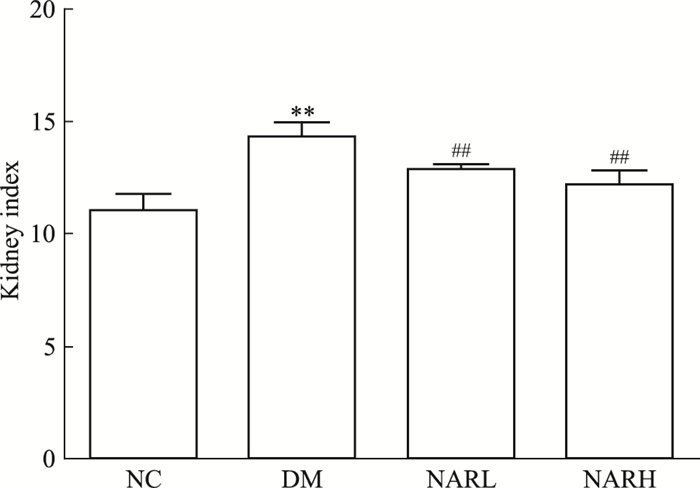
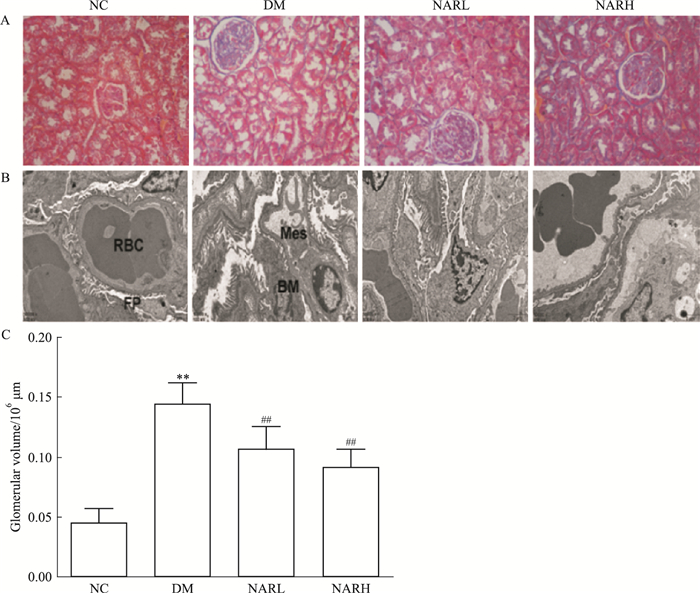
与正常组比较,糖尿病形成4周后,糖尿病小鼠肾脏指数(Fig 2)、肾小球体积(Fig 3C)明显增大(P<0.01);柚皮素给药明显减少糖尿病小鼠的肾脏肥大(P<0.01)。Masson染色显示,DM小鼠肾小球中大量胶原纤维相互交连成网,细胞间质胶原纤维增生,肾小管出现扩张,空泡变性(Fig 3A)。电镜结果表明,模型小鼠肾脏基底膜不均匀增厚,足突部分融合,系膜基质增加(Fig 3B)。柚皮素给药4周后,糖尿病小鼠肾脏上述病理变化明显改善。
|
| Fig 2 Effect of naringenin on kidney index of mice (x±s, n=10) **P < 0.01 vs NC group; ##P < 0.01 vs DM group |
|
| Fig 3 Effect of naringenin on pathological changes of kidney tissues in mice (x±s, n=5) A:Masson staining(×400);B:Transmission electron microscopic examination(×10 000);C:Glomerular volume of mice. BM: basement membrane; FP: foot processes; Mes: mesangial cell; RBC: red blood cell.**P < 0.01 vs NC group; ##P < 0.01 vs DM group. |
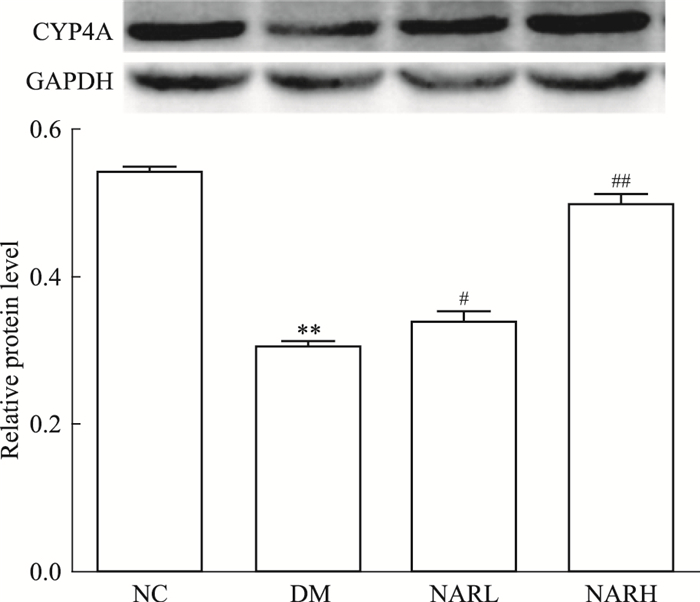
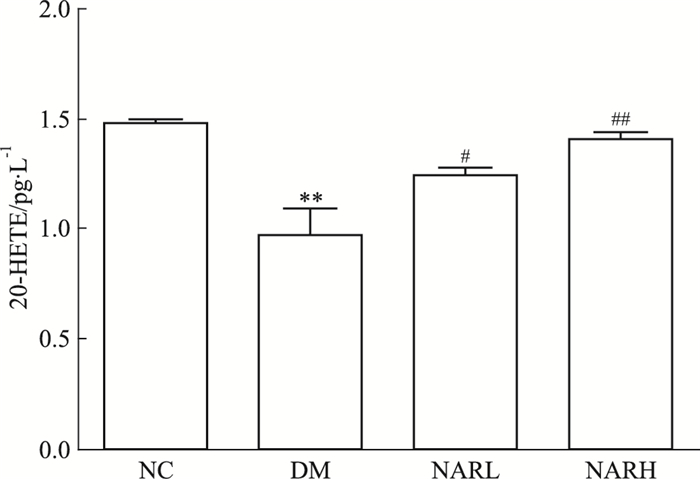
如Fig 4、5所示,与正常组比较,糖尿病小鼠肾脏CYP4A蛋白表达减少了44.44%(P<0.01),血清20-HETE的含量降低了45.09%(P<0.01);柚皮素低、高剂量组使CYP4A蛋白表达分别增加了0.13和0.65倍(P<0.05),20-HETE的含量分别升高了0.22和0.46倍(P<0.05)。
|
| Fig 4 Effect of naringenin on CYP4A protein expression of mice (x±s, n=3) **P < 0.01 vs NC group; #P < 0.05, ##P < 0.01 vs DM group |
|
| Fig 5 Effect of naringenin on 20-HETE levels in serum of mice (x±s, n=10) **P < 0.01 vs NC group; #P < 0.05, ##P < 0.01 vs DM group |
DN是糖尿病引起的危害性最大的一种慢性并发症,是糖尿病全身性微血管病变表现之一,临床特征为蛋白尿、渐进性肾功能损害、高血压等,晚期出现严重肾功能衰竭,是导致糖尿病患者死亡的主要原因。目前,DN的发病机制尚不清楚,也无任何药物获FDA批准用于该病的治疗。目前,西方医学对DN的治疗缺乏有效措施,相比较而言,传统中医药展现出较大治疗优势。植物药,即中草药提取的活性成分,如人参多糖[8]、黄芪多糖[9]、桑叶总黄酮[10]等对DN均有一定疗效。柚皮素广泛存在于天然植物中,具有多种药理学活性,可用于肥胖、高血压、高脂血症、糖尿病等代谢综合征症候群的治疗。在糖尿病整体动物及细胞培养模型,柚皮素除能降糖调脂外,对糖尿病并发的肝、肾损害及血管内皮功能障碍等亦有改善作用[11]。本实验利用高糖高脂饮食联合多次腹腔注射小剂量STZ,诱导小鼠形成糖尿病。4周后,糖尿病小鼠的BUN、SCr、尿白蛋白均升高,且尿白蛋白比正常组高出10倍以上,达到糖尿病并发症联盟网站(AMDCC)所提出的DN动物模型建立标准。同时,肾脏肥大,出现胶原纤维增加、基底膜增厚、足突部分融合等肾脏病理改变。肾功能和病理学检查均提示,糖尿病小鼠出现明显肾脏损伤。柚皮素给药4周剂量依赖地改善模型小鼠肾脏结构和功能的恶化,明显延缓糖尿病小鼠的肾脏损伤。另外,给予柚皮素治疗后,糖尿病小鼠FBG虽然有所降低,但仍远大于11.1 mmol·L-1的糖尿病诊断标准,提示柚皮素有一定程度降低血糖的作用,但对血糖水平的控制不是其产生肾脏保护作用的根本原因。
DN的发病机制较为复杂,炎症及其相关信号通路的作用在其中具有重要意义。众所周知,AA及其代谢产物是重要的炎症介质。AA的环氧化酶和脂氧化酶代谢途径已被广泛研究和了解,其产物如前列腺素类和白三烯类等,在炎症和代谢调节中有重要作用。近年,AA另一条代谢途径——CYP氧化酶途径代谢的生物学及病理生理学意义也逐渐被认识和重视。20-HETE是AA CYP氧化酶途径代谢产物之一,也参与了炎症、心血管系统疾病、糖尿病等的病理过程[3]。有趣的是,现在对20-HETE的研究呈现了矛盾的结果。有文献表明,在STZ诱导的糖尿病大鼠肾脏中,CYP4A和20-HETE的产生均明显降低,甚至20-HETE水平只有正常大鼠的1/5。而且,内源性和外源性的20-HETE对肾小球通透性屏障具有保护作用,可减轻蛋白尿,延缓肾纤维化的进程[5, 12]。但有一些研究提出了相反的结果,在STZ诱导的糖尿病肾脏的微粒体中,CYP4A的表达和功能明显增加[4]。本研究结果显示,糖尿病小鼠出现肾脏损伤同时,CYP4A蛋白表达下调,20-HETE含量较正常组明显减少,与Luo等[5]和John等[12]的研究一致。出现不同研究结果的原因可能是由于动物种属的差异、建模的方法、观察的组织器官、实验条件等不同所致。
目前,对于柚皮素在DN中的作用研究较少,相关机制主要集中于炎症、氧化应激等方面[13],而柚皮素与20-HETE之间的作用未见报道。Senol等[14]的研究显示,20-HETE类似物5, 14-HEDGE通过激活PPARα/β/γ,对感染性休克引起的低血压、心动过速及炎症有保护作用。另有研究发现,PPARα可能介导了20-HETE对炎症因子,如COX-2、IL-6的抑制作用[6]。这些研究提示,20-HETE的作用与PPARs的激活可能有一定关系。值得注意的是,现有研究认为,PPARs受体也介导了柚皮素的药理活性[15]。因此,我们推测,柚皮素的作用可能与其对20-HETE的调节有关。本研究结果显示,柚皮素干预后,糖尿病小鼠肾损伤改善的同时,肾脏CYP4A蛋白表达上调,20-HETE含量亦明显升高。
综上所述,本实验条件下,柚皮素对糖尿病小鼠肾损伤有保护作用,该作用的发生可能与柚皮素上调CYP4A表达,增加20-HETE含量有关。由于CYP在体内分布的广泛性和作用的复杂性,柚皮素对CYP4A-20-HETE的作用还需进行更多深入研究。
( 致谢: 本文实验在重庆医科大学药学院生物化学与分子药理学重点实验室完成,特此致谢!)
| [1] |
冯祝婷, 冯占辉, 王世平, 等. 基于NOD2/RIP2/NF-κB信号通路研究柚皮素对新生大鼠缺血缺氧性脑损伤的保护作用[J]. 中国药理学通报, 2018, 34(3): 418-22. Feng Z T, Feng Z H, Wang S P, et al. Protective effects of naringenin on hypoxic-ischemic brain damage in neonatal rats based on NOD2/RIP2/NF-κB signaling pathway[J]. Chin Pharmacol Bull, 2018, 34(3): 418-22. doi:10.3969/j.issn.1001-1978.2018.03.023 |
| [2] |
Annadurai T, Thomas P A, Geraldine P. Ameliorative effect of naringenin on hyperglycemia-mediated inflammation in hepatic and pancreatic tissues of Wistar rats with streptozotocin-nicotinamide-induced experimental diabetes mellitus[J]. Free Radic Res, 2013, 47(10): 793-803. doi:10.3109/10715762.2013.823643 |
| [3] |
Hoopes S L, Garcia V, Edin M L, et al. Vascular actions of 20-HETE[J]. Prostaglandins Other Lipid Mediat, 2015, 120: 9-16. doi:10.1016/j.prostaglandins.2015.03.002 |
| [4] |
Eid S, Abou-Kheir W, Sabra R, et al. Involvement of renal cytochromes P450 and arachidonic acid metabolites in diabetic nephropathy[J]. J Biol Regul Homeost Agents, 2013, 27(3): 693-703. |
| [5] |
Luo P, Zhou Y, Chang H H, et al. Glomerular 20-HETE, EETs, and TGF-β1 in diabetic nephropathy[J]. Am J Physiol Renal Physiol, 2009, 296(3): F556-63. doi:10.1152/ajprenal.90613.2008 |
| [6] |
Lee D L, Wilson J L, Duan R, et al. Peroxisome proliferator-activated receptor-alpha activation decreases mean arterial pressure, plasma interleukin-6, and COX-2 while increasing renal CYP4A expression in an acute model of DOCA-salt hypertension[J]. PPAR Res, 2011, 2011: 502631. |
| [7] |
Cho K W, Kim Y O, Andrade J E, et al. Dietary naringenin increases hepatic peroxisome proliferators-activated receptor alpha protein expression and decreases plasma triglyceride and adiposity in rats[J]. Eur J Nutr, 2011, 50(2): 81-8. doi:10.1007/s00394-010-0117-8 |
| [8] |
黄倩, 张素萍, 施子禄. 人参多糖通过cAMP/PKA/CREB信号通路抗糖尿病肾病肾纤维化作用机制研究[J]. 中国药理学通报, 2018, 34(5): 695-701. Huang Q, Zhang S P, Shi Z L. Mechanism of ginseng polysaccharides on renal fibrosis in diabetic nephropathy through cAMP/PKA/CREB signaling pathway[J]. Chin Pharmacol Bull, 2018, 34(5): 695-701. doi:10.3969/j.issn.1001-1978.2018.05.021 |
| [9] |
李承德, 王煜, 曲敬蓉, 等. 黄芪多糖对糖尿病大鼠肾脏TGF-β1/Smads信号通路的影响[J]. 中国药理学通报, 2018, 34(4): 512-6. Li C D, Wang Y, Qu J R, et al. Effects of astragalus polysaccharides on TGF-beta 1/Smads signaling pathway in kidneys of diabetic rats[J]. Chin Pharmacol Bull, 2018, 34(4): 512-6. doi:10.3969/j.issn.1001-1978.2018.04.015 |
| [10] |
王文文, 张赛, 朱晓卉, 等. 桑叶总黄酮对1型糖尿病小鼠肾间质纤维化的防治作用及机制[J]. 中国药理学通报, 2017, 33(9): 1278-85. Wang W W, Zhang S, Zhu X H, et al. Preventive effect and mechanism of total flavonoids from mulberry leaves on renal interstitial fibrosis in type 1 diabetic mice[J]. Chin Pharmacol Bull, 2017, 33(9): 1278-85. doi:10.3969/j.issn.1001-1978.2017.09.018 |
| [11] |
Roy S, Banerjee S, Ahmed F, et al. Naringenin ameliorates streptozotocin-induced diabetic rat renal impairment by downregulation of TGF-β1 and IL-1 via modulation of oxidative stress correlates with decreased apoptotic events[J]. Pharm Biol, 2016, 54(9): 1616-27. doi:10.3109/13880209.2015.1110599 |
| [12] |
John Q, Chen Y J. Role of COX-2 in the enhanced vasoconstrictor effect of arachidonic acid in the diabetic rat kidney[J]. Hypertension, 2003, 42(4): 837-43. doi:10.1161/01.HYP.0000085650.29823.F2 |
| [13] |
Tsai S J, Huang C S, Mong M C, et al. Anti-inflammatory and antifibrotic effects of naringenin in diabetic mice[J]. J Agric Food Chem, 2012, 60(1): 514-21. doi:10.1021/jf203259h |
| [14] |
Senol S P, Temiz M, Guden D S, et al. Contribution of PPARalpha/beta/gamma, AP-1, importin-alpha3, and RXRalpha to the protective effect of 5, 14-HEDGE, a 20-HETE mimetic, against hypotension, tachycardia, and inflammation in a rat model of septic shock[J]. Inflamm Res, 2016, 65(5): 367-87. doi:10.1007/s00011-016-0922-5 |
| [15] |
罗映, 李苌清, 周岐新, 等. 柚皮素同hPPARs的亲和力与内在活性研究[J]. 中国药房, 2012, 23(31): 2891-4. Luo Y, Li C Q, Zhou Q X, et al. Affinity and intrinsic activity of naringenin with hPPARs[J]. China Pharm, 2012, 23(31): 2891-4. doi:10.6039/j.issn.1001-0408.2012.31.04 |

