

2. 天津药物研究院新药评价有限公司,天津 300301;
3. 东阿阿胶股份有限公司国家胶类中药工程技术研究中心,山东 聊城 252201
 ,
DI Zhi-quan2,
WANG Yan-tao3,
AN Meng-pei2,
HU Jin-fang2
,
DI Zhi-quan2,
WANG Yan-tao3,
AN Meng-pei2,
HU Jin-fang2
 ,
JIN Yong1,
ZHANG Zong-peng2,
ZHANG Yan3
,
JIN Yong1,
ZHANG Zong-peng2,
ZHANG Yan3
2. Tianjin Institute of Pharmaceutical Research Drug Assessment Co. Ltd, Tianjin 300301, China;
3. National Engineering Research Center for Gelatin-based Traditional Chinese Medicine, Dong'e Ejiao Co.Ltd., Liaocheng Shandong 252201, China
阿胶(Asini Corii Colla)是由马科动物驴的干燥皮或鲜皮经煎煮、浓缩制成的固体胶,具有滋阴润肺、补血止血等功效,与人参、鹿茸并称为“中药三宝”[1]。其成分中蛋白质含量较高(约80%),相对分子质量集中在6×103~2×105 u,现代研究表明,相对分子质量过大会影响吸收入体或生物利用度较低,这一定程度上印证了阿胶“滋腻碍胃”的特性[2-3]。据研究,将大分子阿胶经仿生酶解或者仿生消化得到小分子低聚肽,其具有提高免疫力的作用,并有明显的补血升白作用[2, 4-5]。小分子阿胶为阿胶水解物,分子量的减小使得其服用后更易被机体吸收利用,避免了因分子量大而影响药效发挥的弊端。本研究参考阿胶的药理作用,旨在探究小分子阿胶的抗疲劳、抗氧化及止血作用,为其工艺改进提供一定的理论依据。
1 材料 1.1 实验动物ICR小鼠,SPF级,♂ ♀各半,体质量(19±1)g;SD大鼠,SPF级,♂ ♀各半,体质量(170±10)g,购自北京维通利华实验动物技术有限公司,许可证号:SCXK(京)2016-0006。
1.2 仪器ADVIA2120型血液分析仪(Siemens Healthcare Diagnostics Inc.);ACL9000型凝血分析仪(Instrumentation Laboratory Co.);SHHW21/600A Ⅱ型三用电热恒温水箱(天津市泰斯特仪器有限公司);ST 16R型离心机(Thermo Fisher Scientific Inc.)。
1.3 药品与试剂小分子阿胶(small molecule Asini Corii Colla,SMACC):批号1609001,东阿阿胶股份有限公司;生血丸:批号9880013,天津中新药业集团股份有限公司达仁堂制药厂;乙酰苯肼(acetyl phenylhydrazine,APH):批号20161104,天津市光复精细化工研究所;环磷酰胺(cyclophosphamide,CTX):批号16031225,江苏恒瑞医药股份有限公司;安琪高活性干酵母:生产日期20160810,安琪酵母股份有限公司;肝素钙注射液:批号55151202,天津生物化学制药有限公司;丙二醛(maleic dialdehyde,MDA,批号20161227)、脂质过氧化物(lipid peroxide,LPO,批号20161227)、超氧化物歧化酶(superoxide dismutase,SOD,批号20170118)试剂盒,均购自南京建成生物工程研究所;血液学检测试剂:SIEMENS ADVIA三合一正常值质控全血(批号72025)、全血细胞计数配套试剂(批号45688)、白细胞分类计数配套试剂(批号54747),购自SIEMENS公司;凝血功能检测试剂:质控血浆(批号N0942249)、凝血酶原时间(prothrombin time,PT,批号N0696900)、凝血酶时间(thrombin time,TT,批号N0556567)、活化部分凝血活酶时间(activated partial thromboplastin time,APTT,批号N1058925)、纤维蛋白原(fibrinogen,FIB,批号N0656757),购自美国实验室仪器公司。
2 方法 2.1 剂量设定参考阿胶的用法用量(人的日用量按9 g计),人体质量按60 kg计,小鼠体质量按20 g计,依体表面积换算成小鼠的等效剂量为1.70 g·kg-1,依此进行预实验后,本研究将小分子阿胶的小鼠剂量设置为3.00、1.50、0.75 g·kg-1,大鼠剂量设置为1.500、0.750、0.375 g·kg-1。
2.2 实验动物分组及给药动物随机分为6组,分别为对照组、模型组、阳性药组(生血丸:大鼠1.500 g·kg-1; 小鼠3.00 g·kg-1)、小分子阿胶高、中、低剂量组。采用灌胃法,各组按大鼠10 mL·kg-1,小鼠20 mL·kg-1每天给药1次,对照及模型组给予等量去离子水,连续14 d。
2.3 对复合血虚模型大鼠的影响参考文献[6]方法,选用SD大鼠,于给药d 8,除对照大鼠外,腹腔注射APH 30 mg·kg-1;于d 12,腹腔注射APH 60 mg·kg-1、CTX 100 mg·kg-1,给药结束于d 15,将大鼠放入冰水中游泳计时,记录大鼠的力竭时间(上下沉浮多次为限),随后麻醉大鼠,腹主动脉采集EDTA抗凝血用于血液学检查,采集促凝血,离心获得血清,检测SOD、MDA、LPO。
2.4 对小鼠出血、凝血时间的影响选用ICR小鼠(无模型组),于d 14给药1 h后,毛细管法测定凝血时间(clotting time,CT),剪尾法测定出血时间(bleeding time,BT)。计算改善率:改善率=(给药组时间-对照组时间)/对照组时间×100%。
2.5 对血热复合出血模型大鼠的影响参考文献[7]方法,选用SD大鼠,于给药d 14,除对照大鼠外,皮下注射质量分数为20%的酵母混悬液10 mL·kg-1,5 h后灌胃给药,1 h后灌胃给予1 mL无水乙醇,给药结束于d 15麻醉大鼠,腹主动脉采血,检测血浆TT、APTT、PT、FIB,并进行血液学检查。
2.6 对肝素化出血模型大鼠的影响参考文献[8]方法,选用SD大鼠,d 14末次给药后,皮下注射肝素钙300 U·kg-1复制出血模型,1 h后麻醉大鼠,腹主动脉采血,检测血浆TT、APTT、PT、FIB。
2.7 统计学处理数据均用x±s表示,使用SPSS 20.0软件,组间比较采用单因素方差分析。
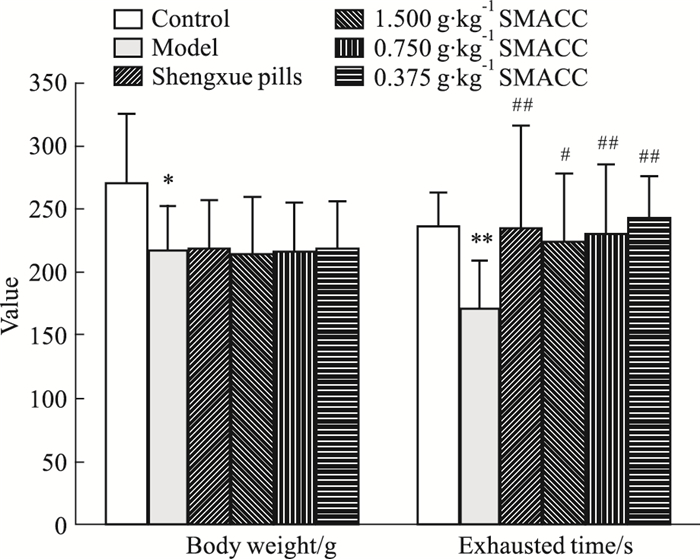
3 结果 3.1 SMACC对复合血虚模型大鼠的影响与对照组比较,模型大鼠体质量明显下降(P<0.05),游泳力竭时间明显缩短(P<0.01),血清中抗氧化成分SOD活性明显降低(P<0.01),氧化产物MDA、LPO含量明显升高(P<0.01),白细胞(white blood cell,WBC)计数、淋巴细胞(lymphocyte,LYM)数量、红细胞(red blood cell,RBC)计数、血红蛋白(hemoglobin,HGB)浓度、红细胞比容(hematocritg,HCT)均明显降低(P<0.01)。相比于模型组,小分子阿胶1.500、0.750、0.375 g·kg-1有效延长大鼠游泳力竭时间(P<0.05,P<0.01),降低血清中MDA、LPO含量(P<0.05,P<0.01),1.500、0.375 g·kg-1剂量组LYM数量明显增加(P<0.05)。见Fig 1、2,Tab 1。
|
| Fig 1 Effect of SMACC on body weight and exhausted time in rats with complex blood deficiency (x±s, n=12) *P < 0.05, **P < 0.01 vs control; #P < 0.05, ##P < 0.01 vs model |

|
| Fig 2 Effect of SMACC on serum SOD, MDA and LPO in rats with complex blood deficiency (x±s, n=12) **P < 0.01 vs control; #P < 0.05, ##P < 0.01 vs model |
| Group | Dose/g·kg-1 | WBC/109·L-1 | LYM/109·L-1 | RBC/1012·L-1 | HGB/g·L-1 | HCT/% |
| Control | - | 11.60±4.65 | 10.03±4.35 | 7.86±0.35 | 152±5 | 49.4±3.2 |
| Model | - | 1.23±0.79** | 0.55±0.36** | 1.76±0.35** | 41±7** | 11.4±2.1** |
| Shengxue pills | 1.500 | 1.58±0.52 | 0.71±0.40 | 2.16±0.59 | 49±11# | 13.5±3.7 |
| SMACC | 1.500 | 1.82±0.87 | 1.00±0.58# | 2.17±0.92 | 50±17 | 13.8±5.0 |
| 0.750 | 1.68±1.12 | 0.70±0.56 | 1.98±0.38 | 46±8 | 12.4±2.4 | |
| 0.375 | 1.87±0.77 | 0.97±0.52# | 2.45±1.16 | 53±21 | 15.2±5.5 | |
| **P < 0.01 vs control; #P < 0.05 vs model | ||||||
如Fig 3所示,相比于对照组,小分子阿胶3.00、1.50 g·kg-1明显缩短CT、BT,差异有统计学意义(P<0.05)。

|
| Fig 3 Effect of SMACC on clotting time and bleeding time in mice (x±s, n=10) *P < 0.05 vs control |
Tab 2、3结果显示,与对照组相比,模型大鼠PT、APTT明显延长(P<0.01),TT缩短(P<0.01),FIB水平明显增加(P<0.01),WBC、LYM、血小板(blood platelet,PLT)数量明显降低(P<0.01)。与模型组比较,小分子阿胶1.500 g·kg-1对PT具有明显缩短作用(P<0.05),增加FIB水平(P<0.01);1.500、0.750 g·kg-1剂量组WBC、LYM、RBC、HGB、HCT均明显升高(P<0.01,P<0.05),1.500、0.375 g·kg-1剂量组PLT升高(P<0.01)。
| Group | Dose /g·kg-1 | PT/s | APTT/s | TT/s | FIB/g·L-1 |
| Control | - | 19.1±1.2 | 16.1±2.2 | 38.8±1.4 | 1.81±0.21 |
| Model | - | 22.3±2.3** | 21.6±2.5** | 22.2±3.3** | 3.93±0.30** |
| Shengxue pills | 1.500 | 21.4±1.4 | 21.8±1.7 | 22.9±0.7 | 4.15±0.16 |
| SMACC | 1.500 | 20.1±2.0# | 22.9±3.4 | 21.4±3.0 | 4.33±0.23## |
| 0.750 | 21.2±1.3 | 21.9±2.3 | 23.2±0.8 | 4.15±0.22 | |
| 0.375 | 21.6±2.1 | 21.8±3.0 | 23.5±0.7 | 4.24±0.32# | |
| **P < 0.01 vs control; #P < 0.05, ##P < 0.01 vs model | |||||
| Group | Dose /g·kg-1 |
WBC /109·L-1 |
LYM /109·L-1 |
RBC /1012·L-1 |
HGB /g·L-1 |
HCT /% |
PLT /109·L-1 |
| Control | - | 6.70±1.62 | 5.42±1.35 | 6.7±0.5 | 134±8 | 41.7±1.4 | 1 065±92 |
| Model | - | 2.98±1.40** | 2.45±1.20** | 6.9±0.3 | 136±5 | 43.0±1.4* | 888±90** |
| Shengxue pills | 1.500 | 6.24±2.10## | 4.79±1.66## | 7.8±0.5## | 153±8## | 47.1±2.2## | 1 093±165## |
| SMACC | 1.500 | 5.93±3.01# | 4.72±2.66# | 8.1±0.5## | 158±6## | 48.6±1.7## | 1 035±119## |
| 0.750 | 5.24±2.51# | 4.19±2.08# | 7.6±0.4## | 151±9## | 46.7±3.1## | 980±159 | |
| 0.375 | 4.75±2.13# | 3.43±1.57 | 7.3±0.6 | 142±13 | 44.0±4.5 | 1 078±177## | |
| *P < 0.05,**P < 0.01 vs control; #P < 0.05, ##P < 0.01 vs model | |||||||
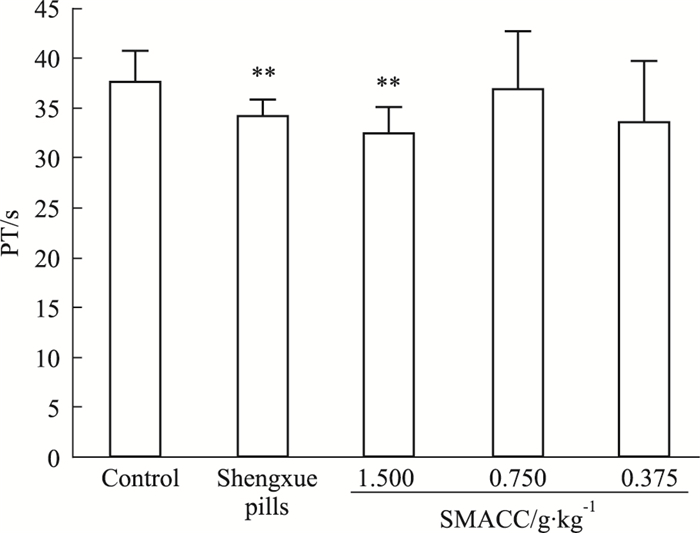
对照组大鼠PT、APTT、TT均明显延长,其中TT、APTT、FIB超过仪器检测限值。与对照组比较,小分子阿胶各剂量组对APTT、TT、FIB无明显影响,仍在仪器检测限值之外,结果不做统计。小分子阿胶1.500 g·kg-1明显缩短PT(P<0.01),见Fig 4。
|
| Fig 4 Effect of SMACC on coagulative function in heparinized bleeding rats (x±s, n=10) **P < 0.01 vs control |
APH具有强氧化作用,通过干扰RBC内的葡萄糖-6-磷酸脱氢酶,引起RBC破坏、HGB减少等溶血性贫血。CTX是一种细胞毒制剂,也是一种免疫抑制剂,不仅对机体的免疫器官有损伤作用,也对增殖周期中各期细胞具有杀灭作用,使骨髓造血功能抑制,从而使动物表现出血虚证状。APH与CTX联合,经两个途径共同造成动物血虚,使各类细胞数量全面下降,免疫器官受到损伤[9-10]。血虚状态下供血不足或血液的濡养功能减退,表现为全身虚弱证候,由于缺血缺氧降低了机体的新陈代谢,能量减少,因此显示出大鼠游泳时间缩短、体温下降等一系列气虚状态[11]。氧自由基增多是机体疲劳主要表现之一,血虚大鼠进行游泳实验时,机体内一系列氧自由基代谢会发生改变,表现为抗氧化能力的下降和脂质过氧化反应的增强[12]。SOD是机体清除氧自由基的重要酶,MDA、LPO是自由基引起的脂质过氧化的主要产物,它们的活性和含量间接反映机体的抗氧化能力,同时,也能间接反映机体的疲劳状态。
血虚大鼠游泳体力耗竭时间的明显延长,血清中氧化产物MDA、LPO含量的明显降低,表明小分子阿胶能够增强大鼠耐力,具有抗疲劳及抗氧化的能力。血中LYM数量呈现明显增加,考虑小分子阿胶作用机制可能是通过清除自由基,保护细胞膜或加快抗氧化物合成代谢的方式,来提高机体应对氧化应激状态的能力,提高机体免疫力,增强大鼠对APH和CTX毒性的抵抗能力,发挥抗氧化及抗疲劳作用。
小鼠断尾出血时间(BT)和毛细管凝血时间(CT)实验广泛用于中药止血、促凝血的活性筛选,综合反映参与止血过程的血管、血小板、凝血系统等多种因素的功能[13]。本研究中,给药小鼠BT、CT明显缩短,表明小分子阿胶能够促进血液凝固、加快伤口的止血速度,对外伤所致的出血情况具有较好的止血功效。
血液凝固是一个多系统参与的复杂过程,是由一系列凝血因子参与的酶促过程,包括内源性、外源性凝血途径及纤溶系统。PT是外源性凝血途径的常用实验指标,反映了外源性凝血系统各因子的活性及是否正常;APTT主要反映内源性凝血因子的活性和含量的变化;TT反映的是内、外源性共同凝血系统;FIB主要反映是否有足够的纤维蛋白原来生成纤维蛋白;PLT在血液凝固过程中发挥着重要作用,它的黏附、聚集、释放起到止血作用,同时它还为各种凝血酶原的活化提供必需的磷脂膜[14]。本研究酵母致血热出血模型以及肝素化出血模型中,均仅见小分子阿胶对PT有明显影响,结果一致,相互印证,提示小分子阿胶的止血作用机制可能在凝血级联反应上游,仅对外源性凝血途径具有激活作用,其作用靶点可能在凝血因子Ⅲ的激活过程。另外,小分子阿胶也通过增加FIB含量,促进纤维蛋白原转变为纤维蛋白的过程,升高大鼠血中PLT数量,影响抗凝和纤溶系统起作用。
干酵母诱导血热复合出血模型中,观察到RBC、HGB水平明显升高,虽未见模型组指标有明显异常,但仍说明在某些机制下,小分子阿胶具有“升红”作用,推测耗氧量增加可能是模型形成的机制之一,小分子阿胶具有抗氧化的作用,从而提高了RBC、HGB水平。小分子阿胶逆转WBC、LYM等血液学指标的不良改变,提示其可能具有一定的“升白”作用,其具体“升红”“升白”作用及机制有待进一步深入研究。
综上研究结果表明,小分子阿胶具有抗疲劳、抗氧化、增加耐力的作用,同时具有止血收敛的作用,将阿胶水解制得小分子阿胶的工艺改进具有可行性。
( 致谢: 本实验于天津药物研究院新药评价有限公司实验室完成,在此对本实验做出贡献的所有人员给予诚挚的感谢。)
| [1] |
国家药典委员会.中华人民共和国药典: 一部[S].北京: 中国医药科技出版社, 2015: 189. Chinese Pharmacopoeia Commission. Pharmacopoeia of the People's Republic of China: Part Ⅰ[S]. Beijing: China Medical Science and Technology Press, 2015: 189. |
| [2] |
庞萌萌, 李敏, 田晨颖, 等. 阿胶酶解液相对分子质量分布及其补血升白作用[J]. 中国实验方剂学杂志, 2017, 23(12): 13-7. Pang M M, Li M, Tian C Y, et al. Distribution of relative molecular mass of Asini Corii Colla hydrolyzate and investigation of its blood enrichment and leukogenic effect[J]. Chin J Exp Tradit Med Formul, 2017, 23(12): 13-7. |
| [3] |
Moure A, Dominguez H, Parajo J C. Antioxidant properties of ultrafiltration recovered soy protein fractions from industrial effluents and their hydrolysates[J]. Process Biochem, 2006, 41(2): 447-56. |
| [4] |
刘元涛, 张惠惠, 王升光, 等. 阿胶仿生酶解前后提高免疫力作用对比研究[J]. 时珍国医国药, 2016, 27(9): 2158-60. Liu Y T, Zhang H H, Wang S G, et al. Comparative study on enhancing immune function before and after enzymatic hydrolysis of Asini Corii Colla[J]. Lishizhen Med Mater Med Res, 2016, 27(9): 2158-60. |
| [5] |
李敏, 庞萌萌, 田晨颖, 等. 不同阿胶酶解液相对分子量分布及补血升白作用对比研究[J]. 中国食品添加剂, 2017(6): 105-11. Li M, Pang M M, Tian C Y, et al. Molecular weight distribution in different donkey-hide gelatin enzymolysis solution and its pharmacology effects[J]. China Food Addit, 2017(6): 105-11. doi:10.3969/j.issn.1006-2513.2017.06.010 |
| [6] |
焦立红, 任雷鸣, 赵寿康. 四种血虚小鼠模型制备方法的比较[J]. 时珍国医国药, 2006, 17(6): 1001-2. Jiao L H, Ren L M, Zhao S K. Comparison of the preparation methods of four blood deficiency mice model[J]. Lishizhen Med Mater Med Res, 2006, 17(6): 1001-2. doi:10.3969/j.issn.1008-0805.2006.06.050 |
| [7] |
包贝华, 赵显, 曹雨诞, 等. 鸡冠花对致热复合出血模型大鼠的凉血止血效应机制研究[J]. 中国药理学通报, 2013, 29(10): 1457-61. Bao B H, Zhao X, Cao Y D, et al. Cooling blood and haemostatic mechanism of Celosia Cristatae Flos in rat model of blood-heat and hemorrhage syndrome[J]. Chin Pharmacol Bull, 2013, 29(10): 1457-61. doi:10.3969/j.issn.1001-1978.2013.10.030 |
| [8] |
刘正君, 吉延慧, 张琪嘉钰, 等. 三七止血作用的实验研究[J]. 陕西中医学院学报, 2015, 38(2): 71-7. Liu Z J, Ji Y H, Zhangqi J Y, et al. The experimental researches on hemostasis function of Sanqi[J]. J Shanxi Coll Tradit Chin Med, 2015, 38(2): 71-7. |
| [9] |
李伟霞, 唐于平, 郭建明, 等. 当归-川芎药对及其组成药味对3种血虚模型补血作用的比较研究[J]. 中国中药杂志, 2011, 36(13): 1808-14. Li W X, Tang Y P, Guo J M, et al. Enriching blood effect comparison in three kinds of blood deficiency model after oral administration of drug pair of Angelicae Sinensis Radix and Chuanxiong Rhizoma and each single herb[J]. China J Chin Mater Med, 2011, 36(13): 1808-14. |
| [10] |
李淑娇, 唐于平, 李伟霞, 等. 当归-红花不同配比对血虚小鼠补血作用的比较研究[J]. 中国药理学通报, 2014, 30(6): 874-9. Li S J, Tang Y P, Li W X, et al. Comparing tonifying blood effects of Danggui-Honghua with different proportions on blood deficiency mice[J]. Chin Pharmacol Bull, 2014, 30(6): 874-9. |
| [11] |
金若敏, 宁炼, 陈长勋, 等. 血虚模型动物制备及当归补血汤的作用研究[J]. 中成药, 2001, 23(4): 268-71. Jin R M, Ning L, Chen C X, et al. Preparation of blood-deficient model and effects of Danggui blood-supplementing decoction on hemopoiesis[J]. Chin Tradit Pat Med, 2001, 23(4): 268-71. doi:10.3969/j.issn.1001-1528.2001.04.013 |
| [12] |
李吉萍, 孙婷婷, 胡天骄, 刘墨祥. 板蓝根活性组分对小鼠耐缺氧及抗疲劳作用的实验研究[J]. 中国药理学通报, 2016, 32(5): 712-5. Li J P, Sun T T, Hu T J, Liu M X. Effects of active component of Radix Isatidis on anti-anoxia and anti-fatigue in mice[J]. Chin Pharmacol Bull, 2016, 32(5): 712-5. doi:10.3969/j.issn.1001-1978.2016.05.023 |
| [13] |
赵菲菲, 杨馨, 徐丹, 等. 白及非多糖组分的止血作用及其机制的初步研究[J]. 中国药理学通报, 2016, 32(8): 1121-6. Zhao F F, Yang X, Xu D, et al. Hemostatic effect and mechanism of a non-polysaccharide fraction of Bletilla striata[J]. Chin Pharmacol Bull, 2016, 32(8): 1121-6. doi:10.3969/j.issn.1001-1978.2016.08.018 |
| [14] |
于生, 陈星, 单鸣秋. 紫菀丸对血热出血大鼠血液流变性、凝血时间及肺部的影响[J]. 中国实验方剂学杂志, 2013, 19(13): 229-33. Yu S, Chen X, Shan M Q. Effects of Ziwan Wan on hemorheological parameters, clotting time and lung presentations in rats with fevered and bleeding[J]. Chin J Exp Tradit Med Formul, 2013, 19(13): 229-33. |