


2. 广州医科大学附属第二医院药学部,广东 广州 510260;
3. 中山大学附属第一医院药学部,广东 广州 510080
2. Dept of Pharmacy, the Second Affiliated Hospital of Guangzhou Medical University, Guangzhou 510260, China;
3. Dept of Pharmacy, the First Affiliated Hospital of Sun Yat-sen University, Guangzhou 510080, China
核因子κB(nuclear factor kappa B,NF-κB)是一种多效转录因子。正常细胞中的NF-κB处于失活状态,它主要以p50/p65二聚体形式与其抑制蛋白(inhibitor kappa B,I-κB)结合,存在于胞质中。活性氧、细胞因子等多种刺激可诱导I-κB磷酸化,使其与p50/p65解离而活化NF-κB,并转移至胞核内,与凋亡相关基因结合促进基因转录,诱导细胞凋亡,造成机体损害。氧化应激是多种疾病炎性病变的重要因素,而NF-κB-诱导型一氧化氮合酶(inducible nitric oxide synthase,iNOS)-NO信号通路是机体内一条重要的氧化应激通路[1-3],NF-κB的活化不仅使许多编码炎症介质、细胞因子等的促炎症基因表达上调,而且可以激活iNOS等相关酶类及血管细胞黏附分子,使炎症反应级联放大,激活炎症介质趋化及相关炎症细胞。
知母为百合科植物知母(Anemarrhena asphodeloides Bge)的干燥根茎,味苦,性寒,归肺、胃、肾经,具有清热泻火、滋阴润燥等功效,主治温热病、高热烦渴、咳嗽气喘、燥咳、便秘、骨蒸潮热、虚烦不眠、消渴淋浊等症,是一种常用的苦寒清热传统中药,其主要的活性成分为知母皂苷(saponins from Anemarrhena asphodeloides Bge,SAaB)。研究表明,SAaB具有抗肿瘤、抗凝血、抗阿尔茨海默病、改善学习记忆、抗血栓、降脂、降糖等作用[4-5]。最新研究发现,SAaB还可明显抑制肥大细胞TNF-α、IL-6合成与释放[6],以及抑制小鼠嗜碱性粒细胞释放各种炎症介质[7]。课题组前期研究发现,SAaB能够明显下调糖尿病大鼠血浆中TNF-α、IL-6含量[8],推测其多种药理作用可能与抗炎活性密切相关,但具体的抗炎机制尚不清楚,可能与Toll样受体4(Toll-like receptor 4,TLR-4)/NF-κB、丝裂原活化蛋白激酶(mitogen-activated protein kinase,MAPK)-细胞外信号调节激酶(extracellular regulated protein kinases,ERK)、JAK-STAT等信号通路有关。目前,SAaB对RAW264.7细胞功能的影响尚未见报道。本研究以脂多糖(lipopolysaccharide,LPS)诱导RAW264.7作为炎症细胞模型,探讨SAaB通过调节NF-κB-iNOS-NO信号通路对RAW264.7细胞功能的影响,进一步从细胞水平阐明其可能的抗炎机制,以期为其后续开发奠定理论基础。
1 材料 1.1 细胞RAW264.7细胞株,购自上海赛齐生物工程有限公司。
1.2 药物与试剂SAaB提取物按实验室前期提取纯化工艺制备(皂苷含量以菝葜皂苷元计52%)[9],精确称取32 mg SAaB,用PBS溶解,配成320 mg·L-1的母液,-20 ℃储存备用。DMEM高糖培养基(批号p002548,Gibco);IL-6 ELISA检测试剂盒(批号020680114)、TNF-α高灵敏度ELISA检测试剂盒(批号0282H80121),均购自杭州联科生物技术股份有限公司;iNOS ELISA检测试剂盒(批号CK-E20450M,艾莱萨生物科技上海有限公司);MTT(批号A1720090,Aladdin);RIPA细胞裂解液、BCA蛋白定量试剂盒(北京普利莱基因技术有限公司);化学发光剂ECL(碧云天生物技术研究所);NF-κB p65抗体(美国Cell Signaling公司);β-actin抗体(批号306010,美国Santa Cruz公司);PE标记山羊抗小鼠、FITC标记山羊抗兔二抗(美国Santa Cruz公司)。
1.3 仪器倒置显微镜(江南显微镜有限公司);酶标仪(美国Bio-Rad);超净工作台(江苏净化设备有限公司);二氧化碳培养箱(SL SHELLAB);超低温冰箱(SANYO);高速冷冻离心机(科大创新股份有限公司中佳分公司)。
2 方法 2.1 细胞培养RAW264.7细胞以完全培养基于37 ℃、5% CO2培养箱培养,当细胞融合度达到80%,吸弃培养基,PBS洗细胞2~3次后,加入胰酶,充分接触消化细胞,吹打收集细胞,1:3传代培养,隔天换液。
2.2 MTT法检测细胞增殖取对数生长期的细胞,消化后计数,调整细胞密度为3×109·L-1,接种于96孔板,培养24 h后,分别设置调零组、空白对照组、SAaB组(160、80、40、20、10、5、2.5、1.75 mg·L-1),每组设置6个复孔,空白组和药物组每孔加入细胞液100 μL,调零组加入完全培养基100 μL,接种至96孔板中,CO2培养箱中培养24 h,吸弃上清,每孔加入100 μL MTT试剂,放入细胞培养箱中培养4 h,吸弃上清,每孔加入150 μL DMSO,置摇床10 min,酶标仪570 nm波长测量每孔的吸光度值。细胞存活率=(ODSAaB干预组-OD调零组)/(OD空白对照组-OD调零组)×100%。
2.3 细胞培养及分组取对数生长期的细胞,消化后计数,调整细胞密度为3×108·L-1,接种96孔板,预培养24 h后,分别设置:①空白对照组:正常培养的RAW264.7细胞组;②炎症模型组(LPS浓度为10 mg·L-1);③LPS+SAaB组(SAaB浓度分别为30、3、0.3 mg·L-1);④LPS+布洛芬组(100 mg·L-1)。每组设置6个复孔。空白组和炎症模型组每孔加入100 μL完全培养基,其余组加入相应含药物的完全培养基,继续培养箱培育1 h。
2.4 Griess法测定RAW264.7细胞中NO含量同“2.3”项下培养细胞并分组,除空白组外,每孔加入100 μL LPS(10 mg·L-1),继续放入培养箱培养24 h后,每孔吸取50 μL细胞上清液至另一新的96孔板中,每孔加入50 μL A液(称取1.0 g无水对氨基苯磺酸于烧杯中,加入6 mL 85%浓磷酸,去离子水溶解定容至100 mL),细胞培养箱孵育10 min后,每孔加入50 μL B液(取0.1 g N-1-萘乙二胺盐酸盐于烧杯中,去离子水溶解定容至100 mL),摇床震荡10 min。酶标仪于546 nm处测量每孔的吸光度,后根据NaNO2标准溶液(精确称取6.9 mg NaNO2于烧杯中,去离子水溶解定容至10 mL)吸光度绘制标准曲线,算出每孔的NO浓度。
2.5 ELISA法测定RAW264.7细胞中TNF-α、IL-6、iNOS的含量同“2.3”项下培养细胞并分组,除空白组外,每孔加入100 μL LPS(10 mg·L-1),继续培养24 h后,吸取细胞液上清,按ELISA试剂盒说明书,测定各组细胞TNF-α、IL-6、iNOS的含量。
2.6 Western blot法检测RAW264.7细胞中NF-кB p65蛋白表达同“2.3”项下培养细胞并分组,除空白组外,每孔加入100 μL LPS(10 mg·L-1),继续培养24 h后,提取细胞总蛋白,采用BCA蛋白定量法检测各组细胞蛋白浓度,95 ℃灭活蛋白5 min,SDS-PAGE凝胶电泳,转膜,8%脱脂奶粉封闭1 h,一抗4 ℃孵育过夜,二抗室温孵育1 h,ECL显色。
2.7 统计学方法实验数据以x±s表示,采用SPSS 19.0统计软件及单因素方差分析(one-way ANOVA)处理数据。
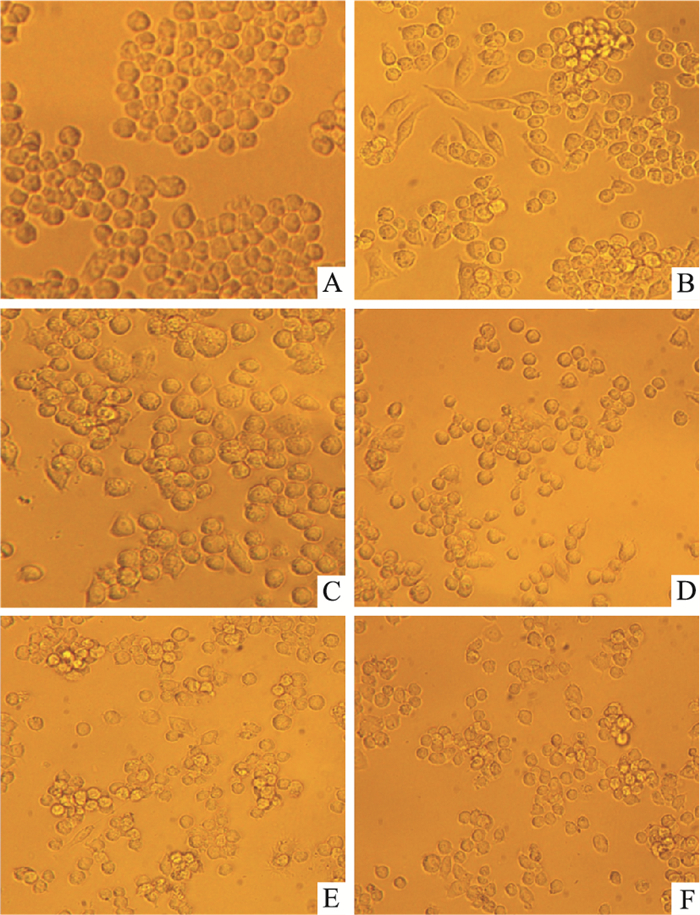
3 结果 3.1 RAW264.7细胞形态特征各组RAW264.7细胞形态如Fig 1所示,正常RAW264.7细胞呈圆形或椭圆形,LPS刺激诱导24 h,模型组细胞形态改变明显,体积增大,拉伸呈梭形。与模型组比较,不同浓度SAaB与LPS共刺激,发现大部分细胞仍为圆形,形态趋向正常细胞。
|
| Fig 1 Effects of SAaB on morphology of RAW264. 7 cells (×200) A: Control group; B: LPS group; C: LPS+Ibuprofen group; D: SAaB (0.3 mg·L-1) +LPS; E: SAaB (3 mg·L-1) +LPS; F: SAaB (30 mg·L-1) +LPS. |
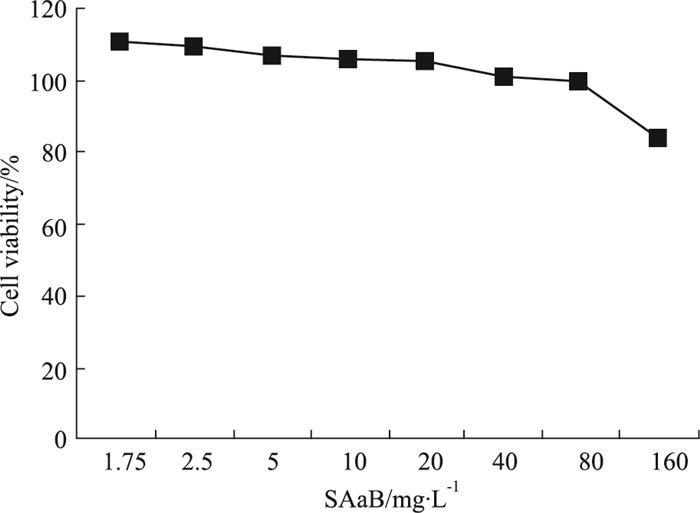
Fig 2的MTT结果显示,SAaB在0~80 mg·L-1对正常RAW264.7细胞无毒性作用,但当浓度达到160 mg·L-1时,细胞活力下降。
|
| Fig 2 Effects of SAaB on proliferation of RAW264.7 cells |
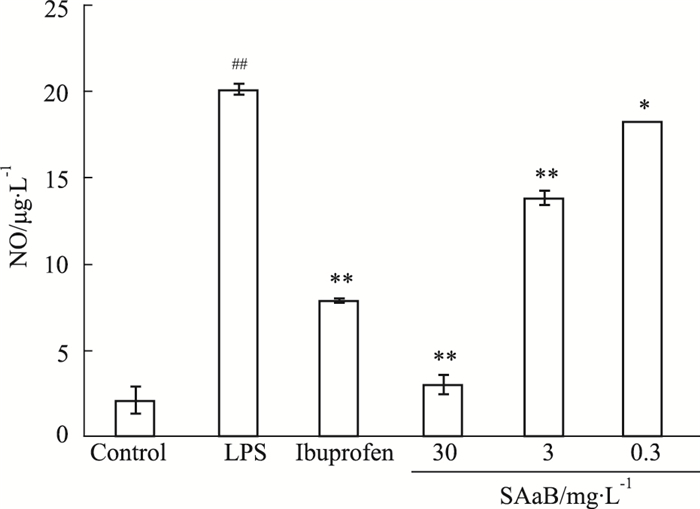
Griess法测定不同浓度SAaB干预下,LPS诱导的RAW264.7炎症细胞中NO含量。如Fig 3所示,与对照组相比,LPS诱导的RAW264.7细胞中NO含量明显增加(P<0.01);与LPS炎症模型组比较,SAaB各组中NO含量均明显下降(P<0.01,P<0.05),且呈现浓度依赖性。
|
| Fig 3 Effects of SAaB on contents of NO in RAW264.7 cells (x±s, n=6) ##P < 0.01 vs control group; *P < 0.05, **P < 0.01 vs LPS group |
Tab 1的ELISA检测结果显示,与对照组相比,LPS诱导的RAW264.7细胞中TNF-α、IL-6和iNOS表达量明显增加(P<0.01);与LPS炎症模型组比较,不同浓度SAaB干预组中TNF-α、IL-6和iNOS表达量明显下降(P<0.01)。
| Group | Concentration/ mg·L-1 |
TNF-α/ μg·L-1 |
IL-6/ μg·L-1 |
iNOS/ μg·L-1 |
| Control | - | 0.83±0.15 | 0.96±0.03 | 5.53±0.54 |
| LPS | 10.00 | 4.80±0.07## | 2.74±0.04## | 15.27±0.97## |
| Ibuprofen | 100.00 | 3.01±0.02** | 1.79±0.07** | 10.17±0.50** |
| SAaB | 30.00 | 2.70±0.04** | 1.98±0.05** | 7.20±0.21** |
| 3.00 | 2.90±0.05** | 2.12±0.04** | 10.09±0.57** | |
| 0.30 | 3.01±0.01** | 2.23±0.03** | 10.61±0.31** | |
| ##P < 0.01 vs control group; **P < 0.01 vs LPS group | ||||
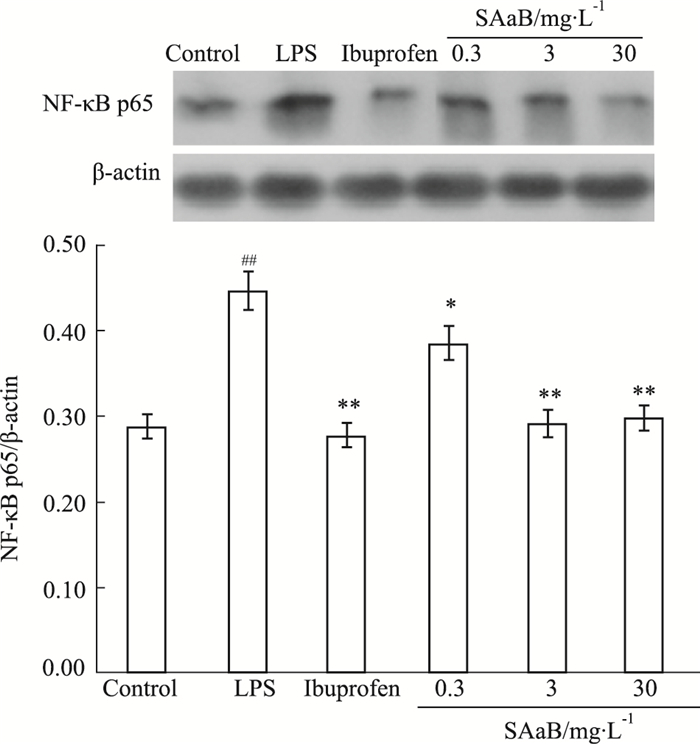
Fig 4的Western blot结果显示,LPS诱导的RAW264.7细胞中NF-κB p65蛋白的表达水平明显增加(P<0.01),而不同浓度SAaB干预组的表达量则明显下降。结果提示,SAaB能够抑制NF-κB p65蛋白的表达,抑制其转移至细胞核内,进而抑制炎症因子进一步活化。
|
| Fig 4 Effects of SAaB on expression levels of NF-κB p65 protein in RAW264.7 cells (x±s, n=6) ##P < 0.01 vs control group; *P < 0.05, **P < 0.01 vs LPS group |
炎症反应是机体受到来自于内部或外部的刺激而产生的防御反应,在一定程度内起到保护机体的作用,但长期、剧烈的炎症反应会参与多种疾病的病理进程,如2型糖尿病、动脉粥样硬化、肿瘤、风湿性关节炎、慢性阻塞性肺疾病、感染性休克等[10-11]。炎症是这些疾病的病理基础,治疗免疫炎症反应,逐渐成为新药开发的重要靶点。
近年来研究表明,SAaB作为知母主要药理活性成分,具有明显的抗炎活性,临床应用前景广阔。然而,SAaB抗炎作用,尤其是对RAW264.7炎症细胞功能的调节机制研究并不深入。因此,本研究以RAW264.7细胞作为载体,采用LPS建立体外细胞炎症模型,探讨SAaB对LPS诱导的RAW264.7细胞功能的调控作用。
本研究结果显示,不同浓度的SAaB与LPS共刺激24 h后,仅160 mg·L-1的SAaB抑制RAW264.7细胞增殖,而浓度在0~80 mg·L-1的SAaB对正常RAW264.7细胞生长无明显抑制。这与160 mg·L-1的SAaB对RAW264.7细胞有细胞毒作用相关,说明实验设置的SAaB高、中、低剂量组(30、3、0.3 mg·L-1)无明显细胞毒性,具有研究意义。显微镜下观察到LPS刺激RAW264.7细胞24 h可以改变其形态,细胞体积增大,呈梭形,而0.3~30 mg·L-1的SAaB和LPS共同作用24 h后,细胞形态变规则,并恢复成圆形。
LPS诱导激活RAW264.7细胞,使iNOS水平明显增加,iNOS活化后会直接催化NO持续生成,导致NO释放量明显升高,进而使得细胞分泌释放重要的炎症标志因子TNF-α,而TNF-α在炎症网络中具有关键作用,是全身炎性反应的始动介质,可诱导IL-1和IL-6表达释放,使炎性损伤的级联效应放大,从而进一步加剧炎症反应[12-14]。NF-κB核转录因子作为炎症过程中起重要作用的转录因子,当细胞受到LPS刺激后,NF-κB活化二聚体会在NF-κB信号通路激活,易位进入细胞核内,并与细胞核内的靶基因在κB位点发生特异性结合,从而调控NO的生成和细胞因子TNF-α、IL-6等的表达和释放[15]。
本研究发现,SAaB可抑制LPS诱导的炎症细胞NO释放增加,并呈浓度依赖性,提示SAaB具有抗炎活性,且不是通过抑制细胞活力来抑制NO分泌。SAaB可下调NF-κB p65蛋白表达水平,同时减少TNF-α、IL-6等炎症因子的产生。此外,实验结果也提示了LPS可引起NF-κB p65的蛋白表达水平增高,并且在LPS诱导的炎症过程中,NF-κB-iNOS-NO三者的激活及产物的生成在时间上具有同步性,而使用阳性对照药(布洛芬)和SAaB后,均可抑制上述效应,进一步揭示了SAaB可通过NF-κB-iNOS-NO信号通路,抑制LPS诱导的炎症反应。以NF-κB-iNOS-NO信号通路为切入点,研究具有下调巨噬细胞该通路活性,并且能产生明显抗炎、抗免疫作用的药物,对于慢性免疫炎症性疾病的治疗具有广阔的应用前景。
综上所述,本研究结果表明SAaB可明显抑制LPS诱导的RAW264.7细胞中炎症因子NO、TNF-α、IL-6、iNOS的释放,并且能下调RAW264.7细胞NF-κB p65蛋白表达水平,表明SAaB能通过下调NF-κB-iNOS-NO信号通路,抑制炎症因子的过度表达,从而抑制炎症反应。本文从细胞水平初步探讨了SAaB抗炎的作用机制,为其临床应用与后续开发奠定了理论基础。
( 致谢: 本实验完成于广东药科大学中心实验室,感谢广州医科大学附属第二医院药学部的老师对本课题的指导,感谢课题组全体老师和同学对实验的支持与帮助。)
| [1] |
Franceschelli S, Pesce M, Ferrone A, et al. Biological effect of licochalcone C on the regulation of PI3K/Akt/eNOS and NF-κB/iNOS/NO signaling pathways in H9c2 cells in response to LPS stimulation[J]. Int J Mol Sci, 2017, 18(4): 690-703. doi:10.3390/ijms18040690 |
| [2] |
Lisakovska O, Shymanskyy I, Mazanova A, et al. Vitamin D3 protects against prednisolone-induced liver injury associated with the impairment of the hepatic NF-κB/iNOS/NO pathway[J]. Biochem Cell Biol, 2017, 95(2): 213-22. doi:10.1139/bcb-2016-0070 |
| [3] |
Wang Z Q, Chen M T, Zhang R, et al. Docosahexaenoic acid attenuates doxorubicin-induced cytotoxicity and inflammation by suppressing NF-κB/iNOS/NO signaling pathway activation in H9C2 cardiac cells[J]. J Cardiovasc Pharmacol, 2016, 67(4): 283-9. doi:10.1097/FJC.0000000000000350 |
| [4] |
钟艳梅, 陈坚平, 钟静君, 等. 知母总皂苷对INS-1胰岛β细胞功能的影响[J]. 中华中医药杂志, 2018, 33(6): 2631-3. Zhong Y M, Chen J P, Zhong J J, et al. Effects of Rhizoma Anemarrhenae total saponins on the function of INS-1 islet β cells[J]. Chin J Tradit Chin Med Pharm, 2018, 33(6): 2631-3. |
| [5] |
谭希, 潘会君, 吴伟达, 等. 知母皂苷AⅢ抑制人脑胶质瘤增殖生长的机制研究[J]. 中国中药杂志, 2017, 42(6): 1160-6. Tan X, Pan H J, Wu W D, et al. Inhibitory mechanisms of timosaponin AⅢ on proliferation and growth of human glioblastoma cells[J]. Chin J Chin Mater Med, 2017, 42(6): 1160-6. |
| [6] |
Makino T, Shiraki Y, Mizukami H. Interaction of gypsum and the rhizome of Anemarrhena asphodeloides plays an important role in anti-allergic effects of byakkokakeishito in mice[J]. J Nat Med, 2014, 68(3): 505-12. doi:10.1007/s11418-014-0827-y |
| [7] |
Kim B R, Cho Y C, Le H, et al. Suppression of inflammation by the rhizome of Anemarrhena asphodeloides via regulation of nuclear factor-κB and p38 signal transduction pathways in macrophages[J]. Biomed Rep, 2017, 6(6): 691-7. doi:10.3892/br.2017.895 |
| [8] |
钟艳梅, 钟静君, 石忠峰, 等. 知母总皂苷干预T2DM大鼠的药效学研究[J]. 时珍国医国药, 2017, 28(1): 71-4. Zhong Y M, Zhong J J, Shi Z F, et al. Hypoglycemic and lipid-decreasing pharmacodynamics study of Rhizoma Anemarrhenae total saponins[J]. Lishizhen Med Mater Med Res, 2017, 28(1): 71-4. |
| [9] |
芮雯, 吴妍, 吉星, 等. 知母降糖有效部位的提取工艺优选及成分分析[J]. 中国实验方剂学杂志, 2013, 19(22): 4-8. Rui W, Wu Y, Ji X, et al. Optimization of extraction process and component analysis of hypoglycemic effective parts from Anemarrhenae Rhizoma[J]. Chin J Exp Tradit Med Form, 2013, 19(22): 4-8. |
| [10] |
魏伟. 炎症免疫反应软调节[J]. 中国药理学通报, 2016, 32(3): 297-303. Wei W. Soft regulation of inflammatory immune responses[J]. Chin Pharmacol Bull, 2016, 32(3): 297-303. doi:10.3969/j.issn.1001-1978.2016.03.001 |
| [11] |
李影, 陈镜宇, 张玲玲, 等. 肿瘤坏死因子受体相关因子参与炎症免疫调节的研究进展[J]. 中国药理学通报, 2015, 31(9): 1206-11. Li Y, Chen J Y, Zhang L L, et al. Research advance of tumor necrosis factor receptor-associated factors in inflammatory immune regulation[J]. Chin Pharmacol Bull, 2015, 31(9): 1206-11. doi:10.3969/j.issn.1001-1978.2015.09.006 |
| [12] |
Su B P, Park G H, Kim H N, et al. Anti-inflammatory effect of the extracts from the branch of Taxillus yadoriki, being parasitic in Neolitsea sericea, in LPS-stimulated RAW264.7 cells[J]. Biomed Pharmacother, 2018, 104: 1-7. doi:10.1016/j.biopha.2018.05.034 |
| [13] |
Park J W, Kwon O K, Kim J H, et al. Rhododendron album Blume inhibits iNOS and COX-2 expression in LPS-stimulated RAW264.7 cells through the downregulation of NF-κB signaling[J]. Int J Mol Med, 2015, 35(4): 987-94. doi:10.3892/ijmm.2015.2107 |
| [14] |
黄小平, 卢金冬, 丁煌, 等. 黄芪和三七的主要有效成分配伍对脑缺血/再灌注小鼠NF-κB信号通路及炎性因子表达的影响[J]. 中国药理学通报, 2015, 31(1): 141-6. Huang X P, Lu J D, Ding H, et al. Effects of main active component combinations between Astragalus and Panax notoginseng on NF-κB signaling pathway and expressions of inflammatory factors after cerebral ischemia-reperfusion in mice[J]. Chin Pharmacol Bull, 2015, 31(1): 141-6. doi:10.3969/j.issn.1001-1978.2015.01.030 |
| [15] |
邓超, 任改艳, 孙阿宁, 等. 豆蔻明对TLR4/MyD88/NF-κB/iNOS信号通路的调节作用[J]. 中国药理学通报, 2016, 32(6): 779-83. Deng C, Ren G Y, Sun A N, et al. The regulatory effect of cardamonin on TLR4/MyD88/NF-κB/iNOS pathway[J]. Chin Pharmacol Bull, 2016, 32(6): 779-83. doi:10.3969/j.issn.1001-1978.2016.06.009 |

