

急性胰腺炎属于临床常见腹部急性病症,轻度易于治疗,重型急性胰腺炎(severe acute pancreatitis,SAP)不但引发胰腺重度炎症、组织坏死,还会影响全身重要器官功能,其中肺部为最易受累的器官。调查显示,SAP中肺损伤发生率高达70%,是导致SAP患者死亡的重要原因[1],因此,探究其发病机制,对于预防及治疗SAP肺损伤者,改善预后,均十分重要。近期研究显示,核因子κB(nuclear factor κB, NF-κB)的激活可导致肺损伤的发生,而抑制其表达后,可减轻肺损伤[2]。丝裂原活化蛋白激酶(mitogen activated protein kinase,MAPK)家族成员主要包括p38、ERK、JNK,参与机体多种炎症反应。研究显示,在肺损伤过程中,激活MAPK通路后,可释放大量炎症因子,加重病情[3]。以上研究表明,MAPK/NF-κB可能作为SAP肺损伤的靶点。
水飞蓟素(silymarin)是从水飞蓟种皮中提取的黄铜木质素化合物。临床研究显示,水飞蓟素不仅可用于肝病预防、治疗,且具有广泛的抗肿瘤作用,如在前列腺癌、肝癌、宫颈癌、乳腺癌中,能够抑制癌细胞增殖分化[4]。张珂等[5]研究显示,水飞蓟素可通过抑制炎症反应及氧化应激损伤,减轻大鼠肺缺血/再灌注损伤。以上研究表明,水飞蓟素对肺损伤具有一定的保护作用,但有关水飞蓟素在SAP引发的肺损伤的作用机制目前研究不多。为此,本研究通过建立SAP大鼠模型,观察水飞蓟素处理对MAPK/NF-κB信号通路的影响,探究其潜在作用机制。
1 材料与方法 1.1 实验动物SPF级♂SD大鼠72只,8周龄,体质量230~260 g,购于上海斯莱克实验动物有限公司,许可证号为2015000504404。所有大鼠均在昼夜交替、自然光照下饲养,饲养过程中维持恒温25 ℃,湿度为50%,期间大鼠自由饮水、摄食,定时对鼠笼进行清理,饲养期间所需水、食物及其他用品等,均经消毒,维持饲养环境清洁,保持通风。
1.2 试剂与仪器水飞蓟素购于上海纯优生物科技有限公司,批号:20160803;地塞米松注射液,广西万德药业股份有限公司,批号:20161107;苏木精、伊红染液购自美国Sigma公司;BCA蛋白检测试剂盒购自美国Thermo Fisher Scientific公司;TNF-α、IL-1β ELISA试剂盒(批号:20161204、20160918),购于美国R&D公司;兔抗鼠p65、p-p65、IκBα、p-IκBα、ERK1/2、p-ERK1/2、JNK、p-JNK抗体,购自美国Santa Cruz公司;兔抗鼠p38、p-p38、辣根过氧化物酶标记羊抗鼠IgG二抗,购自美国R&D公司。蛋白凝胶成像仪,购自Bio-Rad公司;全自动血气分析检测仪,购于美国Beckman公司。
1.3 方法 1.3.1 动物模型的制备根据文献方法[6],制备SAP大鼠模型,制备前大鼠自由饮水,禁食12 h,腹腔注射2%戊巴比妥钠麻醉,随后固定于手术台,常规消毒、铺巾后,于腹部正中部位做一切口,暴露十二指肠,并将其提出体外,识别胰胆管汇入十二指肠系膜乳头开口处,在其下缘肠壁处选取无血管区,用注射器针头穿刺后,将5 cm硬膜外导管(外径0.61 mm PE10聚乙烯导管)置入,朝向开口方向缓慢推进5 cm后,缝扎胰胆管下段及硬膜外导管,于导管末端连接输液转换器,泵入5%牛黄胆酸钠1 mL·kg-1,流速控制在0.2 mL·min-1,2 min后,见胰胆管以及主胰管扩张后,维持10 min,将缝扎线去除,并将导管退出,封闭穿刺孔,复位十二指肠后逐层关腹。
1.3.2 动物分组将大鼠分为假手术组(仅翻动十二指肠、胰腺,不穿刺注药)、模型组、水飞蓟素低、中、高剂量组、地塞米松组(阳性组)。SAP模型制备完成后,水飞蓟素低、中、高剂量组即刻腹腔注射用DMSO配制成的混悬液50、100、200 mg·kg-1,地塞米松组注射2 mg·kg-1地塞米松;假手术组、模型组腹腔注射同量生理盐水,共给药3 d。
1.3.3 标本采集各组随机选取6只大鼠,末次给药后,即刻采集下腔静脉血3 mL,随后剖腹采集腹主动脉血,将大鼠处死后获得胰腺组织、肺组织。
1.3.4 动脉血气指标测定采用全自动血气分析检测仪器,检测腹主动脉血中氧分压(arterial partial pressure of oxygen,PaO2)、二氧化碳分压(arterial partial pressure of carbon dioxide,PaCO2),计算氧合指数(oxygenation index,OI)。
1.3.5 血清中淀粉酶、TNF-α、IL-1β水平的检测下腔静脉血凝固后离心,保留上清液,采用碘比色法检测血清淀粉酶含量;采用ELISA法检测TNF-α、IL-1β水平,具体参照试剂盒说明书进行操作。
1.3.6 大鼠肺泡灌洗液(bronchoalveolar lavage,BAL)中中性粒细胞(polymorphonuclear neutrophils,PMN)计数各组选取6只大鼠进行支气管肺泡灌洗,利用自动血细胞分析仪对BAL中PMN进行计数。
1.3.7 肺组织湿干重(wet weight/dry weight,W/D)测定切除肺组织右肺下叶,用滤纸擦干后,置于玻璃试管中称重,此时为肺组织湿重(W),置于烤箱中,温度设定为60 ℃,连续烘烤、称重,直至肺组织重量不再变化,此时所测重量为干重(D)。
1.3.8 光镜下观察病理学变化制备胰腺、肺组织石蜡切片,进行HE染色,采用Schmidt病理评分法[7],从胰腺水肿、坏死、炎症细胞浸润等方面对染色结果进行评定,分为5个等级,以0、1、2、3、4分进行标记。采用Holfbauer评分法[8],对水肿、出血、炎症浸润等进行评定:肺部无病变为0分;25%视野出现以上病变为1分,50%视野出现病变为2分;75%视野存在以上病变为3分;整个视野均出现以上病变为4分。
1.3.9 Western blot检测肺组织剪碎后,添加蛋白裂解液放置30 min,离心后收集上清液,蛋白提取试剂盒提取细胞中蛋白,BCA试剂盒测定蛋白浓度,随后进行SDS-PAGE电泳。电泳后,将蛋白转移至PVDF膜,添加脱脂牛奶封闭后洗膜,添加1:300稀释的兔抗鼠p65、p-p65、IκBα、p-IκBα、ERK1/2、p-ERK1/2、JNK、p-JNK、p38、p-p38一抗,置于4 ℃过夜,清洗后加二抗,置于37 ℃中孵育2 h,ECL显色后,凝胶成像仪中观察蛋白表达,并保存图像。
1.4 统计学方法采用统计学软件SPSS 22.0进行数据分析。计量资料以x±s描述,两组间比较行t检验,多组间比较行单因素方差分析,进一步两两对比采用SNK-q检验。
2 结果 2.1 动脉血气指标测定结果Tab 1结果显示,与假手术组相比,模型组PaCO2升高,PaO2、OI降低,差异有显著性(P<0.05)。与模型组相比,水飞蓟素低、中、高剂量组和阳性组PaCO2降低,PaO2、OI升高,具有剂量依赖性,差异有显著性(P<0.05)。
| Group | Dose/ mg·kg-1 |
PaO2/ mmHg |
PaCO2/ mmHg |
OI/mmHg |
| Sham | - | 95.68±2.66 | 31.65±1.67 | 451.52±7.52 |
| Model | - | 54.58±3.53* | 58.63±2.84* | 288.63±7.49* |
| Silymarin | 50 | 65.43±2.65# | 47.66±2.57# | 328.44±6.27# |
| 100 | 77.24±2.32# | 41.13±2.33# | 373.59±8.19# | |
| 200 | 84.52±1.84# | 33.76±1.74# | 388.72±7.34# | |
| Dexamethasone | 2 | 87.66±1.51# | 32.84±1.64# | 417.29±9.04# |
| *P < 0.05 vs sham; #P < 0.05 vs model | ||||
Tab 2结果显示,与假手术组相比,模型组淀粉酶活性、TNF-α、IL-1β水平升高,差异有显著性(P<0.05)。与模型组相比,水飞蓟素低、中、高剂量组和阳性组淀粉酶活性、TNF-α、IL-1β水平降低,具有剂量依赖性,差异有显著性(P<0.05)。
| Group | Dose/ mg·kg-1 |
Amylase activity /kU·L-1 |
TNF-α /ng·L-1 |
IL-1β /ng·L-1 |
| Sham | - | 1.68±0.16 | 16.57±4.22 | 6.04±1.06 |
| Model | - | 7.43±0.23* | 241.42±20.64* | 194.74±27.46* |
| Silymarin | 50 | 6.58±0.79# | 171.69±16.53# | 156.97±20.48# |
| 100 | 5.37±0.64# | 120.18±23.44# | 137.53±14.48# | |
| 200 | 2.41±0.23# | 80.23±15.46# | 82.49±9.65# | |
| Dexamethasone | 2 | 2.25±0.51# | 62.54±8.69# | 78.25±10.34# |
| *P < 0.05 vs sham; #P < 0.05 vs model | ||||
Tab 3结果显示,与假手术组相比,模型组胰腺、肺组织W/D、PMN升高,差异有显著性(P<0.05)。与模型组相比,水飞蓟素低、中、高剂量组和阳性组胰腺、肺组织W/D、PMN降低,具有剂量依赖性,差异有显著性(P<0.05)。
| Group | Dose/ mg·kg-1 |
Pancreas W/D |
Lung W/D |
PMN/ ×107·L-1 |
| Sham | - | 4.26±0.27 | 4.52±0.51 | 0.86±0.16 |
| Model | - | 7.37±0.76* | 6.42±0.39* | 2.92±0.35* |
| Silymarin | 50 | 6.25±0.33# | 5.73±0.41# | 2.18±0.32# |
| 100 | 5.28±0.29# | 5.21±0.32# | 1.56±0.24# | |
| 200 | 4.47±0.28# | 4.72±0.37# | 1.18±0.23# | |
| Dexamethasone | 2 | 4.36±0.42# | 4.66±0.51# | 0.95±0.14# |
| *P < 0.05 vs sham; #P < 0.05 vs model | ||||
Fig 1的HE染色显示,假手术组大鼠胰腺组织细胞正常,胰腺小叶完整,间质未出现炎性细胞浸润、充血以及坏死组织。模型组胰腺腺泡细胞出现大量坏死,结构模糊、融合成一片,小叶结构模糊,出现大量炎症细胞浸润,肺泡间间隔明显变宽。水飞蓟素组及阳性组均得到明显改善,且随着处理剂量的增加,肺组织逐渐恢复正常。Tab 4结果显示,与假手术组相比,模型组大鼠胰腺组织病理评分升高,差异有显著性(P<0.05);与模型组相比,阳性组、水飞蓟素组胰腺组织病理评分均降低,随着给药剂量的升高,肺组织病理评分逐渐降低,差异有显著性(P<0.05)。

|
| Fig 1 Pathological staining structure of pancreatic tissues (×100) A: Sham operation group; B: Model group; C: Silymarin low dose group; D: Silymarin medium dose group; E: Silymarin high dose group; F: Dexamethasone group. |
| Group | Dose/ mg·kg-1 |
Pathological grading of lung tissue | Pathological grading of pancreas |
| Sham | - | 0.21±0.06 | 0.28±0.06 |
| Model | - | 3.78±0.74* | 7.56±1.05* |
| Silymarin | 50 | 2.87±0.52# | 6.07±0.93# |
| 100 | 2.28±0.71# | 4.38±0.57# | |
| 200 | 0.97±0.28# | 2.16±0.13# | |
| Dexamethasone | 2 | 0.64±0.17# | 1.94±0.28# |
| *P < 0.05 vs sham; #P < 0.05 vs model | |||
如Fig 2所示,假手术组肺泡结构完整,肺间质未出现水肿、充血、炎性细胞浸润等。模型组肺泡壁变厚、间隔变宽,肺间质出现充血,且伴随大量炎性细胞浸润。水飞蓟素组及阳性组均得到明显改善,且随着处理剂量的增加,肺组织逐渐恢复正常。Tab 4结果显示,与假手术组相比,模型组大鼠肺组织病理评分升高,差异有显著性(P<0.05);与模型组相比,水飞蓟素组及阳性组大鼠肺组织病理评分均降低,随着给药剂量的升高,肺组织病理评分逐渐降低,差异有显著性(P<0.05)。

|
| Fig 2 Pathological staining of lung tissues (×200) A: Sham operation group; B: Model group; C: Silymarin low dose group; D: Silymarin medium dose group; E: Silymarin high dose group; F: Dexamethasone group. |
| Group | Dose/mg·kg-1 | JNK | p-JNK | p38 | p-p38 | ERK1/2 | p-ERK1/2 |
| Sham | - | 0.76±0.04 | 0.17±0.06 | 0.58±0.12 | 0.17±0.03 | 0.56±0.05 | 0.22±0.04 |
| Model | - | 0.73±0.08 | 0.89±0.16* | 0.64±0.11 | 0.95±0.09* | 0.58±0.06 | 0.83±0.08* |
| Silymarin | 50 | 0.74±0.09 | 0.73±0.14# | 0.66±0.11 | 0.78±0.09# | 0.54±0.07 | 0.68±0.13# |
| 100 | 0.72±0.06 | 0.53±0.12# | 0.63±0.14 | 0.64±0.13# | 0.55±0.09 | 0.52±0.06# | |
| 200 | 0.78±0.13 | 0.36±0.08# | 0.61±0.13 | 0.48±0.08# | 0.51±0.07 | 0.38±0.09# | |
| Dexamethasone | 2 | 0.73±0.05 | 0.22±0.03# | 0.59±0.12 | 0.21±0.03# | 0.52±0.12 | 0.26±0.05# |
| *P < 0.05 vs sham; #P < 0.05 vs model | |||||||
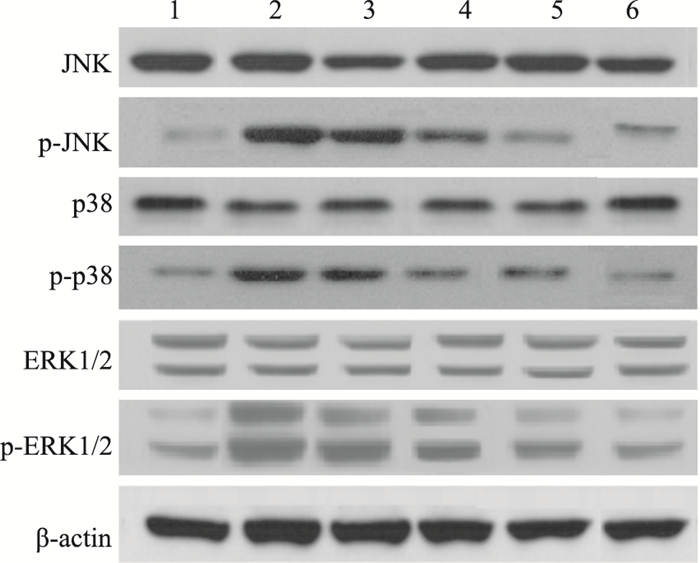
如Fig 3、Tab 5所示,与假手术组相比,模型组p-JNK、p-p38、p-ERK1/2蛋白表达升高(P<0.05)。与模型组相比,水飞蓟素低、中、高剂量组和阳性组p-JNK、p-p38、p-ERK1/2蛋白表达降低,具有剂量依赖性(P<0.05)。各组间JNK、p38、ERK1/2蛋白表达无明显变化,差异无统计学意义(P>0.05)。
|
| Fig 3 Protein expression of MAPK signaling pathway 1: Sham operation group; 2: Model group; 3: Silymarin low dose group; 4: Silymarin medium dose group; 5: Silymarin high dose group; 6: Dexamethasone group. |
如Fig 4、Tab 6所示,与假手术组相比,模型组p-p65、p-IκBα蛋白表达升高(P<0.05)。与模型组相比,水飞蓟素低、中、高剂量组和阳性组p-IκBα蛋白表达降低,具有剂量依赖性(P<0.05)。各组间p65、IκBα蛋白表达无明显变化(P>0.05)。

|
| Fig 4 Protein expression of NF-κB pathway 1: Sham operation group; 2: Model group; 3: Silymarin low dose group; 4: Silymarin medium dose group; 5: Silymarin high dose group; 6: Dexamethasone group. |
| Group | Dose/ mg·kg-1 |
p65 | p-p65 | IκBα | p-IκBα |
| Sham | - | 0.77±0.12 | 0.13±0.02 | 0.60±0.06 | 0.16±0.03 |
| Model | - | 0.79±0.16 | 1.04±0.15* | 0.62±0.09 | 0.92±0.08* |
| Silymarin | 50 | 0.72±0.14 | 0.97±0.08 | 0.64±0.18 | 0.75±0.09# |
| 100 | 0.76±0.11 | 1.24±0.08# | 0.63±0.12 | 0.64±0.11# | |
| 200 | 0.73±0.16 | 1.02±0.07 | 0.65±0.11 | 0.32±0.06# | |
| Dexamethasone | 2 | 0.72±0.18 | 0.83±0.12# | 0.61±0.12 | 0.18±0.04# |
| *P < 0.05 vs sham; #P < 0.05 vs model | |||||
SAP损伤后,病理学主要表现有小叶局部坏死,胰腺细胞中出现大量炎症细胞浸润,胰腺腺泡破坏等病理特征。本研究HE染色显示,模型组大鼠胰腺组织腺泡细胞出现大量坏死,结构模糊、融合成一片,小叶结构模糊,出现大量炎症细胞浸润,肺泡间间隔明显变宽,这与临床上水肿型胰腺炎病理特征相似[9],提示SAP模型大鼠制备成功。而给予水飞蓟素处理后,胰腺组织腺泡细胞破裂减少,随着处理剂量的增加,炎症浸润也明显减轻,以上均提示水飞蓟素可减轻SAP胰腺炎症。肺组织损伤具有典型病理特征,如肺泡结构变化、肺水肿及炎性浸润。本研究进一步对肺组织进行HE染色,结果显示模型组肺泡壁变厚、间隔变宽,肺间质出现充血,且伴随大量炎性细胞浸润,表明SAP可导致大鼠肺组织损伤,而给予水飞蓟素处理后,肺组织损伤程度明显减轻。研究证实,地塞米松对脂多糖诱导的急性肺损伤具有保护作用[10]。本研究以地塞米松作为阳性对照药物,结果显示,水飞蓟素高剂量组大鼠肺组织恢复程度与阳性组相似,提示水飞蓟素可缓解SAP所引发的肺损伤,与地塞米松处理结果相似。
肺泡巨噬细胞可产生大量TNF-α、IL-1β等促炎性细胞因子,引起炎症反应。动物研究发现,IL-1β抗体可减轻急性肺损伤动物模型中的肺损伤[11]。此外,研究发现,IL-1β、TNF-α等细胞因子表达的上调,能够进一步促进中性粒细胞浸润至损伤肺组织中,加重肺组织炎症反应,形成恶性循环[12]。以上表明,中性粒细胞浸润、炎性细胞因子是与肺炎症性损伤有关的关键因素。本研究发现,大鼠血清TNF-α、IL-1β、PMN明显升高,进一步证实SAP大鼠肺组织炎性损伤。水飞蓟素可通过降低机体炎症反应,缓解SAP大鼠肺损伤,与地塞米松处理结果相似,提示水飞蓟素可能通过减少血清中炎症细胞因子,抑制肺组织中性粒细胞浸润,从而减轻肺组织炎症反应,缓解肺组织损伤。
NF-κB/MAPK信号通路过度激活,在肺损伤的发生中发挥重要作用。NF-κB一般情况下被IκB抑制,以非活性状态存在细胞质中,在外界刺激下IκB发生磷酸化被激活后,NF-κB抑制作用被解除,磷酸化后进入细胞核内,促进靶基因的转录。本研究结果显示,模型组大鼠p-p65、p-IκBα蛋白表达升高,说明NF-κB通路被激活。国内学者在肺损伤动物研究中也发现,模型组大鼠NF-κB信号通路相关蛋白表达明显高于正常组大鼠,与本研究结果一致[13]。在给予水飞蓟素后,p-IκBα蛋白表达明显降低,与地塞米松处理结果相似,表明水飞蓟素可能通过抑制NF-κB信号通路活性,缓解肺部炎症损伤。
MAPK信号通路激活后,可促进机体内大量炎症因子的释放,进而加重炎症反应[14]。本研究结果显示,模型组p-JNK、p-p38、p-ERK1/2蛋白表达较假手术组明显升高,与以往报道相符[15],提示SAP大鼠可能通过激活MAPK信号通路,导致肺损伤。进一步研究显示,在给予水飞蓟素后,肺组织中p-JNK、p-p38、p-ERK1/2蛋白表达较模型组明显降低,与地塞米松处理结果相似,说明水飞蓟素可抑制SAP引发的MAPK信号通路激活,进而缓解肺部损伤,保护肺组织。
综上所述,水飞蓟素能够降低SAP大鼠肺部炎症反应,同时抑制NF-κB/MAPK信号通路活性,推测水飞蓟素改善SAP肺损伤可能与抑制NF-κB/MAPK信号通路有关。SAP肺损伤机制较复杂,本研究中水飞蓟素仅能部分缓解肺组织炎症反应,而非逆转SAP引发的大鼠肺损伤,可能与其他因素有关,还有待深入探究,以期为疾病的治疗提供更有力的实验依据。
| [1] |
曹均强, 汤礼军. 全身炎症反应综合征在急性胰腺炎肺损伤中的研究进展[J]. 中华消化外科杂志, 2015, 14(11): 975-9. Cao J Q, Tang L J. Research progress of systemic inflammatory response syndrome in acute pancreatitis-associated lung injury[J]. Chin J Digest Surg, 2015, 14(11): 975-9. doi:10.3760/cma.j.issn.1673-9752.2015.11.019 |
| [2] |
程石, 杨彬, 闫文貌, 等. 抗TNF-α治疗对重症急性胰腺炎肺损伤NF-κB信号通路的影响[J]. 中国普通外科杂志, 2008, 17(3): 219-23. Cheng S, Yang B, Yan W M, et al. The effect of anti-tumor necrosis factor α treatment on NF-κB signaling in lung injury in severe acute pancreatitis in rats[J]. Chin J Gen Surg, 2008, 17(3): 219-23. doi:10.3969/j.issn.1005-6947.2008.03.005 |
| [3] |
武丽娜, 余剑波, 刘大全, 等. p38MAPK信号通路在内毒素性休克诱发急性肺损伤大鼠肺组织HO-1表达上调中的作用[J]. 中华麻醉学杂志, 2012, 32(6): 727-31. Wu L N, Yu J B, Liu D Q, et al. Role of p38MAPK signaling pathway in up-regulation of heme oxygenase-1 expression in lung tissues in rats with acute lung injury induced by endotoxic shock[J]. Chin J Anesthesiol, 2012, 32(6): 727-31. doi:10.3760/cma.j.issn.0254-1416.2012.06.023 |
| [4] |
刘志刚, 李雪玲, 翁立冬, 等. 水飞蓟素药理作用研究进展[J]. 辽宁中医药大学学报, 2012, 14(10): 91-3. Liu Z G, Li X L, Weng L D, et al. Research progress on the pharmacological action of silymarin[J]. J Liaoning Univ Tradit Chin Med, 2012, 14(10): 91-3. |
| [5] |
张珂, 张琬啉, 李洪图. 水飞蓟素对大鼠肺缺血/再灌注损伤的保护作用[J]. 中华实验外科杂志, 2016, 33(8): 1935-7. Zhang K, Zhang W L, Li H T. Protective effect of silymarin on lung ischemia-reperfusion injury[J]. Chin J Exp Surg, 2016, 33(8): 1935-7. doi:10.3760/cma.j.issn.1001-9030.2016.08.015 |
| [6] |
李涛, 刘源, 李冉, 等. 氯膦酸二钠脂质体对大鼠重症急性胰腺炎肺损伤的影响及与Akt、MAPK(ERK1/2)通路的关系[J]. 中国普通外科杂志, 2016, 25(3): 350-6. Li T, Liu Y, Li R, et al. Alleviative effect of liposomal clodronate against lung injury in rats with severe acute pancreatitis and its relations with Akt and MAPK (ERK1/2) pathways[J]. Chin J Gen Surg, 2016, 25(3): 350-6. |
| [7] |
Kaplan M, Yazgan Y, Tanoglu A, et al. Effectiveness of interleukin-1 receptor antagonist (Anakinra) on cerulein-induced experimental acute pancreatitis in rats[J]. Scand J Gastroenterol, 2014, 49(9): 1124-30. doi:10.3109/00365521.2014.926983 |
| [8] |
Bukowczan J, Warzecha Z, Ceranowicz P, et al. Pretreatment with obestatin reduces the severity of ischemia/reperfusion-induced acute pancreatitis in rats.[J]. Eur J Pharmacol, 2015, 760(5): 113-21. |
| [9] |
郭婉薇, 王伟福, 陈晓武, 等. 重症急性胰腺炎大鼠肝内胆管组织病理学变化及胆管细胞凋亡情况[J]. 广东医学, 2016, 37(23): 3502-6. Guo W W, Wang W F, Chen X W, et al. Pathological changes of intrahepatic bile duct tissue and apoptosis of bile duct cells in rats with severe acute pancreatitis[J]. Guangdong Med J, 2016, 37(23): 3502-6. doi:10.3969/j.issn.1001-9448.2016.23.006 |
| [10] |
雷传江, 焦艳, 王关嵩, 等. 受体相互作用蛋白140在脓毒症急性肺损伤大鼠肺泡巨噬细胞中的表达及其作用[J]. 第三军医大学学报, 2015, 37(9): 851-7. Lei C J, Jiao Y, Wang G S, et al. Expression and function of RIP140 in alveolar macrophages of rats with septic acute lung injury[J]. J Third Mil Med Univ, 2015, 37(9): 851-7. |
| [11] |
Takahara M, Aoyama-Ishikawa M, Shuno K, et al. Role of endogenous IL-18 in the lung during endotoxin-induced systemic inflammation[J]. Acute Med Surg, 2014, 1(1): 23-30. |
| [12] |
Yang C M, Luo S F, Hsieh H L, et al. Interleukin-1beta induces ICAM-1 expression enhancing leukocyte adhesion in human rheumatoid arthritis synovial fibroblasts: involvement of ERK, JNK, AP-1, and NF-kappaB[J]. J Cell Physiol, 2010, 224(2): 516-26. doi:10.1002/jcp.22153 |
| [13] |
肖雪飞, 杨明施, 孙圣华. 姜黄素对脓毒症急性肺损伤的炎症反应及NF-κB信号通路的影响[J]. 中国现代医学杂志, 2013, 23(30): 19-22. Xiao X F, Yang M S, Sun S H, et al. Effect of curcumin on inflammation and NF-κB signaling pathway in septic acute lung injury rats[J]. Chin J Mod Med, 2013, 23(30): 19-22. doi:10.3969/j.issn.1005-8982.2013.30.005 |
| [14] |
唐春林, 丁宁, 程傲冰. EGFR-p38 MAPK信号通路参与机械通气肺损伤大鼠肺组织HMGB1的表达[J]. 中国病理生理杂志, 2013, 29(6): 1029-33. Tang C L, Ding N, Cheng A B. EGFR-p38 MAPK signaling pathway is involved in expression of HMGB1 in pulmonary tissues of rats with ventilator-induced lung injury[J]. Chin J Pathophysiol, 2013, 29(6): 1029-33. doi:10.3969/j.issn.1000-4718.2013.06.013 |
| [15] |
张利鹏, 赵焱, 刘国娟, 等. 乌司他丁通过干预p38MAPK/ERK信号通路减轻脓毒症性肺损伤[J]. 中国药理学通报, 2016, 32(9): 1311-6. Zhang L P, Zhao Y, Liu G J, et al. Ulinastatin attenuates lipopolysaccharide-induced acute lung injury by intervening p38 MAPK/ERK signaling pathway[J]. Chin Pharmacol Bull, 2016, 32(9): 1311-6. doi:10.3969/j.issn.1001-1978.2016.09.024 |

