

2. 兰州军区兰州 总医院全军高原环境损伤防治重点实验室,甘肃 兰州 730050
2. Key Lab of the Plateau of Environmental Damage Control, Lanzhou General Hospital of Lanzhou Military Command, Lanzhou 730050, China
肠道菌群是居住在人体内的最主要和最多样的微生物群落[1],包括数百种微生物种类,其计数约为体细胞数量的10倍。肠道菌群的研究主要集中在糖尿病、肥胖等慢性代谢性疾病,以及克罗恩病(Crohn’s disease, CD)、溃疡性结肠炎(ulcerative colitis, UC)等炎症性肠病方面[2]。自20世纪中叶以来,肠道微生物群对药物代谢的影响受到关注,随着肠道微生物群的各种代谢能力被发现,其在药物代谢中的作用也逐渐得到了深入研究。肠道菌群对药物代谢的影响与药物的药效及毒理作用密切相关,从而影响临床上的合理用药。已有研究表明[3-4],急进高原后,药物的药代动力学参数会发生变化,其变化的原因主要集中在代谢酶和转运体方面。基于急进高原环境肠道菌群的改变及肠道菌群对药物代谢的研究,肠道菌群可能是急进高原后药物代谢动力学参数变化的又一影响因素。本文通过综述肠道菌群的分类、功能及其在药物代谢中的作用,明确药物的体内转化过程,一方面利于指导临床合理用药、毒理学风险评估、引导个体化用药及推动药物发现和研发;另一方面,为本课题组今后进一步研究高原环境下肠道菌群对药物代谢的影响提供指导及理论基础。
1 肠道菌群分类人体肠道中栖息着远远超过人体自身细胞数量的微生物,这些微生物被统称为肠道菌群。肠道菌群由大约400~500种不同的细菌组成,其中30~40种占肠道菌群的99%[5]。人体肠道内已鉴定出的细菌共9个门[6],即厚壁菌门(Firmicutes)、拟杆菌门(Bacteroidetes)、变形菌门(Proteobacteria)、放线菌门(Actinobacteria)、梭杆菌门(Fusobacteria)、疣微球菌门(Verrucomicrobia)、蓝细菌门(Cyanobacteria)、螺旋体门(Spirochaeates)、VadinBE97菌门。肠道内98%以上的细菌属于优势菌门,如厚壁菌门和拟杆菌门,而变形菌门、放线菌门、梭杆菌门和疣微球菌门数量及种类较为弱势[6]。此外,根据肠道菌群与宿主的不同关系,肠道菌群可分为以下3类:有益菌、中性菌、有害菌[7],见Tab 1。
| Intestinal flora | Example | Function |
| Beneficial bacteria | Bifidobacteria, Eubacteriu, Lactobacillus | Nutrition, defensing, anti-aging, promoting growth and inhibiting tumor, participating in body metabolism, and regulating intestinal immunity[7] |
| Neutral bacteria | Enterococcus, Enterobacteriaceae | Neutral bacterial imbalance can induce a variety of gastrointestinal diseases, such as inflammatory bowel disease |
| Pathogenic bacteria | Proteusbacillus vulgaris, Pseudomonadaceae, Staphylococcus aureus | Invading the host and causing infection |
正常条件下,肠道菌群相对稳定,但其组成和功能受一系列因素的影响,如饮食、益生菌、药物及环境的变化等都是影响其变化的因素[1, 8]。有研究报道,高脂饮食使得小鼠肠道中拟杆菌门的流行率增加,厚壁菌门及放线菌门的流行率降低[9]。此外,急进高原后肠道菌群失衡,如双歧杆菌数量减少,而大肠埃希菌的数量增加[10]。肠道菌群的失调不仅会使得其结构发生改变,同时也会影响其功能。
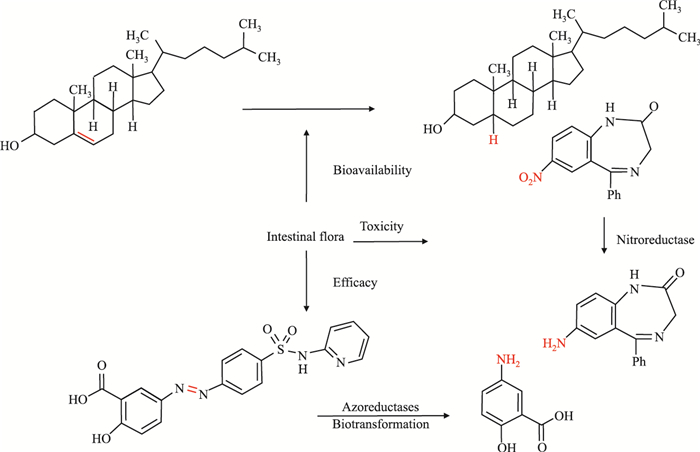
2 肠道菌群的功能人体肠道微生物组是人体庞大而复杂的微生物群落,是人体重要的代谢“器官”。肠道微生物在促进营养物质吸收、肠道黏膜屏障的保护、上皮细胞的生长发育、促进肠道淋巴组织(gut-associated lymphatic tissue, GALT)的形成、免疫应答、肠道pH的调节、生物拮抗、药物的代谢和毒性等方面起重要作用,且与多种疾病的发生、发展密切相关[2, 5, 10],其中,肠道菌群对药物代谢的影响是本文阐述的重点。肝脏是药物代谢的主要部位,但是,口服药物在经胃肠道吸收进入血液之前,被肠黏液、肠黏膜及肠道微生物所富含的酶代谢[9, 11]。因此,肠道菌群在药物代谢及口服生物利用度等方面起主要作用[11-13]。如Fig 1所示,肠道菌群可以产生一些酶,如硝基还原酶、偶氮还原酶等,这些酶在药物的生物转化中发挥重要的作用,影响药物的毒性、有效性、生物利用度等。
|
| Fig 1 Effects of intestinal flora on drug metabolism |
药代动力学是研究药物在生物体内吸收、分布、生物转化和排泄过程的特点和规律的一门学科,即药物分子被机体吸收后,在机体作用下发生的化学结构转化。药物代谢的变化会引起药效和毒性的改变,前期研究药物代谢的影响因素主要集中在代谢酶与转运体方面[3-4],20世纪中叶开始,肠道菌群在药物代谢方面的作用逐渐被各国研究者所关注,并进行了大量研究。
3.1 对中药成分代谢的影响肠道菌群对中药成分的生物转化以水解作用为主,氧化还原作用为辅,所涉及的代谢酶主要包括水解酶、氧化还原酶、裂解酶和转移酶[14]。在这些酶的作用下,中药成分转化成相应的药理或毒理成分而发挥作用。近年来,肠道菌群对中药不同类别成分代谢的研究包括黄酮类、皂苷类、生物碱类、蒽醌类、单萜类、甾体类、木脂素类化合物等。
3.1.1 黄酮类化合物李芳等[15]采用离体粪便温孵法,观察和比较人、正常大鼠、伪无菌大鼠肠道菌群对白花蛇舌草黄酮提取物的代谢作用。结果发现,白花蛇舌草提取物中各组分及其单体容易被肠道菌群快速(人/正常大鼠)代谢,主要代谢为槲皮素;在伪无菌大鼠肠菌孵育液中几乎没有代谢;肠道菌群对提取物中各组分代谢作用弱于相应单体。该结果证实,肠道菌群在黄酮类成分代谢中发挥着重要的作用。
3.1.2 皂苷类化合物皂苷类化合物大都可以被肠道菌群水解代谢。高霞等[16]将三七皂苷R1、人参皂苷Rg1、人参皂苷Rg2、人参皂苷Re、人参皂苷Rd及人参皂苷Rb1与离体大鼠肠道菌群在厌氧条件下孵育8、24 h,通过乙腈沉淀蛋白和乙酸乙酯萃取处理后,采用LC-Q-TOF-MS/MS对代谢产物进行定性分析。结果发现,这6种皂苷在肠道菌群的作用下,分别产生不同数量的代谢产物,这表明肠道菌群对这6种皂苷具有明显的代谢转化作用。
3.1.3 生物碱类化合物双酯二萜类生物碱(diester diterpenoid alkaloids, DDAs)具有抗炎、镇痛、强心等作用,如乌头碱(aconitine, AC)、新乌头碱(mesaconitine, MA)、海帕乌头碱(hypaconitine, HA)等。通过体外粪便悬浮液厌氧温育实验,发现DDAs在肠道细菌的作用下可以发生羟基化、脱氧、去甲基化、去氧化脱甲基、酯水解(C-8、C-14位)及C-8位与长短链脂肪酸的酯交换等过程,完成生物转化[17]。
3.1.4 蒽醌类化合物中药大黄中含有蒽醌苷类化合物,宋瑞等[18]在比较生大黄、酒大黄、熟大黄、炭大黄4种大黄饮片水提液在大鼠肠道菌群中代谢转化情况的研究中发现,蒽醌类化合物如大黄酚葡萄糖苷、大黄素葡萄糖苷及芦荟大黄素葡萄糖苷,在肠道菌群的作用下可以被转化,生成相应的大黄酚、大黄素及芦荟大黄素,这些物质可以被肠道菌群进一步转化为其他物质。糖苷键水解、醌式结构被还原和(或)乙酰氧基取代等,是肠道菌群作用下蒽醌苷类化合物的主要代谢途径。
3.1.5 单萜类化合物龙胆苦苷是环烯醚萜类化合物,为常用中药龙胆的主要有效成分,有保肝、利胆、抗炎等作用。杨肖锋等[19]通过HPLC法测定龙胆苦苷肠内菌培养液和大鼠灌服龙胆苦苷后血清中的龙胆苦苷及其代谢产物龙胆碱和龙胆醛的含量,对比培养液与血清中药物成分的变化,发现龙胆苦苷最终被肠道菌群代谢为其活性代谢产物龙胆醛。
3.1.6 木脂素类化合物木脂素在肠道菌群的作用下,通过糖苷键的水解、脱甲基、脱羟基、不对称加氢、环合等过程,被转化成具有生物活性的肠内脂(enterolactone, ENL)、肠二醇(enterodiol, END)。膳食中摄入的木脂素对人体健康产生一系列积极作用,如抗氧化、抗增殖、雌激素样性质,以及预防乳腺癌、前列腺癌、心血管疾病、糖尿病等。亚麻木脂素(secoisolariciresinol diglucoside, SDG)是西方饮食中最常见的木脂素之一。Quartieri等[20]通过SDG体外粪便孵育实验及给予志愿者亚麻籽补充剂,观察SDG粪便孵育液、志愿者粪便及尿液中的SDG代谢物,结果发现在所有培养液中,SDG去糖基化生成开环异松木醇(secoisolariciresinol, SECO),SECO进一步发生脱羟基、去甲基化,生成END和ENL,这说明了肠道菌群在SDG的生物转化中起重要作用。
3.1.7 甾类化合物甾体皂苷是由螺甾烷类化合物衍生的寡糖苷,是一类具有改善心血管活性、抗癌、抗痴呆、抗病原微生物、降血糖等作用的重要中药活性成分,存在于多种中药如知母中。张钰哲[21]通过体外大鼠肠道菌群药物温育及灌胃给予大鼠甾体皂苷样品实验,采用LC/MS/MS法检测离体肠内菌对甾体皂苷样品的代谢产物,以及给药后不同时间尿样及粪样中甾体皂苷样品的代谢产物。结果表明,甾体皂苷样品容易被大鼠消化道菌群代谢,其主要代谢产物为代谢物M1,且随着代谢时间的延长,代谢物M1的量逐渐增多,而甾体皂苷样品的量则下降迅速。
目前,研究肠道菌群对中药成分的代谢主要采用体外粪便处理液与药物温孵的方法,该方法简单快捷,其缺点在于不能客观地反映药物在肠道内的动态变化及药物在肠道内的时间依赖性代谢,且粪便容易受到外界环境的污染。此外,由于肠道菌群的复杂性及少数细菌不可培养性,肠道菌群影响中药成分代谢的机制、参与其生物转化的细菌种类及所产生的酶尚不清楚,且高原环境下肠道菌群在中药成分代谢中的影响尚未见报道。
3.2 对化学药物代谢的影响肠道菌群对化学药物的代谢一方面以其代谢产物,如丁酸、胆汁酸为介导,这些产物可以作为核受体的配体,间接影响药物代谢[22]。另一方面,肠黏膜及肠腔中的CYP450酶、Ⅱ相代谢酶及肠微生物酶、细菌膜转运蛋白等,都会对药物代谢产生影响[8]。治疗肠应激综合征的柳氮磺胺吡啶(sulfasalazine, SSZ),其分子中含有通过偶氮键连接在一起的5-氨基水杨酸(5-aminosalicylic acid, 5-ASA)和磺胺吡啶(sulfapyridine, SP),SSZ的效力依赖于肠道菌群所产生的偶氮还原酶,肠道菌群通过破坏偶氮键,将SSZ转化为两种主要的代谢产物5-ASA和SP,其中5-ASA是治疗肠应激综合征的活性成分[11]。Yoo等[23]将人和大鼠的粪便经厌氧稀释液处理后,与洛伐他汀药物厌氧孵育5 d,从孵育液中分离得到去甲基丁酰基代谢物、羟基化代谢物、活性羟基酸代谢物及羟化的羟基酸代谢物4种代谢产物,该结果说明了肠道菌群参与了洛伐他汀的代谢过程。此外,从药物的肝微粒体酶孵育液中分离得到洛伐他汀的羟基化代谢物和羟基酸代谢物,该结果说明药物的肠道菌群代谢和肝代谢存在重叠,肠道菌群可以被视为与肝相当的具有代谢潜能的器官。Kim等[24]在研究抗生素对阿司匹林药理作用的影响时,通过分析大鼠粪便样品的焦磷酸测序和选择性培养基培养的实验结果,发现氨苄青霉素处理会导致肠道微生物的数量和组成变化。这些结果表明,抗生素可以通过抑制肠道微生物群的代谢活性来调节阿司匹林的药代动力学,从而增强阿司匹林的疗效。
3.3 高原环境下肠道菌群对药物代谢的影响目前,研究肠道菌群对化学药物代谢的影响,都是在低海拔地区下给予抗生素干扰后,对其进行研究探讨,但是高原环境下肠道菌群对药物代谢的影响尚未见报道。
高原环境具有低氧、低气压、强紫外线、寒冷、干燥等基本特点,其中低氧是影响人类生命活动的主要因素。文仁国等[25]采用核磁共振波谱仪(1H-NMR)检测同龄紫绀型先天性心脏病婴幼儿和健康儿童尿液马尿酸的含量,探讨长期缺氧对紫绀先天性心脏病婴幼儿肠道菌群代谢的影响。结果发现,与对照组相比,缺氧组的马尿酸含量降低,这表明长期缺氧会影响婴幼儿肠道菌群的代谢。此外,杨文翠[10]报道,急进高原大鼠的肠道菌群会失衡,他们通过比较不同海拔(500 m、3 848 m、4 767 m)肠道菌群的失衡率,发现与对照组相比,海拔3 848 m组和海拔4 767 m组肠道菌群失衡率分别为53%和86%,并通过肠道细菌培养实验发现,与对照组相比,高海拔组大鼠肠道中的双歧杆菌数量减少,而大肠埃希菌的数量增多。如果肠道微生态系统的动态平衡被打破,肠道菌群就会失调,对药物的代谢产生影响,进而影响药理活性。
课题组前期研究表明,急进高原后多种药物的代谢及其药代动力学参数会发生变化,且有文献报道,急进高原后肠道菌群会失调[10],那么高原环境所导致的肠道菌群紊乱是否为引起药物代谢变化的关键因素,这是一个值得我们深入研究的问题。课题组前期通过16S rRNA方法,测定高原环境下肠道菌群的变化情况,并探究其对化学药物硝苯地平代谢的影响,结果表明,高原环境所引起的肠道菌群失调会引起硝苯地平代谢的改变,为后期研究高原环境下药物代谢动力学参数变化提供了新的研究思路,也为指导急进高原人群合理用药提供了理论依据。
4 总结与展望肠内菌群与药物代谢相关性的研究,已成为受国际关注的重要研究课题。口服药物进入胃肠道,可能与肠道菌群发生相互作用,对药物在体内的生物转化具有非常重要的影响。目前,研究肠道菌群对药物代谢的影响多在低海拔地区进行,而高原环境下肠道菌群对药物代谢的影响鲜有文献报道。研究肠道菌群对药物代谢的影响,有利于了解药物在体内的整个代谢过程,并利于阐明药效产生的基础。因此,研究高原环境下肠道菌群对药物代谢的影响是一个亟待解决的问题。肠道菌群作为人体“隐形器官”,影响药物的药效、毒性及生物利用度,这表明肠道菌群在药物代谢方面发挥着重要作用。通过综述国内外文献,课题组发现肠道微生物对药物代谢的影响是研究高原低氧环境下药物代谢变化机制的一个突破点,这有助于我们更进一步了解体内药物代谢变化的过程,从而更好地指导急进高原及高原人群的合理用药。
| [1] |
Human Microbiome Project Consortium. Structure, function and diversity of the healthy human microbiome[J]. Nature, 2012, 486(7402): 207-14. doi:10.1038/nature11234 |
| [2] |
Mai V, Draganov P V. Recent advances and remaining gaps in our knowledge of associations between gut microbiota and human health[J]. World J Gastroenterol, 2009, 15(1): 81-5. doi:10.3748/wjg.15.81 |
| [3] |
Wang R, Sun Y, Yin Q, et al. The effects of metronidazole on cytochrome P450 activity and expression in rats after acute exposure to high altitude of 4300m[J]. Biomed Pharmacother, 2016, 85: 296-302. |
| [4] |
张明霞, 王荣, 李文斌, 等. 高原缺氧对药物转运体影响的研究进展[J]. 中国药理学通报, 2018, 34(3): 316-21. Zhang M X, Wang R, Li W B, et al. Advances of studies on effect of drugtran sporter under hypoxia[J]. Chin Pharmacol Bull, 2018, 34(3): 316-21. doi:10.3969/j.issn.1001-1978.2018.03.005 |
| [5] |
Pai R, Kang G. Microbes in the gut: a digestable account of host-symbiont interactions[J]. Indian J Med Res, 2008, 128(5): 587-94. |
| [6] |
Eckburg P B, Bik E M, Bernstein C N, et al. Diversity of the human intestinal microbial flora[J]. Science, 2005, 308(5728): 1635-8. doi:10.1126/science.1110591 |
| [7] |
周正华. 肠道微环境与溃疡性结肠炎[J]. 世界华人消化杂志, 2016, 24(11): 1695-700. Zhou Z H. Intestinal micro-ecology and ulcerative colitis[J]. World Chin J Digestol, 2016, 24(11): 1695-700. |
| [8] |
Stojančević M, Bojić G, Salami H A, et al. The influence of intestinal tract and probiotics on the fate of orally administered drugs[J]. Curr Issues Mol Biol, 2014, 16(2): 55-68. |
| [9] |
Bagarolli R A, Tobar N, Oliveira A G, et al. Probiotics modulate gut microbiota and improve insulin sensitivity in DIO mice[J]. J Nutr Biochem, 2017, 50: 16-25. doi:10.1016/j.jnutbio.2017.08.006 |
| [10] |
杨文翠.谷氨酰胺对急进高原缺氧大鼠肠道微生态影响的实验研究[D].兰州: 兰州大学, 2010. Yang W C. Effect of glutamine on change of intestinal microecology in rats exposed to acute plateau hypoxia[D]. Lanzhou: Lanzhou University, 2010. http://www.cnki.com.cn/Article/CJFDTotal-GYYZ201001017.htm |
| [11] |
Haiser H J, Turnbaugh P J. Developing a metagenomic view of xenobiotic metabolism[J]. Pharmacol Res, 2013, 69(1): 21-31. |
| [12] |
Lee H J, Zhang H, Orlovich D A, et al. The influence of probiotic treatment on sulfasalazine metabolism in rat[J]. Xenobiotica, 2012, 42(8): 791-7. doi:10.3109/00498254.2012.660508 |
| [13] |
Takeno S, Sakai T. Involvement of the intestinal microflora in nitrazepam-induced teratogenicity in rats and its relationship to nitroreduction[J]. Teratology, 1991, 44(2): 209-14. |
| [14] |
祖先鹏, 林璋, 谢海 胜., 等. 中药有效成分与肠道菌群相互作用的研究进展[J]. 中国中药杂志, 2016, 41(10): 1766-72. Zu X P, Lin Z, Xie H S, et al. Interaction of effective ingredients from traditional Chinese medicines with intestinal microbiota[J]. Chin J Chin Mater Med, 2016, 41(10): 1766-72. |
| [15] |
李芳, 杨培民, 曹广尚, 等. 体外培养肠道菌群对白花蛇舌草黄酮提取物的代谢研究[J]. 医药导报, 2016, 35(8): 809-13. Li F, Yang P M, Cao G S, et al. Study on the metabolism of Hedyotis Diffusa flavonoid extract by intestinal bacteria in vitro[J]. Her Med, 2016, 35(8): 809-13. doi:10.3870/j.issn.1004-0781.2016.08.002 |
| [16] |
高霞, 耿婷, 马阳, 等. 离体大鼠肠道菌对6种皂苷类成分代谢研究[J]. 中国中药杂志, 2016, 41(12): 2329-38. Gao X, Gen T, Ma Y, et al. Metabolism of six saponins by rat intestinal bacteria in vitro[J]. Chin J Chin Mater Med, 2016, 41(12): 2329-38. |
| [17] |
Zhang M, Peng C S, Li X B. In vivo and in vitro metabolites from the main diester and monoester diterpenoid alkaloids in a traditional Chinese herb, the aconitum species[J]. Evid Based Complement Alternat Med, 2015, 2015(20): 252434. |
| [18] |
宋瑞, 田媛, 张尊建. 大黄4种饮片水提液体外肠道菌群转化比较研究[J]. 中国中药杂志, 2012, 37(12): 1755-60. Song R, Tian Y, Zhang Z J. Comparison of transformation of four processed rhubarb aqueous extracts in intestinal bacteria in vitro[J]. Chin J Chin Mater Med, 2012, 37(12): 1755-60. |
| [19] |
杨肖锋, 宋纯清. 龙胆苦苷的肠内菌群代谢研究[J]. 中国中药杂志, 2000, 25(11): 673-6. Yang X F, Song C Q. Studies on the metabolism of gentiopcroside by rat intestinal flora[J]. Chin J Chin Mater Med, 2000, 25(11): 673-6. doi:10.3321/j.issn:1001-5302.2000.11.011 |
| [20] |
Quartieri A, García-Villalba R, Amaretti A, et al. Detection of novel metabolites of flaxseed lignans in vitro and in vivo[J]. Mol Nutr Food Res, 2016, 60(7): 1590-601. doi:10.1002/mnfr.v60.7 |
| [21] |
张钰哲. 离体大鼠肠内菌群对知母甾体皂苷代谢研究[J]. 大理学院学报(综合版), 2012, 11(3): 5-8. Zhang Y Z. In vitro study of rat Coliform bacteria metabolism of steroidal sponin extract from Anemarrhena asphodeloides[J]. J Dali Univ, 2012, 11(3): 5-8. |
| [22] |
Swanson H I. Drug metabolism by the host and gut microbiota: a partnership or rivalry[J]. Drug Metab Dispos, 2015, 43(10): 1499-504. doi:10.1124/dmd.115.065714 |
| [23] |
Yoo D H, Kim I S, Van Le T K, et al. Gut microbiota-mediated drug interactions between lovastatin and antibiotics[J]. Drug Metab Dispos, 2014, 42(9): 1508-13. doi:10.1124/dmd.114.058354 |
| [24] |
Kim I S, Yoo D H, Jung I H, et al. Reduced metabolic activity of gut microbiota by antibiotics can potentiate the antithrombotic effect of aspirin[J]. Biochem Pharmacol, 2016, 122(15): 72-9. |
| [25] |
文仁国, 孙国林, 彭晓波, 等. 长期缺氧对婴幼儿肠道菌群代谢的影响[J]. 局解手术学杂志, 2014, 23(2): 121-2. Wen R G, Sun G L, Peng X B, et al. Chronic hypoxia in altering metabolism of intestinal flora of infants[J]. J Reg Anat Oper Surg, 2014, 23(2): 121-2. |

