

2. 贵州医科大学基础医学院 组织工程与干细胞实验中心, 贵州 贵阳 550025
2. Res Center of Tissue Engineering and Stem Cell, School of Basic Medical Science, Guizhou Medical University, Guiyang 550025, China
内皮祖细胞(endothelial progenitor cells, EPCs)是一类可替代修复损伤血管内皮, 促进血管网络重建的内皮细胞前体细胞, 利用体外扩增的EPCs治疗缺血性心血管疾病具有较好的应用前景[1-2]。然而, EPCs在体外传代培养中常因老化而难以维持增殖, 如何干预EPCs的衰老, 提高EPCs的数量和质量, 是临床治疗缺血性心血管疾病急需解决的一个难点。前期研究表明, 黄精可通过提高端粒酶活性来保护衰老大鼠骨髓EPCs的功能[3], 在此基础上, 本文将进一步探讨黄精在老年大鼠骨髓EPCs体外传代培养衰老进程中, 对细胞功能及活性氧(reactive oxygen species, ROS)水平的影响。
1 材料与方法 1.1 材料 1.1.1 实验动物健康SPF级20月龄SD大鼠20只, 体质量(520~580) g; 3月龄SD大鼠40只, 体质量(220~260) g, ♀♂各半。全部动物由北京维通利华实验动物技术有限公司提供, 合格证号:11400700111130。动物饲养环境:温度(22~25) ℃, 湿度50%~60%, 光照12 h, 采用标准鼠饲料和灭菌饮用水喂养。本动物实验方案获得贵州医科大学动物伦理委员会批准。
1.1.2 药物与试剂黄精(批号:20150525)购自贵州百灵药业; M199培养液(批号:NAA1326)购自Hyclone公司; 胎牛血清(批号:A15112-0279)购自PAA公司; 大鼠淋巴细胞分离液(批号:TBD 2013LR)购自天津灏洋生物科技有限公司; 血管内皮生长因子(vascular endothelial growth factor, VEGF, 批号:011210)、碱性成纤维细胞生长因子(basic fibroblast growth factor, bFGF, 批号:081308)购自PeproTech公司; Dil标记的乙酰化低密度脂蛋白(Dil labeled acetyl low density lipoprotein, Dil-ac-LDL, 批号:YB-0013)购自广州奕源生物科技有限公司; FITC标记的荆豆凝集素1(FITC-labeled Ulex europarus agglutinin-1, FITC-UEA-1, 批号:055M4077V)购自Sigma公司; β-半乳糖苷酶染色试剂盒购自Biovision公司; 体外成血管试剂盒购自Millipore公司; ROS检测试剂盒购自碧云天公司。
1.1.3 仪器TS100倒置显微镜(日本Nikon公司); IX71荧光显微镜(日本Olympus公司); 流式细胞仪(美国BD公司); 多功能酶标仪(美国Thermo Fisher公司); CO2培养箱(美国Thermo Forma公司)。
1.2 方法 1.2.1 黄精含药血清的制备黄精产自贵州, 经贵阳市药检所鉴定为道地药材, 按《中国药典》(2005)制备黄精水煎液, 水浴浓缩备用。将3月龄SD大鼠随机分为对照组、黄精高、中、低剂量组, 每组10只。灌胃药量按人与动物体表面积换算, 即低剂量组为临床等效剂量2 g·kg-1, 中剂量为5倍临床等效剂量即10 g·kg-1, 高剂量为10倍临床等效剂量即20 g·kg-1, 对照组灌服生理盐水。每天灌胃2次, 连续3 d, d 4早上1次性灌服全天剂量后采血, 离心取上清, 过滤除菌。
1.2.2 大鼠骨髓EPCs的培养鉴定及细胞分组将20月龄健康SD大鼠麻醉处死后, 无菌取出双侧胫骨、股骨, 采用密度梯度离心法分离骨髓单个核细胞, PBS洗涤2次, 用M199全培养基(含体积分数为0.2的胎牛血清, 10 mg·L-1的VEGF和bFGF)重悬后, 接种于24孔板中, 每隔3 d换液1次, 收集培养第2代的细胞, 与Dil-ac-LDL和FITC-UEA-1共同孵育, 采用双染色法鉴定EPCs。将培养第2代的细胞同步化24 h后, 随机分为4组:对照组加入空白血清, 黄精各剂量组加入黄精高、中、低剂量含药血清, 使各组血清的体积分数为0.1, 每隔3 d换液1次, 继续培养至第4、6、8代, 分别检测以下指标。
1.2.3 细胞衰老程度检测按β-半乳糖苷酶染色试剂盒操作说明, PBS洗涤细胞1次, 加入1 mL固定液, 室温固定15 min; PBS洗涤细胞3次, 每次3 min, 加入1 mL预热的染色工作液, 37 ℃无CO2条件下孵育, 直到细胞呈现蓝色, 用封口膜封住孔板防止液体蒸发, 除去染色工作液, 加入2 mL PBS缓冲液洗涤, 荧光显微镜下随机选取5个视野(×200), 每个视野至少100个细胞, 胞质染色者为衰老细胞, 计算衰老细胞占观察细胞总数的百分比。
1.2.4 细胞增殖功能检测将等量EPCs接种在96孔培养板中, 贴壁24 h后, 每孔加5 g·L-1的MTT 15 μL, 继续培养4 h, 吸弃上清液, 再加入DMSO, 于微量震荡器充分震荡10 min后, 置酶标仪, 于波长570 nm处测吸光值。
1.2.5 细胞迁移功能检测消化收集贴壁细胞, 将等量EPCs加入Transwell小室的上室, 下室加入含50 mg·L-1 VEGF的M199培养液, 培养24 h, 擦去上室中的细胞, 多聚甲醛固定, 吉姆萨染色, 镜下随机选取5个视野(×200), 计数迁移至下层的细胞, 取其平均数。
1.2.6 细胞成血管功能检测[4]EPCs成血管功能与增殖、黏附及迁移功能密切相关, 按体外血管生成试剂盒操作说明, 将ECMatfixTM胶液和ECM 10×稀释液置于4 ℃冰箱过夜冻融, 每900 μL ECMatfixTM胶液加入ECM 10×稀释液100 μL, 将混匀液加入96孔板, 每孔50 μL, 孵育1 h凝固成胶; 将各处理组细胞以5×103个/孔接种于胶上; 37 ℃培养24 h后, 镜下随机选取5个视野(×200), 计数长度为宽度的4倍以上的细胞, 取其平均数。
1.2.7 细胞ROS水平的检测按ROS检测试剂盒操作说明, 胰酶消化收集各组细胞, 计数后, 每管加入1 :1 000用无血清培养液稀释的2′, 7′-二氯荧光黄双乙酸盐(DCFH), 使每管终体积为100 μL, 37 ℃孵育20 min, PBS洗涤2次, 上流式细胞仪检测。
1.2.8 统计学分析数据用x±s表示, 采用SPSS 18.0统计软件分析, 方差齐性条件下, 采用单因素方差分析, 两两比较采用LSD检验。
2 结果 2.1 大鼠EPCs的分离培养及鉴定刚分离的大鼠骨髓单个核细胞呈圆形, 传代培养至第2代时细胞呈典型的铺路石样, 贴壁细胞经FITC-UEA-1和Dil-ac-LDL处理后, 荧光显微镜下同时结合FITC-UEA-1和摄取Dil-ac-LDL的细胞为正在分化的EPCs(Fig 1)。

|
| Fig 1 Identification of EPCs(×200) A:Adherent cells with Dil-ac-LDL are red; B:Cells binding FITC-UEA-1 are green; C:Double positive cells are differentiating EPCs |
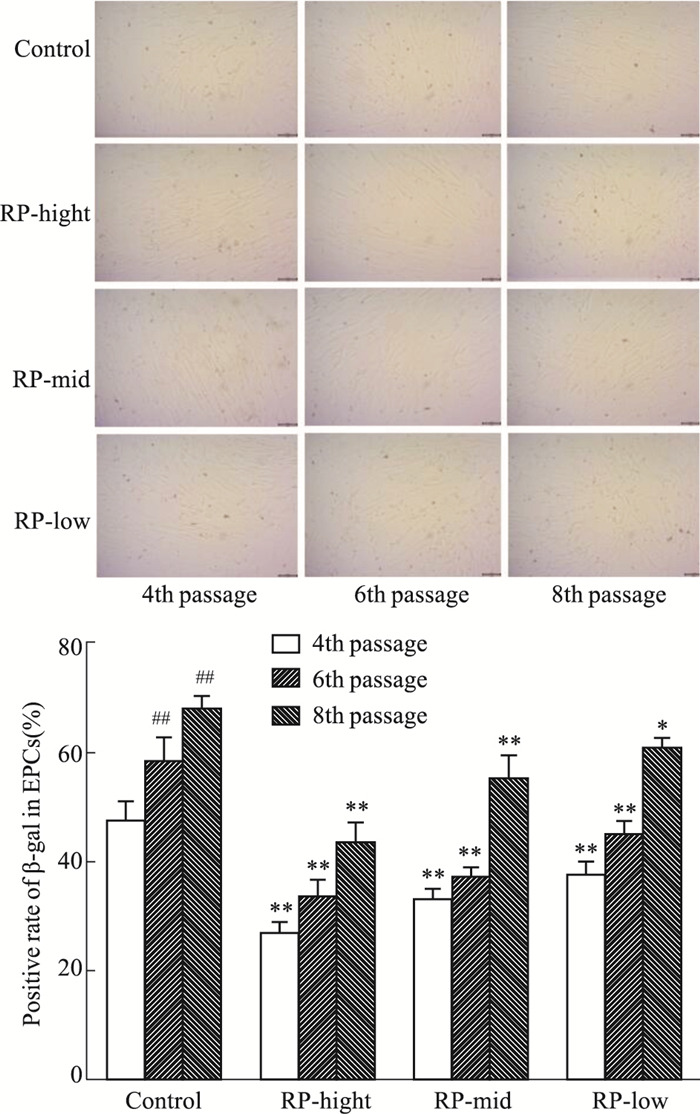
β-半乳糖苷酶染色阳性细胞即为衰老细胞, Fig 2结果显示, 随细胞传代次数增多, 细胞染色阳性率明显上升(P < 0.01), 经黄精各剂量干预后, 细胞在传代培养中染色阳性率明显下降(P < 0.05)。
|
| Fig 2 Effect of RP on positive rate of β-gal in EPCs(x±s, n=3) *P < 0.05, **P < 0.01 vs control; ##P < 0.01 vs 4th passage in control group |
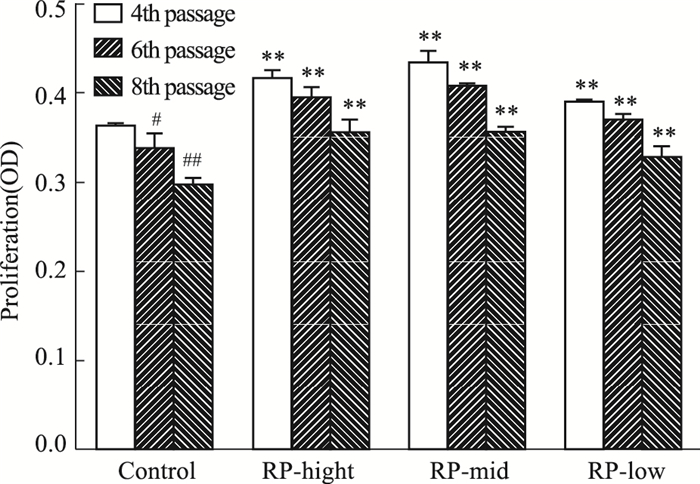
如Fig 3所示, 随细胞传代次数的增多, 细胞增殖功能明显降低(P < 0.01), 经黄精各剂量干预后, 细胞增殖功能明显增强(P < 0.01)。
|
| Fig 3 Effect of RP on proliferation in EPCs(x±s, n=3) **P < 0.01 vs control; #P < 0.05, ##P < 0.01 vs 4th passage in control group |
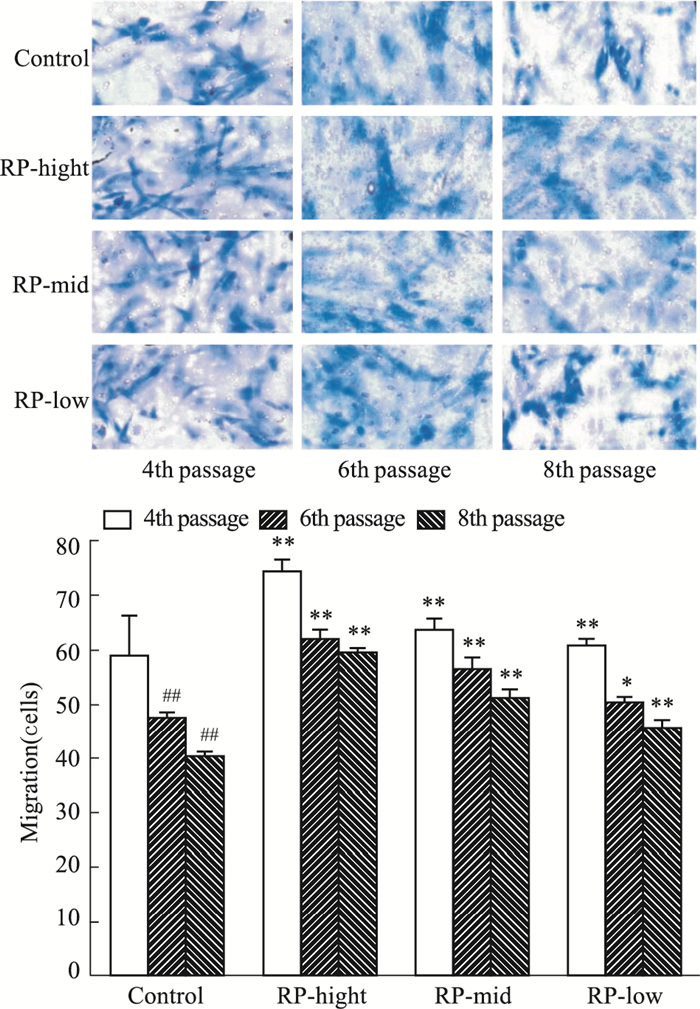
如Fig 4所示, 随细胞传代次数的增多, 迁移细胞数量明显降低(P < 0.01), 经黄精各剂量干预后, 迁移细胞数量明显上升(P < 0.01)。
|
| Fig 4 Effect of RP on migration in EPCs(x±s, n=3) *P < 0.05, **P < 0.01 vs control; ##P < 0.01 vs 4th passage in control group |
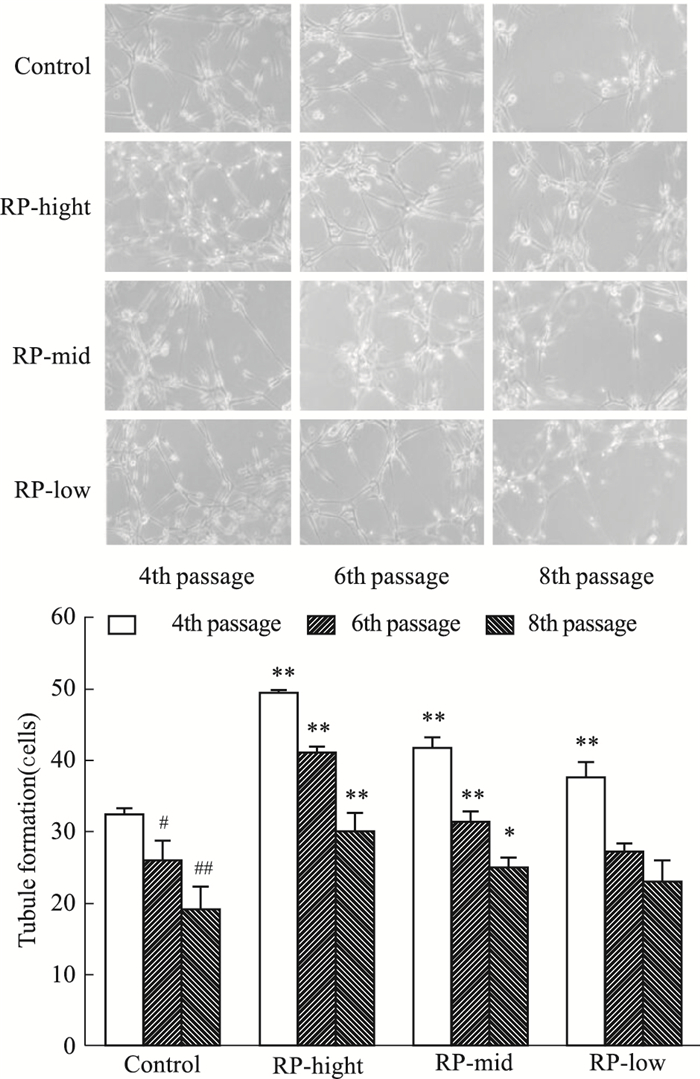
如Fig 5所示, 随细胞传代次数的增多, 成小管细胞数量明显降低(P < 0.01), 经黄精高、中剂量干预后, 成小管细胞数量明显增多(P < 0.01), 黄精低剂量仅能增强第4代的细胞成血管功能, 对第6、8代细胞成血管功能无明显影响。
|
| Fig 5 Effect of RP on tubule formation in EPCs(x±s, n=3) **P < 0.01 vs control; #P < 0.05, ##P < 0.01 vs 4th passage in control group |
流式细胞仪检测到的DCFH荧光强度可反映细胞ROS的水平, 且呈正相关。Fig 6结果表明, 随细胞传代次数增多, 其ROS水平迅速上升(P < 0.01), 经黄精各剂量干预后, 细胞ROS水平明显降低(P < 0.01)。

|
| Fig 6 Effect of RP on level of ROS in EPCs(x±s, n=3) **P < 0.01 vs control; ##P < 0.01 vs 4th passage in control group |
EPCs是一类具有巨大增殖潜力的内皮细胞前体细胞, 在血管损伤、缺血缺氧等条件下, EPCs不仅可向损伤血管迁移募集, 参与受损内皮的修复及血管网络的构建, 还能分泌多种细胞因子, 促进血管的修复重建。因此, 由EPCs介导的缺血性心血管疾病的治疗已成为目前再生医学研究的热点[1-2, 5]。
然而, EPCs会随机体衰老出现老化迹象, 这主要由年龄、遗传、端粒酶等决定[3, 6]。同时, EPCs在体外培养过程中也会出现复制时间延长, 甚至停滞等老化迹象, 这可能是因为细胞在短期内不断复制, 又无体内环境的保护, 多种外界局部因素对细胞的各种有害刺激逐渐积累所致。本研究也表明, 取自老年大鼠骨髓的EPCs在体外传代培养过程中迅速衰老, 并伴有细胞功能的明显衰退。
衰老自由基学说认为, 衰老过程是机体组织细胞不断产生自由基积累的结果。活性氧类是细胞氧化系统产生的含有ROS功能基团的化合物, 也是体内最重要的自由基。正常情况下, 细胞内ROS的产生和清除处于平衡, 但在细胞衰老进程或刺激因子存在时, 其胞内清除ROS的调节机制失衡, 积累增多的ROS又会损害细胞功能, 加速细胞衰老[7-8]。可见, ROS的异常增多是加速EPCs衰老的一个关键因素。本研究也表明, EPCs在体外传代培养老化进程中伴有ROS异常迅速增多, 而增多的ROS又可继续加重EPCs老化, 并损伤EPCs功能。
黄精是疗效确切的抗衰老中药, 现代药理学研究已表明, 黄精及其主要成分黄精多糖可增强机体抗氧化功能, 有效清除自由基, 减轻炎症损伤反应; 可有效提高EPCs的端粒酶活性, 延缓在体EPCs的衰老[3, 9-10]。本研究进一步表明, 黄精可有效干预老年大鼠EPCs的体外传代培养老化进程, 其机制可能是通过降低细胞ROS水平, 减轻细胞氧化损伤来保护衰老进程中EPCs功能。由于线粒体是ROS产生的主要场所, 也是ROS作用最敏感的部位, 线粒体功能损伤是ROS异常增多最主要的原因之一, 与细胞衰老关系密切, 黄精是否可以通过维护线粒体功能来达到抗EPCs衰老的机制, 尚待后续研究。
| [1] |
Assmus B, Schachlinger V, Teupe C, et al. Transplantation of progenitor cells and re-generation enhancement in acute myocardial infarction (TOPCARE-AMI)[J]. Circulation, 2002, 106(24): 3009-17. doi:10.1161/01.CIR.0000043246.74879.CD |
| [2] |
Assmus B, Honold J, Schachinger V, et al. Transcoronary transplantation of progenitor cells after myocardial infarction[J]. N Engl J Med, 2006, 355(12): 1222-32. doi:10.1056/NEJMoa051779 |
| [3] |
宰青青, 秦臻, 叶兰. 黄精对自然衰老大鼠内皮祖细胞功能及端粒酶活性的影响[J]. 中国中西医结合杂志, 2016, 36(12): 1480-5. Zai Q Q, Qin Z, Ye L. Effect of Rhiaoma Polygonati on the function of endothelial progenitor cells and telomerase activity in nature senescent rats[J]. Chin J Integr Tradit West Med, 2016, 36(12): 1480-5. doi:10.7661/CJIM.2016.12.1480 |
| [4] |
秦臻, 黄水清. 当归补血汤含药血清对内皮祖细胞功能及其PI3K/Akt通路影响的研究[J]. 中国药理学通报, 2013, 29(9): 1320-3. Qin Z, Huang S Q. Influence of drug-serum containing Dangguibuxue decoction on fuctional activity and PI3K/Akt pathway of endothelial progenitor cells[J]. Chin Pharmacol Bull, 2013, 29(9): 1320-3. doi:10.3969/j.issn.1001-1978.2013.09.033 |
| [5] |
Zampetaki A, Kirton J P, Xu Q. Vascular repair by endothelial progenitor cells[J]. Cardiovasc Res, 2008, 78(3): 413-21. |
| [6] |
Umemura T, Soga J, Hidaka T, et al. Aging and hypertension are independent risk factors for reduced number of circulating endothelial progenitor cells[J]. Am J Hypertens, 2008, 21(11): 1203-9. doi:10.1038/ajh.2008.278 |
| [7] |
Imanishi T, Tsujioka H, Akasaka T. Endothelial progenitor cells dysfunction and senescence:contribution to oxidative stress[J]. Curr Cardiol Rev, 2008, 4(4): 275-86. doi:10.2174/157340308786349435 |
| [8] |
陈永红, 杜冠华. 线粒体与衰老[J]. 中国药理学通报, 2000, 16(5): 485-8. Chen Y H, Du G H. Mitochondria and aging[J]. Chin Pharmacol Bull, 2000, 16(5): 485-8. doi:10.3321/j.issn:1001-1978.2000.05.002 |
| [9] |
马志茹, 袁倬斌. 电化学法研究黄精及枸杞子对活性氧自由基的清除作用[J]. 中国药学杂志, 1999, 34(10): 665-7. Ma Z R, Yuan Z B. Scavenging effect of fructus lycii and rhizoma polygonati on active oxygen free radicals[J]. Chin Pharmacol J, 1999, 34(10): 665-7. doi:10.3321/j.issn:1001-2494.1999.10.008 |
| [10] |
雷升萍, 王靓, 龙子江, 等. 黄精多糖通过TLR4-MyD88-NF-κB通路抑制缺氧/复氧H9c2心肌细胞炎性因子释放[J]. 中国药理学通报, 2017, 33(2): 255-60. Lei S P, Wang L, Long Z J, et al. Inhibitory effect of Polygonatum sibiricum polysaccharides on release of inflammatory cytokines of anoxia/reoxygenation H9c2 myocardial cells through TLR4-MyD88-NF-κB signaling pathway[J]. Chin Pharmacol Bull, 2017, 33(2): 225-60. |

