

2. 风湿病发生与干预湖北省重点实验室, 湖北 恩施 445000
武璐璐(1990-), 女, 硕士生, 研究方向:中医药防治痹证, 共同第一作者, E-mail:810121323@qq.com。
2. Hubei Provincial Key Lab of Occurrence and Intervention of Rheumatic Diseases, Enshi Hubei 445000, China
类风湿关节炎(rheumatoid arthritis, RA)是一种常见的自身免疫性慢性炎症性疾病, 其病理特征为炎性细胞与滑膜细胞的增殖和浸润, 导致多关节炎症、滑膜增厚、骨与软骨组织受损、关节破坏畸形, 甚而多脏器损伤[1]。传统中医药在RA治疗方面积累了丰富的经验, 而中草药的天然特性及其多环节、多靶点的综合作用方式, 使其在RA的治疗方面具有独特的优势。湖北枫杨(Pterocarya hupehensis Skan)可解热杀虫、祛风除湿、消肿止痛, 常用来治疗风湿麻木、寒湿骨痛、关节疼痛、跌打损伤[2], 是恩施民间常用的治疗RA的土家药。本实验主要观察了湖北枫杨乙醇提取物对胶原诱导性关节炎(collagen-induced arthritis, CIA)大鼠模型的影响, 初步探讨了其可能的作用机制, 为湖北枫杨应用于临床提供一定的理论实验基础。
1 材料 1.1 实验动物清洁级♂SD大鼠60只, 体质量(200±20)g, 购自三峡大学实验动物中心, 许可证号:SCXK(鄂)2011-0012。适应性喂养1周后开始实验。
1.2 药品与试剂湖北枫杨由湖北民族学院医学院中草药标本中心集中采购, 经相关机构鉴定为胡桃科(Juglandaceae)枫杨属(Pterocarya Kunth)植物的干燥茎皮; 雷公藤多苷片(浙江得恩德制药有限公司, 国药准字Z3302042);无水乙醇、冰醋酸(上海沪试国药集团股份有限公司); 牛Ⅱ型胶原(美国Chondrex公司); 弗氏完全佐剂(美国Sigma公司); TUNEL试剂盒(瑞士Roche公司); TNF-α、IL-1β试剂盒(杭州联科生物技术股份有限公司); p-NF-κB p65、cleaved caspase-3、Bcl-2、Bax抗体(美国Abcam公司); β-actin抗体(武汉博士德生物工程有限公司)。
1.3 仪器旋蒸仪、真空冷冻干燥机(瑞士Buchi公司); 电热恒温箱(美国GOLO-SIM公司); 多功能酶标仪(美国Thermo Scientific公司); 电子显微镜(日本Olympus公司); 低速离心机、高速冷冻离心机(德国Eppendorf公司); 电泳槽、电转膜仪(美国Bio-Rad公司); 超灵敏化学发光成像分析仪(美国GE公司)。
2 方法 2.1 湖北枫杨乙醇提取物的制备取湖北枫杨干燥茎皮1 kg, 粉碎, 用10倍体积75%乙醇浸泡24 h, 后用超声浸提40 min, 反复提取5次, 每次过滤取滤液, 合并5次滤液, 离心去渣, 减压浓缩后真空冷冻干燥, 得湖北枫杨乙醇提取物200.11 g, 使用时用蒸馏水配制成所需浓度。
2.2 CIA模型的建立从60只适龄♂SD大鼠中随机取出10只作为阴性对照组(N组), 其余大鼠用于建立CIA模型。将完全弗氏佐剂与用冰醋酸溶解后4 ℃过夜的牛Ⅱ型胶原, 按1 :1比例在冰浴条件充分乳化, 配制成混合乳剂。在大鼠右后足趾部、尾部、背部多点皮内注射混合乳剂每只0.3 mL, 阴性对照组在相同部位注射等体积的生理盐水[3]。14 d后重复上述步骤。二次免疫3~7 d后, 免疫组大鼠足趾肿胀度和关节炎指数明显增加, 膝关节滑膜增厚, 同时伴大量炎症细胞浸润, 即CIA模型构建成功。
2.3 分组及给药将二次免疫7 d后的50只大鼠, 随机分为模型组(M组)、阳性对照雷公藤多苷组(TG组)、湖北枫杨乙醇提取物低(PL)、中(PM)、高(PH)剂量组。当天灌胃给药, 阳性对照组给予6.25 mg·kg-1·d-1的雷公藤多苷(参考60 kg成人临床常用剂量1 mg·kg-1·d-1, 折算成等效大鼠剂量), 治疗组分别给予0.42、0.84、1.68 g·kg-1·d-1的湖北枫杨乙醇提取物(低剂量参考60 kg成人临床常用水煎液剂量0.33 g·kg-1·d-1乘以醇提物约20%的提取率后, 折算成等效大鼠剂量, 中、高剂量分别为低剂量的2倍、4倍), 阴性对照组、模型组灌胃等量生理盐水, 连续灌胃28 d。
2.4 指标检测 2.4.1 大鼠体质量的测定从第2次免疫d 7(给药治疗d 0)起, 测量各组大鼠体质量, 每隔7 d观察记录1次。观察各用药组对CIA大鼠体质量的影响。
2.4.2 大鼠足跖肿胀度的测定用水容积法测量每只大鼠左后足的容积, 从第2次免疫d 7起, 每隔7 d测量1次各组大鼠左后足容积。观察各用药组对CIA大鼠足肿胀度的影响。
2.4.3 大鼠关节炎指数的测定从第2次免疫d 7起, 计算大鼠关节炎指数, 每隔7 d观察记录1次。大鼠关节炎指数计算采取5级评分法:0分, 关节无红肿; 1分, 趾关节红肿; 2分, 趾关节和足趾肿胀; 3分, 踝关节以下的足爪肿胀; 4分, 踝关节和所有足爪肿胀、关节严重变形。大鼠所有关节炎指数之和即为每只大鼠关节炎指数(arthritis index, AI)值, 最高分值为16分。
2.4.4 大鼠膝关节滑膜组织病理形态学观察给药28 d后, 麻醉大鼠, 心尖取血, 取大鼠左后足膝关节滑膜, 用4%的多聚甲醛溶液固定后脱钙, 乙醇逐级脱水, 二甲苯透明, 浸蜡包理, 切片, 进行HE染色; 同时左后足膝关节滑膜按照TUNEL凋亡检测试剂盒进行细胞凋亡检测。显微镜下观察、拍照, 计算滑膜细胞凋亡细胞数。取右膝关节滑膜置-80 ℃冰箱备用。
2.4.5 大鼠血清ALT、AST、BUN、SCr及TNF-α、IL-1β含量的测定将取出的大鼠全血室温静置2 h后, 3 500 r·min-1离心10 min, 取上层血清, 分装。一部分用全自动生化分析仪检测各组大鼠血清中ALT、AST、BUN、SCr的含量; 另一部分按照相应ELISA试剂盒, 检测各组大鼠血清中TNF-α、IL-1β的含量。
2.4.6 大鼠膝关节滑膜中p-p65、cleaved caspase-3、Bax、Bcl-2蛋白检测冰上提取各组大鼠右膝关节滑膜总蛋白, 蛋白上样缓冲液变性后, 进行SDS-PAGE电泳, 转膜, 5%脱脂牛奶封闭, 洗膜, 分别加相应一抗p-p65(1 :1 000)、cleaved caspase-3(1 :800)、Bcl-2(1 :1 000)、Bax(1 :1 000) 4 ℃孵育过夜, 洗膜后, 加入HRP标记的二抗(1 :20 000), 室温下在摇床上孵育2 h。洗膜后, 加入ECL发光剂, 用凝胶成像系统拍照成像。用Quantity One软件分析条带灰度值, 以内参β-actin作对照, 计算各组目的蛋白的相对表达量。
2.5 统计学分析用SPSS 20.0软件对实验结果进行统计分析, 计量资料以x±s表示, 组间比较用方差分析。
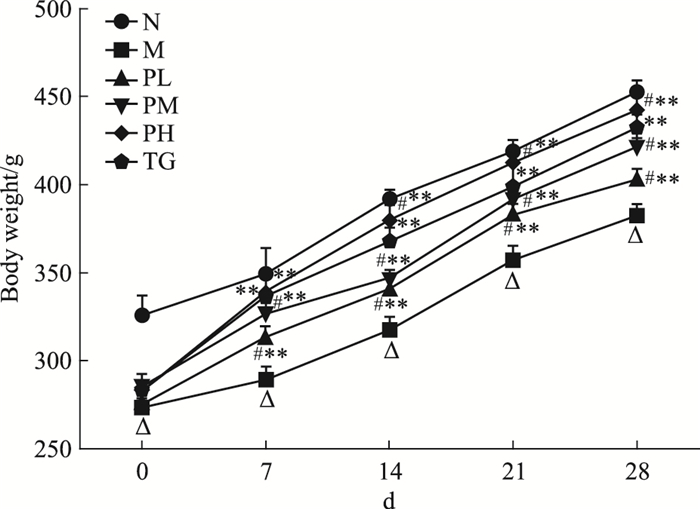
3 结果 3.1 湖北枫杨乙醇提取物对大鼠体质量的影响大鼠第1次免疫后开始出现倦怠、食欲减退, 随之体质量下降。如Fig 1所示, 与对照组比较, 模型组大鼠的体质量下降(P < 0.05);用药后, 各治疗组大鼠体质量较模型组增加(P < 0.05);湖北枫杨乙醇提取物高剂量组大鼠体质量增加较雷公藤多苷组明显(P < 0.05)。
|
| Fig 1 Changes of body weight of rats in each group(x±s, n=10) △P < 0.05 vs normal group; **P < 0.01 vs model group; #P < 0.05 vs TG group |
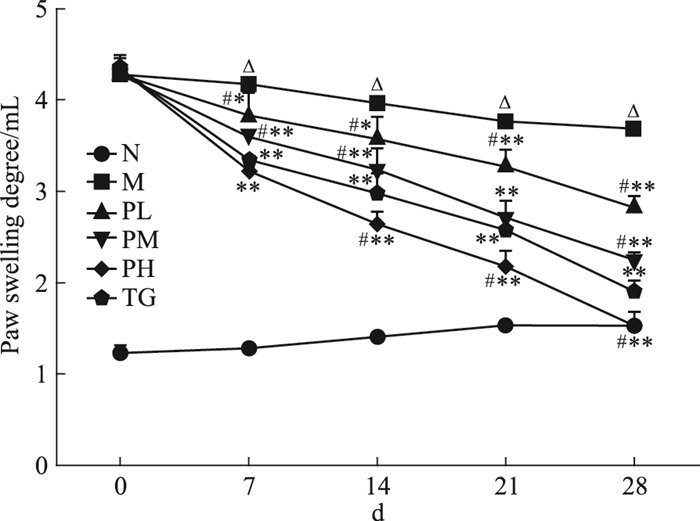
如Fig 2所示, 与对照组比较, 模型组大鼠足跖肿胀度明显增加(P < 0.05), 出现严重的红肿甚至变形, 足掌的宽度、厚度均明显增加; 与模型组比较, 治疗1周后, 各用药组大鼠足跖肿胀度明显下降, 并持续至用药4周后(P < 0.05);湖北枫杨乙醇提取物高剂量组足跖肿胀情况在用药2周后下降, 较雷公藤多苷组明显(P < 0.05)。
|
| Fig 2 Changes of paw swelling degreeof rats in each group(x±s, n=10) △P < 0.05 vs normal group; *P < 0.05, **P < 0.01 vs model group; #P < 0.05 vs TG group |
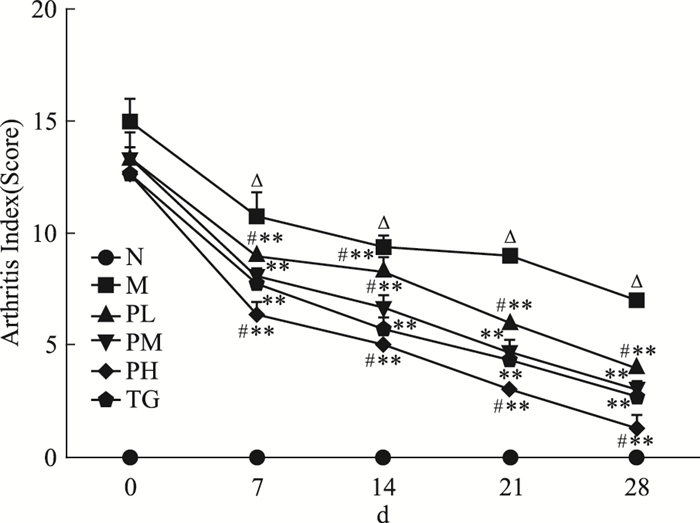
如Fig 3所示, 大鼠二次免疫后, 四肢关节相继出现肿胀、发红, 随着时间延长, 继而出现皮肤溃烂、关节畸形等症状。与对照组比较, 模型组大鼠关节炎指数明显增加(P < 0.05);与模型组比较, 各治疗组大鼠关节炎指数在给药后持续下降(P < 0.05);湖北枫杨乙醇提取物高剂量组大鼠关节炎指数较雷公藤多苷组下降明显(P < 0.05)。
|
| Fig 3 Changes of arthritis indexof rats in each group(x±s, n=10) △P < 0.05 vs normal group; *P < 0.05, **P < 0.01 vs model group; #P < 0.05 vs TG group |
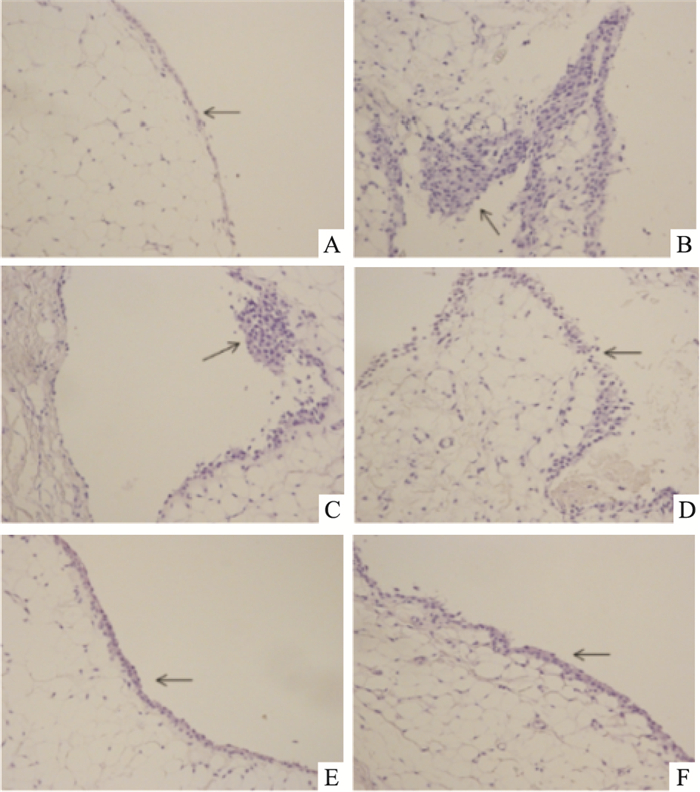
大鼠滑膜HE染色显示(Fig 4), 对照组膝关节滑膜无增生、突起, 无炎细胞浸润; 模型组滑膜增生明显, 滑膜衬细胞分层增多、增厚, 并伴有大量炎性细胞浸润; 雷公藤多苷组滑膜增生减轻, 炎性细胞浸润明显减少; 湖北枫杨乙醇提取物低剂量组滑膜增生有所改善, 炎性细胞浸润稍减; 中剂量组滑膜增生明显减轻, 炎性细胞浸润减少; 高剂量组滑膜轻度增生, 炎性细胞浸润明显减少。
|
| Fig 4 HE staining of knee synovial membrane of rats in each group(×200) A:Normal group; B:Model group; C:PL group; D:PM group; E:PH group; F:TG group.The arrows indicate the synovial tissue |
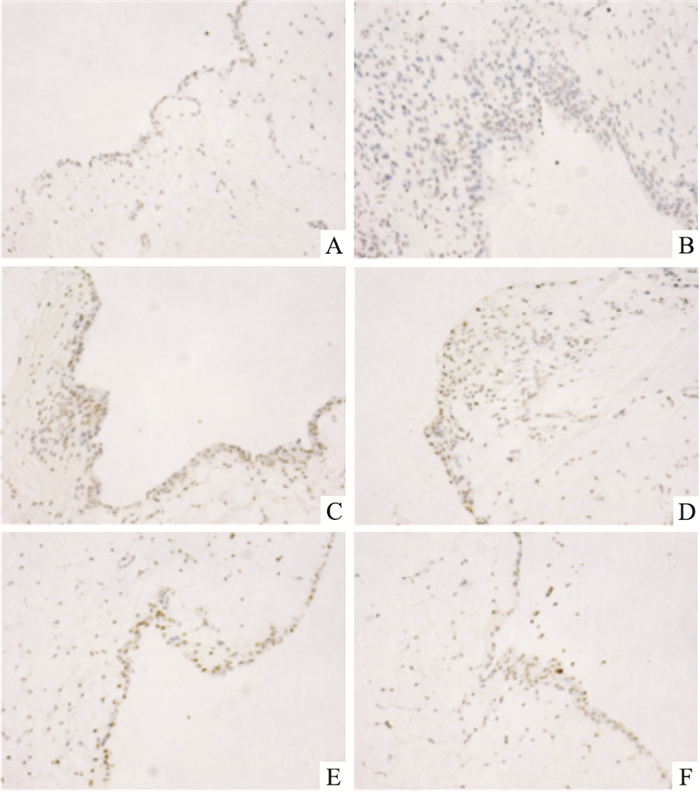
经TUNEL染色后, 凋亡细胞呈棕色(阳性细胞), 正常细胞呈蓝色。大鼠滑膜TUNEL染色计数结果显示(Fig 5), 模型组滑膜细胞有少量凋亡, 凋亡指数与对照组比较差异无显著性; 各组大鼠凋亡指数显示(Tab 1), 与模型组比较, 各用药组阳性细胞数量皆增多, 凋亡指数升高(P < 0.05);湖北枫杨乙醇提取物高剂量组滑膜细胞凋亡指数高于雷公藤多苷组(P < 0.05)。
|
| Fig 5 TUNEL staining of knee synovial membrane of rats in each group(×200) A:Normal group; B:Model group; C:PL group; D:PM group; E:PH group; F:TG group |
| Group | Apoptotic index/% |
| Normal | 5±0 |
| Model | 8±3 |
| PL | 18±6**# |
| PM | 28±6**# |
| PH | 50±2**# |
| TG | 39±2** |
| **P < 0.01 vs model; #P < 0.05 vs TG | |
如Tab 2所示, 与对照组比较, 模型组大鼠血清中TNF-α、IL-1β含量明显增加(P < 0.05);给药后, 各治疗组血清中TNF-α、IL-1β含量较模型组下降(P < 0.05);湖北枫杨乙醇提取物高剂量组血清中TNF-α、IL-1β含量较雷公藤多苷组下降较为明显(P < 0.05)。
| Group | TNF-α/ng·L-1 | IL-1β/ng·L-1 |
| Normal | 39.2±3.9 | 197.3±97.1 |
| Model | 55.5±3.2△ | 1387.8±441.3△ |
| PL | 53.4±3.9 | 740.1±185.5**# |
| PM | 48.0±3.4** | 544.4±219.1**# |
| PH | 39.7±4.8**# | 326.6±195.0**# |
| TG | 44.5±2.5* | 399.6±461.8** |
| △P < 0.05 vs normal; *P < 0.05, **P < 0.01 vs model; #P < 0.05 vs TG | ||
如Tab 3所示, 与对照组比较, 模型组血清ALT、AST、BUN、SCr水平增加(P < 0.05);湖北枫杨乙醇提取物低、中、高剂量组较模型组下降(P < 0.05);雷公藤多苷组与模型组相比差异无显著性。
| Group | ALT/U·L-1 | AST/U·L-1 | BUN/mmol·L-1 | SCr/mmol·L-1 |
| Normal | 43.6±10.14 | 116.4±23.99 | 7.976±0.90 | 32.7±4.98 |
| Model | 71.2±4.82△ | 172±20.82△ | 10.824±1.10△ | 52.84±25.46△ |
| PL | 57±14.51*# | 141.4±17.24**# | 8.77±1.46* | 35.84±7.14* |
| PM | 54.4±14.05**# | 132.2±16.39**# | 8.756±2.10** | 35.04±10.28** |
| PH | 50.2±5.12**# | 124.2±34.71**# | 6.772±1.78**# | 34.10±9.81**# |
| TG | 60.2±6.98* | 167±14.92** | 8.97±1.46* | 42.82±8.20** |
| △P < 0.05 vs normal; *P < 0.05, **P < 0.01 vs model; #P < 0.05 vs TG | ||||
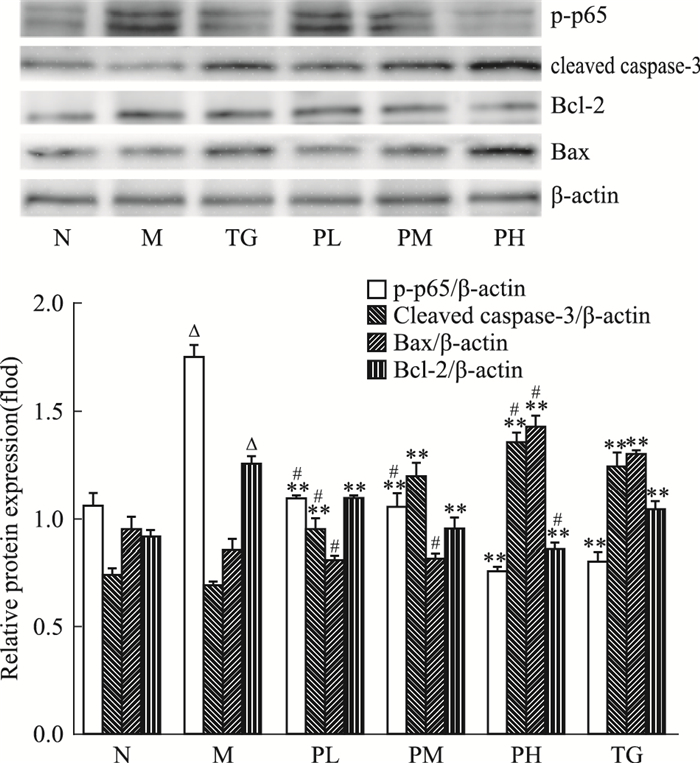
如Fig 6所示, 模型组大鼠膝关节滑膜中p-p65、Bcl-2表达较对照组明显增加(P < 0.05);用药后, 各治疗组滑膜内p-p65、Bcl-2表达减少(P < 0.01), cleaved caspase-3、Bax表达增加(P < 0.01);与雷公藤多苷组比较, 湖北枫杨高剂量组cleaved caspase-3、Bax、Bcl-2改变明显(P < 0.05)。
|
| Fig 6 Changes of p-p65, cleaved caspase-3, Bax and Bcl-2proteins in synovial membrane of rats in each group(x±s, n=3) △P < 0.05 vs normal group; *P < 0.05, **P < 0.01 vs model group; #P < 0.05 vs TG group |
如Tab 4所示, TNF-α、IL-1β分别与大鼠体质量呈负相关, 与大鼠关节肿胀率、关节炎指数呈正相关。
| Indicator | Correlation coefficient r | ||
| Body weight | Joint swelling rate | AI | |
| TNF-α | -0.852* | 0.903# | 0.872△ |
| IL-1β | -0.924* | 0.962# | 0.917△ |
| *P < 0.05 vs body weight; #P < 0.05 vs joint swelling rate; △P < 0.05 vs AI | |||
目前, RA的病因病机尚未完全明确。RA的主要病理特点为促炎细胞因子的高水平分泌和病变关节滑膜细胞的增殖, 表现为炎症的反复发作、滑膜增厚、血管翳形成和功能异常, 最终引起骨和关节的病变[4]。
炎性反应介质的持续作用在RA的发病和进展中发挥着重要的作用。TNF-α是在RA发病过程中起重要调控作用的细胞因子之一, 有研究表明, 在RA的活动期和进展期, TNF-α分泌水平增高[5]。TNF-α可增加趋化因子的合成、分泌, 影响黏附分子的表达, 刺激成纤维细胞和软骨细胞产生前列腺素和胶原酶, 刺激软骨细胞分泌金属蛋白酶, 加重炎性反应, 促进骨和关节的破坏[6]。IL-1β亦是一种重要的促炎细胞因子, 可增强单核细胞和淋巴细胞的黏附性和趋化性[7], 使其在炎症区域游走与聚集; 亦可促进前列腺素、金属蛋白酶的合成和释放, 促进滑膜细胞和淋巴细胞的增殖[8], 在软骨破坏和骨侵蚀中起着重要作用。另外, IL-1β还可调节多种炎症因子的表达, 协同促进炎症因子增加[9]。本实验结果显示, 湖北枫杨乙醇提取物可降低大鼠的足跖肿胀率和关节炎指数, 增加大鼠体质量, 同时, 大鼠血清中TNF-α、IL-1β含量也下降, 且TNF-α、IL-1β含量与足跖肿胀率、关节炎指数呈正相关, 与大鼠体质量呈负相关。说明湖北枫杨乙醇提取物可能通过抑制炎症因子TNF-α、IL-1β的表达, 减轻CIA大鼠的炎症反应, 从而达到保护关节滑膜和软骨的目的。
滑膜细胞的过度增殖活化是RA发病的重要基础, 成纤维滑膜细胞(fibroblast-like synoviocyte, FLS)凋亡不足是其关键因素。正常情况下, FLS增殖与凋亡处于动态平衡中。当RA机体内微环境改变时, 如在TNF-α、IL-1β等细胞因子刺激下, FLS出现凋亡缺陷, 开始异常增殖, 呈肿瘤样侵袭特性, 同时又释放大量细胞因子、基质金属蛋白酶, 继而刺激滑膜细胞增殖、炎性细胞浸润、血管翳形成, 侵蚀骨和关节[10]。本实验结果显示, 给予湖北枫杨乙醇提取物治疗后, 大鼠滑膜细胞出现不同程度的凋亡, 滑膜增生减轻, 炎性细胞浸润减少, 同时大鼠血清中TNF-α、IL-1β含量降低。说明湖北枫杨乙醇提取物可能通过抑制炎症因子的释放, 促进滑膜细胞凋亡, 抑制滑膜增生, 从而改善RA的病情。研究表明, 只有当核因子NF-κB p65的活性被抑制时, TNF-α才发挥促凋亡作用[11], 而IL-1β亦可通过抑制NF-κB的活性来诱导细胞凋亡[12]。caspase-3作为细胞凋亡过程中的主要效应因子, 是细胞凋亡的关键执行者, 当细胞受到凋亡信号刺激时被激活, 导致许多蛋白或激酶失活, 引起细胞结构改变、细胞周期阻滞及DNA修复异常, 使细胞凋亡[13]。在本实验中, 湖北枫杨乙醇提取物治疗组滑膜内p-p65表达降低, cleaved caspase-3表达增加, 说明湖北枫杨乙醇提取物可能通过降低p-p65的释放, 激活caspase级联反应来诱导滑膜细胞凋亡。另外, 本实验还发现, 湖北枫杨乙醇提取物治疗组滑膜内Bcl-2表达减少, Bax表达增加, Bcl-2/Bax比值降低。Bcl-2是抗凋亡蛋白, Bax是促凋亡蛋白, 当Bcl-2/Bax比值降低时, 可使线粒体外膜通透性增加, 细胞色素C等膜间隙蛋白释放[14], 激活下游caspases级联反应, 诱导凋亡。说明湖北枫杨乙醇提取物可能通过调控Bcl-2、Bax蛋白的表达, 进而诱导滑膜细胞凋亡。
本研究结果显示, 与对照组比较, 模型组血清ALT、AST、BUN、SCr水平增加, 说明CIA模型对大鼠的肝脏和肾脏有一定的损伤。湖北枫杨乙醇提取物低、中、高剂量组较模型组下降, 说明湖北枫杨乙醇提取物可改善CIA模型对肝、肾的损伤。雷公藤多苷组血清ALT、AST、BUN、SCr水平与模型组差异无显著性。另有研究报道, 雷公藤多苷可对肝、肾有一定程度的损伤[15]。由此可见, 在保护肝、肾方面, 湖北枫杨乙醇提取物优于雷公藤多苷。
综上所述, 湖北枫杨乙醇提取物对SD大鼠CIA模型有很好的治疗效果, 并可通过调控相关细胞因子TNF-α、IL-1β及p-p65、凋亡蛋白cleaved caspase-3、Bcl-2、Bax的表达, 起到很好的抗炎和诱导滑膜细胞凋亡的作用。而湖北枫杨乙醇提取物中何种成分影响上述细胞因子和蛋白的传导, 具体通过哪种机制, 以及是否还通过其他途径达到抗炎、促凋亡目的, 我们将在后续的实验中研究和探索。
| [1] |
Shaw A T, Gravallese E M. Mediators of inflammation and bone remodeling in rheumatic disease[J]. Semin Cell Dev Biol, 2016, 49: 2-10. doi:10.1016/j.semcdb.2015.10.013 |
| [2] |
湖北省恩施地区中草药研究小组编. 恩施中草药手册[M]. 恩施: 湖北省恩施地区中草药研究小组, 1970: 856-7. Enshi Herbal Medicine Research Group, Enshi, Hubei Province. Enshi Chinese Herbal Medicine Handbook[M]. Enshi: Herbal Medicine Research Group, Enshi Prefecture, Hubei Province, 1970: 856-7. |
| [3] |
白琳, 杨雨欣, 万巧凤, 等. 黄芩苷经TLR2/NF-κB途径减轻类风湿关节炎大鼠滑膜炎[J]. 中国药理学通报, 2017, 33(11): 1569-73. Bai L, Yang Y X, Wan Q F, et al. Baicalin alleviates synovitis in rats with rheumatoid arthritis via TLR2/NF-κB pathway[J]. Chin Pharmacol Bull, 2017, 33(11): 1569-73. doi:10.3969/j.issn.1001-1978.2017.11.018 |
| [4] |
Iwasaki Y, Yamamoto K. Basic research overview in rheumatoid arthritis[J]. Nihon Rinsho, 2016, 74(6): 889-96. |
| [5] |
刘德芳, 郭明阳, 呼永河, 等. 类风湿关节炎湿热痹阻型患者血清和关节液IL-1、IL-6、TNF-α的表达研究[J]. 免疫学杂志, 2014, 30(5): 447-51. Liu D F, Guo M Y, Hu Y H, et al. Expression of IL-1, IL-6 and TNF-α in serum and synovial fluid of rheumatoid arthritis patients with damp-heat stasis syndrome[J]. Chin J Immunol, 2014, 30(5): 447-51. |
| [6] |
Lai N S, Yu H C, Tung C H, et al. The role of aberrant expression of T cell miRNAs affected by TNF-alpha in the immunopathogenesis of rheumatoid arthritis[J]. Arthritis Res Ther, 2017, 19(1): 261. doi:10.1186/s13075-017-1465-z |
| [7] |
Mitroulis I, Kambas K, Ritis K. Neutrophils, IL-1β, and gout:is there a link?[J]. Semin Immunopathol, 2013, 35(4): 501-12. doi:10.1007/s00281-013-0361-0 |
| [8] |
Choi Y J, Lee W S, Lee E G, et al. Sulforaphane inhibits IL-1β-induced proliferation of rheumatoid arthritis synovial fibroblasts and the production of MMPs, COX-2, and PGE2[J]. Inflammation, 2014, 37(5): 1496-503. doi:10.1007/s10753-014-9875-4 |
| [9] |
Wu Q, Wang Y, Wang Q, et al. The bispecific antibody aimed at the vicious circle of IL-1β and IL-17A, is beneficial for the collagen-induced rheumatoid arthritis of mice through NF-κB signaling pathway[J]. Immunol Lett, 2016, 179: 68-79. doi:10.1016/j.imlet.2016.09.001 |
| [10] |
McInnes I B, Schett G. The pathogenesis of rheumatoid arthritis[J]. N Engl J Med, 2011, 365(23): 2205-19. doi:10.1056/NEJMra1004965 |
| [11] |
Bartok B, Firestein G S. Fibroblast-like synoviocytes:key effector cells in rheumatoid arthritis[J]. Immunol Rev, 2010, 233(1): 233-55. doi:10.1111/imr.2009.233.issue-1 |
| [12] |
Hong H, Zeng Y, Jian W, et al. CDK7 inhibition suppresses rheumatoid arthritis inflammation via blockage of NF-kappaB activation and IL-1beta/IL-6 secretion[J]. J Cell Mol Med, 2018, 22(2): 1292-301. |
| [13] |
Song Y, Zhong M, Cai F C. Oxcarbazepine causes neurocyte apoptosis and developing brain damage by triggering Bax/Bcl-2 signaling pathway mediated caspase 3 activation in neonatal rats[J]. Eur Rev Med Pharmacol Sci, 2018, 22(1): 250-61. |
| [14] |
Howells C C, Baumann W T, Samuels D C, et al. The Bcl-2-associated death promoter(BAD) lowers the threshold at which the Bcl-2-interacting domain death agonist(BID) triggers mitochondria disintegration[J]. J Theor Biol, 2011, 271(1): 114-23. doi:10.1016/j.jtbi.2010.11.040 |
| [15] |
刘雪梅, 刘志宏, 张晶, 等. 雷公藤临床应用及不良反应的研究进展[J]. 药学实践杂志, 2015, 33(2): 110-3. Liu X M, Liu Z H, Zhang J, et al. Research progress of clinical application and adverse reactions of Tripterygium Wilfordii[J]. J Pharm Pract, 2015, 33(2): 110-3. doi:10.3969/j.issn.1006-0111.2015.02.004 |

