

肝脏是人体最重要的消化器官之一, 关系着人体的健康。急性肝损伤是常见的肝脏疾病之一, 其病因复杂, 病情紧急。目前临床医治方法不断进步及完善, 但其治疗方法主要是对症治疗, 尚无根治方法。急性肝损伤的预防及治疗仍面临严峻的形势。因此, 研究开发疗效肯定的保肝药物成为医药工作者的共识。
杨桃(Averrhoa carambola L.)为醡浆草科多年生植物, 主要入药部位为根。研究表明, 杨桃根提取物(extract of Averrhoa carambola L.root, EACR)及其单体化合物2-十二烷基-6-甲氧基-2, 5-二烯-1, 4-环己二酮(2-dodecyl-6-methoxycyclohexa-2, 5-diene-1, 4-dione)对糖尿病及其并发症[1-2]、乳腺癌[3]等多种疾病具有疗效。本课题组前期研究发现, EACR对糖尿病引起的肝糖代谢紊乱具有明显疗效。因此我们推测, EACR对其他因素引起的肝损伤可能具有疗效, 并且尚未有文献报道。本研究旨在初步探讨EACR对四氯化碳(carbon tetrachloride, CCl4)诱导小鼠急性肝损伤的影响及其作用机制。
1 材料与方法 1.1 实验动物与试剂昆明种小鼠, SPF级, ♂, 体质量(20±2)g, 购自广西医科大学实验动物中心, 实验动物生产许可证:SCXK桂2014-0002, 实验动物使用许可证:SYXK桂2014-0003。动物饲养于通风良好环境中, 温度(18~25) ℃, 相对湿度40%-70%, 12 h光照昼夜循环。EACR的提取过程如下:5 kg杨桃根药材经80%乙醇浸泡提取3次(第1次2 h, 第2次和第3次各1.5 h), 浓缩干燥后得到500 g干膏, 低温冷藏保存, 临用时用双蒸水稀释成所需浓度。CCl4(天津市光复科技发展有限公司); 联苯双酯滴丸(北京协和药厂); 谷草转氨酶(aspartate aminotransferase, AST)、丙氨酸氨基转移酶(alanine aminotransferase, ALT)、超氧化物歧化酶(superoxide dismutase, SOD)、丙二醛(malondialehyde, MDA)、还原型谷胱甘肽(glutathione, GSH)、谷胱甘肽过氧化物酶(glutathione peroxidase, GSH-Px)、总蛋白定量测定试剂盒(南京建成生物工程研究所); 白细胞介素1(interleukin-1, IL-1)、白细胞介素6(interleukin-6, IL-6)ELISA试剂盒(上海源叶生物科技有限公司); 肿瘤坏死因子α(tumor necrosis factor α, TNF-α)、核转录因子-κB(nuclear factor-kappa B, NF-κB)、caspase-3抗体(Cell Signaling Technology)。
1.2 仪器SpectraMaxPlus384连续光谱扫描式酶标仪(Molecular Devices公司); 5810R高速低温离心机(Eppendorf公司); 垂直电泳仪、转膜仪(Bio-Rad公司); 化学发光成像系统(Sagecreation公司); BX53显微镜(Olympus公司)。
1.3 动物分组、给药方法及模型建立取60只♂小鼠, 随机分为6组:正常对照组(生理盐水, 20 mL·kg-1)、模型组(生理盐水, 20 mL·kg-1)、阳性对照组(联苯双酯滴丸, 0.02 g·kg-1)、EACR高剂量组(1.2 g·kg-1, 相当于12 g生药·kg-1)、EACR中剂量组(0.6 g·kg-1, 相当于6 g生药·kg-1)、EACR低剂量组(0.3 g·kg-1, 相当于3 g生药·kg-1), 每组10只。预防性提前给予相应药物7 d, 1 d 1次。末次给药后1 h, 正常组注射等剂量橄榄油, 其他各组小鼠腹腔注射0.15% CCl4橄榄油(10 mL·kg-1, 均一次性注射), 建立急性肝损伤模型。
1.4 标本采集采用4%水合氯醛麻醉小鼠后, 颈椎脱臼处死小鼠, 摘除眼球采血, 离心后收集上层血清。剖腹取其肝脏, PBS冲洗干净后, 拭干, 称重, 存放于液氮中, 备用。
1.5 指标检测 1.5.1 血清学指标的测定小鼠麻醉后, 摘除眼球采血, 4 ℃、3 500 r·min-1离心10 min, 收集上层血清。严格按照试剂盒说明检测血清ALT、AST、IL-1、IL-6。
1.5.2 肝脏组织指标的测定取适量肝组织, 洗去积血后, 按1 :9加入生理盐水制备成10%的肝组织匀浆。按照试剂盒的说明测定SOD、MDA、GSH、GSH-Px及蛋白的含量。另取约0.1 g肝脏组织, 加入10倍量的RIPA裂解液, 提取蛋白。采用Western blot法检测肝脏组织中的TNF-α、NF-κB、caspase-3的蛋白表达水平。
1.5.3 肝组织病理学检查肝组织经10%甲醛固定24 h后, 常规脱水, 石蜡包埋, 进行HE染色, 光镜下观察组织形态。
1.6 统计学分析采用SPSS 21.0分析数据, 数据结果以x±s表示, 两组间的比较采用t检验, 多组间的比较采用One-way ANOVA。
2 结果 2.1 小鼠的一般情况小鼠饲养期间, 体质量均有所增加, 但各组间差异无显著性。建立急性肝损伤模型后, 与正常组相比, 模型小鼠出现狂躁, 继而精神萎蔫, 反应迟钝, 毛色暗淡。与模型小鼠相比, EACR 3个剂量组小鼠的行为、精神及外观等一般状态均有所改善。
2.2 EACR对小鼠肝脏指数的影响由Tab 1可知, 与正常组小鼠相比, 模型组小鼠的肝脏指数明显升高(P < 0.01);与模型组相比, EACR高、中剂量组肝脏指数明显降低(P < 0.05或P < 0.01), EACR低剂量组差异无显著性。
| Group | Dose/g·kg-1 | Liver index |
| Normal | - | 1.03±0.09 |
| Model | - | 1.24±0.20** |
| Positive | 0.02 | 1.06±0.07# |
| EACR | 1.2 | 1.02±0.17## |
| 0.6 | 1.05±0.16## | |
| 0.3 | 1.18±0.19 | |
| **P < 0.01 vs normal; #P < 0.05, ##P < 0.01 vs model | ||
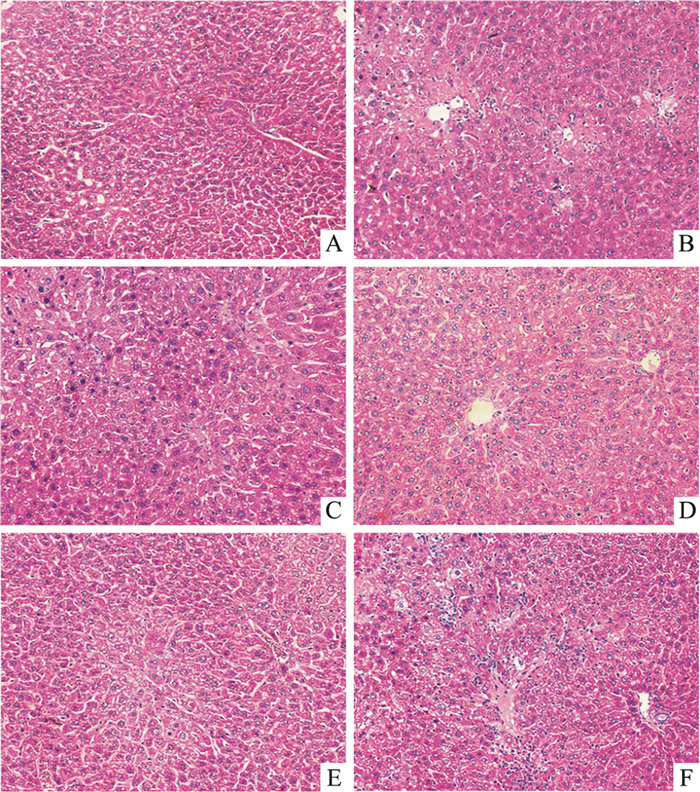
Fig 1肝脏病理染色结果表明, 正常组小鼠肝细胞结构清晰, 核大而圆, 肝索呈星状排列, 肝间质无炎症细胞浸润。模型组小鼠肝细胞变性, 部分胞质崩解, 肝索边界模糊, 肝小叶中央区及周边可见大量炎症细胞浸润, 局部坏死。EACR低剂量组肝细胞核固缩, 肝索排列紊乱, 肝间质间有较多炎症细胞浸润, 少部分出现坏死。EACR高、中剂量组及阳性组小鼠肝细胞形态结构较清晰, 少量炎症细胞浸润, 肝索排列较整齐, 未见明显充血。
|
| Fig 1 HE staining of liver tissues (×200) A:Normal; B:Model; C:Positive control; D:EACR high dose group; E:EACR middle dose group; F:EACR low dose group. |
由Tab 2可知, 与正常组小鼠相比, 模型组小鼠的AST、ALT、IL-1、IL-6明显升高(P < 0.01)。与模型组小鼠相比, EACR 3个剂量组小鼠的AST、ALT、IL-1、IL-6水平明显下降, 差异具有统计学意义(P < 0.01)。
| Group | Dose/g·kg-1 | AST/U·L-1 | ALT/U·L-1 | IL-1/ng·L-1 | IL-6/ ng·L-1 |
| Normal | - | 22.2±3.2 | 17.9±6.4 | 97.5±3.8 | 116.8±12.7 |
| Model | - | 82.2±22.5** | 198.4±48.5** | 196.4±18.0** | 197.2±24.5** |
| Positive | 0.02 | 44.8±20.2## | 109.0±55.5## | 108.1±11.1## | 124.7±16.1## |
| EACR | 1.2 | 37.6±17.4## | 114.7±36.1## | 110.7±7.3## | 116.3±13.1## |
| 0.6 | 39.0±10.7## | 120.7±26.2## | 124.5±6.3## | 142.6±17.8## | |
| 0.3 | 42.8±13.6## | 145.7±35.1## | 140.0±3.3## | 162.3±22.3## | |
| **P < 0.01 vs normal; #P < 0.05, ##P < 0.01 vs model | |||||
由Tab 3可知, 与正常组小鼠比较, 模型组小鼠的SOD、GSH、GSH-Px明显降低(P < 0.01), MDA明显升高(P < 0.01);与模型组小鼠相比, EACR能够明显提高小鼠肝脏SOD、GSH、GSH-Px活性, 明显下调MDA水平(P < 0.05或P < 0.01), EACR低剂量组的GSH虽然有所升高, 但差异无显著性。
| Group | Dose/g·kg-1 | SOD/kU·g-1 Pro | MDA/μmol·g-1 Pro | GSH/μmol·g-1 Pro | GSH-Px/μmol·g-1 Pro |
| Normal | - | 121.4±9.7 | 1.6±0.5 | 37.0±12.0 | 644.4±85.2 |
| Model | - | 61.6±27.0** | 5.8±1.7** | 15.5±6.8** | 422.9±87.2** |
| Positive | 0.02 | 110.8±8.3## | 2.8±0.3## | 24.5±5.9# | 682.6±141.5## |
| EACR | 1.2 | 117.9±17.3## | 2.1±0.6## | 27.9±5.0## | 692.5±145.8## |
| 0.6 | 114.1±12.5## | 2.2±0.4## | 24.9±4.4# | 688.5±173.4## | |
| 0.3 | 110.0±21.9## | 2.3±0.6## | 23.5±6.6 | 663.0±143.0## | |
| **P < 0.01 vs normal; #P < 0.05, ##P < 0.01 vs model | |||||
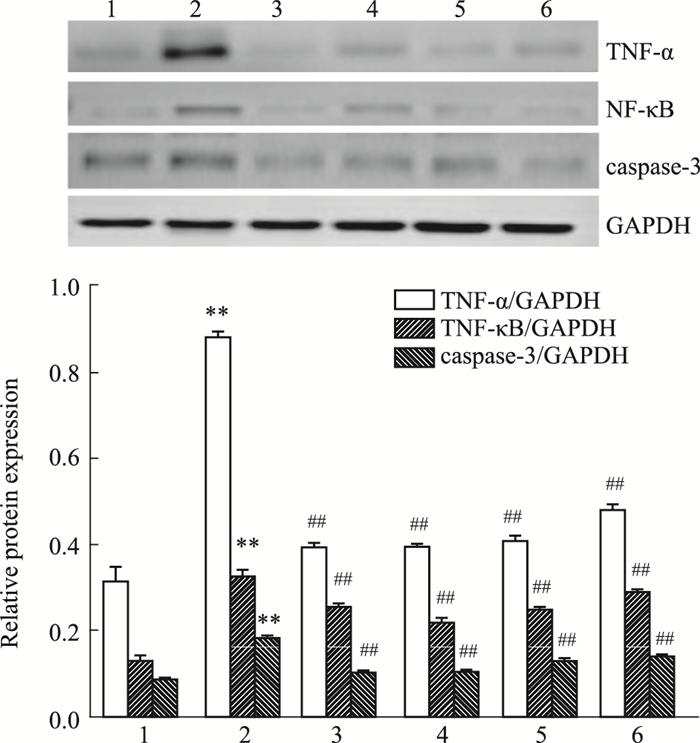
如Fig 2所示, 与正常组小鼠相比, 模型组小鼠肝脏中的TNF-α、NF-κB、caspase-3蛋白表达明显增加(P < 0.01);与模型组相比, EACR 3个剂量组小鼠的TNF-α、NF-κB、caspase-3蛋白的表达明显降低(P < 0.01)。
|
| Fig 2 Effects of EACR on expressions of TNF-α, NF-κB and caspase-3 in liver tissues of mice(x±s, n=4) 1:Normal; 2:Model; 3:Positive control; 4:EACR high dose group; 5:EACR middle dose group; 6:EACR low dose group.**P < 0.01 vs normal group; ##P < 0.01 vs model group. |
CCl4是亲肝毒物, 被认为是化学性肝损伤模型的经典诱导剂[4]。化学性肝损伤是保肝药物筛查常用的模型[5]。正常情况下, AST、ALT主要存在于胞质内, 极少存在于血清中。CCl4进入机体后, 在肝微粒体酶的作用下代谢为三氯甲基, 三氯甲基可破坏肝细胞膜结构, 增加肝细胞膜的通透性[6], 导致胞内酶AST、ALT从胞内大量释放到血液中, 引起血液中的AST、ALT升高。因此, 血清中的AST、ALT可以直接反映肝脏的损伤程度[7]。本研究结果表明, 模型组小鼠的AST、ALT明显升高, 说明造模成功。联苯双脂滴丸阳性对照组及EACR各给药组的AST、ALT明显降低, 说明预防性给予EACR能减轻CCl4对小鼠肝脏造成的损伤。CCl4在体内经过氧化还原反应产生大量的自由基, 这些自由基可攻击细胞膜上的不饱和脂肪酸, 诱发脂质过氧化反应[8]。MDA是脂质过氧化反应的终产物之一, 在CCl4诱导肝损伤的过程中逐渐积累, 并与生物大分子结合成醛, 进一步破坏肝细胞膜的结构和功能[9]。SOD作为有效的金属酶, 能够催化超氧化物阴离子歧化为H2O2和O2。GSH-Px催化毒性过氧化物还原成无毒的羟基化合物, 同时还能将H2O2和氢过氧化物还原成水, 从细胞膜上除去脂质过氧化氢, 从而终止脂质过氧化反应[10]。GSH是细胞内主要的抗氧化剂, 能与细胞色素P450的代谢产物结合, 达到清除自由基的作用, 进而保护肝脏。本研究结果表明, 阳性对照组及EACR 3个给药组能有效降低MDA水平, 提高SOD、GSH、GSH-Px的水平, 表明EACR的保肝作用可能与其参与氧化应激反应有关。
研究表明, 细胞凋亡及炎症反应可能参与CCl4诱导的急性肝损伤。IL-1、IL-6通常被认为是炎症反应的生物标志物。CCl4进入机体后, 刺激枯否细胞分泌IL-1、IL-6, 使得IL-1、IL-6的分泌增加, 加速炎症反应[11]。TNF-α是由单核巨噬细胞分泌的内源性细胞因子, 它通过激活细胞内的通路以调节炎症因子和细胞增殖, 加速炎症反应的进程[12]。NF-κB参与调控炎症因子的转录, 抑制其表达能够抑制炎症反应的进行[13]。凋亡是由多个基因控制的细胞生理自我灭亡的过程[14]。caspase-3是caspase家族中一种重要的促进细胞凋亡的蛋白酶, 是细胞凋亡的中心效应物, 它能在裂开它的基底物的同时改变细胞的形态及生化特性, 促进炎症细胞的凋亡[15]。本实验结果表明, 阳性对照组及EACR各给药组能降低IL-1、IL-6的水平, 下调TNF-α、NF-κB、caspase-3的蛋白表达。表明EACR的保肝作用可能与其参与抑制炎症因子有关。
综上所述, EACR通过清除氧自由基及抑制炎症因子释放, 从而减轻CCl4对小鼠肝脏的损害。
| [1] |
Xu X, Liang T, Wen Q, et al. Protective effects of total extracts of Averrhoa carambola L. (Oxalidaceae) roots on streptozotocin-induced diabetic mice[J]. Cell Physiol Biochem, 2014, 33(5): 1272-82. doi:10.1159/000358695 |
| [2] |
徐小惠, 范氏泰和, 韦晓洁, 等. 杨桃根总提取物对糖尿病小鼠肾功能及其抗氧化应激作用的研究[J]. 中国药理学通报, 2017, 33(1): 95-100. Xu X H, Pham H T, Wei X J, et al. Study of the extract of Averrhoacarambola L.root on renal function in diabetic mice and its anti-oxidative action[J]. Chin Pharmacol Bull, 2017, 33(1): 95-100. doi:10.3969/j.issn.1001-1978.2017.01.017 |
| [3] |
Gao Y, Huang R, Gong Y, et al. The antidiabetic compound 2-dodecyl-6-methoxycyclohexa-2, 5-diene-1, 4-dione, isolated from Averrhoa carambola L., demonstrates significant antitumor potential against human breast cancer cells[J]. Oncotarget, 2015, 6(27): 24304-19. |
| [4] |
Cetinkaya A, Kantarceken B, Bulbuloglu E, et al. The effects of L-carnitine and N-acetylcysteine on carbontetrachloride induced acute liver damage in rats[J]. Bratisl Lek Listy, 2013, 114(12): 682-8. |
| [5] |
Weber L W, Boll M, Stampfl A. Hepatotoxicity and mechanism of action of Haloalkanes:carbon tetrachloride as a toxicological model[J]. Crit Rev Toxicol, 2003, 33(2): 105-36. doi:10.1080/713611034 |
| [6] |
Wang W, Wang S, Liu J, et al. Sesquiterpenoids from the root of Panax Ginseng protect CCl4-induced acute liver injury by anti-inflammatory and anti-oxidative capabilities in mice[J]. Biomed Pharmacother, 2018, 102: 412-9. doi:10.1016/j.biopha.2018.02.041 |
| [7] |
Domitrovi′c R, Rashed K, Cvijanovi′c O, et al. Myricitrin exhibits antioxidant, anti-inflammatory and antifibrotic activity in carbon tetrachloride-intoxicated mice[J]. Chem Biol Interact, 2015, 230: 21-9. doi:10.1016/j.cbi.2015.01.030 |
| [8] |
Yang C, Li L, Ma Z, et al. Hepatoprotective effect of methyl ferulic acid against carbon tetrachloride-induced acute liver injury in rats[J]. Exp Ther Med, 2018, 15(3): 2228-38. |
| [9] |
Roy S, Benz F, Alder J, et al. Down-regulation of miR-192-5p protects from oxidative-stress induced-acute liver injury[J]. Clin Sci (Lond), 2016, 130(14): 1197-207. doi:10.1042/CS20160216 |
| [10] |
Tang D, Wang F, Tang J, et al. Dicranostiga leptopodu (Maxim.) Fedde extracts attenuated CCl4-induced acute liver damage in mice through increasing anti-oxidative enzyme activity to improve mitochondrial function[J]. Biomed Pharmacother, 2017, 85: 763-71. doi:10.1016/j.biopha.2016.11.097 |
| [11] |
Park E J, Lee J H, Yu G Y, et al. Dietary and genetic obesity promote liver inflammation and tumorigenesis by enhancing IL-6 and TNF expression[J]. Cell, 2010, 140(2): 197-208. doi:10.1016/j.cell.2009.12.052 |
| [12] |
Parola M, Leonarduzzi G, Biasi F, et al. Vitamin E dietary supplementation protects against carbon tetrachloride-induced chronic liver damage and cirrhosis[J]. Hepatology, 2010, 16(4): 1014-21. |
| [13] |
Xia Z B, Meng F R, Fang Y X, et al. Inhibition of NF-κB signaling pathway induces apoptosis and suppresses proliferation and angiogenesis of human fibroblast-like synovial cells in rheumatoid arthritis[J]. Medicine (Baltimore), 2018, 97(23): e10920. doi:10.1097/MD.0000000000010920 |
| [14] |
Green D R, Fitzgerald P. Just so stories about the evolution of apoptosis[J]. Curr Biol, 2016, 26(13): R620-7. doi:10.1016/j.cub.2016.05.023 |
| [15] |
Shin S, Sung B J, Cho Y S, et al. An anti-apoptotic protein human survivin is a direct inhibitor of caspase-3 and -7[J]. Biochemistry, 2001, 40(4): 1117-23. doi:10.1021/bi001603q |

