

2. 西北大学生命科学学院 陕西省生物医药重点实验室, 陕西 西安 710069
2. Biomedicine Key Lab of Shanxi Province, College of Life Science, Northwest University, Xi′an 710069, China
抑郁症是一种情感障碍类疾病, 在中国医学属于抑郁类病症的范畴, 从青少年时期开始发病, 具有高发病率和高自杀率, 严重威胁人类健康。其发病机制不明, 致使抗抑郁的药物疗效有限[1]。近年来, 中医、中药作为研究抑郁的发病机制以及抗抑郁药用资源, 引发了人们广泛的关注[2]。尽管抑郁症的确切病因及病理机制尚不清楚, 但在前人的研究基础上, 已形成了多种有关抑郁症的神经生物学假说, 包括单胺能假说、神经退行性假说、细胞因子假说等, 其中基于5-羟色胺(5-hydroxytryptamine, 5-HT)系统的单胺类递质失调假说在研究抑郁发生机制中起到重要作用[3]。
5-HT作为一种抑制性的神经递质, 在大脑皮层及神经突触内含量极高, 必须通过相应受体的介导才能产生作用。大量研究表明, 5-HT1A受体在抑郁的发病与抗抑郁行为中起调节作用, 可能作为抗抑郁药的作用靶点[4-5]。脑内5-HT1A受体能调节应激适应过程, 而且对应激刺激引起的情感障碍具有保护作用。与5-HT1A受体不同的是, 5-HT转运体只有一种5-HT转运蛋白(serotonin transporters, 5-HTT)。5-HTT清除突触间隙的5-HT含量, 决定了突触后受体介导信号的量以及持续时间, 在5-HT神经传递系统具有重要作用[3]。也正因如此, 5-HTT的表达也与抑郁症密切相关。氟西汀作为一种选择性的5-HT重摄取抑制剂, 在抑郁症、抑郁障碍等方面都有较好应用[6]。因此, 在本实验中, 将氟西汀作为阳性药使用。欧前胡素(imperatorin, IMP)是从中草药白芷中提取分离的呋喃香豆类化合物, 用于保持传统抗癫痫药剂的活性, 改善认知损伤, 此外还有抗惊厥和镇静催眠作用[2, 7-8]。目前, IMP作用于情绪障碍的研究有所进展, 但在产前应激(prenatal stress, PS)引起的抑郁样作用未见报道。本实验拟通过产前束缚应激模型, 建立子代抑郁模型, 探究IMP对PS子代大鼠的抗抑郁作用及相关机制。
1 材料 1.1 实验动物Sprague-Dawley(SD)大鼠, 购买于西安交通大学动物研究中心。在西北大学SPF动物房饲养, 使用许可证号:SYXK(陕)2010-004, 室温控制在(23~27)℃, 湿度50%~60%, 昼夜各12 h, 提供充足的水和食物。
1.2 药物与试剂IMP(陕西慧科植物开发有限公司), 经高效液相色谱测定, 其纯度>98%;氟西汀(常州四药, 生产批号:201711161);5-HT ELISA试剂盒(美国ADL公司); RNA提取试剂盒、反转录试剂盒(宝生物工程有限公司)。
1.3 仪器光学显微镜(日本Olympus公司); 酶标仪(美国PerkinElmer公司); 大鼠束缚应激容器(西安玻璃制品厂); 摄像机(日本东京Sony公司); 实时定量PCR仪(Bio-Rad公司); 离心机(德国Eppendorf公司)。
2 方法 2.1 动物分组与造模SD大鼠以3 :1将♀大鼠(250±20)g与♂大鼠(280±20)g进行合笼。次日清晨进行阴道涂片检测, 如果涂片有精子呈阳性, 记为妊娠d 0, 怀孕的♀鼠单独饲养。在♀大鼠怀孕的d 14~20进行单独的束缚应激(将孕鼠放入1个瓶底和瓶盖都开孔、通气的透明瓶子里, 1 d 3次, 每次45 min, 每次束缚应激间隔时间不少于2 h, 直径6.8 cm)。♂子代大鼠分为5组, 每组8只。分别是正常组、模型组、阳性组、IMP低、高剂量组(15、30 mg·kg-1·d-1)。正常组与模型组每天灌服等体积的0.5%羧甲基纤维素钠溶液(CMC-Na), 阳性组灌服盐酸氟西汀溶液(10 mg·kg-1·d-1)。给药组从子代出生后d 30开始, 灌胃给药4周, 使用0.5%的CMC-Na溶解IMP。
2.2 糖水偏好实验测定前禁水、禁食24 h, 测定4 h饮用2%蔗糖溶液的量[9], 糖水偏好的计算公式为:糖水消耗量/总液体消耗×100%。
2.3 强迫游泳实验水温(23~25) ℃的圆桶(桶高50 cm, 直径20 cm)水深40 cm, 强迫游泳8 min, 记录大鼠的不动时间(s), 大鼠在水中处于被动漂浮, 同时停止挣扎达到3 s以上, 则认为大鼠为不动状态。不动时间的计算公式为:不动时间/总时间×100%。
2.4 旷场实验旷场箱为白线5×5等分(150 cm×150 cm×49.5 cm, 四壁涂为黑色, 底部绿色), 箱子的中心区域(3×3=9的方块)再细分为1个大的中心区域和8个小的中心区域, 每次放入1只大鼠在小的中心区域的同一侧, 观察大鼠的行为, 记录5 min内大鼠在中心区域逗留的时间, 穿越总格子数、穿越中心格子数、直立次数以及理毛次数。
2.5 ELISA实验行为学结束后, 对5组♂子代大鼠断头取脑, 分离出前额叶皮层和海马, 并用液氮冰冻, -80 ℃保存。按照ELISA说明书, 使用相对应定量的抗体对5-HT含量进行测定, 将样品加入到预先涂有一抗的96孔板的每一个孔里, 之后每个孔加入生物素结合试剂和酶结合试剂, 将孔板在37 ℃孵育30 min, 将板子用蒸馏水清洗5次, 并用酶标仪测量, 数据以ng·g-1的蛋白含量显示。
2.6 RNA提取和实时定量PCR总RNA用TRIzol法从组织中提取, 使用纳米级分光光度法进行定量。每个mRNA样品使用随机引物和逆转录试剂盒提取1 μg合成cDNA链。使用SYBR Green real-time PCR Master Mix扩增5-HTT、5-HT1AR PCR产物。大鼠特异性引物5-HTT正向序列:5′- GGCGGAGATGAGGAATGAAG-3′, 反向序列:5′-AAGAAGATGATGGCAAAGAACG-3′; 5-HT1AR正向序列:5′- CCACGGCTACACCATCTAC-3′, 反向序列:5′- TGACAGTCTTGCGGATTCG -3′。
2.7 统计学分析实验数据以x±s表示。通过GraphPad Prism software 5.0软件, 使用单因素方差分析法对不同组的数据进行分析, 多样本均数间两两比较采用LSD法进行分析。
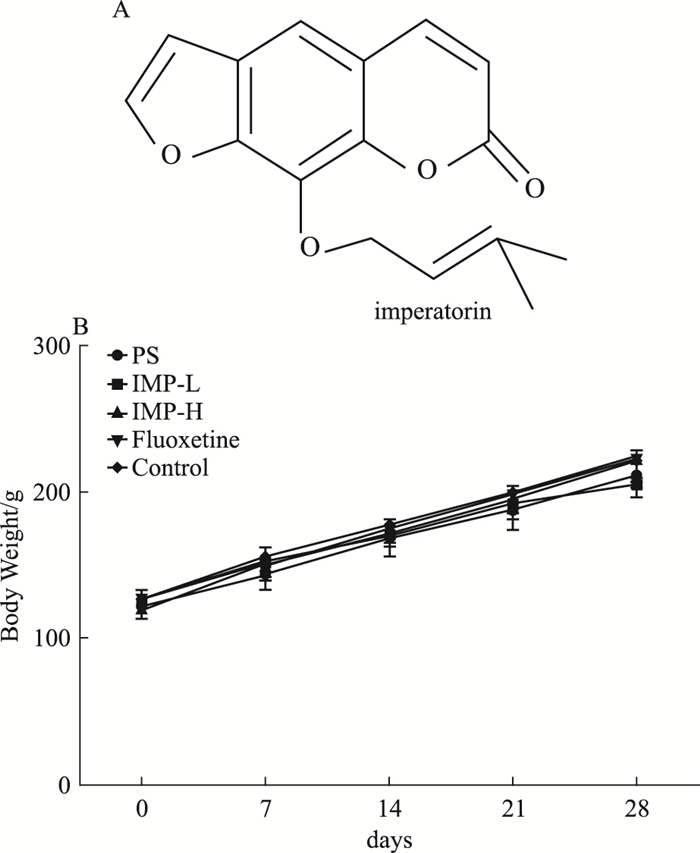
3 结果 3.1 IMP对PS子代大鼠体质量的影响如Fig 1所示, 与对照组相比, IMP给药组或者氟西汀组的子代♂大鼠体质量在d 0、7、14、21、28并没有明显变化。
|
| Fig 1 Chemical structure(A) and effect of IMP on body weight in prenatally stressed male offspring rats(B) |
如Tab 1所示, 与对照组相比, PS组子代♂大鼠对2%的糖水消耗百分比明显减少(P < 0.01)。IMP组和氟西汀组的子代♂大鼠糖水偏好百分比明显增长(P < 0.01), IMP给药组与氟西汀组比较差异无显著性。
| Group | Dose/mg·kg-1 | Sucrose preference/% |
| Control | - | 11.60±1.72 |
| Model | - | 4.67±0.84## |
| Fluoxetine | 10 | 16.17±2.04** |
| IMP | 15 | 14.60±0.75** |
| IMP | 30 | 13.80±1.36** |
| ##P < 0.01 vs control; **P < 0.01 vs model | ||
如Tab 2所示, 与对照组相比, PS组不动时间和不动时间百分比明显增加(P < 0.01)。IMP组和氟西汀组的子代♂大鼠不动时间和不动时间百分比都明显减少(P < 0.05, P < 0.01), IMP给药组与氟西汀组比较差异无显著性。
| Group | Dose/ mg·kg-1 |
Immobility time/s |
Immobility time/% |
| Control | - | 31.13±2.945 | 6.48±0.61 |
| Model | - | 154.30±30.77## | 38.75±6.23## |
| Fluoxetine | 10 | 93.75±19.47* | 19.74±1.97* |
| IMP | 15 | 70.00±16.06** | 16.46±3.31** |
| IMP | 30 | 49.00±11.15** | 14.38±4.58** |
| ##P < 0.01 vs control; *P < 0.05, **P < 0.01 vs model | |||
如Tab 3所示, PS组穿越总格子数、穿越的中央格子数、直立次数、理毛次数较对照组明显减少(P < 0.01)。IMP组和氟西汀组的子代♂大鼠穿越总格子数、穿越的中央格子数、直立次数、理毛次数均明显增加(P < 0.05, P < 0.01), IMP给药组与氟西汀组比较差异无显著性。
| Group | Dose/mg·kg-1 | Number of total crossing | Number of center crossing | Number of rearing | Number of grooming |
| Control | - | 174.70±4.37 | 64.67±2.78 | 30.75±2.30 | 6.83±0.60 |
| Model | - | 113.00±4.08## | 33.50±4.20## | 11.00±2.74## | 2.83±0.60## |
| Fluoxetine | 10 | 184.30±3.98** | 70.67±3.27** | 34.00±4.62** | 6.83±0.60** |
| IMP | 15 | 164.30±8.91** | 50.83±3.01* | 28.33±3.21* | 5.50±0.43* |
| IMP | 30 | 197.70±3.19** | 68.50±4.33** | 33.00±5.76** | 7.33±0.49** |
| ##P < 0.01 vs control; *P < 0.05, **P < 0.01 vs model | |||||
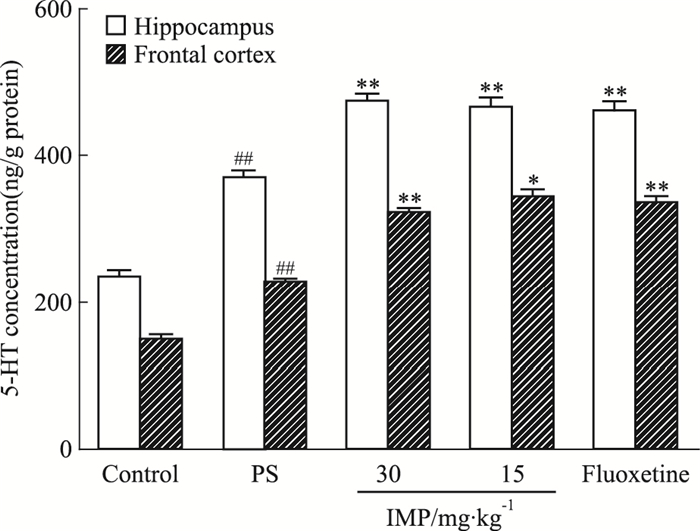
如Fig 2所示, PS组的5-HT浓度明显低于对照组(P < 0.01)。IMP给药4周后, 能够明显逆转PS子代大鼠海马和前额叶皮层组织中5-HT的浓度(P < 0.05, P < 0.01), 与氟西汀组的结果有着相同的趋势, 差异无显著性。
|
| Fig 2 Effect of IMP on 5-HT concentration in hippocampus andfrontal cortex of prenatally stressed male offspring(x±s, n=8) ##P < 0.01 vs control; *P < 0.05, **P < 0.01 vs PS |
如Fig 3所示, 与对照组相比, PS组5-HT1AR mRNA表达明显减少, 而5-HTT mRNA的表达明显增加(P < 0.05, P < 0.01)。与PS组相比, IMP给药4周后, 5-HT1AR mRNA表达明显增加, 而5-HTT mRNA表达明显减少(P < 0.05, P < 0.01), IMP给药组与氟西汀组比较差异无显著性。

|
| Fig 3 Effect of IMP on 5-HTT(A) and5-HT1AR(B) mRNA expression in hippocampus andfrontal cortex of prenatally stressed male offspring(x±s, n=8) #P < 0.05, ##P < 0.01 vs control; *P < 0.05, **P < 0.01 vs PS |
随着社会经济的快速发展, 人们长期承受来自工作、生活、家庭等各种压力, 过度长期应激可增加人们精神负担、不良情绪和疾病的易患性, 特别是某些特定生理阶段应激对健康的影响更为明显。妊娠期是妇女生活的重要时期, 是女性应激的易患期。临床资料显示, 新生儿及成年后焦虑、抑郁、认知障碍等疾病发病率的不断升高, 与母代在妊娠期遭受慢性应激有关。有研究表明, 孕妇处于长期情绪困扰, 可增加子代焦虑、抑郁等情绪障碍的发病率[10]。动物实验也表明, 产前应激后的子代大鼠表现出明显的焦虑及抑郁样行为。IMP是一种广泛存在于白芷、川芎、香菜等中药及食材中的呋喃香豆素类化合物, 已被证明具有抗炎、舒张血管、抗惊厥、镇静催眠等功效[11]。在本实验研究发现, 与对照组相比, IMP组或者阳性药氟西汀组的子代♂大鼠体质量在d 0、7、14、21、28并无明显变化。通过4周的IMP灌胃给药, 可明显上调子代抑郁♂大鼠的糖水偏好度、强迫游泳不动时间、穿越总格子数、穿越中间格子数、直立和理毛次数。提示IMP可明显改善♂子代大鼠抑郁样行为。
抑郁病的发病机制与遗传、神经递质紊乱、激素异常、不良社会心理因素等一系列因素相关, 由这些因素导致的5-HT缺乏是普遍认可的抑郁症发病机制之一。由于5-HT1A受体被看作应激调节过程的一个重要媒介, 在应激引起的抗精神紊乱过程中起保护作用。与此同时, 5-HT的摄取过程由5-HTT控制, 所以研究5-HT1AR、5-HTT对了解抑郁症发病机制有重要意义。5-HT浓度的增加有助于海马神经形成, 从而使抑郁症得以改善, 促进抑郁样行为的恢复[12]。多数研究和抑郁症自杀者的尸检结果证实, 在抑郁症患者脑内, 分布于皮质-边缘系统的突触后5-HT受体表达降低, 结合能力下降[4]。本实验结果表明, IMP可以提高海马及前额叶皮层中5-HT浓度及5-HT1A受体的mRNA表达, 并下调5-HTT mRNA表达。IMP对5-HTT的下调可能与降低5-HT的再摄取有关, 从而增加5-HT的浓度。这表明IMP抗抑郁作用可能与5-HT的浓度以及5-HT1AR、5-HTT mRNA的表达量有关。
研究发现, IMP可以抑制尼古丁引起的焦虑, 并改善学习记忆行为[13]。此外, IMP还可通过改变谷氨酸释放, 改善癫痫发作[14]。IMP不仅广泛存在于常见中草药白芷中, 而且在烹调香料如香菜、茴香中也有较高含量。本研究结果表明, IMP可明显降低产前应激引起的子代抑郁样行为, 其机制可能与5-HT能神经系统有关, 提示IMP可能可以作为一个潜在用于预防和治疗抑郁样行为的药物。
| [1] |
张兵, 李扬. 针对谷氨酸能系统的抗抑郁药物的研究进展[J]. 中国药理学通报, 2014, 30(9): 1197-2000. Zhang B, Li Y. Research progress of the antidepressants targeting the glutamate receptors[J]. Chin Pharmacol Bull, 2014, 30(9): 1197-2000. doi:10.3969/j.issn.1001-1978.2014.09.004 |
| [2] |
Luszczki J J, Wojda E, Andres-Mach M, et al. Anticonvulsant and acute neurotoxic effects of imperatorin, osthole and valproate in the maximal electroshock seizure and chimney tests in mice:a comparative study[J]. Epilepsy Res, 2009, 85(2-3): 293-9. doi:10.1016/j.eplepsyres.2009.03.027 |
| [3] |
郑莉明, 史亚飞, 吴皓萌, 等. 中枢5-HT能系统在早发性抑郁中的作用研究[J]. 中国药理学通报, 2015, 31(1): 19-23. Zheng L M, Shi Y F, Wu H M, et al. Research on effect of central 5-HTergic system in early-onset depression[J]. Chin Pharmacol Bull, 2015, 31(1): 19-23. doi:10.3969/j.issn.1001-1978.2015.01.005 |
| [4] |
陈红霞, 张黎明, 薛瑞, 等. 以5-HT1A受体为靶标的抗抑郁药物研究进展[J]. 军事医学, 2013, 37(8): 624-30. Chen H X, Zhang L M, Xue R, et al. Progress of antidepressant drugs based on 5-HT1A receptor as a new target[J]. Milit Med Sci, 2013, 37(8): 624-30. |
| [5] |
Sharp T, Cowen P J. 5-HT and depression:is the glass half-full[J]. Curr Opin Pharmacol, 2011, 11(1): 45-51. doi:10.1016/j.coph.2011.02.003 |
| [6] |
Kiryanova V, Meunier S J, Dyck R H. Behavioural outcomes of adult female offspring following maternal stress and perinatal fluoxetine exposure[J]. Behav Brain Res, 2017, 331(7): 84-91. |
| [7] |
Budzynska B, Boguszewska-Czubara A, Kruk-Slomka M, et al. Effects of imperatorin on scopolamine-induced cognitive impairment and oxidative stress in mice[J]. Psychopharmacology, 2015, 232(5): 931-42. doi:10.1007/s00213-014-3728-6 |
| [8] |
Shi M M, Piao J H, Xu X L, et al. Chinese medicines with sedative-hypnotic effects and their active components[J]. Sleep Med Rev, 2016, 29(3): 108-18. |
| [9] |
Wang S S, Mu R H, Li C F, et al. MicroRNA-124 targets glucocorticoid receptor and is involved in depression-like behaviors[J]. Prog Neuropsychopharmacology Biol Psychiatry, 2017, 79(ptB): 417-25. |
| [10] |
Fatima M, Srivastav S, Mondal A C. Prenatal stress and depression associated neuronal development in neonates[J]. Int J Dev Neurosci, 2017, 60: 1-7. doi:10.1016/j.ijdevneu.2017.04.001 |
| [11] |
Cao Y J, He X, Wang N, et al. Effects of imperatorin, the active component from Radix Angelicae(Baizhi), on the blood pressure and oxidative stress in 2K, 1C hypertensive rats[J]. Phytomedicine, 2013, 20(12): 1048-54. doi:10.1016/j.phymed.2013.04.021 |
| [12] |
Han X, Wu H, Yin P, et al. Electroacupuncture restores hippocampal synaptic plasticity via modulation of 5-HT receptors in a rat model of depression[J]. Brain Res Bull, 2018, 139: 256-62. doi:10.1016/j.brainresbull.2018.03.004 |
| [13] |
Łuszczki J J, Andres-Mach M, Gleńsk M, et al. Anticonvulsant effects of four linear furanocoumarins, bergapten, imperatorin, oxypeucedanin, and xanthotoxin, in the mouse maximal electroshock-induced seizure model:a comparative study[J]. Pharmacol Rep, 2010, 62(6): 1231-6. doi:10.1016/S1734-1140(10)70387-X |
| [14] |
Wang S J, Lin T Y, Lu C W, et al. Osthole and imperatorin, the active constituents of Cnidium monnieri(L.) Cusson, facilitate glutamate release from rat hippocampal nerve terminals[J]. Neurochem Int, 2008, 53(6-8): 416-23. doi:10.1016/j.neuint.2008.09.013 |

