


天然多胺(polyamine, PA)包括腐胺(putrescine, Put)、精脒(spermidine, Spd)和精胺(spermine, Spm),是一类在真核细胞中普遍存在的、带高密度正电荷的有机小分子[1],可通过静电作用力与细胞中DNA、RNA、蛋白质、磷脂等带负电荷的生物大分子产生相互作用,参与细胞增殖、分化、发育、细胞应激等重要的生理过程[2-3]。研究发现,细胞内多胺水平升高能促进肿瘤的发生发展,而多胺含量降低则能抑制肿瘤细胞增殖,多胺代谢途径因此逐渐成为肿瘤防治和抗癌药物设计的新靶标[4-5]。
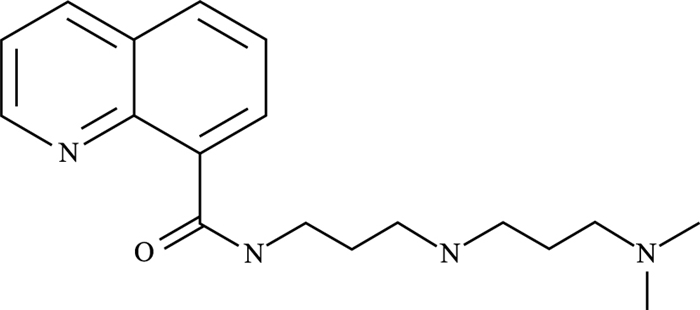
多种酶和蛋白因子参与了细胞内多胺代谢的调控,其中精胺氧化酶(spermine oxidase, SMO)在多胺分解代谢中发挥重要作用。该酶直接以Spm为底物,将其氧化为Spd,同时生成3-氨基丙醛和H2O2[6]。研究发现,SMO表达异常导致的多胺代谢紊乱与包括肿瘤在内的多种疾病的发生、发展密切相关[7],提示特异性靶向SMO的小分子抑制剂在相关疾病的防治中具有重要潜在应用价值。由于目前国内外对SMO小分子抑制剂的研究报道不多,这在很大程度上限制了SMO作为抗肿瘤分子靶点的基础与临床应用研究。本研究在前期工作中,运用基于药效团的计算机辅助药物设计和高通量虚拟筛选技术,结合分子和细胞水平上的实验验证,获得了一种新型SMO小分子抑制剂SI-4650(SMO inhibitor-4650,其分子结构见Fig 1),并发现该抑制剂对人非小细胞肺癌A549细胞具有明显抑制活性。为进一步评价SI-4650的抑瘤谱和对不同肿瘤细胞的杀伤效应,本研究分析了SI-4650对人胶质瘤U87MG细胞多胺代谢、增殖、迁移、凋亡和自噬的影响,为SI-4650在肿瘤防治中的应用提供基础研究支撑。
|
| Fig 1 Molecular structure of SI-4650 |
人胶质瘤U87MG细胞购于中国培养物典藏中心(武汉),由本实验室传代保存。
1.2 试剂SI-4650(荷兰Specs生物特殊化合物公司);二甲基亚砜(dimethyl sulfoxide,DMSO, 美国Sigma公司);DMEM培养基(美国Gibco公司);胎牛血清、青霉素/链霉素双抗(天津灏洋生物);BCA蛋白定量试剂盒、ECL超敏显影液(美国Thermo Scientific公司);RIPA蛋白裂解液(武汉Servicebio公司);LC3-Ⅰ/Ⅱ抗体、P62抗体、Beclin-1抗体、聚腺苷二磷酸-核糖聚合酶(poly-ADP-ribose polymerase, PARP)抗体,均购自美国CST公司;Bax抗体、Bcl-2抗体(美国Santa Cruz公司);β-actin抗体(北京科美博瑞);pEGFP-LC3质粒(美国Add Gene公司);FITC-Annexin V凋亡检测试剂盒(美国BD公司)。
1.3 仪器细胞超净台(上海新苗);MCD175型恒温CO2细胞培养箱、-80 ℃低温冷冻冰箱(日本SANYO公司);5424R台式高速冷冻离心机(德国Eppendorf公司);Waters e2695高效液相色谱分析仪(美国Waters公司);FACSVerse流式细胞仪(美国BD公司);A1+激光共聚焦显微镜、TE2000-S荧光倒置显微镜(日本Nikon公司);全波长酶标仪(美国Thermo公司);Sirius化学发光检测仪(德国Berthold公司);ChemiScope mini化学发光成像显影仪(上海勤翔)。
2 方法 2.1 SI-4650的配制称取SI-4650干粉溶解于DMSO中,配制成浓度为100 mmol·L-1的药物储存液,于-20 ℃低温保存。使用前,用DMEM完全培养基将药物储存液稀释至所需浓度。
2.2 MTT检测细胞增殖情况将对数生长期的U87MG细胞悬液(5×106·L-1)接种于96孔细胞培养板中,每孔200 μL(1.0×103个/孔)。置37 ℃、5% CO2细胞培养箱中24 h后,换用含不同浓度SI-4650的DMEM培养基继续培养,每个药物浓度设置4个复孔。分别继续培养24、48、72 h后,弃培养基,每孔加入MTT试剂200 μL(终浓度0.2 g·L-1),于37 ℃、5% CO2培养箱中孵育4 h后,弃MTT试剂,每孔加入150 μL DMSO充分溶解沉淀,使用酶标仪于490 nm波长处检测每孔吸光度值(A)。药物对U87MG细胞生长的抑制率=[1-(实验组A值-空白组A值)/(阴性对照组A值-空白组A值)]×100%。
2.3 化学发光法分析SI-4650对U87MG细胞内SMO、乙酰多胺氧化酶(N1-acetylpolyamine oxidase, APAO)酶活性的影响向用不同浓度SI-4650处理48 h后和对照U87MG细胞中,加入0.083 mol·L-1甘氨酸缓冲液(pH 8.0)200 μL,-80 ℃条件低温冻融法裂解细胞,4 ℃、12 000 r·min-1离心10 min,收集上清,并用BCA法测定其总蛋白含量。各样本取相同质量的总蛋白液,根据参考文献配制酶反应体系[8],以化学发光法检测上清液中SMO和APAO的酶活性。
2.4 HPLC法检测细胞内多胺含量收集用不同浓度SI-4650处理48 h后和对照U87MG细胞,加入800 μL细胞裂解液,冰上裂解30 min,4 ℃、12 000 r·min-1离心15 min后,收集上清液至新的4 mL EP管中。BCA法测定上清中的蛋白浓度后,取总蛋白含量相同的细胞裂解液,用ddH2O补足体积至800 μL。加入1 mmol·L-1 DAH 20 μL(内标分子)、2 mol·L-1 NaOH 500 μL、苯甲酰氯10 μL,涡旋振荡30 s,40 ℃水浴20 min后,加入2 mL饱和NaCl溶液终止反应。反应液用2 mL乙醚颠倒混匀萃取,静置分层后,留取上层乙醚液,重复萃取3次,合并上层萃取乙醚液,通风橱中挥发至干。用1 mL甲醇溶解沉淀后,经0.22 μm微孔滤膜过滤至样品瓶中,上Waters-e2695高效液相色谱分析仪进行HPLC分析。HPLC的分析条件:Luna C18色谱柱(150 mm×4.6 mm,5 μm)为固定相,乙腈-水(40 :60)为流动相,流速1 mL·min-1,检测波长为254 nm,柱温30 ℃。
2.5 Transwell法分析细胞迁移能力收集用不同浓度SI-4650处理48 h后和对照U87MG细胞,并用含0.2% BSA的DMEM培养基重悬(2.5×108·L-1)。向24孔细胞培养板中加含20% FBS的DMEM培养基(每孔800 μL),将Transwell小室放入加有上述培养基的培养孔中,并分别向小室内加入细胞悬液200 μL,置37 ℃、5% CO2培养箱中继续培养48 h后,取出Transwell小室,轻轻吸弃小室内的细胞培养基,用1×PBS润洗小室3次,后用4%多聚甲醛固定小室30 min。用1×PBS润洗小室3次,再以结晶紫溶液染色15 min,再次用1×PBS润洗小室3次后,以湿棉签拭去小室内侧面的细胞,将小室放在滴有1×PBS的载玻片上,于倒置显微镜下随机选取3个观察视野,计数每个视野中的细胞数。
2.6 流式细胞术检测细胞周期收集用不同浓度SI-4650分别处理24、48 h后及对照U87MG细胞,室温1 000 r·min-1离心3 min后,弃上清。用1.5 mL预冷75%乙醇(1×PBS配制)重悬细胞,4 ℃固定过夜。室温1 000 r·min-1离心5 min后,弃上清,加1.5 mL 1×PBS洗涤细胞,室温1 000 r·min-1离心5 min,弃上清。用500 μL 1×Binding buffer(PBS配制,含50 μg·L-1 RNase和0.1% TritonX-100)重悬细胞后,加0.5 g·L-1碘化丙啶(propidium iodide, PI)20 μL,37 ℃水浴避光条件下染色30 min后,经300目尼龙网将细胞悬液过滤于流式分析试管中,上流式细胞仪检测细胞周期。
2.7 流式细胞术检测细胞凋亡收集用不同浓度SI-4650处理48 h后和对照U87MG细胞,室温1 000 r·min-1离心3 min后,弃上清。参照FITC-Annexin V检测试剂盒说明书,用100 μL 1×Binding buffer重悬细胞,加5 μL FITC-Annexin V和5 μL PI后混匀,25 ℃避光孵育15 min,再以400 μL 1×Binding buffer重悬混匀后,上流式细胞仪检测细胞凋亡。
2.8 激光共聚焦显微镜观察细胞自噬小体形成将U87MG细胞悬液(5×107·L-1)接种于Confocal专用玻璃底细胞培养皿中,每皿接种3 mL(1.5×105个细胞/皿)。继续培养至细胞融合度约80%时,根据Thermo TurboFect转染试剂标准说明书,用2 μg pEGFP-LC3质粒转染U87MG细胞。转染培养24 h后,换用含不同浓度SI-4650的DMEM培养基继续培养48 h,然后在激光共聚焦显微镜下观察外源性重组绿色荧光蛋白GFP-LC3的亚细胞定位,分析U87MG细胞中自噬小体的形成情况。
2.9 Western blot检测细胞凋亡、自噬相关蛋白表达收集用不同浓度SI-4650处理48 h后和对照U87MG细胞,加100 μL RIPA裂解液冰上裂解30 min,4 ℃、12 000 r·min-1离心15 min,将上清液转移至新的1.5 mL EP管中。BCA法测定上清中的总蛋白浓度,取含60 μg总蛋白的上清液,加1/4体积5×上样缓冲液,100 ℃加热10 min。蛋白样品经SDS-PAGE电泳分离后,电转至用5%脱脂牛奶(TBST配制)PVDF膜,室温封闭2 h后,以TBST洗膜10 min×3次;加对应一抗于4 ℃孵育过夜,TBST洗膜10 min×3次;再用对应二抗室温孵育2 h,TBST洗膜10 min×3次,最后用ECL化学发光法显影并记录结果。
2.10 统计学方法采用SPSS 13.0统计软件。计量资料以x±s表示,两组间比较采用独立样本t检验,设置检验水准为α=0.05。
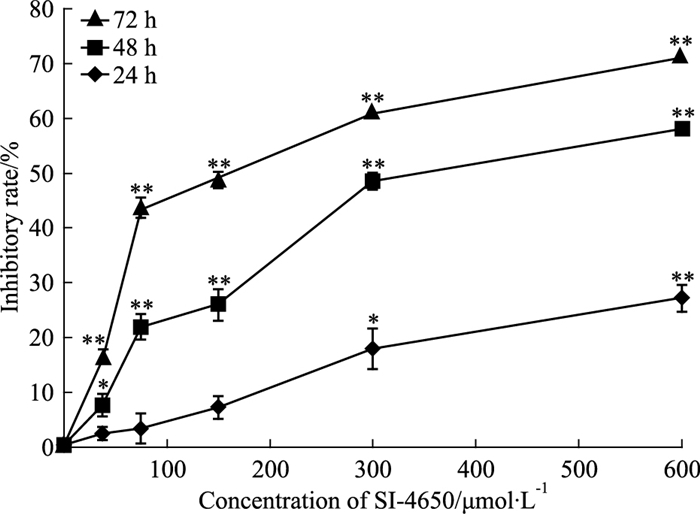
3 结果 3.1 SI-4650抑制U87MG细胞增殖用SI-4650(0、37.5、70、150、300、600 μmol·L-1)分别处理U87MG细胞24、48、72 h后,MTT法分析药物对细胞增殖能力的影响。Fig 2结果显示,SI-4650对U87MG细胞增殖具有明显的抑制作用,抑制效果随时间的延长和浓度的增加而增强。利用GraphPad Prism7软件进行统计分析发现,在处理48 h的条件下,SI-4650作用于U87MG细胞的IC50值为(303.475±27.94)μmol·L-1。依据上述结果,后续实验使用终浓度分别为150、300 μmol·L-1的SI-4650处理的细胞作为实验组,以0 μmol·L-1处理的细胞作为对照组。
|
| Fig 2 SI-4650 inhibited proliferation of U87MG cells(x±s, n=3) U87MG cells were treated with SI-4650(0, 37.5, 70, 150, 300, 600 μmol·L-1) for 24, 48 and 72 h, and then the inhibitory rate of cell proliferation was detected by MTT assay.*P < 0.05, **P < 0.01 vs control(0 μmol·L-1). |
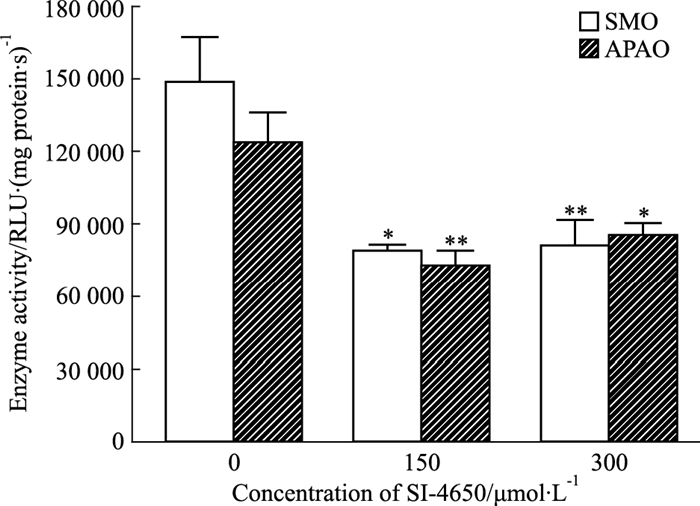
用150、300 μmol·L-1 SI-4650分别处理U87MG细胞48 h,收集细胞并制备细胞裂解液,每样本取总蛋白质量为18.65 μg的裂解液,以化学发光法分析SI-4650对U87MG细胞中SMO和APAO酶活性的影响,酶活性以单位总蛋白质量(mg)、单位时间内(s)内的化学发光强度(RLU)表示。如Fig 3所示,与对照组细胞相比,经SI-4650处理后的U87MG细胞中SMO和APAO的酶活性均明显下降。
|
| Fig 3 Effect of SI-4650 on enzyme activity ofSMO and APAO in U87MG cells(x±s, n=3) *P < 0.05, **P < 0.01 vs control(0 μmol·L-1) |
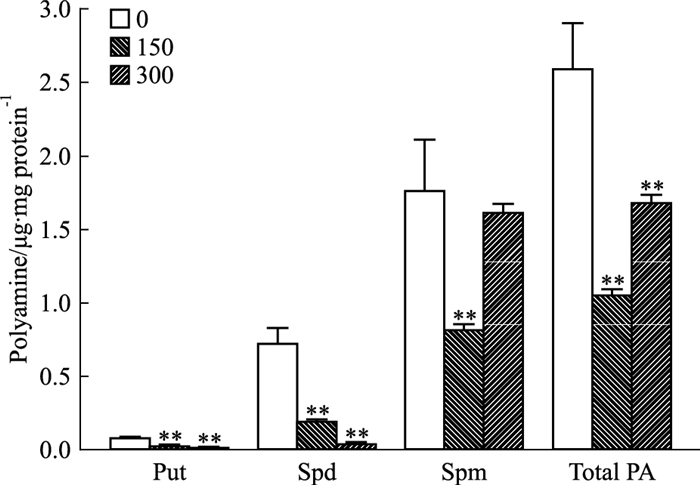
用150、300 μmol·L-1 SI-4650分别处理U87MG细胞48 h,收集细胞并制备细胞裂解液,以HPLC法分析SI-4650对U87MG细胞内多胺含量的影响。如Fig 4所示,与对照组细胞相比,经SI-4650处理的U87MG细胞中,Put和Spd含量随药物浓度增加而明显下降,Spm含量仅在药物浓度为150 μmol·L-1时明显下降,细胞总多胺含量在两种药物浓度作用下均明显降低。
|
| Fig 4 Effect of SI-4650 on polyaminecontent in U87MG cells(x±s, n=3) **P < 0.01 vs control(0 μmol·L-1) |
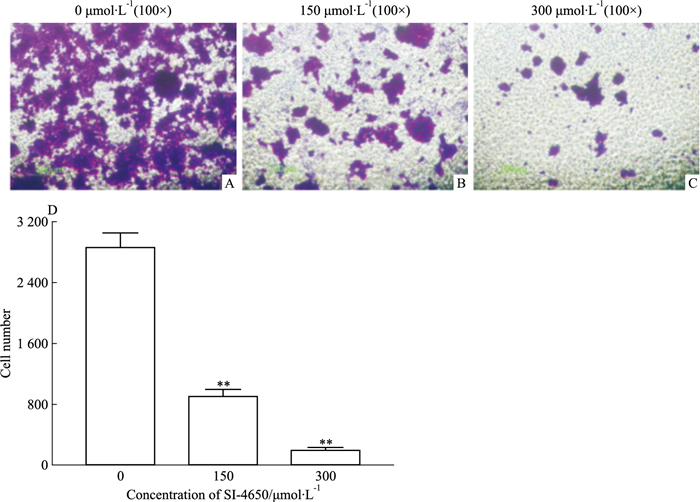
分别用150、300 μmol·L-1 SI-4650处理U87MG细胞48 h后,以Transwell法分析SI-4650对U87MG细胞迁移能力的影响。如Fig 5所示,SI-4650可明显抑制U87MG细胞的迁移能力,且抑制能力随药物浓度增加而增强。
|
| Fig 5 Effect of SI-4650 on migration ability of U87MG cells(100×) A: U87MG cells treated by 0 μmol·L-1 SI-4650; B: U87MG cells treated by 150 μmol·L-1 SI-4650; C: U87MG cells treated by 300 μmol·L-1 SI-4650; D: Quantized graph(x±s, n=3).**P < 0.01 vs control(0 μmol·L-1) |
用150、300 μmol·L-1 SI-4650分别处理U87MG细胞48 h后,收集细胞,流式细胞术分析SI-4650对U87MG细胞周期的影响。如Tab 1所示,与对照组细胞相比,SI-4650处理U87MG细胞后可使G0/G1期细胞数量增多,而G2期细胞数量减少,提示SI-4650可诱导U87MG细胞发生G0/G1周期阻滞。
| SI-4650/ μmol·L-1 |
G0/G1/% | S/% | G2/% |
| 0 | 56.21±0.38 | 19.37±0.68 | 24.39±0.52 |
| 150 | 61.80±0.52** | 19.07±0.49 | 18.73±0.67** |
| 300 | 64.40±0.55** | 17.29±0.83 | 18.80±0.46** |
| **P < 0.01 vs control(0 μmol·L-1) | |||
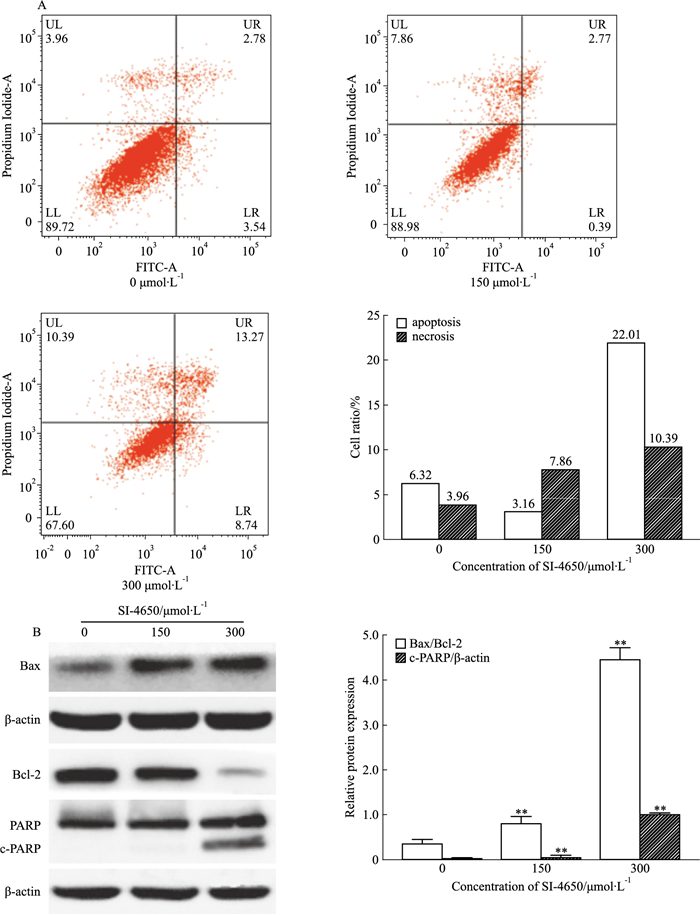
用150、300 μmol·L-1 SI-4650分别处理U87MG细胞48 h后,收集细胞,并用PI/FITC-Annexin V双染,流式细胞术分析SI-4650对U87MG细胞凋亡的影响。如Fig 6A所示,高剂量SI-4650可诱导U87MG细胞发生凋亡。进一步的Western blot结果显示(Fig 6B),高浓度SI-4650能明显上调促凋亡蛋白Bax表达,下调凋亡抑制蛋白Bcl-2的表达水平,Bax/Bcl-2比值升高,且标志性凋亡降解蛋白c-PARP水平明显增加。值得注意的是,如Fig 6A所示,SI-4650处理后,U87MG细胞坏死的比例也明显增加。提示除凋亡外,SI-4650还能导致U87MG细胞发生其它方式的死亡。
|
| Fig 6 Effect of SI-4650 on apoptosis of U87MG cells A:FCM was used to determine effect of SI-4650 on apoptotic rate of U87MG cells; B:Western blot assay was used to determine expression levels of apoptosis-related proteins(x±s, n=3).**P < 0.01 vs control(0 μmol·L-1) |
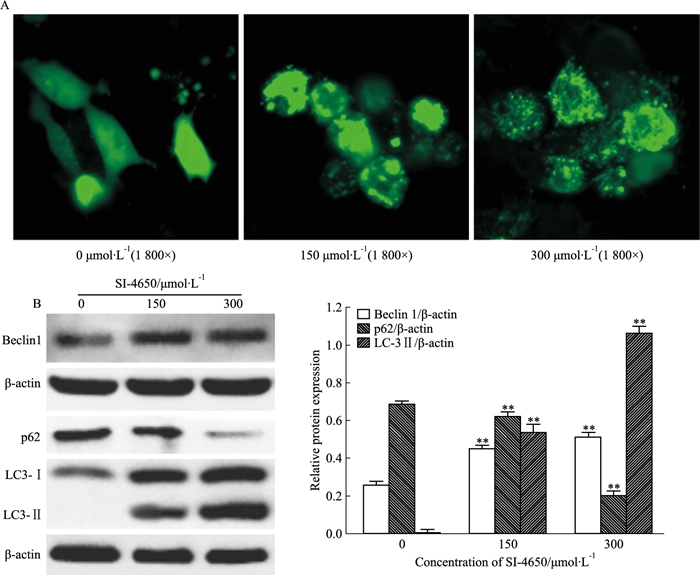
为分析SI-4650能否诱导U87MG细胞发生自噬,首先用不同浓度的SI-4650处理转染过pEGFP-LC3真核表达质粒24 h后的U87MG细胞,激光共聚焦显微镜下观察U87MG细胞中外源性表达的GFP-LC3融合蛋白的荧光强度及亚细胞定位。如Fig 7A所示,在未经SI-4650处理的对照组细胞中,GFP荧光蛋白在细胞中呈弥散性均匀分布,而SI-4650处理后,细胞中GFP荧光蛋白呈斑点状聚集。提示SI-4650能明显诱导细胞发生自噬,使得GFP-LC3融合蛋白大量向自噬小体发生转移和聚集。
|
| Fig 7 Effect of SI-4650 on autophagy of U87MG cells A: LSCM was used to observe subcellular distribution of GFP-LC3 fusion protein in U87MG cells; B:Western blot assay was used to determine expression levels of autophagy-related proteins(x±s, n=3).**P < 0.01 vs control(0 μmol·L-1) |
进一步Western blot法分析SI-4650对U87MG细胞中自噬相关蛋白Beclin-1、P62、LC3-Ⅰ/Ⅱ表达水平的影响。Fig 7B结果显示,SI-4650处理使自噬活化蛋白Beclin-1和自噬微管蛋白LC3-Ⅱ表达水平随药物浓度的增高而大幅增加,而自噬底物蛋白P62的水平则减少。
4 讨论SMO作为一种多胺分解代谢的关键酶,其表达水平异常导致的多胺代谢紊乱与包括肿瘤在内的多种疾病的发生、发展关系密切[7]。SMO由此成为抗肿瘤药物设计和治疗的潜在分子靶点。由于目前尚缺乏高效且特异性靶向SMO的小分子抑制剂,使该领域的基础和临床研究受到极大限制。SI-4650是本研究前期工作中设计和筛选出的一种SMO小分子抑制剂,为进一步分析SI-4650的抑瘤谱和对不同肿瘤细胞的抗肿瘤活性,本研究在细胞水平上,探索了SI-4650对人胶质瘤U87MG细胞增殖、迁移、凋亡和自噬的影响及其机制。
结果发现,SI-4650能有效抑制U87MG细胞增殖(48 h时IC50约为300 μmol·L-1),并诱导U87MG细胞发生G0/G1周期阻滞。由于SI-4650是以药效团为基础设计和筛选的小分子SMO靶向抑制剂,本实验分析了该抑制剂对U87MG细胞中SMO活性的影响,结果表明,SI-4650能有效抑制U87MG细胞中SMO的酶活性。此外,该抑制剂对细胞内的APAO也具有明显抑制作用。APAO是参与多胺降解代谢的另一种胺氧化酶,它与SMO之间有较高程度的结构相似性[6]。上述实验结果提示,SI-4650能通过多靶点途径干扰细胞内的多胺代谢。
进一步用HPLC法分析了SI-4650对U87MG细胞内多胺含量的影响,结果发现,SI-4650处理后,细胞内总多胺含量下降,Spd(SMO催化反应的产物)含量随药物浓度增加而明显下降,这与预期结果相符合;但Spm(SMO催化反应的底物)含量未见升高,在低浓度SI-4650(150 μmol·L-1)处理时还有明显下降。产生该现象的可能原因是多胺降解代谢受阻后,Spm经精眯/精胺N1乙酰基转移酶(spermidine/spermine N1-acetyltransferase, SSAT)催化转变为乙酰精胺后,通过U87MG细胞膜表面的多胺转运载体[9-10]而排出至细胞外。
随后我们分析了SI-4650对U87MG细胞迁移、凋亡和自噬的影响。结果发现,SI-4650能有效抑制U87MG细胞的迁移能力,并诱导U87MG细胞发生凋亡和自噬。细胞凋亡和细胞自噬分别被称为Ⅰ型和Ⅱ型程序性细胞死亡,二者之间虽然在死亡机制、细胞形态改变、死亡细胞清除方式等方面存在明显差异,但这两种死亡方式之间也存在相互影响和相互联系的复杂关系。目前研究认为,二者之间的关系主要有3种特征:相互促进、相互拮抗和相互协调。在特定的情况下,两者之间可以相互转化,形成一种促进细胞死亡的“双保险”机制[11-13]。本研究发现,相较于对照细胞,高浓度SI-4650(300 μmol·L-1)处理后的U87MG细胞与FITC-Annexin V结合的比率明显升高,促凋亡蛋白Bax表达上调,凋亡抑制蛋白Bcl-2表达下调,同时细胞内凋亡降解底物c-PARP水平大幅增高,提示SI-4650可明显诱导U87MG细胞发生凋亡。
除诱导凋亡外,本研究还发现SI-4650可有效诱导U87MG细胞发生自噬性死亡。用SI-4650处理转染有GFP-LC3融合基因的U87MG细胞后,细胞内的GFP荧光信号由弥散状向斑点聚集状转化,表明SI-4650处理促使GFP-LC3融合蛋白大量转移聚集到了自噬小体上。LC3-Ⅱ是自噬体形成的特异性分子标记物,它由LC3-Ⅰ在自噬发生过程中转化而来,而P62是选择性的自噬底物,它能结合到LC3-Ⅱ上,在自噬过程中被运输到自噬小体中降解[14-15]。本研究发现,用SI-4650处理后,U87MG细胞中自噬激活相关蛋白Beclin-1和LC3-Ⅱ的表达增多,但P62蛋白水平降低,这些结果提示SI-4650可明显诱导U87MG细胞发生自噬性死亡。
值得的注意的是,SI-4650本身是甲酰喹啉与一种三胺分子的共价缀合物,尚需进一步探索的是,除抑制SMO活性外,该小分子抑制剂是否还能通过其它不依赖于SMO的途径,抑制肿瘤细胞增殖,诱导细胞自噬和凋亡。此外,SI-4650中的三胺部分与天然精脒结构类似,它是否能扮演一种多胺类似物的角色,竞争性抑制细胞内天然多胺的代谢与功能,进而发挥多重抗肿瘤效应,这也需要在后续实验中展开深入分析研究。
综上所述,本研究证实SMO小分子抑制剂SI-4650可明显干扰U87MG细胞内的多胺代谢,有效降低多胺含量,可以抑制U87MG细胞的增殖和迁移能力,并诱导U87MG细胞发生凋亡和自噬性死亡。本研究结果提示SI-4650在神经胶质瘤治疗中的潜在应用价值。
| [1] |
Pegg A E. Functions of polyamines in mammals[J]. J Biol Chem, 2016, 291(29): 14904-12. doi:10.1074/jbc.R116.731661 |
| [2] |
Bachrach U. Naturally occurring polyamines: interaction with macromolecules[J]. Curr Protein Pept Sci, 2005, 6(6): 559-66. doi:10.2174/138920305774933240 |
| [3] |
Miller-Fleming L, Olin-Sandoval V, Campbell K, et al. Remaining mysteries of molecular biology: the role of polyamines in the cell[J]. J Mol Biol, 2015, 427(21): 3389-406. doi:10.1016/j.jmb.2015.06.020 |
| [4] |
Battaglia V, DeStefano Shields C, Murray-Stewart T, et al. Polyamine catabolism in carcinogenesis: potential targets for chemotherapy and chemoprevention[J]. Amino Acids, 2014, 46(3): 511-9. doi:10.1007/s00726-013-1529-6 |
| [5] |
Murray-Stewart T R, Woster P M, Casero R A. Targeting polyamine metabolism for cancer therapy and prevention[J]. Biochem J, 2016, 473(19): 2937-53. doi:10.1042/BCJ20160383 |
| [6] |
Cervelli M, Salvi D, Polticelli F, et al. Structure-function relationships in the evolutionary framework of spermine oxidase[J]. J Mol Evol, 2013, 76(6): 365-70. doi:10.1007/s00239-013-9570-3 |
| [7] |
Cervelli M, Amendola R, Polticelli F, et al. Spermine oxidase: ten years after[J]. Amino Acids, 2012, 42(2-3): 441-50. doi:10.1007/s00726-011-1014-z |
| [8] |
Goodwin A C, Murray-Stewart T R, Casero R A. A simple assay for mammalian spermine oxidase: A polyamine catabolic enzyme implicated in drug response and disease[J]. Methods Mol Biol, 2011, 720: 173-81. doi:10.1007/978-1-61779-034-8 |
| [9] |
Dai F, Yu W, Song J, et al. Extracellular polyamines-induced proliferation and migration of cancer cells by ODC, SSAT, and Akt1-mediated pathway[J]. Anticancer Drugs, 2017, 28(4): 457-64. doi:10.1097/CAD.0000000000000465 |
| [10] |
Abdulhussein A A, Wallace H M. Polyamines and membrane transporters[J]. Amino Acids, 2014, 46(3): 655-60. doi:10.1007/s00726-013-1553-6 |
| [11] |
唐琪, 布文奂, 王丹丹, 等. 自噬与凋亡的相互作用及其对肿瘤发展过程影响的研究进展[J]. 吉林大学学报(医学版), 2015, 41(6): 1303-6. Tang Q, Bu W H, Wang D D, et al. Advance research on interaction between autophagy and apoptosis and its influence in development of tumors[J]. J Jilin Univ(Med Sci Ed), 2015, 41(6): 1303-6. |
| [12] |
刘芳, 周小江, 陈乃宏. Cdk5介导的凋亡与自噬交互作用对脑缺血的调控[J]. 中国药理学通报, 2018, 34(4): 463-6. Liu F, Zhou X J, Chen N H. Regulation on intercross effect between Cdk5 mediated apoptosis and autophagy after cerebral ischemia[J]. Chin Pharmacol Bull, 2018, 34(4): 463-6. doi:10.3969/j.issn.1001-1978.2018.04.006 |
| [13] |
Choi A M, Ryter S W, Levine B. Autophagy in human health and disease[J]. N Engl J Med, 2013, 368(19): 1845-6. doi:10.1056/NEJMc1303158 |
| [14] |
Chen H Y, Huang T C, Shieh T M, et al. Isoliquiritigenin induces autophagy and inhibits ovarian cancer cell growth[J]. Int J Mol Sci, 2017, 18(10): 2025. doi:10.3390/ijms18102025 |
| [15] |
Li C J, Liao W T, Wu M Y, et al. New insights into the role of autophagy in tumor immune microenvironment[J]. Int J Mol Sci, 2017, 18(7): 1566. doi:10.3390/ijms18071566 |

