


2. 哈尔滨医科大学(大庆)药学院生物技术制药教研室,黑龙江 大庆 163319
范玉华(1983-),男,博士,副教授,研究方向:药理学,共同第一作者,E-mail: fyh198306@126.com。
 ,
FAN Yu-hua2
,
FAN Yu-hua2 ,
PAN Yu1,
FANG Kun2,
ZHAO Bao-shan1,
WANG Lin1,
CHEN Hong-yang2,
JIANG Ya-nan2,
SONG Yin-li1
,
PAN Yu1,
FANG Kun2,
ZHAO Bao-shan1,
WANG Lin1,
CHEN Hong-yang2,
JIANG Ya-nan2,
SONG Yin-li1

2. Biotechnological Pharmaceutics Faculty, College of Pharmacy, Harbin Medical University, Daqing, Heilongjiang 163319, China
白藜芦醇(resveratrol, Rev)是一类天然多酚化合物,主要存在于葡萄、红酒和传统药材虎杖的根中。研究发现,Rev具有广泛的生物学功能,包括抗炎、抗氧化、抗凋亡、抗肿瘤等作用[1]。动脉粥样硬化(atherosclerosis, AS)是引发心血管疾病的主要原因,Rev具有良好的抗AS作用。众所周知,Rev可以多靶点改善内皮功能障碍,抑制平滑肌细胞的增殖和迁移,减少巨噬细胞浸润和泡沫细胞的形成,以及减少脂质堆积等,发挥预防和治疗AS的作用[1]。
AS是一类以炎性浸润和脂质积聚为特征的慢性炎症性疾病,其中,动脉壁中持续的巨噬细胞积聚是发病机制的基础。人们发现,在患者动脉斑块中存在着大量的巨噬细胞,这些巨噬细胞是由内膜中单核细胞分化而来的,通过分泌促炎细胞因子(如IL-6、IL-1β、TNF-α),吸收胆固醇、脂质形成泡沫细胞,以及引发细胞凋亡等,促进AS斑块的形成、发展和破裂[2-3]。
长链非编码RNA(long non-coding RNA, lncRNAs)是一类由RNA聚合酶Ⅱ转录,长度超过200个核苷酸,且缺乏蛋白编码能力的内源性非编码RNA。过去,人们认为lncRNAs是转录过程中的“噪音”,近年来发现它在心血管疾病的发生和发展中具有重要的意义。人类肺腺癌转移相关转录本1(metastasis associated in lung denocarcinoma transcript1, MALAT1)是目前研究最为深入的一种高度丰富和保守的lncRNAs,其长度约为8 000 nt,定位于染色体11q13[4]。据报道,MALAT1参与多种心血管疾病的病理生理过程[5-6]。Han等[7]发现,MALAT1在糖尿病AS大鼠的巨噬细胞中表达增高,提示MALAT1与AS密切相关。尽管有研究表明,氧化型低密度脂蛋白可通过促进MALAT1转录,进而增强巨噬细胞中的脂质摄取[8],但MALAT1在AS中的确切作用机制仍尚不明确,有待进一步研究。由于Rev的潜在抗动脉硬化作用,以及MALAT1参与糖尿病AS发生发展过程,因此,本研究旨在探讨Rev调控MALAT1发挥抗AS作用的机制,并阐明MALAT1在AS中的潜在作用,为指导临床用药提供理论依据。
1 材料与方法 1.1 材料 1.1.1 实验动物8周龄ApoE-/-小鼠,♂,体质量(27±3)g,购自南京君科生物工程有限公司[SCXK(苏)2016-0010]。所用动物饲养在标准实验动物房内,温度(23±1) ℃,湿度55%~60%,可自由摄食饮水。ApoE-/-小鼠12只,随机分为ApoE-/-高脂饮食(high fat diet, HFD)组和ApoE-/-高脂饮食加Rev(10 mg·kg-1)组,每组6只,高脂组和Rev组分别给予高脂饮食饲养16周。高脂饲料含78.85%基础饲料、0.15%胆固醇、21%脂肪。16周后,每组取6只小鼠,异戊烷吸入麻醉下,取血管及心脏,-80 ℃或4%多聚甲醛固定保存备用。
1.1.2 药物与试剂Rev购自美国Sigma公司,称取Rev粉末,溶于DMSO中,配制成终浓度为100 mmol·L-1的Rev储存液,4 ℃避光保存备用;脂多糖(lipopolysaccharides, LPS)、游离胆固醇(free cholesterol, FC)、巯基乙酸培养基(thioglycollate medium),均购自Sigma公司;转染试剂Lipofectamine 2000购自Invitrogen公司;逆转录试剂盒、PCR试剂盒、引物购自TaKaRa公司;MALAT1干扰RNA(siMALAT1-1、siMALAT1-2、siMALAT1-3)及阴性对照(siNC)由上海吉玛制药有限公司合成。
1.1.3 仪器Eppendorf 5430R高速离心机、Eppendorf-flexlid梯度PCR仪(德国艾本德公司);NanDrop One核算蛋白定量仪(美国赛默飞世尔公司);Sunrisere Tecan光吸收酶标仪(奥地利帝肯公司);H-7650日立透射电子显微镜(日本日立公司)。
1.2 方法 1.2.1 巨噬细胞的提取与分离正常C57BL6小鼠腹腔注射3%巯基乙酸肉汤,4 d后通过腹膜灌洗法获得腹腔巨噬细胞,将细胞接种于含有10%胎牛血清,含100 kU·L-1青霉素和100 kU·L-1链霉素的DMEM培养液的培养皿中。4 h后,将非贴壁细胞洗去,并将腹腔巨噬细胞孵育在含有10%胎牛血清和20% L929上清的DMEM培养液中2 d,每天更换新鲜培养液。
1.2.2 HE染色法将不同处理组心脏取出,4%多聚甲醛固定过夜,脱水,透明,浸蜡,包埋,切片。主动脉窦的石蜡切片苏木素染色5 min,自来水冲洗1 min,盐酸乙醇分化30 s,自来水冲洗1 min,伊红30 s,自来水冲洗1 min,80%乙醇30 s,90%乙醇30 s,100%乙醇3 min,二甲苯10 min,中性树脂封片。
1.2.3 实时定量PCR检测细胞通过药物或转染试剂处理后,用TRIzol法提取细胞总RNA,取1μg总RNA逆转录成cDNA,产物分别进行MALAT1、IL-6、IL-1β、TNF-α及GAPDH的扩增,采用PCR仪运行此实验。反应循环为40个。MALAT1引物序列为上游:5'-CCCCAGCTTTTCCAGAATCC-3',下游:5'-GCATCAAGGTGAGGGGTGAA-3';IL-6引物序列为上游:5'-GGCGGATCGGATGTTGTGAT-3',下游:5'-GGACCCCAGACAATCGGTTG-3';IL-1β引物序列为上游:5'-GCAACTGTTCCTGAACTCAACT-3',下游5'-ATCTTTTGGGGTCCG TCAACT-3';TNF-α引物序列为上游:5'-GGAACACGTCGTGGGATAATG-3',下游5'-GGCAGACTTTGGATGCTTCTT-3';GAPDH引物序列为上游:5'-AGTGGCAAAGTGGAGATT-3',下游5'-GTGGAGTCATACTGGAACA-3'。
1.2.4 电镜观察取模型组斑块组织及给药处理组斑块处,用2.5%戊二醛固定30 min后,制成超薄切片,在1万倍下采取20个视野,随机选取7处。电子显微镜下观察斑块中泡沫细胞形成及数量。
1.2.5 统计学处理采用SPSS 12.0软件进行数据分析,数据采用x±s表示。3组或3组以上组间比较运用单因素方差分析(One-Way ANOVA)。两组间比较用独立样本的配对t检验。
2 结果 2.1 Rev减少泡沫细胞缩小动脉斑块Fig 1A结果显示,连续给予Rev能够明显降低动脉血管壁及主动脉弓斑块的形成。HE染色结果表明,给予Rev 16周能够明显降低主动脉根部动脉斑块面积(Fig 1B)。进一步采用电镜观察发现,Rev处理组能够明显降低泡沫细胞的形成(Fig 1C)。

|
| Fig 1 Rev attenuatedformation of atherosclerosis plaques in ApoE-/- mice A:Representative aorta preparations of the total aorta treated with Rev(10 mg·kg-1) or without Rev in ApoE-/- mice fed a HFD diet for 16 weeks; B: Representative histological analysis of cross-sections of the aortic sinus(scale bar: 400 μm); C:Macrophage-derived foam cells were filled with abundant lipid droplets. |
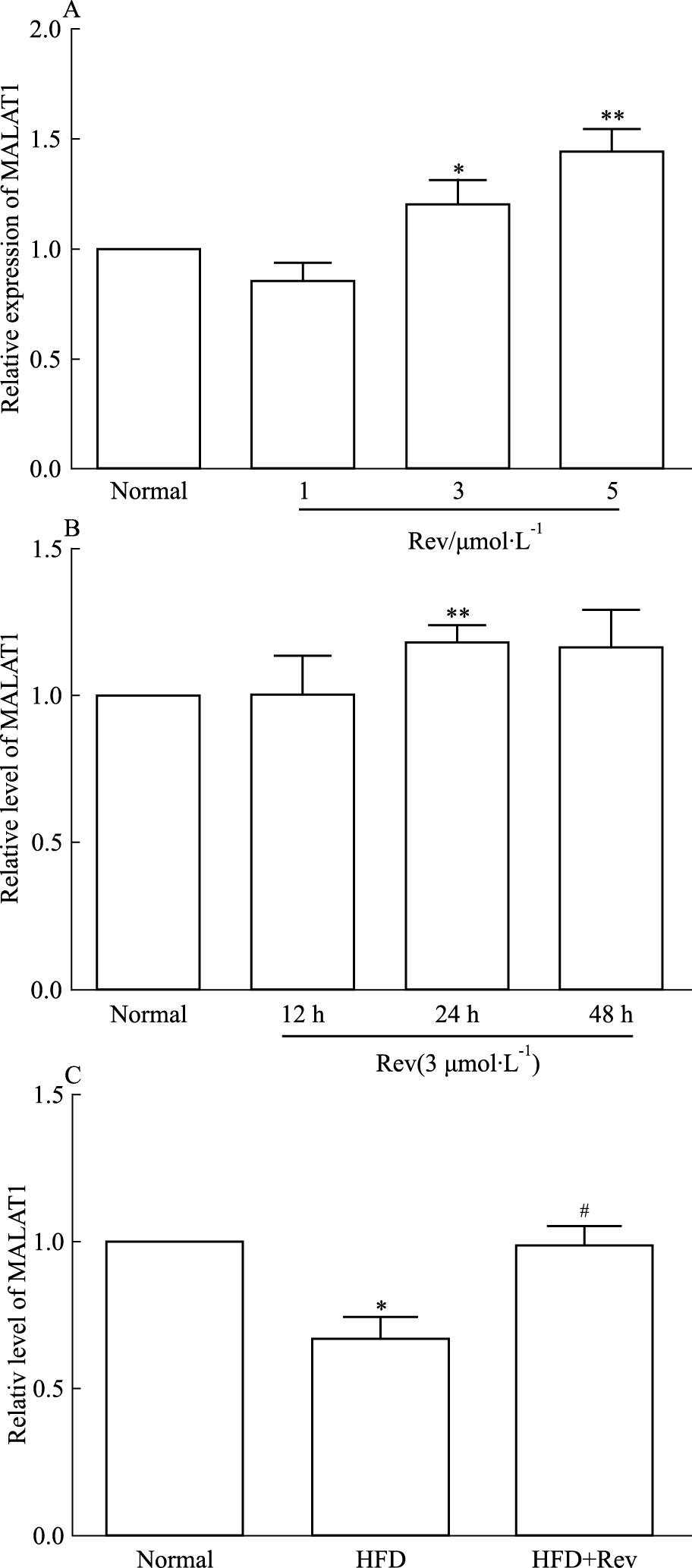
我们进一步研究Rev是否通过调控MALAT1,进而发挥抗AS作用。Fig 2A结果表明,Rev(1、3、5 μmol·L-1)处理腹腔巨噬细胞24h,能够剂量依赖性地上调MALAT1的表达。为了进一步验证Rev对MALAT1表达的作用,采用real time PCR检测Rev(3 μmol·L-1)分别处理12、24、48 h后MALAT1的表达。Fig 2B结果显示,Rev处理12 h对MALAT1 mRNA表达影响不明显,处理24 h MALAT1 mRNA表达明显增加,处理48 h MALAT1 mRNA无法继续上调。可见,Rev对MALAT1调控作用不是时间依赖性,提示Rev可能部分通过调控MALAT1表达发挥抗AS作用。
|
| Fig 2 Effects of Rev on expression of lncRNAMALAT1 in peritoneal macrophage(x±s, n=6) A:Rev could reduce the level of MALAT1 in a dose-dependent manner; B: Rev could increase expression of MALAT1 at the 24 h incubation; C: MALAT1 decreased in HFD diet in ApoE-/- mice, while Rev could elevate the level of MALAT1 in HFD diet in ApoE-/- mice.*P < 0.05, **P < 0.01 vs normal group; #P < 0.05 vs HFD group. |
为了进一步验证MALAT1在AS中的作用,我们采用real time PCR检测动脉斑块中MALAT1表达水平。结果显示,给予HFD的ApoE-/-小鼠动脉斑块中MALAT1 mRNA水平明显下调。此外,Rev明显逆转高脂饮食引起的ApoE-/-小鼠斑块中MALAT1 mRNA的下调(Fig 2C)。可见,MALAT1参与AS发生、发展进程。
2.3 Rev抑制IL-6、IL-1β、TNF-α mRNA表达正常小鼠的腹腔巨噬细胞给予Rev刺激24 h后,100 μg·L-1 LPS刺激3 h,采用real time PCR检测Rev对炎症因子表达的影响。Tab 1结果表明,LPS能够显著刺激IL-6、IL-1β、TNF-α mRNA表达,而Rev能明显降低IL-6、IL-1β、TNF-α mRNA表达。
| Group | IL-6 | IL-1β | TNF-α |
| Normal | 1.00±0.00 | 1.00±0.00 | 1.00±0.00 |
| LPS | 79.25±12.5## | 60.75±6.50## | 3.5±0.55## |
| LPS+Rev | 53.50±6.19* | 45.25±8.77** | 2.38±0.46** |
| ##P < 0.01 vs normal; *P < 0.05, **P < 0.01 vs LPS | |||
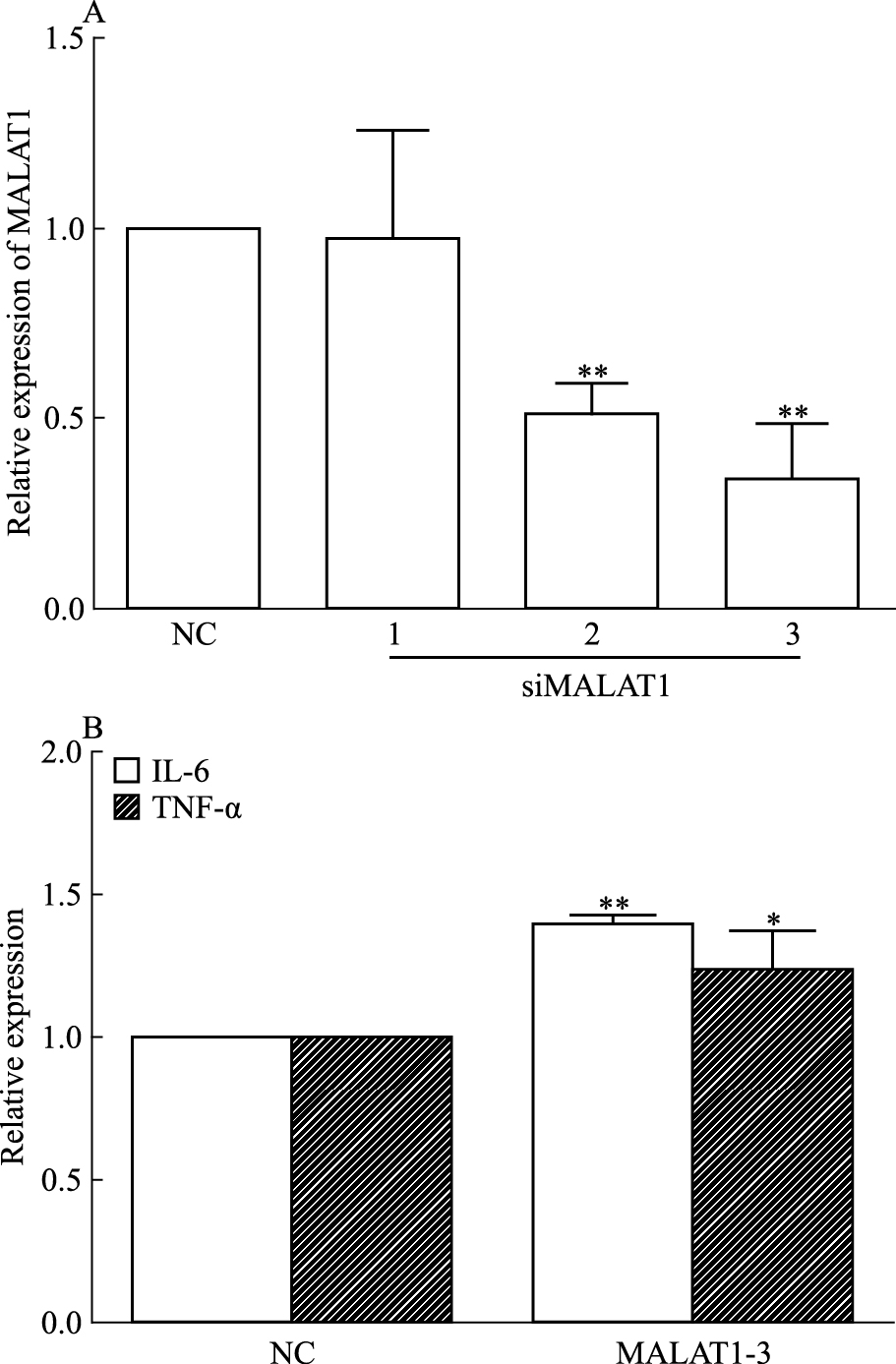
巨噬细胞给予siMALAT1(1-3)或阴性对照(NC)处理36 h后,实时定量PCR检测不同处理组对MALAT1表达的影响。Fig 3A结果表明,siMALAT1-3能够明显降低MALAT1 mRNA表达。继续选用siMALAT1-3孵育细胞36 h后,给予100 μg·L-1 LPS刺激3h,实时定量PCR检测siMALAT1-3对炎症因子表达的影响。Fig 3B结果表明,siMALAT1-3孵育36 h能明显促进IL-6、TNF-α mRNA表达。
|
| Fig 3 Effects of MALAT1 on mRNA expressionof IL-6 and TNF-α in macrophages(x±s, n=6) A:siMALAT1-3 could significantly decrease the level of MALAT1; B:The mRNA levels of IL-6 and TNF-α were dominantly elevated by treatment with siMALAT1-3.*P < 0.05, **P < 0.01 vs NC group. |
FC(10 mg·L-1)刺激巨噬细胞3、6、12 h,Fig 4结果表明,FC刺激3、6h能够明显降低MALAT1 mRNA表达。提示Rev可能通过调控胆固醇,进而影响MALAT1表达,从而调控炎症因子IL-6和TNF-α表达,发挥抗AS作用。

|
| Fig 4 Effects of cholesterol onMALAT1 in macrophages(x±s, n=6) *P < 0.05 vs normal group |
心血管疾病是导致人类高死亡率的主要病因。长期以来,天然产品广泛用于预防和治疗包括心血管疾病在内的慢性疾病。Rev作为研究最多的膳食天然产品之一,已显示出对多种疾病具有保护作用。然而,Rev在AS中的保护作用及潜在机制尚未完全清楚。最近研究表明,Rev可以减少三甲胺-N-氧化物(trimethylamine-N-oxide, TMAO)诱导的AS鼠的主动脉斑块面积[9]。此外,Chang等[10]发现,HFD诱导的AS鼠中,每天给予高剂量Rev(25mg·kg-1)8周,可以明显降低低密度脂蛋白胆固醇和IL-6水平。
本研究结果表明,每天给予Rev(10mg·kg-1)16周,能够明显降低ApoE-/-小鼠主动脉弓部及根部斑块的面积和泡沫细胞的数量。Arslan等[11]发现,MALAT1在AS斑块中表达减少,这与我们的结果是一致的。在本研究中,腹腔巨噬细胞给予Rev后,发现MALAT1的表达量升高,且这种升高具有剂量依赖性,通过进一步验证MALAT1在AS中的作用,我们发现Rev明显逆转高脂饮食引起的ApoE-/-小鼠斑块中MALAT1的下调。进一步研究表明,Rev能够抑制炎症因子IL-6、IL-1β、TNF-α的表达。Tang等[12]发现,MALAT1具有抗炎作用,保护内皮细胞免受氧化型低密度脂蛋白损伤。Zhao等[13]的研究表明,MALAT1参与调节先天免疫和炎症反应,敲低MALAT1会增加LPS诱导的TNF-α和IL-6的表达。因此,我们假设MALAT1可能通过调控炎症来发挥抗AS作用。与我们预期相一致的是,在腹腔巨噬细胞中敲降MALAT1后,qPCR结果显示能够明显增加LPS诱导的炎症因子IL-6和TNF-α的表达。虽然本研究并没有发现敲低MALAT1对IL-1β有明显的抑制作用,但是Rev对MALAT1的调控,以及MALAT1对炎症因子的调控作用已明确,且实验结果表明,Rev对炎症因子IL-6和TNF-α同样具有调控作用。因此,我们推断Rev抗AS作用部分通过调控MALAT1。
胆固醇是AS病变中的主要成分,过多的胆固醇可使巨噬细胞形成泡沫细胞,泡沫细胞的大量积聚可形成脂质条纹和斑块。因此,巨噬细胞中胆固醇的平衡流动是避免脂质积累和控制AS发展所必需的。Voloshyna等[14]研究表明,Rev可通过上调胆固醇转运蛋白(ABCA1、ABCG1、SR-BI)的表达,减少THP-1巨噬细胞中的游离胆固醇和胆固醇酯含量。此外,Rev也可通过降低血浆极低密度脂蛋白水平,促进巨噬细胞的胆固醇流出[15]。本实验,FC刺激腹腔巨噬细胞后,发现MALAT1的表达明显下降。本研究表明,Rev能够抑制AS发生发展,且Rev可能通过调控MALAT1及胆固醇发挥抗AS的作用。但Rev是通过直接还是间接调控MALAT1,发挥抗AS作用并未证明,且未深入探讨MALAT1下游调控的潜在靶点。因此,我们后续实验会全面地阐明MALAT1的作用机制,以及Rev对MALAT1的调控机制。
总之,本实验部分揭示了Rev可能部分通过调控MALAT1,进而抑制炎症因子的表达来发挥抗AS作用。此外,本研究结果表明,Rev可能通过调控FC,进而调控MALAT1表达发挥抗AS作用。然而,我们仍需要大量实验证实Rev确切作用及MALAT1的作用机制。
( 致谢: 本实验是在哈尔滨医科大学(大庆)检验中心完成,感谢课题组成员对实验的帮助!)
| [1] |
Bonnefont-Rousselot D. Resveratrol and cardiovascular diseases[J]. Nutrients, 2016, 8(5): 250. doi:10.3390/nu8050250 |
| [2] |
Dong W P, Wang X Y, Bi S H, et al. Inhibitory effects of resveratrol on foam cell formation are mediated through monocyte chemotactic protein-1 and lipid metabolism-related proteins[J]. Int J Mol Med, 2014, 33(5): 1161-8. doi:10.3892/ijmm.2014.1680 |
| [3] |
Canfran-Duque A, Rotllan N, Zhang X B, et al. Macrophage deficiency of miR-21 promotes apoptosis, plaque necrosis, and vascular inflammation during atherogenesis[J]. EMBO Mol Med, 2017, 9(9): 1244-62. doi:10.15252/emmm.201607492 |
| [4] |
赵斌, 吴毓婷, 黄成, 等. 沉默MALAT1基因对蜂毒素诱导HepG2细胞增殖和凋亡的影响[J]. 中国药理学通报, 2016, 32(2): 211-6. Zhao B, Wu Y T, Huang C, et al. Effects of silencing MALAT1 on proliferation and apoptosis in HepG2 cells induced by Melittin[J]. Chin Pharmacol Bull, 2016, 32(2): 211-6. doi:10.3969/j.issn.1001-1978.2016.02.013 |
| [5] |
Zhang M Y, Gu H M, Chen J C, et al. Involvement of long noncoding RNA MALAT1 in the pathogenesis of diabetic cardiomyopathy[J]. Int J Cardiol, 2016, 202: 753-5. doi:10.1016/j.ijcard.2015.10.019 |
| [6] |
Guo D, Ma J, Yan L, et al. Down-Regulation of lncRNA MALAT1 attenuates neuronal cell death through suppressing Beclin1-dependent autophagy by regulating miR-30a in cerebral ischemic stroke[J]. Cell Physiol Biochem, 2017, 43(1): 182-94. doi:10.1159/000480337 |
| [7] |
Han Y, Qiu H, Pei X, et al. Low-dose sinapic acid abates the pyroptosis of macrophages by downregulation of lncRNA-MALAT1 in rats with diabetic atherosclerosis[J]. J Cardiovasc Pharmacol, 2018, 71(2): 104-12. |
| [8] |
Ning H F, Xu Z Y, Zheng W Y, et al. LncRNA MALAT1 regulates oxLDL-induced CD36 expression via activating beta-catenin[J]. Biochem Biophys Res Commun, 2018, 495(3): 2111-7. doi:10.1016/j.bbrc.2017.12.086 |
| [9] |
Chen M L, Yi L, Zhang Y, et al. Resveratrol attenuates trimethylamine-N-oxide(TMAO)-induced atherosclerosis by regulating TMAO synthesis and bile acid metabolism via remodeling of the gut microbiota[J]. MBio, 2016, 7(2): e02210-5. |
| [10] |
Chang G R, Chen P L, Hou P H, et al. Resveratrol protects against diet-induced atherosclerosis by reducing low-density lipoprotein cholesterol and inhibiting inflammation in apolipoprotein E-deficient mice[J]. Iran J Basic Med Sci, 2015, 18(11): 1063-71. |
| [11] |
Arslan S, Berkan Ö, Lalem T, et al. Long non-coding RNAs in the atherosclerotic plaque[J]. Atherosclerosis, 2017, 266: 176-81. doi:10.1016/j.atherosclerosis.2017.10.012 |
| [12] |
Tang Y, Jin X, Xiang Y, et al. The lncRNA MALAT1 protects the endothelium against ox-LDL-induced dysfunction via upregulating the expression of the miR-22-3p target genes CXCR2 and AKT[J]. FEBS Lett, 2015, 589(20Pt B): 3189-96. |
| [13] |
Zhao G, Su Z Y, Song D, et al. The long non-coding RNA MALAT1 regulates the lipopolysaccharide-induced inflammatory response through its interaction with NF-kappaB[J]. FEBS Lett, 2016, 590(17): 2884-95. doi:10.1002/1873-3468.12315 |
| [14] |
Voloshyna I, Hai O, Littlefield M J, et al. Resveratrol mediates anti-atherogenic effects on cholesterol flux in human macrophages and endothelium via PPARγ and adenosine[J]. Eur J Pharmacol, 2013, 698(1-3): 299-309. doi:10.1016/j.ejphar.2012.08.024 |
| [15] |
Berbee J F, Wong M C, Wang Y N, et al. Resveratrol protects against atherosclerosis, but does not add to the antiatherogenic effect of atorvastatin, in APOE*3-Leiden[J]. J Nutr Biochem, 2013, 24(8): 1423-30. doi:10.1016/j.jnutbio.2012.11.009 |