

2-甲氧基雌二醇(2-methoxyestradiol,2-ME2)是一种雌性激素类药物,为17β-雌二醇体内生理代谢物。2-ME2能够不依赖雌激素受体而选择性杀伤肿瘤细胞,并且对正常细胞无毒性[1-4],根据2-ME2的这些药效特点,该药被普遍用于抗癌基础实验方面的研究。体外实验研究表明,2-ME2可抑制许多不同组织来源的肿瘤细胞生长[2],动物体内的模型研究结果同样表明,2-ME2可明显抑制动物肿瘤模型的体内生长,且可以大幅度消减肿瘤负荷。虽然2-ME2的抗肿瘤相关研究国内外均有文献报道,但关于抗肿瘤方面的机制仍不清楚。早期实验证实,人急性T淋巴细胞白血病CEM细胞对2-ME2具有高度敏感性,表现为体外增殖受到明显抑制,细胞凋亡现象普遍可见[5-6]。为了进一步验证2-ME2是否对耐药相关的急性T淋巴细胞白血病具有杀伤作用,本研究选择耐6-巯基嘌呤的人急性T淋巴细胞白血病细胞6T-CEM作为体外研究的目标细胞,探讨2-ME2对6T-CEM细胞增殖、凋亡等生物学行为的影响及初步机制。
1 材料与方法 1.1 材料 1.1.1 细胞株人来源的急性T淋巴细胞白血病细胞6T-CEM,购自中科院上海细胞库。
1.1.2 试剂RPMI 1640培养液、小牛血清(美国Gibco公司); 2-ME2、二甲基亚砜(DMSO),购自美国Sigma公司,DMSO配制2-ME2的初始浓度为2 mmol·L-1,保存于4℃冰箱,临用时培养液稀释至所需浓度,药物中DMSO终浓度小于0.1%;MTT,美国Amresco公司产品; Akt、p-Akt(Ser473)、Bcl-2、Bax、procaspase-3兔多抗,均购自美国Cell Signaling Technology公司; 内参蛋白β-actin鼠单抗,购自湖北武汉博士德科技公司; 蛋白酶抑制剂,购自上海康成生物工程公司; 化学发光底物相关试剂、辣根过氧化物酶(HRP)标记的二抗,均购自美国Pierce公司。
1.1.3 仪器FAX2100型酶标仪(美国STAT公司); DU640型紫外分光光度仪(美国贝克曼公司); 水平电泳槽(北京东方仪器厂); 垂直电泳槽、转膜仪器(美国Bio-Rad公司)。
1.2 方法 1.2.1 6T-CEM细胞的培养冻存于液氮罐的6T-CEM细胞复苏后,培养于含有10%小牛血清的RPMI 1640培养液中。6T-CEM细胞在5% CO2、37℃条件下培养,每3 d传代1次。实验中所采用的6T-CEM细胞均处在对数生长期。
1.2.2 MTT法观察6T-CEM细胞生长变化6T-CEM细胞按1×108·L-1的密度接种至96孔板,每孔200 μL。2-ME2(0.5、1、2、4、8 μmol·L-1)分别处理6T-CEM细胞,培养24、48 h,每个浓度组均设置3个复孔。实验结束前4 h,向各孔中加入MTT溶液,继续培养4 h,终止培养,离心后吸弃上清液,每孔加入150 μL DMSO,振荡结晶物充分溶解。492 nm和630 nm波长下,酶标仪测定各孔光吸收值。按文献[5]计算抑制率,细胞生长抑制率/%=(1-实验组平均吸光度值/对照组平均吸光度值)×100%。
1.2.3 DNA梯度片段法检测6T-CEM细胞凋亡2-ME2(0、1、2、4 μmol·L-1)处理6T-CEM细胞24 h,离心弃上清液,收集1×106数量级细胞,加入含蛋白酶K的样品裂解液,振荡混匀,充分裂解细胞。50℃水浴箱放置12 h,加入500 μL Tris平衡苯酚,振荡混匀,吸取上清液,加入10 mmol·L-1醋酸铵和无水乙醇,颠倒混匀,沉淀DNA -20℃过夜。离心后,吸弃上清液,自然风干DNA,立即加入蒸馏水溶解DNA,40 V电压下,于2%琼脂糖凝胶电泳3 h后观察结果。
1.2.4 蛋白印迹法检测p-Akt、Akt、Bcl-2、Bax、Procaspase-3的表达处于对数生长期的6T-CEM细胞,加入2 μmol·L-1 2-ME2,培养0、24、48、72 h后,离心收集细胞,加入细胞裂解液,提取细胞总蛋白,于4℃、12 000 r·min-1离心10 min,BCA法蛋白定量。取20 μg的待测蛋白,加入上样缓冲液,99℃蛋白变性5 min,10%~15%的SDS-PAGE凝胶电泳,转移至硝酸纤维素膜。膜放入5%的脱脂牛奶封闭2 h,分别加入待测蛋白一抗,4℃孵育过夜。加入二抗,室温孵育2 h,用TBST缓冲液洗膜3次,每次10 min,利用化学发光试剂进行检测和分析。
1.3 统计学方法使用SPSS 17.0软件分析数据。组间比较采用F检验。
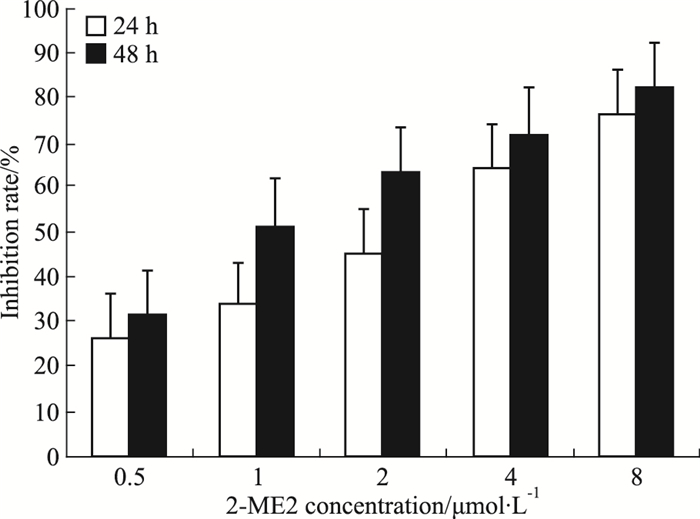
2 结果 2.1 2-ME2对6T-CEM细胞增殖的影响设置2-ME2(0.5、1、2、4、8 μmol·L-1)药物处理组和只加培养液处理的对照组,观察24、48 h两个处理时间点的细胞增殖情况。Fig 1的MTT结果显示,0.5 μmol·L-1 2-ME2作用6T-CEM细胞24 h后,6T-CEM细胞生长受抑,随着药物浓度的增加,细胞生长抑制率也逐渐增强,药物浓度为8 μmol·L-1时,细胞生长抑制率达到80%。不同浓度2-ME2作用6T-CEM细胞48 h后,细胞增殖明显受抑制,细胞增殖抑制率随着药物浓度增高而逐步增加,2 μmol·L-1 2-ME2使6T-CEM细胞增殖抑制率达到50%。提示2-ME2抑制6T-CEM细胞增殖存在着一定的量效、时效关联性。
|
| Fig 1 Effects of 2-ME2 on proliferation of 6T-CEM cells in 24 h and 48 h(x±s, n=3) |
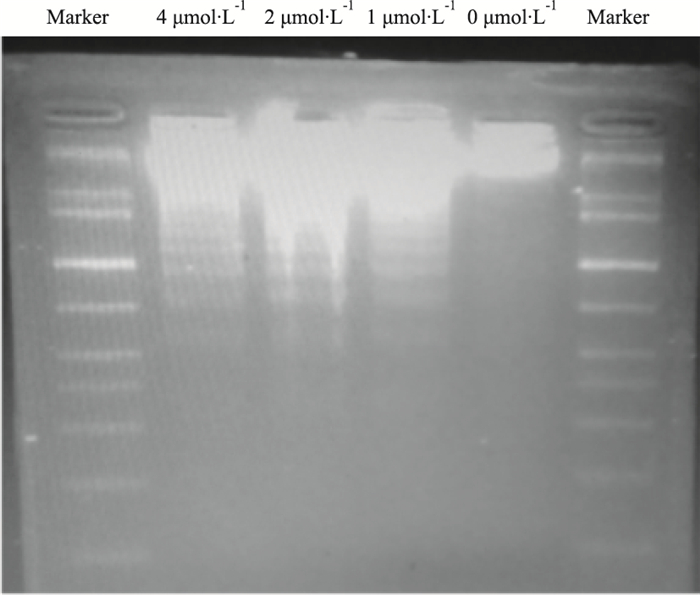
2-ME2(1、2、4 μmol·L-1)作用于6T-CEM细胞24 h,DNA Ladder法检测细胞凋亡情况。Fig 2电泳结果显示,1 μmol·L-1的2-ME2处理细胞后,可见到典型的梯状片段,随着2-ME2浓度的增加,仍显示出典型的梯状片段改变,结果表明2-ME2能够诱导6T-CEM细胞凋亡的发生。添加培养液处理的对照组细胞未见DNA片段化现象,表现一完整的DNA基因组,表明对照组6T-CEM细胞无凋亡改变。
|
| Fig 2 Effect of 2-ME2 on apoptosis of 6T-CEM cells in 24 h by DNA ladder |
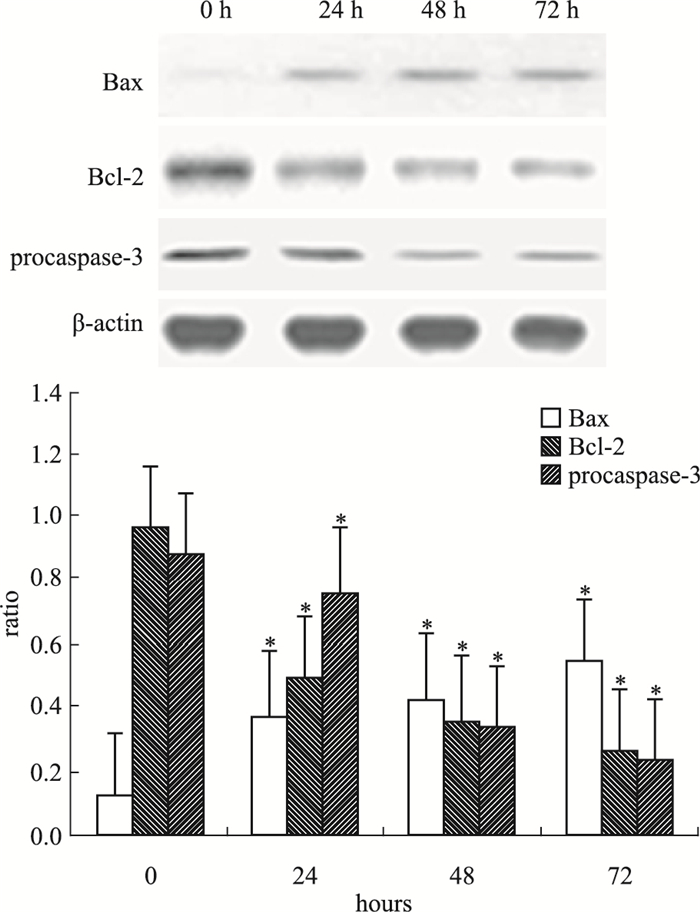
2 μmol·L-1的2-ME2作用6T-CEM细胞0、24、48、72 h后,蛋白印迹法检测细胞内蛋白表达。如Fig 3所示,作用24 h后,与对照组比较,p-Akt蛋白表达呈现下降趋势,随着药物处理时间的延长,其表达水平逐步下降(P < 0.05),而Akt蛋白表达无明显变化,提示2-ME2抑制6T-CEM细胞增殖的过程涉及了Akt蛋白活化受抑制。如Fig 4所示,抗凋亡蛋白Bcl-2表达随着药物作用时间延长,逐渐下调; 促凋亡蛋白Bax表达则逐渐上调; 随着2-ME2作用时间的延长,Procaspase-3表达水平逐渐下降,考虑存在促凋亡蛋白物质的活化。提示2-ME2诱导6T-CEM细胞凋亡过程中存在着线粒体凋亡途径的激活。

|
| Fig 3 Effect of 2-ME2(2 μmol·L-1) on expression of Akt and p-Akt in 6T-CEM cells(x±s, n=3) *P < 0.05 vs control |
|
| Fig 4 Effect of 2-ME2(2 μmol·L-1) on expression of Bax, Bcl-2 and procaspase-3 in 6T-CEM cells(x±s, n=3) *P < 0.05 vs control |
2-ME2作为一种人体内雌二醇的内源性的生理代谢产物,有着广泛抗肿瘤效应,并且临床相关的毒副作用非常少,其抗肿瘤活性得到了国内外研究人员的关注。前期大量研究证实,2-ME2对多种非血液淋巴系统恶性肿瘤具有抗肿瘤效果,在血液系统肿瘤方面也显示出良好的抗肿瘤功效[3-7]。急性T淋巴细胞白血病是起源于造血干祖细胞恶性血液病,采取多药化疗的治疗,大多数病患可达到形态学缓解,但大部分病例仍存在复发,且大多数病人容易出现耐药,严重影响这类白血病患者的长期生存率,仍需要寻求新的药物提高总的治疗疗效[8]。在前期研究2-ME2抗急性T淋巴细胞白血病CEM细胞的基础上[5-6],我们选取CEM耐6-巯基嘌呤细胞系6T-CEM作为研究对象,探讨2-ME2对耐药白血病细胞的影响。实验结果证实,2-ME2不同浓度处理可抑制6T-CEM细胞增殖。2-ME2(1、2、4 μmol·L-1)处理6T-CEM细胞,经过DNA Ladder方法检测到药物处理组细胞DNA密度梯度片段化,提示细胞凋亡的发生,说明2-ME2可通过诱导6T-CEM细胞凋亡,达到抑制其增殖的作用。
有研究报道[9],2-ME2诱导人宫颈癌细胞凋亡的过程中,涉及Bax/Bcl-2比率的改变。我们前期研究发现[10],2-ME2诱导人慢性粒细胞白血病K562细胞凋亡的过程中,存在Bcl-2下降,Bax表达升高,Bax/Bcl-2比率改变。Bcl-2和Bax均属于Bcl-2家族成员[11],通过控制线粒体膜表面上的通透性来改变细胞的归属,如激活细胞色素C释放至细胞质中,通过一系列的生理反应,激活caspase-3,启动线粒体凋亡途径,引起细胞凋亡。本研究结果证实,2-ME2作用各个时间点,可抑制Bcl-2、procaspase-3表达,上调Bax表达。这些结果证实了2-ME2能影响6T-CEM细胞的增殖和凋亡。
细胞内存在多种信号转导通路,这些通路都与细胞的生存、增殖、凋亡等生物学行为密切相关。PI3K/Akt信号可通过影响其下游的多种蛋白效应分子的激活和失活,在维持细胞生命过程中发挥关键的监管作用[12-13]。研究证实,该信号通路的异常激活与肿瘤有很大的关联性[13-14]。该通路在人急性T淋巴细胞白血病中也存在持续活化状态,并参与白血病的发展以及耐药、复发等病理生理过程。表明该通路上的蛋白效应分子可能是抗白血病治疗的靶点之一[15]。前期研究证明,2-ME2可抑制p-Akt表达而影响细胞的生存能力,总Akt表达无改变[11]。表明2-ME2影响K562细胞行为可能与抑制Akt蛋白的活化,进而干扰PI3K/Akt信号通路相关。本研究中,蛋白印迹法观察到6T-CEM经2-ME2处理24 h后,p-Akt表达减少,其表达与药物处理时间具有相关性,而总Akt蛋白表达无改变。提示2-ME2处理6T-CEM细胞后,6T-CEM细胞表现出增殖受抑、发生凋亡,与其干预PI3K/Akt通路有关。因此,今后的研究工作将继续深入探讨2-ME2干扰该信号通路的具体机制。
6T-CEM属于6-巯基嘌呤耐药细胞,多药耐药相关蛋白(multidrug resistance-associated protein, MRP)和P-糖蛋白(P-glycoprotein, P-gp)等异常表达在白血病耐药过程中起重要作用。2-ME2抑制6T-CEM细胞增殖并诱导其凋亡的过程中,是否涉及到对MRP、P-gp等耐药蛋白的作用,有待于进一步研究。
综上所述,本实验结果表明,2-ME2可明显抑制6T-CEM细胞增殖,促进细胞凋亡,其抗白血病作用的机制可能与调节Bcl-2、Bax表达,改变了两者之间的比率,进而激活caspase-3,启动内源性凋亡途径有关。同时,降低p-Akt蛋白表达,干扰PI3K/Akt途径转导也参与了2-ME2影响6T-CEM细胞生物学行为的过程。
| [1] |
Martucci C P, Fishman J. P450 enzymes of estrogen metabolism[J]. Pharmacol Ther, 1993, 57(2-3): 237-57. doi:10.1016/0163-7258(93)90057-K |
| [2] |
Fotsis T, Zhang Y, Pepper M S, et al. The endogenous oestrogen metabolite 2-methoxyoestradiol inhibits angiogenesis and suppresses tumour growth[J]. Nature, 1994, 368(6468): 237-9. doi:10.1038/368237a0 |
| [3] |
Lis A, Ciesielski M J, Barone T A, et al. 2-Methoxyestradiol inhibits proliferation of normal and neoplastic glial cells, and induces cell death, in vitro[J]. Cancer Lett, 2004, 213(1): 57-65. doi:10.1016/j.canlet.2004.04.021 |
| [4] |
LaValee T M, Zhan X H, Herbstritt C J. 2-Methoxyestradiol inhibits proliferation and induces apoptosis independently of estrogen receptors a and b[J]. Cancer Res, 2002, 62(13): 3691-7. |
| [5] |
张学亚, 潘敬新, 郭熙哲, 等. 2-甲氧基雌二醇对白血病细胞CEM增殖的影响及其机制研究[J]. 中国药理学通报, 2011, 27(1): 103-6. Zhang X Y, Pan J X, Guo X Z, et al. Effects of 2-methoxyestradiol on CEM cells and its underlying mechanism[J]. Chin Pharmacol Bull, 2011, 27(1): 103-6. |
| [6] |
Zhang X, Huang H, Xu Z, et al. 2-Methoxyestradiol blocks cell-cycle progression at G2/M phase and induces apoptosis of human acute T lymphoblastic leukemia CEM cells[J]. Acta Biochim Biophys Sin, 2010, 42(9): 615-22. doi:10.1093/abbs/gmq065 |
| [7] |
Huang P, Feng L, Oldham E A, et al. Superoxide dismutase as a target for the selective killing of cancer cells[J]. Nature, 2000, 407(6802): 390-5. doi:10.1038/35030140 |
| [8] |
Pui C H, Relling M V, Downing J R. Acute lymphoblastic leukemia[J]. N Engl J Med, 2004, 350(15): 1535-48. doi:10.1056/NEJMra023001 |
| [9] |
Joubert A, Maritz C, Joubert F. Influence of prostaglandin A2 and 2-methoxyestradiol on Bax and Bcl-2 expression levels in cervical carcinoma ceIls[J]. Biomed Res, 2005, 26(2): 87-90. doi:10.2220/biomedres.26.87 |
| [10] |
张学亚, 战榕, 黄豪博, 等. 2-甲氧基雌二醇诱导K562细胞凋亡及其机制研究[J]. 中国实验血液学杂志, 2009, 17(2): 340-4. Zhang X Y, Zhan R, Huang H B, et al. Mechanism underlying on 2-methoxyestradiol inducing apoptosis of K562 cells[J]. J Exp Hematol, 2009, 17(2): 340-4. |
| [11] |
Green D R, Reed J C. Mitochondria and apoptosis[J]. Science, 1998, 281(5381): 1309-12. doi:10.1126/science.281.5381.1309 |
| [12] |
Levine D A, Bogomolniy F, Yee C J, et al. Frequent mutation of the PIK3CA gene in ovarian and breast cancers[J]. Clin Cancer Res, 2005, 11(8): 2875-8. doi:10.1158/1078-0432.CCR-04-2142 |
| [13] |
Rudelius M, Pittaluga S, Nishizuka S, et al. Constitutive activation of Akt contributes to the pathogenesis and survival of mantle cell lymphoma[J]. Blood, 2006, 108(5): 1668-76. doi:10.1182/blood-2006-04-015586 |
| [14] |
石雪萍, 李静, 冉建华, 等. 人参皂苷Rh2调控PI3K/AKT/GSK-3β信号通路诱导人结肠癌细胞凋亡[J]. 中国药理学通报, 2017, 33(1): 114-9. Shi X P, Li J, Ran J H, et al. Ginsenoside Rh2 induced human colorectal cancer cell apoptosis through PI3K/AKT/GSK-3β pathway[J]. Chin Pharmacol Bull, 2017, 33(1): 114-9. doi:10.3969/j.issn.1001-1978.2017.01.020 |
| [15] |
Vitale A, Guarini A, Ariola C, et al. Adult T cell acute lymphoblastic leukemia: biologic profile at presentation and correlation with response to induction treatment in patients enrolled in the GIMEMA LAL 0496 protocol[J]. Blood, 2006, 107(2): 473-9. doi:10.1182/blood-2005-04-1754 |

