

2. 桂林医学院 广西肝脏损伤与修复分子医学重点实验室,广西 桂林 541004;
3. 桂林医学院 科学实验中心,广西 桂林 541004
2. Key Lab of Liver Injury and Repair Molecular Medicine of Guangxi, Guilin Medical University, Guilin Guangxi 541004, China;
3. the Center for Science Research, Guilin Medical University, Guilin Guangxi 541004, China
原发性肝癌(hepatocellular carcinoma,HCC)是全球范围内发病率和死亡率最高的恶性肿瘤之一,全国每年约有38.3万人死于肝癌,占全球肝癌死亡总人数的51%[1]。目前,医治HCC仍以手术为主,兼物理疗法、化学药物疗法等在内的综合治疗。临床常用的肝癌化疗药物如蒽环类抗瘤药等,缺乏高度的组织选择性,在发挥疗效的同时,往往产生较严重的全身性毒副作用[2]。因此,如何使化疗药物既提高肿瘤化疗效果,又减轻化疗药物的毒副作用,已成为肿瘤药物治疗亟待解决的关键问题。
强心苷类(Cardiac glycosides,CGS)是一类从植物中提取的类固醇衍生物,能明显兴奋心肌细胞,目前作为心衰和心房颤动的常用治疗药物。自1960年,相继有研究发现,洋地黄毒苷、地高辛、哇巴因等强心苷类药物具有预防和治疗肿瘤的作用[3]。Stenkvist等[4]研究表明,乳腺癌患者在使用洋地黄治疗后,肿瘤转变为良性的比例升高,且在乳房切除术5年后,使用洋地黄治疗的患者乳腺癌复发率仅为对照组的10.42%。同时,Goldin等[5]在给予127位癌症患者使用洋地黄治疗后,发现21例癌症死亡中仅有1例属于洋地黄组。并且CGS能选择性地抑制肿瘤细胞的增殖,诱导其凋亡,而对正常细胞无明显影响[6],因而强心苷类化合物被认为是一类新型的抗癌药物。为了进一步证实CGS抗肿瘤治疗的临床价值,美国FDA正在进行小规模的Ⅰ期和Ⅱ期临床试验,结果尚未公布。本实验采用不同浓度的毛花苷C(lanatoside C)溶液干预肝癌Huh-7细胞,研究毛花苷C对其增殖、凋亡及凋亡相关酶caspase-7活化的影响,初步探讨毛花苷C对肝癌的抑制作用,为其临床应用提供基础。
1 材料与方法 1.1 材料 1.1.1 细胞株肝癌Huh-7细胞株购自中科院上海生物科学研究所细胞资源中心。
1.1.2 试剂毛花苷C(上海旭东海普药业有限公司,CAS:#17575-22-3),采用嘧啶试剂作溶剂溶解毛花苷C,使其终浓度为20 g·L-1,过滤除菌后,室温避光存放备用。DMEM高糖培养基(Gibco公司,货号11885-076);胎牛血清FBS(Corille公司,C1015-05);Cell Counting Kit-8试剂(上海同仁化学研究所,CK04);caspase-7单克隆抗体(12827)购自CST公司; 抗β-actin一抗(SC-47778)购自Santa Cruz公司; Annexin V-FITC/PI凋亡试剂盒(上海东仁化学科技,AD10)。
1.1.3 仪器Elix3+30L+3YNERGY超纯水系统(美国Millipore公司); 311气套式CO2培养箱(美国Thermo公司); Infinite M200 pro Nano Quant光栅型连续波长酶标仪(瑞士TECAN公司); Allegra X-22R冷冻离心机(美国贝克曼库尔特公司); ChemiDoc XRS+凝胶成像系统(美国Bio-Rad公司); BD FACSAriaⅢ分选型流式细胞仪(美国BD公司); LSM710激光共聚焦扫描显微镜(德国蔡司公司)。
1.2 方法 1.2.1 细胞培养将Huh-7细胞接种于含支原体抗生素的改良DMEM培养基中,培养于37℃、5% CO2培养箱中,胰蛋白酶常规消化传代,选择处于对数生长期的细胞进行实验。
1.2.2 细胞增殖实验胰酶室温常规消化细胞后,用含FBS的DMEM培养基吹打成分布均匀的单细胞悬液,按1×103个/孔接种于96孔板中,培养于37℃、5% CO2培养箱中,细胞贴壁24 h后,加入毛花苷C使其终浓度为0.003 2、0.016、0.08、0.4、2 mg·L-1,以等体积嘧啶作为对照,同一浓度设置3个复孔,分别培养2 h及1、3、5、7 d后,弃去培养基,每孔加入CCK-8溶液100 μL,继续培养2 h后,使用酶标仪检测450 nm波长处吸光值。增殖抑制率/%=(对照组A450值-加药组A450值)/对照组A450值×100%。
1.2.3 克隆形成实验胰酶室温常规消化细胞后,用含FBS的DMEM培养基吹打成分布均匀的单细胞悬液,按1.6×103个/孔接种于6孔板中,继续培养于恒温培养箱中。培养10 d后加毛花苷C,使其终浓度为0.003 2、0.016、0.08、0.4、2 mg·L-1,以等体积嘧啶代替毛花苷C作为对照组,同一浓度设置3个复孔,再继续培养6 d后弃去上层培养基,PBS轻柔洗板2次,细胞用4%多聚甲醛固定15 min,弃多聚甲醛,结晶紫溶液染色15 min,清水反复浸洗,室温晾干,采集图像保存后,每孔加入2 mL 10%的冰醋酸溶液溶解结晶紫,每孔再取100 μL置于96孔板中,使用酶标仪检测各孔560 nm波长处吸光度值,并按以下公式计算克隆抑制率[7]。克隆抑制率/%=(对照组A560值-加药组A560值)/对照组A560值×100%。
1.2.4 细胞凋亡检测取处于对数期的Huh-7细胞,以1×106个细胞接种于培养皿,培养24 h细胞贴壁后,加入毛花苷C,使其终浓度为0.003 2、2 mg·L-1,加等体积嘧啶作为对照组。待毛花苷C作用48 h后,消化细胞,收集细胞悬液并离心,弃上清,D-PBS重悬清洗1次,离心弃上清液,1×Annexin V Binding buffer重悬细胞,并吹打混匀,加入10 μL Annexin V/FITC和10 μL PI染色液(20 mg·L-1), 避光染色30 min。300目筛网过滤细胞悬液,使用流式细胞仪测定并采集数据[8]。并通过激光共聚焦显微镜采集加入毛花苷C 48 h后,以及相应对照组Annexin V/FITC及PI染色图像,FITC检测波长为510~550 nm。
1.2.5 Western blot检测将Huh-7细胞室温消化后接种于培养皿中,24 h贴壁后,加入毛花苷C,使其终浓度为0.003 2、0.016、0.08、0.4、2 mg·L-1,加等体积嘧啶作为对照组,作用48 h后收集细胞,采用RIPA裂解细胞提取细胞总蛋白,用BCA蛋白定量试剂盒测定蛋白质浓度,再在蛋白样品中加入上样缓冲液混匀后,95℃金属浴10 min,冰上放置10 min后,保存于-20℃冰箱备用。采用SDS-PAGE凝胶电泳分离总蛋白样品,转移至NC膜上,5%脱脂奶粉(TBST配制)室温摇床封闭1.5 h,4℃孵育一抗过夜,TBST洗膜5次,每次10 min,室温孵育二抗1.5 h,TBST洗膜5次,每次5 min,与ECL发光液反应2~3 min后,X线片曝光、显影、定影,采用Gel-Pro Analyzer图像分析系统计算分析X线片吸光度值。
1.3 统计学分析以上实验均重复3次,所有数据均采用SPSS 18.0软件进行统计学分析,数据均以x±s表示,多个样本间的均数比较采用单因素ANOVA分析。
2 结果 2.1 毛花苷C抑制Huh-7细胞增殖Tab 1的CCK-8实验结果显示,在加入毛花苷C后3 d,可发现毛花苷C对Huh-7细胞增殖的抑制作用随着药物浓度的增加而明显增强。加药5 d时,Huh-7细胞生长抑制率分别为(3.86±1.45)%、(8.64±1.43)%、(14.11±4.87)%、(79.72±2.23)%、(84.27±0.04)%。其中,0.003 2 mg·L-1毛花苷C组与对照组相比,无明显差异(P>0.05);0.016、0.08、0.4、2 mg·L-1毛花苷C组与相应对照组相比,呈现明显差异(P < 0.05)。
| Group | Concentration/ mg·L-1 |
OD450 nm | ||||
| 2 h | 1 d | 3 d | 5 d | 7 d | ||
| Control | - | 0.591 9±0.021 7 | 0.990 1±0.074 9 | 1.564 5±0.023 7 | 2.129 3±0.065 7 | 2.617 3±0.035 4 |
| Lanatoside C | 0.003 2 | 0.555 5±0.031 8 | 1.006 7±0.049 1 | 1.571 5±0.042 2 | 2.194 2±0.065 0 | 2.428 8±0.038 4 |
| 0.016 | 0.562 5±0.032 2 | 0.974 4±0.062 1 | 1.679 6±0.102 1 | 1.981 2±0.030 3* | 2.221 2±0.213 8 | |
| 0.08 | 0.528 6±0.027 1 | 0.868 0±0.013 9 | 1.659 0±0.031 9 | 1.835 4±0.072 8* | 1.742 6±0.069 9 | |
| 0.4 | 0.550 4±0.029 0 | 0.745 1±0.032 0 | 0.504 1±0.016 2 | 0.430 9±0.042 6* | 0.327 3±0.018 9 | |
| 2 | 0.556 6±0.026 0 | 0.660 0±0.014 5 | 0.379 4±0.019 2 | 0.316 7±0.004 3* | 0.276 7±0.022 1 | |
| *P<0.05 vs control | ||||||
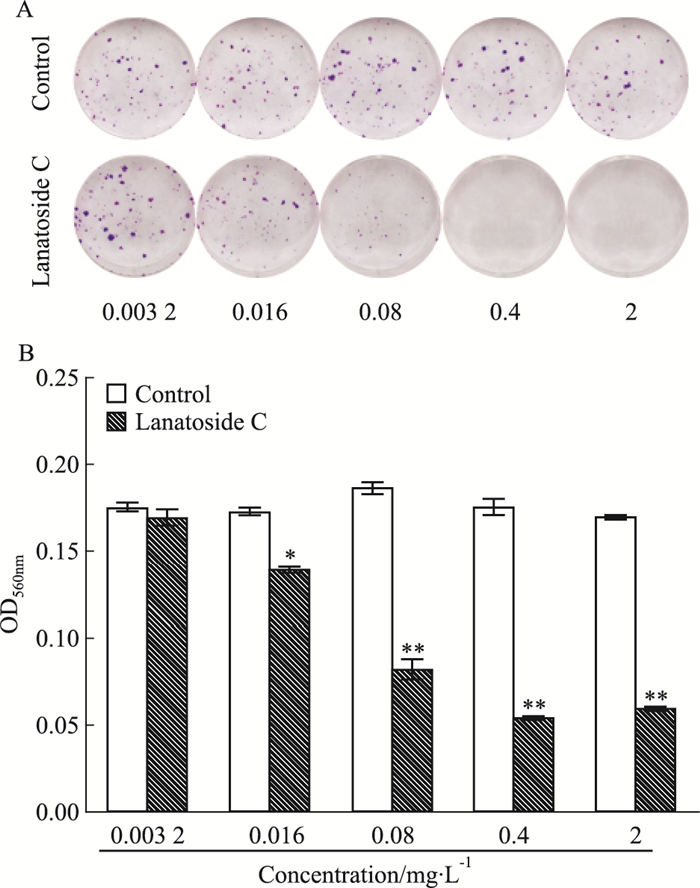
Fig 1的克隆形成实验结果显示,毛花苷C对Huh-7细胞克隆形成具有明显的抑制作用(P < 0.05),随着毛花苷C浓度增高,Huh-7细胞克隆抑制率随之增大。0.003 2、0.016、0.08、0.4、2 mg·L-1的毛花苷C干预Huh-7细胞10 d后,克隆抑制率分别为(3.29±2.84)%、(19.41±2.66)%、(56.08±3.66)%、(69.03±1.81)%、(65.02±1.12)%。其中,0.003 2 mg·L-1毛花苷C组与对照组相比无明显差异(P>0.05),0.016、0.08、0.4、2 mg·L-1毛花苷C组较对照组表现出明显差异(P < 0.05)。
|
| Fig 1 Lanatoside C inhibited hepatocellular Huh-7 cell clonal proliferation(x±s, n=3) A:Different concentrations of lanatoside C inhibited clonal proliferation of Huh-7 cells; B: Comparison of different concentrations of lanatoside C inhibiting Huh-7 cell clonal formation(A560 nm).*P < 0.05, **P < 0.01 vs control. |
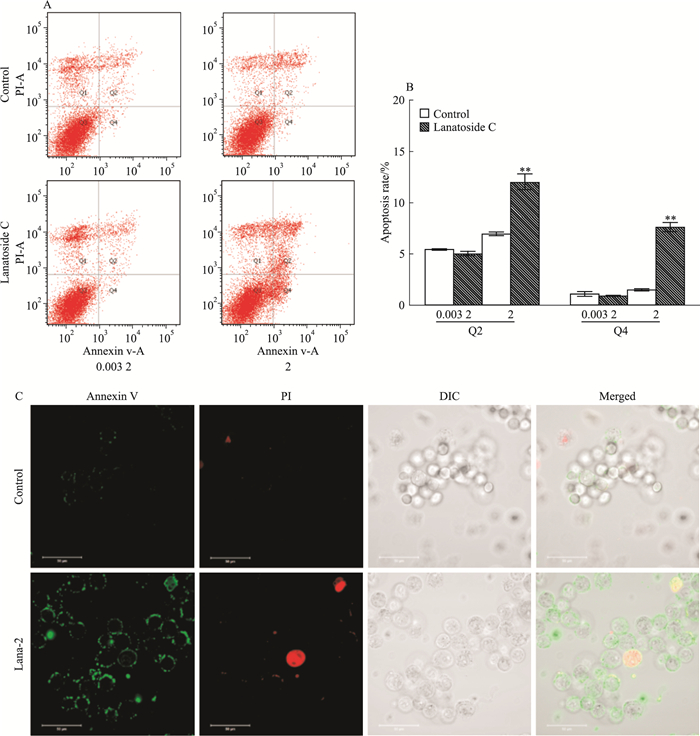
取对数生长期的Huh-7细胞,给予不同浓度的毛花苷C培养48 h后,离心收集细胞,以Annexin-V/PI双重染色后,使用流式细胞仪分析。如Fig 2A、2B所示,2 mg·L-1毛花苷C组与对照组晚期凋亡细胞(Q2)分别为(12.03±1.09)%、(6.97±0.25)%,早期凋亡细胞(Q4)分别为(7.63±0.61)%、(1.50±0.14)%,差异明显(P < 0.01)。通过激光共聚焦显微镜观察(Fig 2C),发现2 mg·L-1毛花苷C组Annexin-V染色(绿色荧光)高于对照组。
|
| Fig 2 Lanatoside C promoted Huh-7 cell apoptosis A: The apoptotic ratio of Huh-7 cells was measured by flow cytometry using Annexin V-FITC and PI staining; B:The apoptotic ratio was quantified by BD FACS software(x±s, n=3).**P < 0.01 vs control; C: Confocal laser scanning microscopy was used to observe the Annexin-V staining results of 2 mg·L-1 lanatoside C group(bar=50 μm) |
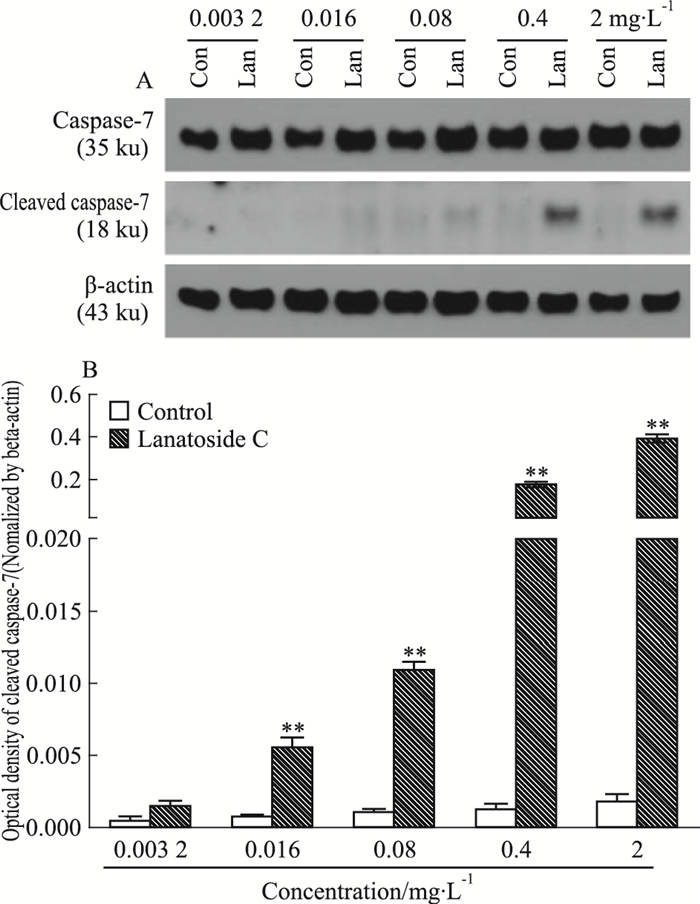
不同浓度毛花苷C干预Huh-7细胞48 h后,Fig 3蛋白免疫印迹结果显示,毛花苷C可以明显促进Huh-7细胞caspase-7蛋白从35 ku全长蛋白形式,活化为18 ku活性蛋白形式,对照组caspase-7蛋白并未出现明显活化。
|
| Fig 3 Lanatoside C up-regulated activation of caspase-7 in Huh-7 cells(x±s, n=3) A:Protein expression levels of caspase-7 and cleaved caspase-7;B:Optical density of cleaved caspase-7 normalized by β-actin. **P < 0.01 vs control |
2000年,Haux等[9]对9 271例使用洋地黄治疗的患者进行分析,虽未发现该化合物具有明显的抗癌作用,但血药浓度高能降低患白血病和尿道癌风险,为强心苷的抗癌作用研究提供了基础,现已有上千篇报道强心苷类化合物体外抗癌特性的论文发表。
强心苷类物质抗癌机制包括抑制Na+/K+-ATP酶活性、抑制缺氧诱导因子1活性、抑制成纤维细胞因子2(fibroblast growth factor-2, FGF-2)和NFκB、抑制拓扑异构酶的活性、阻断ER、诱导细胞凋亡等[10]。而化疗药物引起癌细胞死亡的关键机制为诱导细胞凋亡,caspase是参与细胞凋亡的主要蛋白酶。Badr等[11]在人恶性胶质瘤细胞研究发现,毛花苷C可激活caspase蛋白的表达,从而诱导其发生凋亡。Caspase最初以酶原存在于细胞中,当起始凋亡蛋白酶如caspase-8、caspase-9通过低聚反应而激活时,进一步激活caspase-3、caspase-6、caspase-7等效应凋亡蛋白酶,从而导致与凋亡表型相关的一系列生物化学及形态学变化[12]。
Caspase可通过外源性途径及线粒体内源性途径激活[13],当FasL与肿瘤坏死因子(tumor necrosis factor,TNF)分别与细胞膜上的死亡受体Fas及肿瘤坏死因子受体TNFR发生特异性结合,随即引发死亡诱导信号复合体(death-inducing signaling complex,DISC)的形成,DISC募集caspase-8,并促进下游的caspase酶原激活。而内源性途径则是由各种细胞内外应激如癌基因的活化、DNA损伤、细胞缺氧等引起[14]。在内源性凋亡途径中,激活后线粒体外膜通透性增加,从而使细胞色素C及其他促凋亡因子由线粒体向胞质释放,这一过程主要受Bcl-2蛋白家族调控。Bcl-2蛋白家族的Bak、Bax等激活后,与线粒体外膜受体结合,在线粒体膜上形成孔道,使线粒体内部一些大分子蛋白如Smac/DIAB- LO、HtrA家族成员Omi/HtrA2以及细胞色素C由孔道释放到细胞质中,细胞色素C上存在caspase活化因子1(Apaf-1)特异性结合位点,Apaf-1与之反应后,诱导别构效应而激活[15],Apaf-1上具有与caspase-9同源的caspase募集与激活结合域(caspase raised and activating domain,CRAD),活化的Apaf-1能够以CARD-CARD方式聚集并活化caspase-9,形成由细胞色素C、Apaf-1、caspase-9组成的凋亡小体,该凋亡小体可激活caspase-7,进而诱导下游蛋白的降解,最终引起细胞凋亡。在本实验中,采用不同浓度的毛花苷C干预肝癌Huh-7细胞,结果显示,毛花苷C能明显抑制Huh-7细胞增殖,促进Huh-7细胞凋亡,增强caspase-7的活化水平。提示毛花苷C诱导细胞Huh-7发生凋亡可能与细胞内源性凋亡途径有关,具体作用机制尚不明确,需要进一步实验进行证实。
( 致谢: 本实验在桂林医学院科学实验中心完成,感谢对本课题研究给予帮助的老师和同学。)
| [1] |
吕桂帅, 陈磊, 王红阳. 我国肝癌研究的现状与前景[J]. 生命科学, 2015, 27(3): 237-48. Lyu G S, Chen L, Wang H Y. Research progress and prospect of liver cancer in China[J]. Chin Bull Life Sci, 2015, 27(3): 237-48. |
| [2] |
Lencioni R, Petruzzi P, Crocetti L. Chemoembolization of hepatocellular carcinoma[J]. Semin Intervent Radiol, 2013, 30(1): 3-11. |
| [3] |
王发亮, 侯金超. 强心苷类药物抗肿瘤作用的研究进展[J]. 癌症进展, 2017, 15(3): 217-20. Wang F L, Hou J C. Advances in research of anti-tumor effects of cardiac glycosides[J]. Oncol Prog, 2017, 15(3): 217-20. |
| [4] |
Stenkvist B, Bengtsson E, Eriksson O, et al. Cardiac glycosides and breast cancer, revisited[J]. N Engl J Med, 1982, 306: 484. |
| [5] |
Goldin A, Safa A. Digitalis and cancer[J]. Lancet, 1984, 1(8386): 1134. |
| [6] |
Cerella C, Mario D, Marc D, et al. Assembling the puzzle of anti-cancer mechanisms triggered by cardiac glycosides[J]. Mitochondrion, 2013, 13(3): 225-34. doi:10.1016/j.mito.2012.06.003 |
| [7] |
钟磊, 师健友. 耐吉非替尼的HCC827GR细胞的高效诱导及其药理学特性[J]. 中国药理学通报, 2016, 32(9): 1284-8. Zhong L, Shi J Y. Efficient induction of gefitinib-resistant cell line HCC827GR and its pharmacological properties[J]. Chin Pharmacol Bull, 2016, 32(9): 1284-8. doi:10.3969/j.issn.1001-1978.2016.09.019 |
| [8] |
王建超, 余翥, 胡艳梅, 等. 毛花苷C促进肝癌SMMC-7721细胞凋亡及抑制survivin的表达[J]. 世界华人消化杂志, 2016, 24(9): 1331-41. Wang J C, Yu Z, Hu Y M, et al. Lanatoside C promotes apoptosis and inhibits survivin expression in hepatocarcinoma SMMC-7721 cells[J]. WCJD, 2016, 24(9): 1331-41. |
| [9] |
Haux J, Klepp O, Spigset O, et al. Digitoxin medication and cancer; case control and internal dose-response studies[J]. BMC Cancer, 2001, 1(1): 11. doi:10.1186/1471-2407-1-11 |
| [10] |
Pan L, Zhang Y, Zhao W, et al. The cardiac glycoside oleandrin induces apoptosis in human colon cancer cells via the mitochondrial pathway[J]. Cancer Chemother Pharmacol, 2017, 80(1): 91-100. doi:10.1007/s00280-017-3337-2 |
| [11] |
Badr C E, Wurdinger T, Nilsson J M, et al. Lanatoside C sensitizes glioblastoma cells to tumor necrosis factor-related apoptosis-inducing ligand and induced an alternative cell death pathway[J]. Neuro Oncol, 2011, 13(11): 1213-24. doi:10.1093/neuonc/nor067 |
| [12] |
张红艳, 翟丽, 王婷婷, 等. 胡黄连苷Ⅱ通过抑制cyto C/caspase-9/caspase-3通路发挥神经保护作用[J]. 中国药理学通报, 2017, 33(5): 668-74. Zhang H Y, Zhai L, Wang T T, et al. Picroside Ⅱ plays a neuroprotective effect by inhibiting cyto C/caspase-9/caspase-3 signal pathway following ischemia/reperfusion injury in rats[J]. Chin Pharmacol Bull, 2017, 33(5): 668-74. doi:10.3969/j.issn.1001-1978.2017.05.016 |
| [13] |
Chao M W, Chen T H, Huang H L, et al. Lanatoside C, a cardiac glycoside, acts through protein kinase Cδ to cause apoptosis of human hepatocellular carcinoma cells[J]. Sci Rep, 2017, 7: 46134. doi:10.1038/srep46134 |
| [14] |
Wang D H, Hu J R, Wang L Y, et al. The apoptotic function analysis of p53, Apaf1, Caspase3 and Caspase7 during the spermatogenesis of the Chinese fire-bellied newt Cynops orientalis[J]. PLoS One, 2012, 7(6): e39920. doi:10.1371/journal.pone.0039920 |
| [15] |
Reubold T F, Eschenburg S A. molecular view on signal transduction by the apoptosome[J]. Cell Signal, 2012, 24(7): 1420-5. doi:10.1016/j.cellsig.2012.03.007 |

