

2. 遵义医学院珠海校区药理学教研室,广东 珠海 519041
2. Dept of Pharmacology, Zunyi Medical University, Zhuhai Campus, Zhuhai Guangdong 519041, China
肺动脉高压(pulmonary arterial hypertension, PAH)是以肺动脉重构、肺小动脉痉挛为主要特征的一种恶性心血管疾病。其中,肺动脉重构是PAH最常见的病理表现,也是PAH形成的重要标志[1-2]。肺动脉平滑肌细胞的增殖与凋亡失衡是肺动脉腔变窄、肺血管阻力增加,引发肺动脉重构的重要原因[2-3]。近年研究表明,在野百合碱(monocrotaline, MCT)诱导的PAH模型中,肺动脉平滑肌细胞明显增殖,且加重了肺动脉重构的发生[3-4]。因此,抑制肺动脉平滑肌细胞的增殖,促进其凋亡是抑制肺动脉重构、治疗PAH的关键。淫羊藿次苷Ⅱ(icarisideⅡ, ICSⅡ)是小檗科植物淫羊藿的主要活性成分之一,具有抗癌、抗炎、抗氧化、抗衰老等作用[5-7]。已有研究表明,ICSⅡ对多发性骨髓瘤细胞U266、肝母细胞瘤HepG2等多种肿瘤细胞均具有促凋亡作用[8-10]。故本课题组推测,ICSⅡ可能对肺动脉平滑肌细胞也有促凋亡的作用。因此,本研究以MCT诱导的肺动脉重构大鼠为研究对象,观察ICSⅡ对肺动脉重构的作用,并探讨其机制是否与促进肺动脉平滑肌细胞的凋亡有关。
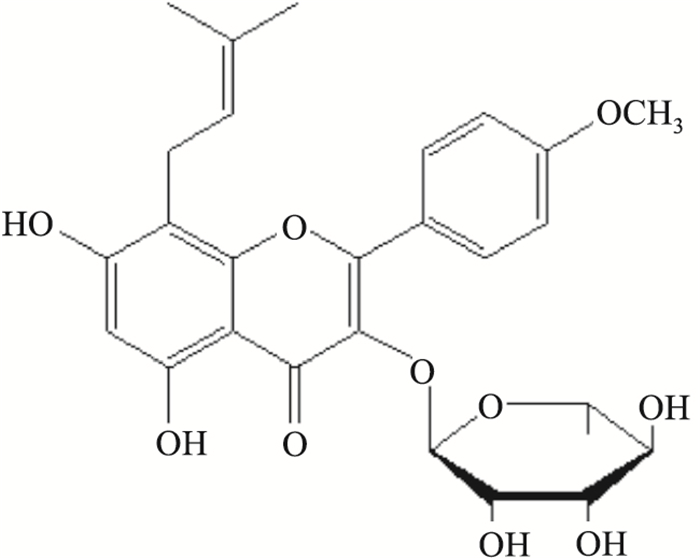
1 材料与方法 1.1 实验动物、药物及试剂SD大鼠,♂,体质量(210±10)g,购自第三军医大学大坪医院实验动物中心,SPF级,许可证号:SCXK(渝)2012-0005。ICSⅡ(纯度≥98%,南京泽朗医药科技有限公司,结构式见Fig 1);MCT(纯度≥98%,美国Sigma公司); TUNEL原位细胞凋亡检测试剂盒(德国Roche公司); Bax、Bcl-2、活化的caspase-3抗体(美国Abcam公司); HRP标记的β-actin抗体(上海康成生物技术有限公司); ECL发光剂(七海生物有限公司)。
|
| Fig 1 The structural formula of ICS Ⅱ |
Mini-PROTEAN3电泳仪、Mini Trans-Blot Turbo转印系统、CCD成像系统(美国Bio-Rad公司); Olympus光学显微镜(日本Olympus公司)。
1.3 MCT的配制称取0.5 g MCT溶于10 mL 0.5 mo1·L-1的盐酸中,用0.5 mo1·L-1氢氧化钠调pH至7.4,加生理盐水定容至50 mL。
1.4 实验分组、造模及给药40只大鼠随机分为对照组(Control)、模型组(Model)、ICSⅡ低剂量组(ICSⅡ-L,4 mg·kg-1)、ICSⅡ中剂量组(ICSⅡ-M,8 mg·kg-1)、ICSⅡ高剂量组(ICSⅡ-H,16 mg·kg-1),每组8只。对照组经颈背部一次性皮下注射生理盐水5 mL·kg-1,其余4组注射MCT 50 mg·kg-1诱导肺动脉重构模型。ICSⅡ各剂量组于造模后d 1开始每天灌胃给药,至d 28结束。空白组和模型组灌胃给予等量溶媒。
1.5 肺小动脉形态学观察取各组大鼠左肺远离肺门处5 mm左右的肺组织,于4%甲醛溶液中固定48 h后,脱水、包埋、切片,进行HE染色,光镜下观察肺小动脉形态学变化,并拍照记录。
1.6 肺动脉平滑肌细胞凋亡的检测TUNEL法测定肺动脉平滑肌细胞凋亡,光镜下观察每组肺动脉平滑肌细胞凋亡情况,计算400倍视野下凋亡细胞数目占总细胞数的百分比。其中正常细胞核显蓝色,凋亡阳性细胞核呈棕黄色或褐色。
1.7 肺组织Bax、Bcl-2、活化的caspase-3蛋白的检测取各组肺组织约100 mg,提取总蛋白后采用BCA法定量。12%的SDS-PAGE凝胶电泳分离后,半干转至PVDF膜上,室温封闭2 h后,加入一抗Bax(1 :1 000稀释)、Bcl-2(1 :1 000稀释)、活化的caspase-3(1 :5 000稀释)、β-actin(1 :5 000稀释)4℃孵育16 h,室温孵育二抗1 h,ECL化学发光显色,Quantity One定量分析软件进行灰度分析。
1.8 统计学处理数据以x±s表示,用SPSS 19.0软件进行One-way ANOVA分析,方差齐采用LSD法,方差不齐采用Dunnett’T3法。
2 结果 2.1 ICSⅡ对MCT所致大鼠肺小动脉形态学的影响对肺小动脉形态初步观察发现,与对照组相比,模型组大鼠肺小动脉中膜及管壁增厚、管腔狭窄、血管周围及肺间质炎症细胞浸润明显。与模型组相比,ICSⅡ给药组大鼠肺小动脉中膜及管壁变薄、管腔增大、血管周围及肺间质炎症减轻(Fig 2)。

|
| Fig 2 Effect of ICS Ⅱ on pulmonary histomorphology induced by MCT in rats(×200) A: Control; B: Model; C: ICS Ⅱ-L; D: ICS Ⅱ-M; E: ICS Ⅱ-H. |
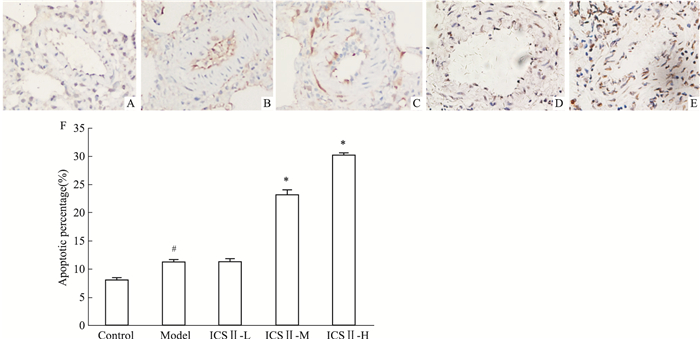
如Fig 3所示,与对照组相比,模型组肺动脉平滑肌细胞发生凋亡,TUNEL阳性细胞比率升高(P < 0.05)。与模型组相比,ICSⅡ中、高剂量组肺动脉平滑肌细胞凋亡数均明显增加,TUNEL阳性细胞比率升高(P < 0.05)。
|
| Fig 3 Effect of ICS Ⅱ on pulmonary artery smooth muscle cell apoptosis induced by MCT in rats(×400) A: Control; B: Model; C: ICSⅡ-L; D: ICSⅡ-M; E: ICSⅡ-H; F: Apoptotic cell percentage. #P < 0.05 vs control; *P < 0.05 vs model. |
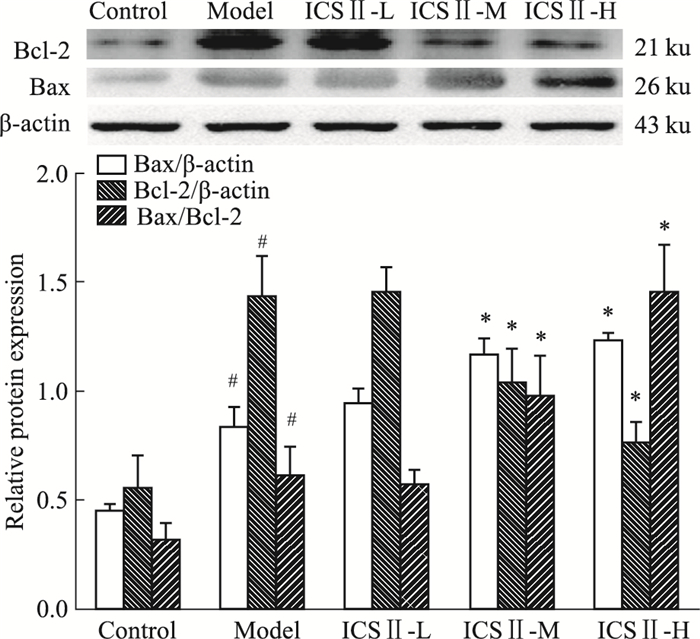
如Fig 4所示,与对照组相比,模型组大鼠肺组织Bax、Bcl-2蛋白表达上调(P < 0.05),Bax/Bcl-2的比值升高(P < 0.05)。与模型组相比,ICSⅡ中、高剂量组大鼠肺组织Bax蛋白的表达明显上调(P < 0.05),Bcl-2蛋白的表达明显下调(P < 0.05),Bax/Bcl-2的比值升高(P < 0.05)。
|
| Fig 4 Effect of ICS Ⅱ on the expression of Bax and Bcl-2 in MCT-induced rats(x±s, n=3) #P < 0.05 vs control; *P < 0.05 vs model |
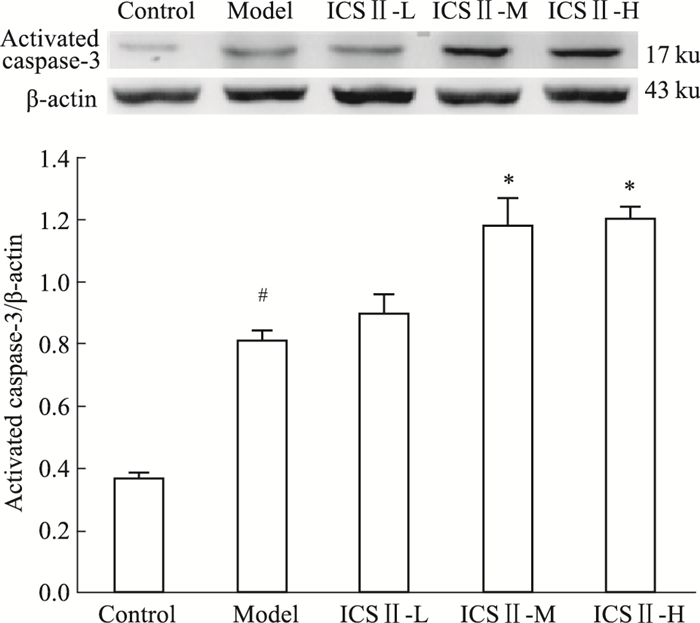
如Fig 5所示,与对照组相比,模型组大鼠肺组织活化的caspase-3的水平升高(P < 0.05)。与模型组相比,ICSⅡ中、高剂量组大鼠肺组织活化的caspase-3的水平明显升高(P < 0.05)。
|
| Fig 5 Effect of ICS Ⅱ on the expression of apoptosis-related protein activated caspase-3 in MCT-induced rats(x±s, n=3) #P < 0.05 vs control; *P < 0.05 vs model |
随着对PAH研究的不断深入,肺动脉重构在PAH中的作用日益受到重视。肺动脉重构是不同原因所致PAH的共同病理生理基础,亦是近年PAH发病机制的主要研究方向。本研究采用MCT诱导的肺动脉重构模型,观察ICSⅡ对肺动脉重构的作用,并探讨其机制是否与促进肺动脉平滑肌细胞的凋亡有关。本研究结果显示,与对照组比,模型组肺小动脉中膜明显增厚、管腔变窄、炎症细胞浸润明显,提示模型成功,与文献报道一致[11]。与模型组比,ICSⅡ给药组大鼠肺小动脉中膜变薄、管腔增大、炎症减轻,提示ICSⅡ具有抗MCT所致大鼠肺动脉重构的作用。
为进一步探讨ICSⅡ抗肺动脉重构的作用机制,本研究采用TUNEL染色观察了ICSⅡ对MCT所致大鼠肺动脉平滑肌细胞凋亡的影响。结果发现,与模型组比,给予ICSⅡ后大鼠的肺动脉平滑肌细胞凋亡明显增加,TUNEL阳性细胞比率升高。提示ICSⅡ抗肺动脉重构的作用与促进肺动脉平滑肌细胞的凋亡有关。细胞凋亡是外界刺激和细胞自身因素共同作用的结果。Bcl-2家族是调控细胞凋亡的重要因子,按其功能可分为促凋亡蛋白和抗凋亡蛋白两种。Bax是Bcl-2家族中主要的促凋亡蛋白,Bcl-2是主要的抗凋亡蛋白,Bax/Bcl-2的比值是影响细胞凋亡的关键因素。细胞发生凋亡的同时会引起线粒体释放细胞色素C,激活caspase-3,使caspase-3活化,从而促进细胞凋亡[12]。
淫羊藿又名仙灵脾,为小檗科淫羊属(EpimediumL.)植物,是中国传统的益补中药之一,具有“补肝阳、强筋骨、阳益精和祛风湿”的功效。ICSⅡ是淫羊藿的主要活性成分之一。已有研究表明,ICSⅡ可通过促进caspase-3的活化,促进胶质母细胞瘤细胞的凋亡[13]。在本研究中,与模型组比,给予ICSⅡ后肺组织Bax/Bcl-2比值增加,caspase-3的活化水平明显上调。提示ICSⅡ促进肺动脉平滑肌细胞凋亡的机制可能与下调Bcl-2,上调Bax和活化的caspase-3的表达有关。
有趣的是,与对照组比,模型组肺组织中Bax/Bcl-2比值上调,caspase-3的活化水平也增加。Shi等[3]研究发现,在MCT诱导的PAH模型中,模型组肺组织中Bax/Bcl-2的比值和caspase-3的活化水平均较对照组明显上调,与本研究结果一致。分析其原因可能是由于肺动脉平滑肌细胞的凋亡速率远低于其增殖速率,也可能与肺动脉内皮细胞的凋亡有关。内皮细胞损伤是引发肺动脉重构的起始因素,也是导致肺动脉平滑肌细胞异常增殖及凋亡受阻的重要原因[14],故在本研究中即使肺动脉平滑肌细胞发生了凋亡,但肺动脉重构依然明显。
( 致谢: 本文所有实验均在遵义医学院基础药理教育部重点实验室暨特色民族药教育部国际合作联合实验室完成,感谢实验室所有老师的支持与帮助。)
| [1] |
王丹姝, 方莲花, 杜冠华. 转化生长因子β1在肺动脉高压中作用的研究进展[J]. 中国药理学通报, 2017, 33(6): 741-4. Wang D S, Fang L H, Du G H. Research progress on role of TGF-β1 in pulmonary artery hypertension[J]. Chin Pharmacol Bull, 2017, 33(6): 741-4. doi:10.3969/j.issn.1001-1978.2017.06.001 |
| [2] |
宋洁梅, 温小安, 孙宏斌. 肺动脉高压发生机制及治疗药物的研究进展[J]. 中国药科大学学报, 2013, 44(1): 1-10. Song J M, Wen X A, Sun H B. Progress in pathogenesis and therapeutic drugs of pulmonary arterial hypertension[J]. J Chin Pharm Univ, 2013, 44(1): 1-10. |
| [3] |
Shi R Z, Wei Z H, Zhu D Y, et al. Baicalein attenuates monocrotaline-induced pulmonary arterial hypertension by inhibiting vascular remodeling in rats[J]. Pulm Pharmacol Ther, 2018, 48: 124-35. doi:10.1016/j.pupt.2017.11.003 |
| [4] |
Chen F, Wang H, Yan J, et al. Grape seed proanthocyanidin reverses pulmonary vascular remodeling in monocrotaline-induced pulmonary arterial hypertension by down-regulating HSP70[J]. Biomed Pharmacother, 2018, 101: 123-8. doi:10.1016/j.biopha.2018.02.037 |
| [5] |
Peng Y G, Zhang L. Baohuoside-I suppresses cell proliferation and migration by up-regulating miR-144 in melanoma[J]. Pharm Biol, 2018, 56(1): 43-50. doi:10.1080/13880209.2017.1418391 |
| [6] |
Deng Y, Long L, Wang K, et al. Icariside Ⅱ, a broad-spectrum anti-cancer agent, reverses beta-amyloid-induced cognitive impairment through reducing inflammation and apoptosis in rats[J]. Front Pharmacol, 2017, 8: 39. |
| [7] |
Deng Y, Xiong D, Yin C, et al. Icariside Ⅱ protects against cerebral ischemia-reperfusion injury in rats via nuclear factor-κB inhibition and peroxisome proliferator-activated receptor up-regulation[J]. Neurochem Int, 2016, 96: 56-61. doi:10.1016/j.neuint.2016.02.015 |
| [8] |
Kim S H, Ahn K S, Jeong S J, et al. Janus activated kinase 2/signal transducer and activator of transcription 3 pathway mediates icariside Ⅱ-induced apoptosis in U266 multiple myeloma cells[J]. Eur J Pharmacol, 2011, 654(1): 10-6. doi:10.1016/j.ejphar.2010.11.032 |
| [9] |
Geng Y D, Zhang C, Shi Y M, et al. Icariside Ⅱ-induced mitochondrion and lysosome mediated apoptosis is counterbalanced by an autophagic salvage response in hepatoblastoma[J]. Cancer Lett, 2015, 366(1): 19-31. doi:10.1016/j.canlet.2015.05.032 |
| [10] |
Khan M, Maryam A, Qazi J I, Ma T. Targeting apoptosis and multiple signaling pathways with icariside Ⅱ in cancer cells[J]. Int J Biol Sci, 2015, 11(9): 1100-12. doi:10.7150/ijbs.11595 |
| [11] |
李叶丽, 王颖婉, 李利生, 等. 蛇床子素通过上调p53、下调增殖细胞核抗原和Ki67的表达抗野百合碱所致肺小动脉重构[J]. 中国新药与临床杂志, 2015, 34(10): 773-7. Li Y L, Wang Y W, Li L S, et al. Osthole reverses pulmonary artery remodeling induced by monocrotaline through increasing expression of p53 and reducing the expression of proliferating cell nuclear antigen and Ki67[J]. Chin J New Drugs Clin Remedies, 2015, 34(10): 773-7. |
| [12] |
吴雨婷, 付舒, 岳云, 等. 淫羊藿次苷Ⅱ改善自发性高血压大鼠左心室心肌细胞凋亡[J]. 中国药理学通报, 2017, 33(12): 1744-9. Wu Y T, Fu S, Yue Y, et al. Icariside Ⅱ improves left ventricular cardiomyocyte apoptosis in spontaneously hypertensive rats[J]. Chin Pharmacol Bull, 2017, 33(12): 1744-9. doi:10.3969/j.issn.1001-1978.2017.12.023 |
| [13] |
Quan K, Zhang X, Fan K, et al. Icariside Ⅱ induces cell cycle arrest and apoptosis in human glioblastoma cells through suppressing Akt activation and potentiating FOXO3a activity[J]. Am J Transl Res, 2017, 9(5): 2508-19. |
| [14] |
Huertas A, Perros F, Tu L, et al. Immune dysregulation and endothelial dysfunction in pulmonary arterial hypertension: a complex interplay[J]. Circulation, 2014, 129(12): 1332-40. doi:10.1161/CIRCULATIONAHA.113.004555 |

