

随着人们生活水平的提高和饮食习惯的改变,近几十年来痛风的发病率逐年升高[1]。痛风是因为血尿酸浓度过高,导致尿酸盐(monosodium urate,MSU)晶体沉积在关节及其周围组织中,激发机体产生的无菌性炎症反应。越来越多的资料提示,MSU诱导的核因子κB(nuclear factor κB,NF-κB)活化和炎性介质大量产生在痛风炎症发生、发展中起了重要作用[2]。在非活化状态下,NF-κB p65蛋白与NF-κB抑制蛋白(inhibitor of NF-κB,IκB)α结合而存在于细胞质中。MSU可与关节局部细胞,如巨噬细胞、单核细胞、成纤维样滑膜细胞表面的Toll样受体(Toll-like receptor,TLR)-2和TLR-4结合,通过磷脂酶C和D、Src酪氨酸激酶、G蛋白或者丝裂原激活的蛋白激酶等信号通路,促使IκBα泛素化降解,导致p65蛋白核转移,促进多种炎性介质基因如肿瘤坏死因子α(tumor necrosis factor α,TNF-α)、白细胞介素(interleukin,IL)-1β和IL-6大量转录,最终促进痛风炎症的发生与发展[3]。
在中医药临床实践中,牡丹皮是用于痛风治疗的常用中药之一。丹皮酚是牡丹皮中主要的药理成分,已被证实具有抗炎、镇痛、降血糖、降血脂、抗动脉粥样硬化、抗心律失常、抗菌、抗肿瘤等药理作用[4]。丹皮酚抗炎药理作用已经在多种动物炎性模型上得到证实[5],但是丹皮酚对MSU诱导的痛风炎症发生、发展影响如何,至今未见报道。本研究拟采用MSU诱导的大鼠痛风性关节炎(MSU-induced gouty arthritis,MGA)模型,观察丹皮酚对关节肿胀、关节功能、关节病理损伤、炎性介质表达和NF-κB活化的影响,以明确丹皮酚是否有抗痛风的药理作用及其潜在的药理机制,为利用丹皮酚研发新的抗痛风药物提供科学依据。
1 材料 1.1 试剂丹皮酚、尿酸、抗酒石酸酸性磷酸酶(tartrate-resistant acid phosphatase,TRAP)试剂盒,均购自美国Sigma公司; 秋水仙碱(colchicine)片购自云南植物药业有限公司(国药准字H5302016,批号20160802);TNF-α抗体、IL-1β抗体、IL-6抗体、免疫组织化学染色试剂盒(二步法),均购自北京中杉金桥生物技术有限公司; IκBα抗体、p65抗体、β-actin抗体,均购自美国Santa Cruz公司; PVDF膜和ECL试剂购自美国Milipore公司; RIPA裂解液和BCA蛋白测定试剂盒均购自碧云天生物技术有限公司; 其他试剂均为国产分析纯。
1.2 仪器RC24型高速冷冻离心机(Thermo Scientific Sorvall公司); PBC7140足体积检测仪(Ugo Basile公司); Infinite M200型全标仪(BioTek公司); ChemiDoc XRS型成像系统(Bio-Rad公司); 80i型正置荧光显微镜(Nikon公司)。
1.3 实验动物SD大鼠,♂,体质量(200~240) g,购自重庆医科大学实验动物中心,动物合格证号:SCXK(渝)2016-0012。所有动物适应性喂养1周后开始实验。
2 方法 2.1 MSU晶体的制备[6]4 g尿酸溶解于预热至60℃的800 mL蒸馏水中,用0.5 mol·L-1氢氧化钠调整pH至8.9后,4℃静置过夜。溶液经4 000 r·min-1离心10 min,取沉淀为MSU晶体,纯乙醇洗3次,干燥后高压灭菌。
2.2 模型制备与分组给药SD大鼠随机分为6组,每组10只,具体如下:对照组(Control)、模型组(MGA)、阳性对照组(0.3 mg·kg-1秋水仙碱)、丹皮酚组(50、100、200 mg·kg-1)。丹皮酚、秋水仙碱组连续灌胃给药7 d,每天1次,对照组与模型组给予同体积生理盐水。d 5给药后1 h给予大鼠右后足踝关节腔内注射0.1 mL MSU溶液[7](MSU混悬于生理盐水,终浓度为20 g·L-1),对照组大鼠右踝关节腔注射0.1 mL生理盐水。继续给药2 d,于造模后48 h麻醉处死动物,取材进行相关检测。
2.3 关节体积检测分别于造模前(0 h),造模后2、6、12、24、48 h检测右踝关节体积。
2.4 步态评分检测造模后24 h检测大鼠步态评分,评分标准如下[7],0分:双足正常行走; 1分:轻度跛行,左后足可着地; 2分:中度跛行,左后足可着地但马上收回; 3分:重度跛行,左后足不能着地,只能3足着地行走。
2.5 组织学评分检测取大鼠右后足踝关节,于4%多聚甲醛缓冲液中固定24 h,10% EDTA溶液脱钙28 d,常规脱水,透明,包埋,切片,苏木精伊红染色,然后进行组织学评分[8]。评分参数包括组织肿胀、炎性细胞浸润、滑膜组织增生和组织坏死。计分标准如下,0分:正常; 1分:轻度病变; 2分:中度病变; 3分:重度病变。关节体积、步态分析及组织学评分检测均由不知道本研究方案的实验员完成。
2.6 TRAP染色检测取上述实验所制备的切片,按照TRAP染色试剂盒说明书进行染色,100倍镜下计数TRAP阳性(酒红色)染色细胞数作为破骨细胞数量。
2.7 免疫组织化学染色检测取上述实验制备的切片,按照“二步法”免疫组织化学染色试剂盒说明书操作。所用抗体分别为抗TNF-α、抗IL-1β、抗IL-6抗体。DAB显色,中性树胶封片。200倍镜下分析阳性染色的光密度值,随机取同组10张切片的平均光密度值代表该细胞因子的表达值。
2.8 Western blot检测取大鼠左后足踝关节滑膜组织,加入RIPA裂解液及蛋白酶抑制剂反复匀浆,4℃下12 000 r·min-1离心15 min后取上清。取等量蛋白进行SDS-PAGE电泳,转移蛋白至PVDF膜,5%脱脂奶粉封闭,4℃下与IκBα抗体、p65抗体或者β-actin抗体共同孵育过夜,再与相应的二抗室温共同孵育1 h,加入ECL发光试剂后,成像系统检测分析信号。以目的蛋白与内参蛋白的光密度比值代表该目的蛋白的表达值。
2.9 统计学分析数据用x±s表示,采用单因素方差分析,用SPSS 18.0软件进行统计学处理。
3 结果 3.1 丹皮酚对MGA大鼠足肿胀和步态评分的影响如Tab 1所示,与对照组相比,踝关节腔内注射MSU 6 h后大鼠即出现明显的足肿胀(P<0.01),12 h后足肿胀达到最高值(P<0.01),并持续至注射MSU后48 h(P<0.01),而对照组大鼠足体积则无明显变化。与MGA组相比,给予0.3 mg·kg-1秋水仙碱、丹皮酚(100、200 mg·kg-1)治疗后,均使得MSU致炎48 h后的大鼠足肿胀明显减轻(P<0.05或P<0.01);但给予50 mg·kg-1丹皮酚治疗对MSU致炎48 h后的大鼠足肿胀无明显影响。与此同时,如Tab 2所示,踝关节腔内注射MSU 24 h导致大鼠步态评分数值明显增高。与MGA组相比,给予0.3 mg·kg-1秋水仙碱、丹皮酚(100、200 mg·kg-1)治疗后,均使MGA大鼠步态评分明显降低(P<0.05或P<0.01),但给予50 mg·kg-1丹皮酚治疗对MGA大鼠步态评分无明显影响。
| Group | Dose/ mg·kg-1 |
Paw volume/mL | |||||
| 0 h | 6 h | 12 h | 24 h | 48 h | |||
| Control | - | 0.39±0.03 | 0.39±0.04 | 0.38±0.04 | 0.41±0.03 | 0.39±0.04 | |
| MGA | - | 0.40±0.05 | 1.21±0.08## | 1.33±0.08## | 1.12±0.08## | 0.99±0.07## | |
| Colchicine | 0.3 | 0.40±0.03 | 0.89±0.05** | 0.98±0.06** | 0.78±0.05** | 0.66±0.05** | |
| Paeonol | 50 | 0.39±0.04 | 1.18±0.08 | 1.29±0.05 | 1.11±0.07 | 0.97±0.08 | |
| 100 | 0.40±0.04 | 1.14±0.07 | 1.20±0.08* | 1.01±0.07* | 0.82±0.05* | ||
| 200 | 0.40±0.03 | 1.06± 0.05* | 1.08±0.06** | 0.92±0.07** | 0.76±0.06** | ||
| ##P < 0.01 vs control; *P < 0.05, **P < 0.01 vs MGA | |||||||
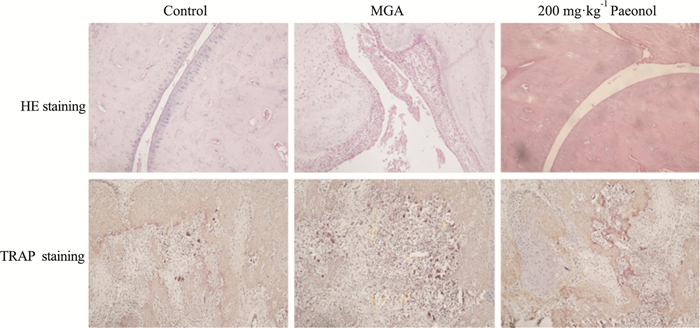
如Tab 2、Fig 1所示,与对照组比较,注射MSU 48 h后,大鼠踝关节出现明显的滑膜增生、肿胀,严重者出现坏死,同时伴随有大量的炎性细胞浸润,因此模型组组织学评分数值明显升高。与此同时,注射MSU 48 h后大鼠踝关节TRAP阳性染色细胞数量也比对照组明显增加(P<0.01)。与MGA组比较,给予0.3 mg·kg-1秋水仙碱、丹皮酚(100、200 mg·kg-1)治疗则明显降低了MGA大鼠组织学评分和TRAP阳性染色细胞数(P<0.05或P<0.01),且呈剂量依赖性; 但给予50 mg·kg-1丹皮酚治疗对MGA大鼠组织学评分和TRAP阳性染色细胞数均无明显影响。
| Group | Dose/ mg·kg-1 |
Gait score | Histological score | Osteoclast number |
| Control | - | 0 | 0 | 13.7±3.9 |
| MGA | - | 2.6±0.5 | 2.7±0.5 | 84.0±8.9## |
| Colchicine | 0.3 | 1.4±0.5** | 1.6±0.5** | 42.5±7.2** |
| Paeonol | 50 | 2.5±0.5 | 2.5±0.5 | 82.4±8.5 |
| 100 | 2.0±0.5* | 2.1±0.7* | 75.0±7.9* | |
| 200 | 1.6±0.5** | 2.0±0.7** | 64.7±13.9** | |
| ##P<0.01 vs control; *P<0.05, **P<0.01 vs MGA | ||||
|
| Fig 1 Effect of paeonol on histological damage and osteoclast formation in MGA rats (×100) |
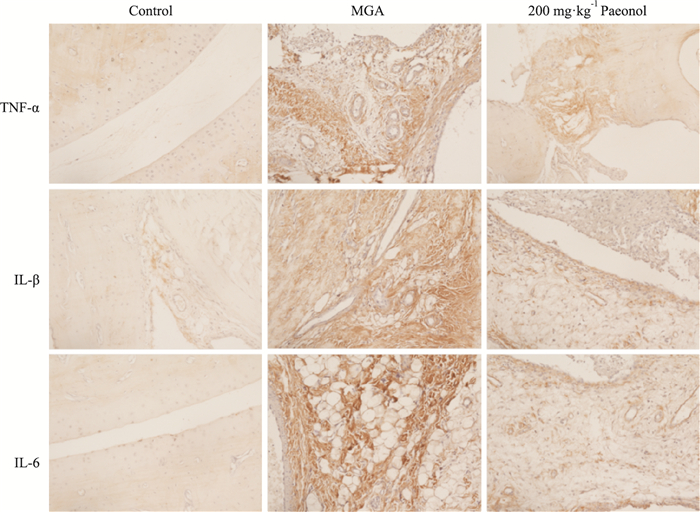
如Tab 3、Fig 2所示,与对照组相比,注射MSU 48 h后大鼠关节组织中TNF-α、IL-1β、IL-6表达均明显升高(P<0.01)。与MGA组相比,给予0.3 mg·kg-1秋水仙碱、丹皮酚(100、200 mg·kg-1)治疗明显降低了MGA大鼠关节组织中TNF-α、IL-1β和IL-6表达,且呈现出剂量依赖性(P<0.05或P<0.01);但给予50 mg·kg-1丹皮酚治疗对MGA大鼠关节组织中TNF-α、IL-1β和IL-6表达无明显影响。
| Group | Dose/mg·kg-1 | TNF-α(n=10) | IL-1β(n=10) | IL-6(n=10) | p65(n=3) | IκBα(n=3) |
| Control | - | 0.05±0.04 | 0.08±0.04 | 0.06±0.05 | 0.63±0.09 | 3.51±0.45 |
| MGA | - | 0.89±0.05## | 0.92±0.08## | 1.02±0.07## | 2.27±0.17## | 0.74±0.09## |
| Colchicine | 0.3 | 0.42±0.06** | 0.63±0.07** | 0.65±0.04** | 1.36±0.12** | 2.67±0.17** |
| Paeonol | 50 | 0.79±0.08 | 0.89±0.06 | 0.96±0.08 | 2.24±0.07 | 0.71±0.19 |
| 100 | 0.69±0.06* | 0.82±0.7* | 0.82±0.06* | 2.31±0.13 | 1.11±0.12* | |
| 200 | 0.58±0.07** | 0.75±0.07** | 0.77±0.09** | 2.10±0.12 | 1.13±0.13* | |
| ##P<0.01 vs control; *P<0.05, **P<0.01 vs MGA | ||||||
|
| 图 2 Effects of paeonol on expressions of TNF-α, IL-1β and IL-6 in ankle joints of MGA rats analyzed by immunohistochemistry staining (×200) |
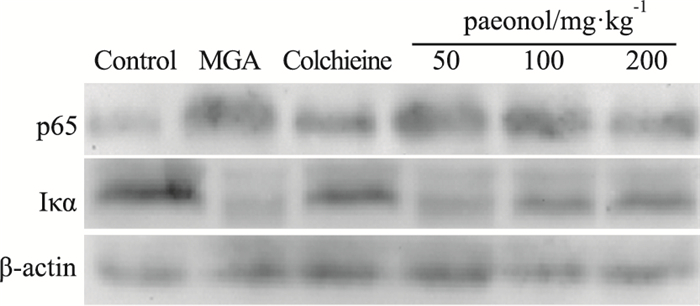
如Tab 3、Fig 3所示,与对照组相比,注射MSU 48 h后大鼠关节滑膜中p65蛋白水平明显升高,IκBα蛋白水平则明显降低(P<0.01)。与MGA组相比,给予0.3 mg·kg-1秋水仙碱、丹皮酚(100、200 mg·kg-1)治疗明显提高了MGA大鼠关节滑膜中IκBα蛋白水平(P<0.05);但给予50 mg·kg-1丹皮酚治疗对MGA大鼠关节滑膜IκBα蛋白水平无明显影响。同时,本研究中不同剂量的丹皮酚对MGA大鼠关节滑膜中p65蛋白水平均无明显影响。
|
| Fig 3 Effects of paeonol on levels of p65 and IκBα in synovium of MGA rats (x±s, n=3) |
本研究应用大鼠MGA模型,证实了丹皮酚(100、200 mg·kg-1)可明显减轻大鼠足肿胀,改善步态评分、组织学评分和破骨细胞形成,降低关节组织中TNF-α、IL-1β、IL-6表达,提高IκBα蛋白水平,但对p65蛋白水平无明显影响。
由于近几十年痛风发病率明显上升,MSU诱导痛风炎症发生、发展的分子机制逐渐成为研究热点。MSU被证实是最强有力的促炎信号之一,其可激活巨噬细胞、单核细胞、中性粒细胞、滑膜成纤维细胞等表达促炎细胞因子、趋化因子、黏附分子和组织蛋白酶,启动痛风炎症的发生、发展和关节结构的病理损伤[9]。因此,通过向实验动物关节腔注射MSU诱导关节炎症(MGA模型)已成为国内外广泛认同和使用的痛风动物模型[10]。在本研究中,我们发现关节腔内注射MSU后6 h就快速诱导了大鼠关节肿胀,12 h关节肿胀达到峰值,注射后48 h关节肿胀仍然明显,这一结果与Silva等[20]研究结论相一致。MSU注射后的步态评分和病理评分均明显升高,提示MSU导致了关节功能障碍和组织病理损伤。给予丹皮酚治疗后,关节肿胀明显减轻,步态评分和病理评分均明显降低。破骨细胞是介导炎症状态下关节骨质破坏的主要效应细胞,这一结论在类风湿关节炎、骨关节炎、痛风性关节炎等疾病中均得到证实[11]。本研究中,我们应用TRAP染色法观察到MSU诱导激活了大量破骨细胞,而丹皮酚治疗后激活的破骨细胞数量明显减少。综合上述结果表明,丹皮酚缓解了MSU诱导的关节炎症状,改善了关节功能障碍和关节病理损伤,提示丹皮酚有抗大鼠MGA的药理作用。
由于炎症因子在痛风炎症发生、发展中扮演着关键角色,在初步证实了丹皮酚抗大鼠MGA发展的基础上,我们接着探讨了丹皮酚对MGA大鼠炎症因子表达的影响。众多的炎症因子如TNF-α、IL-1β、IL-6均在痛风炎症发展中起了关键作用,其中尤以IL-1β的作用备受关注[9]。IL-1β既可刺激多种炎性细胞表达趋化因子、黏附分子和其它促炎细胞因子,也可诱导破骨细胞活化而导致关节结构的病理损伤,还可作用于神经元,导致痛风患者对炎症疼痛过度敏感。可溶性IL-1诱饵受体列洛西普、IL-1β单克隆抗体卡那单抗均表现出优异的抗痛风疗效,更加凸显了IL-1β在痛风炎症病理过程中的核心地位[12]。本研究中,我们首先观察到MGA大鼠病变关节组织中TNF-α、IL-1β、IL-6的表达均明显升高,这一结果与文献报道基本一致,也再次证明了炎症因子在MGA发展中的核心作用[3]。以往的研究已经证实了经典抗痛风药物秋水仙碱对MSU诱导的多种炎性介质表达有抑制作用[13]。本研究中,我们也观察到秋水仙碱明显降低了MGA大鼠病变关节组织中TNF-α、IL-1β、IL-6的表达。给予丹皮酚治疗后,MGA大鼠病变关节组织中TNF-α、IL-1β、IL-6的表达都明显降低,提示丹皮酚抗大鼠MGA的药理作用与拮抗炎症因子的表达密切相关。
已有的研究结果提示,激活转录因子NF-κB是MSU诱导炎症因子表达的核心机制之一。MSU可直接结合TLR-2和TLR-4,通过多个信号转导通路促进IκBα的泛素化降解,使得p65蛋白游离并核转移,从而增加炎性细胞因子、黏附分子、趋化因子、组织蛋白酶等基因表达,促进痛风炎症的发生、发展和关节组织的病理损伤[3]。与此同时,研究人员还发现了MSU诱导NF-κB活化的另一个机制。MSU晶体可被单核细胞、巨噬细胞等吞噬进入细胞质,通过钾离子流出、活性氧或者溶酶体损伤等机制,激活细胞质中的NALP3炎性体复合体,然后活化caspase-1,促进前体IL-1β剪切成为成熟体IL-1β并分泌至细胞外[14]。胞外的IL-1β通过与炎性细胞胞膜上相应受体结合,激活NF-κB,最终促进痛风炎症的发展。因此,我们在证实了丹皮酚抑制MGA大鼠炎症因子表达的基础上,观察了丹皮酚对MSU诱导的NF-κB活化的影响。本实验发现,MGA大鼠病变关节组织中IκBα水平明显降低,提示MSU诱导了IκBα降解,从而促进了NF-κB活化。给予丹皮酚治疗后,MGA大鼠病变关节组织中IκBα水平明显增高,提示丹皮酚阻遏了MSU诱导的IκBα降解,提高了组织中IκBα水平,从而抑制了NF-κB活化。有意思的是,我们发现丹皮酚对MGA大鼠关节组织中p65蛋白表达水平无明显影响,提示丹皮酚抑制NF-κB活化的药理作用主要是通过阻断其活化的信号途径,而非影响其表达量而实现。
综上所述,本研究证实了丹皮酚可明显抑制大鼠痛风性关节炎的发展,其机制与抑制关节组织中NF-κB活化,从而降低炎性介质表达密切相关。本研究为中医临床应用中药牡丹皮治疗痛风的科学性提供了证据,也为利用丹皮酚研发新的抗痛风药物提供了初步的药理实验依据。
( 致谢: 本实验在重庆工商大学重庆市天然药物研究重点实验室完成,感谢孔淑贞博士、殷钟意高级实验师给予的技术支持。)
| [1] |
Kuo C F, Grainge M J, Zhang W, et al. Global epidemiology of gout: prevalence, incidence and risk factors[J]. Nat Rev Rheumatol, 2015, 11(11): 649-62. doi:10.1038/nrrheum.2015.91 |
| [2] |
Jaramillo M, Naccache P H, Olivier M. Monosodium urate crystals synergize with IFN-gamma to generate macrophage nitric oxide: involvement of extracellular signal-regulated kinase 1/2 and NF-kappa B[J]. J Immunol, 2004, 172(9): 5734-42. doi:10.4049/jimmunol.172.9.5734 |
| [3] |
Lin T H, Pajarinen J, Lu L, et al. NF-κB as a therapeutic target in inflammatory-associated bone diseases[J]. Adv Protein Chem Struct Biol, 2017, 107: 117-54. doi:10.1016/bs.apcsb.2016.11.002 |
| [4] |
耿帅, 赵育林, 曾凯, 等. 丹皮酚的研究进展[J]. 中国新药与临床杂志, 2016, 35(5): 310-3. Geng S, Zhao Y L, Zeng K, et al. Research progress of paeonol[J]. Chin J New Drugs Clin Rem, 2016, 35(5): 310-3. |
| [5] |
武海军, 徐继辉, 李月玲, 等. 丹皮酚的抗炎作用研究[J]. 包头医学院学报, 2008, 24(3): 238-9. Wu H J, Xu J H, Li Y L, et al. Study of anti-inflammatory effects of paeonol[J]. J BaoTou Med Col, 2008, 24(3): 238-9. doi:10.3969/j.issn.1006-740X.2008.03.007 |
| [6] |
dos Santos R M, Oliveira S M, Silva C R, et al. Anti-nociceptive and anti-edematogenic effects of glibenclamide in a model of acute gouty attack in rats[J]. Inflamm Res, 2013, 62(6): 617-25. doi:10.1007/s00011-013-0615-2 |
| [7] |
王璐, 那莎, 陈光亮. 萆薢总皂苷对大鼠急性痛风性关节炎NALP3炎性体信号通路的影响[J]. 中国药理学通报, 2017, 33(3): 354-60. Wang L, Na S, Chen G L. Effect of total saponin of Dioscorea on NALP3 inflammasome signaling pathway with acute gouty in rats[J]. Chin Pharm Bull, 2017, 33(3): 354-60. doi:10.3969/j.issn.1001-1978.2017.03.013 |
| [8] |
单玮, 阙华发. 三妙丸类方及川牛膝对急性痛风性关节炎大鼠炎症反应的作用机制研究[J]. 世界中医药, 2013, 8(2): 189-93. Shan W, Que H F. On action mechanism of Sanmiao Pill and medicinal cyathula root for inflammatory reaction of acute gouty arthritis[J]. W Chin Med, 2013, 8(2): 189-93. |
| [9] |
So A K, Martinon F. Inflammation in gout: mechanisms and therapeutic targets[J]. Nat Rev Rheumatol, 2017, 13(11): 639-47. doi:10.1038/nrrheum.2017.155 |
| [10] |
Galvão I, Dias A C, Tavares L D, et al. Macrophage migration inhibitory factor drives neutrophil accumulation by facilitating IL-1β production in a murine model of acute gout[J]. J Leukoc Biol, 2016, 99(6): 1035-43. doi:10.1189/jlb.3MA0915-418R |
| [11] |
Schlesinger N, Thiele R G. The pathogenesis of bone erosions in gouty arthritis[J]. Ann Rheum Dis, 2010, 69(11): 1907-12. doi:10.1136/ard.2010.128454 |
| [12] |
Dumusc A, So A. Interleukin-1 as a therapeutic target in gout[J]. Semin Immunopathol, 2015, 27(2): 156-63. |
| [13] |
Leung Y Y, Yao Hui L L, Kraus V B. Colchicine—Update on mechanisms of action and therapeutic uses[J]. Semin Arthritis Rheum, 2015, 45(3): 341-50. doi:10.1016/j.semarthrit.2015.06.013 |
| [14] |
Martinon F, Pétrilli V, Mayor A, et al. Gout-associated uric acid crystals activate the NALP3 inflammasome[J]. Nature, 2006, 440(7081): 237-41. doi:10.1038/nature04516 |

