

2. 华北理工大学临床医学院,河北 唐山 063000;
3. 华北理工大学冀唐学院,河北 唐山 063000;
4. 华北理工大学基础医学院,河北 唐山 063000;
5. 河北省慢性疾病重点实验室,唐山市慢性病临床基础研究重点实验室,河北 唐山 06300
 ,
WEI Min2,
ZHANG Dan-dan2,
GAO Qing-yao2,
HUANG Han-xue1,
Wang Jian-xing3,
HAN Shu-ying4,5
,
WEI Min2,
ZHANG Dan-dan2,
GAO Qing-yao2,
HUANG Han-xue1,
Wang Jian-xing3,
HAN Shu-ying4,5

2. School of Clinical Medicine, North China University of Science and Technology, Tangshan Hebei 063000, China;
3. School of Jitang, North China University of Science and Technology, Tangshan Hebei 063000, China;
4. School of Basic Medical Science, North China University of Science and Technology, Tangshan Hebei 063000, China;
5. Hebei Key Lab on Chronic Diseases and Tangshan Basic Clinical Diseases, Tangshan Hebei 063000, China
2型糖尿病的发展会导致多种并发症,肝损伤是其中之一[1-2]。肝脏与糖脂代谢密切相关[3],探究保护糖尿病肝损伤的作用机制,对于糖尿病的治疗和预后都很重要。
D-手性肌醇(D-chiro-inositol,DCI)是羟基环己醇的一种手性结构,具有促进肝脏脂代谢、胰岛素增敏、降血糖、抗氧化等作用[4],有希望应用于2型糖尿病的临床治疗[5]。目前,已有文献对DCI降低血糖的机制进行初步探究,表明DCI通过作用于PI3K/Akt信号通路,降低Ⅱ型糖尿病大鼠的血糖[6]。另有研究表明,DCI可以通过抑制肝糖输出(hepatic glucose output,HGO),在体内发挥抗糖尿病作用[7]。但国内外还未见有关DCI对糖尿病肝脏保护作用机制的研究报道。本实验通过给予db/db小鼠不同剂量DCI,观察DCI的降糖作用及其对肝损伤的抑制作用,并探讨可能机制,为DCI进一步研发和应用提供实验依据。
1 材料 1.1 实验动物35只10周龄♀SPF级db/db小鼠(体质量39~48 g),10只同源同周龄♀ db/m小鼠(体质量17~20 g),购自常州卡文斯实验动物有限公司,许可证号:SCXK(苏)2016-0010,饲养于华北理工大学动物实验中心SPF级实验室。60Co辐射小鼠颗粒饲料(南京贝斯弗饲料有限公司,生产批号:20171050001MF01)。
1.2 药物与试剂DCI(Sigma公司,Lot:#BCBQ3950V,货号:101678071,白色结晶,纯度99%);天门冬氨酸氨基转移酶(aspartate aminotransferase,AST)和丙氨酸转氨酶(alanine amino-transferase, ALT)测定试剂盒(南京建成生物工程研究所,货号C010-2、C009-2);葡萄糖转运蛋白4 (glucose transporters 4,GLUT4)抗体(武汉博士德公司,货号:BM2162);胰岛素受体底物2(insulin receptor substrate 2,IRS2)抗体[EPR904(2)](Abcam公司,货号:ab134101);胰岛素受体(insulin receptor,IR)抗体(Gene Tex公司,货号:GTX101136);BCA蛋白浓度测定试剂盒(北京雷根生物技术有限公司,货号:PT0001);Masson染色试剂(索莱宝科技有限公司,批号:20160913)。
1.3 仪器罗氏血糖仪及配套血糖试纸(德国罗氏诊断有限公司);200PRO酶标仪(瑞士Tecan公司);Universal Hood Ⅲ凝胶成像分析系统(美国伯乐);5180R高速低温离心机(Eppendorf公司);HMIAS-2000真彩病理图像分析系统(高腾科技有限公司);BX5光学显微镜(日本Olympus公司);RM2245轮转式切片机(Leica公司);H-7650透射电镜(日本日立公司)。
2 方法 2.1 小鼠分组与给药将小鼠适应性饲养1周,测定随机血糖值,连续2次血糖均值>16.1 mmol·L-1的纳入实验,选取符合要求的30只小鼠(剔除血糖和体质量差异较大的小鼠),随机分为模型对照组(MCG)、高剂量DCI组(HDCI)和低剂量DCI组(LDCI);db/m为正常对照组(NCG)。每组10只。HDCI与LDCI给药量分别70、35 mg·kg-1·d-1,MCG与NCG给予同体积纯水。于每日上午9时按照体质量分别灌胃,持续6周。
2.2 观察指标 2.2.1 一般表征观察给药期间密切观察小鼠的精神状态、活动、毛色及大小便等有无改变。每周测定小鼠的饮水量、进食量和体质量变化。
2.2.2 血糖测定首次给药血糖动态观察:用血糖仪测定第1次给药前及给药后禁食0、1、2、4 h的血糖。随机血糖测定:于给药0周、2周、4周、6周,测定db/db小鼠随机血糖(给药后2 h)。
2.2.3 血清AST、ALT和肝重指数测定末次给药后,禁食14 h,吸入性七氟烷麻醉(将小鼠口鼻对准含七氟烷瓶口约5~6 s)小鼠,迅速摘眼球取血于1.5 mL EP管中,分离血清。微板法测定血清中AST和ALT的水平。小鼠取血后,立即剖腹取肝脏,于生理盐水中漂洗,用滤纸吸去表面液体,称重。计算肝重指数(liver weight index,LI),LI/%=肝重/体重×100%。
2.2.4 肝脏病理形态观察肝脏称重后,于小鼠肝脏右叶切取1 mm3组织块,用体积分数为0.025戊二醛溶液固定12 h,磷酸缓冲液冲洗8 h,体积分数为0.01锇酸中浸泡2 h,冲洗脱水后使用Epon812包埋,切片(70 nm),使用枸橼酸铅染色,透射电镜观察、拍照。
切取适宜大小肝脏右叶于体积分数为0.04多聚甲醛中固定72 h,修块置于包埋盒中,纯水冲洗8 h,常规石蜡包埋处理(软、硬蜡比例为1:3),4 μm厚切片。于65℃烤片2 h,进行常规HE染色;按照说明书步骤进行Masson染色。光镜下观察db/db小鼠肝脏形态结构变化。
2.2.5 免疫组织化学法测定肝组织GLUT4蛋白的表达将肝脏组织石蜡切片脱蜡水化,EDTA高压加热煮沸修复抗原,PBS洗净,封闭血清,一抗GLUT4以1:200稀释覆盖组织切片,置于冰箱中4℃过夜,PBS冲洗后滴加二抗,置于37℃恒温箱中孵育,冲洗后,DAB试剂显色50 s,苏木精复染细胞核1 min。改用PBS代替一抗,其他实验条件相同进行上述实验设为阴性对照组。光镜下可见阳性信号呈棕黄色,观察GLUT4蛋白表达及分布,并应用Image-Pro Plus 6.0软件测定平均积分吸光度。
2.2.6 Western blot检测IR和IRS-2蛋白表达冰上切取冻存肝脏组织约30 mg,加300 μL RIPA裂解液,低温高速匀浆3次,冰上裂解2 h,4℃离心吸取上清2次,BCA蛋白定量,调整蛋白浓度为5 g·L-1。样品中加入5×loading buffer,沸水浴变性,上样量20 μL。配制12%分离胶用于IRS2(137 ku)的检测,配制8%分离胶用于IR(30 ku)的检测,配制5%浓缩胶。电泳、转膜后,5%脱脂奶粉封闭;加入一抗(IR 1:1 000,IRS-2 1:1 000)4℃摇床过夜,TBST洗涤3次;加入二抗(1:5 000)室温孵育2 h,TBST洗涤3次;吸取显影液(1:1)200 μL均匀涂在膜上,置于自动显影仪中显影。应用Image J软件测定IR、IRS-2与β-actin显影条带的灰度值,内参为β-actin。
2.3 统计学方法应用SPSS 19.0进行统计学分析,实验数据以x±s表示,各组间采用单因素方差分析。
3 结果 3.1 DCI对db/db小鼠一般表征的影响NCG组小鼠精神状态良好、活泼好动、反应敏捷、毛发光亮;MCG组小鼠精神萎靡、动作迟缓、毛发稀疏无光泽、多饮、多食、多尿;高、低剂量DCI干预组小鼠上诉一般表征有不同程度的改善,HDCI改善更明显。
3.2 DCI对db/db小鼠血糖的影响 3.2.1 DCI首次给药对db/db小鼠血糖的影响首次给予DCI后禁食,观察小鼠血糖动态变化见Tab 1,NCG组禁食4 h血糖无明显变化,MCG、HDCI、LDCI组各点血糖值明显高于NCG组(P < 0.01);与MCG组相比,高、低剂量DCI给药后各时间点血糖值均有不同程度降低,LDCI组与MCG组相比无明显差异(P>0.05),HDCI组血糖下降明显(P < 0.01);高、低剂量给药组进行比较,给药后1、2、4 h存在明显差异(P < 0.01),高剂量DCI组血糖值下降更明显。
| Group | 0 h | 1 h | 2 h | 4 h |
| NCG | 6.49±0.30 | 6.56±0.36 | 6.48±0.46 | 5.42±0.44 |
| MCG | 18.65±2.33** | 18.08±2.87** | 15.75±3.17** | 14.56±3.47** |
| HDCI | 18.58±2.52** | 14.29±2.28**## | 10.83±2.72**## | 9.32±2.05**## |
| LDCI | 18.76±2.08** | 17.61±2.73**△△ | 14.20±2.37**△△ | 13.24±1.81**△△ |
| **P < 0.01 vs NCG; ##P < 0.01 vs MCG; △△P < 0.01 vs HDCI | ||||
DCI对db/db小鼠随机血糖的动态变化见Tab 2,给药6周内NCG组随机血糖无变化,MCG组随机血糖明显高于NCG组(P < 0.01),且第6周最高;与MCG组相比,LDCI组和HDCI组随机血糖不同程度地下降(P < 0.01),其中给药第4周降低幅度最大。HDCI组随机血糖值与LDCI组比较没有明显差异(P>0.05)。
| Group | 0 wk | 2 wks | 4 wks | 6 wks |
| NCG | 6.49±0.58 | 6.60±0.46 | 6.48±0.36 | 6.44±0.50 |
| MCG | 18.88±2.87** | 17.57±3.44** | 18.20±2.88** | 20.30±3.38** |
| HDCI | 18.19±2.21** | 13.31±2.37**## | 13.11±3.06**## | 13.69±2.88**## |
| LDCI | 18.50±2.73** | 15.06±3.16** | 14.45±2.10**## | 14.60±1.79**## |
| **P < 0.01 vs NCG; ##P < 0.01 vs MCG | ||||
Tab 3结果显示,MCG组小鼠血清AST活性高于NCG组(P < 0.05);高、低剂量DCI对血清AST有不同程度降低作用,但与NCG、MCG组相比,均无统计学差异(P>0.05)。各组db/db小鼠血清ALT活性明显较db/m小鼠升高(P < 0.01);HDCI与LDCI组血清ALT值有降低趋势,但与MCG组比较差异无显著性(P>0.05)。各组db/db小鼠LI值明显高于db/m小鼠(P < 0.01),LDCI和HDCI组LI值较MCG组略有升高(P>0.05)。
| Group | AST/U·L-1 | ALT/U·L-1 | LI/% |
| NCG | 155.32±24.38 | 76.47±26.16 | 0.041±0.005 |
| MCG | 184.56±22.17* | 129.47±30.41** | 0.062±0.004** |
| HDCI | 176.73±41.46 | 111.64±26.78** | 0.065±0.007** |
| LDCI | 180.25±35.68 | 117.35±27.64** | 0.066±0.006** |
| *P < 0.05, **P < 0.01 vs NCG | |||
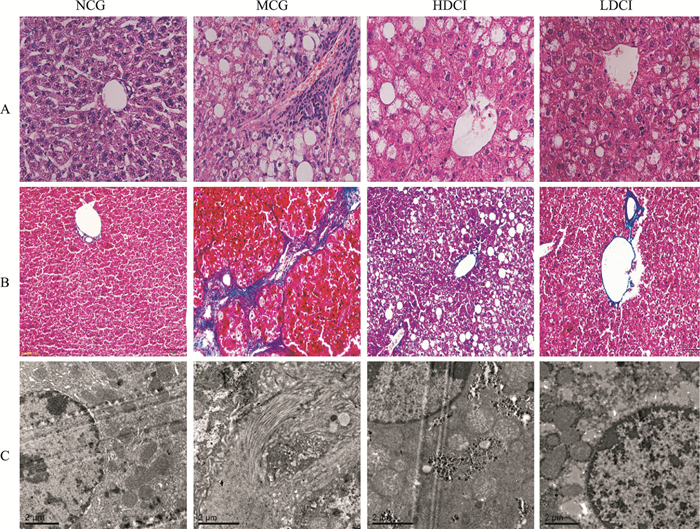
Fig 1A的HE染色结果显示,各组小鼠肝组织细胞核被染成蓝色,肝细胞质被染成粉红色。NCG组小鼠肝细胞形态结构正常,胞质染色均匀,未出现水肿,肝小叶清晰,未出现脂肪变性;MCG组小鼠肝细胞条索状排列基本消失,肝细胞明显肿胀变形,有部分肝细胞发生溶解性坏死,可见有炎细胞大量聚集,肝血窦狭窄或闭锁,大量肝细胞脂肪变性,形成脂滴空泡;与MCG组相比,HDCI组、LDCI组小鼠肝脏的病理变化明显减轻,肝细胞基本呈条索状排列,脂滴空泡有所减少。HDCI组小鼠肝组织损伤减轻更明显。
|
| Fig 1 Morphological structure of hepatic tissues in db/db mice A: HE staining; B: Masson staining; C: Electronic microscope |
Fig 1B的Masson染色结果显示,NCG组小鼠肝组织只在门静脉处见少许蓝染物质,MCG组则出现明显的蓝色胶原纤维,主要分布在血管、汇管区及Disse间隙;LDCI组与HDCI组蓝染胶原纤维较MCG组明显减少。
Fig 1C的透射电镜结果显示,NCG组小鼠肝细胞质中内质网、高尔基体等细胞器形态正常,结构清晰,线粒体丰富;MCG组小鼠肝细胞内质网断裂,线粒体减少、变形,正常结构几乎消失,可见散在脂滴和大量胶原纤维;HDCI组和LDCI组较MCG组肝细胞器形态结构明显改善,少见胶原纤维。
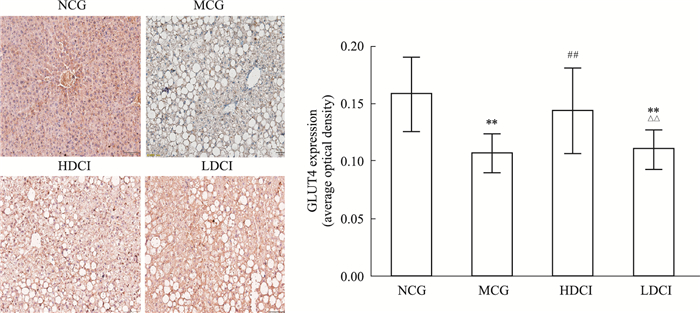
3.4 DCI对db/db小鼠肝脏组织中GLUT4、IR和IRS2蛋白表达的影响 3.4.1 免疫组化法检测GLUT4蛋白表达如Fig 2所示,NCG组小鼠肝脏组织细胞质和细胞膜上出现大量的棕黄色染色,且分布均匀,为高表达,细胞核内未见阳性表达。MCG组小鼠肝脏细胞中GLUT4蛋白表达程度偏低,可见少许棕黄色颗粒分布。HDCI组与LDCI组GLUT4的表达明显高于MCG组,棕黄色阳性染色大面积分布,且表达均匀,但HDCI组染色切片总体颜色要深于LDCI组。计算GLUT4阳性表达百分比结果表明,MCG组GLUT4的蛋白表达明显低于NCG组(P < 0.01);HDCI组的GLUT4表达明显高于MCG组(P < 0.01);HDCI组的表达最高,与NCG组结果相近(P>0.05);HDCI组明显高于LDCI组(P < 0.01)。
|
| Fig 2 Immunohistochemistry of GLUT4 protein expression in hepatic tissues of db/db mice(x±s, n=10) **P < 0.01 vs NCG; ##P < 0.01 vs MCG; △△P < 0.01 vs HDCI |
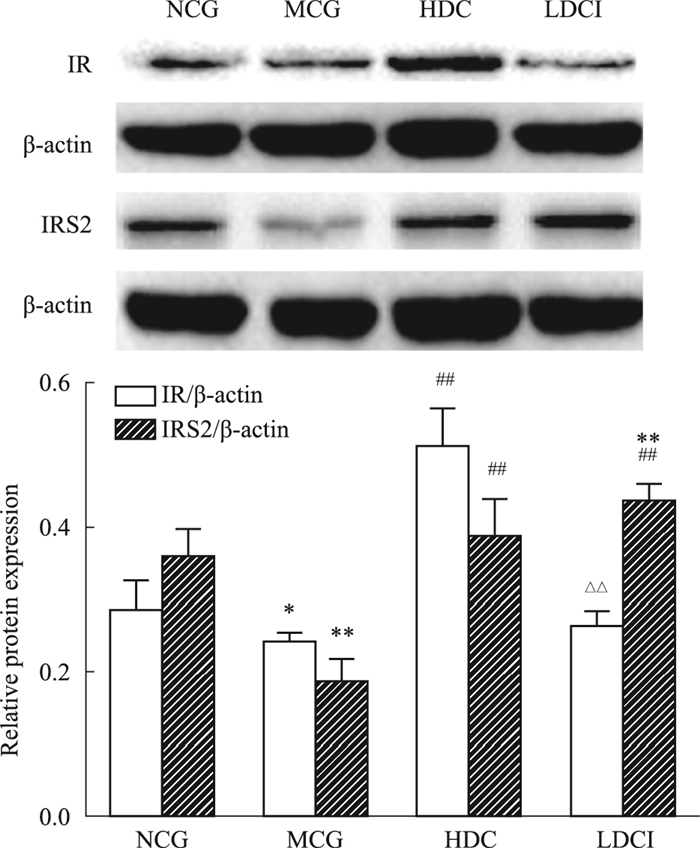
如Fig 3所示,MCG组IR表达明显低于NCG组(P < 0.01);高剂量DCI组IR蛋白表达水平明显高于模型组、NCG组和LDCI组(P < 0.01);低剂量DCI组与MCG组比较结果相近(P>0.05)。MCG组IRS2蛋白表达低于NCG组(P < 0.01);高剂量DCI组表达水平与MCG组比较明显升高(P < 0.01),与NCG组表达结果相近(P>0.05);低剂量DCI组IRS2的表达水平高于MCG组和NCG组(P < 0.01),与HDCI组表达结果无差异(P>0.05)。
|
| Fig 3 Western blot of IR and IRS2 in hepatic tissues of db/db mice(x±s, n=10) *P < 0.05, **P < 0.01 vs NCG; #P < 0.05, ##P < 0.01 vs MCG; △P < 0.05, △△P < 0.01 vs HDCI |
2型糖尿病严重危害人类健康,该病可致多种器官的损伤,尤以肝损伤更为明显,长期高血糖能发展成为各种肝脏的并发症[8]。db/db小鼠是国际公认的自发2型糖尿病动物模型,具有典型的高血糖、肥胖和肝、肾等器官损伤的特点[9],该小鼠瘦素受体基因自然突变而缺陷,4周龄开始出现血糖升高和肥胖,早期肝就可出现脂肪性病变,随着时间推移肝脏逐渐向纤维化、肝硬化发展[10]。
本文应用db/db小鼠动物模型,观察了DCI口服给药对db/db小鼠血糖和肝损伤的影响,并探讨其可能机制。结果表明,DCI首次给药1 h就能明显降低db/db小鼠血糖,连续给药6周能持续降低随机血糖,高剂量DCI降血糖作用更明显。说明DCI降糖作用起效较快、持续时间长,进一步证明了DCI有较好的降低血糖作用。通过观察血清AST、ALT、肝重指数及肝脏组织形态结构的变化,考察DCI对糖尿病肝损伤的影响情况。结果显示,DCI对db/db小鼠血清AST和ALT有一定的降低作用,但无统计学差异,是由于实验后期模型组小鼠肝损伤已经非常严重,大部分肝细胞已经发生脂肪变性坏死,产生AST和ALT明显减少,所以给药组与模型组比较无明显差异;肝重指数给药组略高于模型对照组(无统计学差异),是由于模型组体质量较高,所以肝重指数有一定程度升高,但DCI是否有一定的抑制脂肪生成作用,有待深入研究。从光镜和电镜观察可见,DCI可减轻肝组织的脂肪变性、纤维化程度、炎症细胞浸润及细胞内线粒体和内质网等细胞器的损伤,缓解了db/db小鼠肝脏损伤的进展程度。应用免疫印迹和免疫组化法进一步探究了DCI的作用机制,通过测定肝组织IR、IRS2、GLUT4的蛋白表达发现,DCI可不同程度上调IR、IRS2和GLUT4蛋白的表达,HDCI组表达上调更明显。说明DCI是通过影响IR、IRS2及GLUT4的表达,在胰岛素信号转导通路中发挥积极作用,从而有效缓解胰岛素抵抗,降低血糖。
IR是与胰岛素结合的靶蛋白,大量存在于肝脏细胞膜上,激活后促使IRS磷酸化,从而进行下一步的信号转导。研究表明,IR表达的下调会使人体内胰岛素抵抗,IR的过量表达会对糖尿病患者造成低血糖的风险[11]。IRS2是IR下端信号因子,IRS2在促进肝脏糖原合成,以及抑制HGO中具有重要作用[12]。GLUT4是细胞中胰岛素信号转导末端因子,其主要作用为促使胞外葡萄糖的跨膜转运[13]。
DCI在胰岛素转导通路中发挥重要作用。张泽生等[4, 14]报道,人体内缺乏DCI会导致胰岛素抵抗,DCI能有效增加胰岛素抵抗HepG2细胞的葡萄糖消耗量,促进2型糖尿病大鼠糖原的合成,改善胰岛素抵抗。本研究结果也证明了DCI的降糖作用,但从IR、IRS2和GLUT4蛋白表达的角度探究DCI的作用机制,目前未见文献报道。有文献报道,DCI有抗氧化、降低肝脏脂质含量,并能缓解酒精性脂肪肝的作用[15]。本研究首次从胰岛素转导通路为基础,探究DCI对糖尿病肝损伤的保护作用和作用机制,表明DCI对糖尿病肝损伤有明显的抑制作用。
综上所述,DCI具有降低db/db小鼠血糖,抑制胰岛素抵抗,减轻肝脏组织的脂肪变性和抑制肝脏纤维化的作用。推断可能是由于DCI提高了小鼠肝脏组织中的IR、IRS2和GLUT4蛋白的表达,促进葡萄糖的摄取利用,缓解了胰岛素抵抗,降低血糖,从而产生保护肝脏的作用。但DCI的作用机制可能是多靶点多途径,还需要进一步的研究。
| [1] |
包书茵, 韩淑英, 朝日雅, 等. 沙蓬粗寡糖对GK大鼠肝、肾保护作用及机制探讨[J]. 中国药理学通报, 2018, 34(1): 147-8. Bao S Y, Han S Y, Chao R Y, et al. The protective effects of Agiophyllum Oligo saccharides on rat liver and kidney[J]. Chin Pharmacol Bull, 2018, 34(1): 147-8. doi:10.3969/j.issn.1001-1978.2018.01.031 |
| [2] |
Kim J Y, Lee S H, Song E H, et al. A critical role of STAT1 in streptozotocin-induced diabetic liver injury in mice: controlled by ATF3[J]. Cell Signal, 2009, 21(12): 1758-67. doi:10.1016/j.cellsig.2009.07.011 |
| [3] |
Tian W, Chen L, Zhang L, et al. Effects of ginsenoside Rg1 on glucose metabolism and liver injury in streptozotocin-induced type 2 diabetic rats[J]. Genet Mol Res, 2017, 16(1). doi:10.4238/gmr16019463 |
| [4] |
张泽生, 张梦娜, 高云峰, 等. D-手性肌醇及D-松醇对缓解HepG2细胞胰岛素抵抗的作用[J]. 中国食品添加剂, 2016(9): 58-62. Zhang Z S, Zhang M N, Gao Y F, et al. Effects of D-chiro-inositol and D-pinitolon mitigation of insulin resistance in HepG2 cells[J]. Chin Food Addi, 2016(9): 58-62. doi:10.3969/j.issn.1006-2513.2016.09.002 |
| [5] |
Yoshida K, Yamaguchi M, Morinaga T, et al. Genetic modification of Bacillus subtilis for production of D-chiro-inositol, an investigational drug candidate for treatment of type 2 diabetes and polycystic ovary syndrome[J]. Appl Environ Microbiol, 2006, 72(2): 1310-5. doi:10.1128/AEM.72.2.1310-1315.2006 |
| [6] |
Gao Y F, Zhang M N, Wang T X, et al. Hypoglycemic effect of D-chiro-inositol in type 2 diabetes mellitus rats through the PI3K/Akt signaling pathway[J]. Mol Cell Endocrinol, 2016, 433: 26-34. doi:10.1016/j.mce.2016.05.013 |
| [7] |
Whiting L, Danaher R N, Ruggiero K, et al. D-chiro-inositol attenuates epinephrine-stimulated hepatic glucose output in the isolated perfused liver independently of insulin[J]. Horm Metab Res, 2013, 45(5): 394-7. |
| [8] |
赵旭敏, 李社莉. 胰岛素抵抗与2型糖尿病肝损伤的研究进展[J]. 心血管康复医学杂志, 2015, 24(1): 113-6. Zhao X M, Li S L. Research progress of insulin resistance related with liver damage of type 2 diabetes mellitus[J]. Chin J Cardiovasc Rehabil Med, 2015, 24(1): 113-6. doi:10.3969/j.issn.1008-0074.2015.01.34 |
| [9] |
Hummel K P, Dickie M M, Coleman D L. Diabetes, a new mutation in the mouse[J]. Science, 1966, 153(3740): 1127-8. doi:10.1126/science.153.3740.1127 |
| [10] |
邢玮, 王政霖, 吕甜甜, 等. 2型糖尿病db/db小鼠的生物学特性[J]. 中国比较医学杂志, 2017, 27(8): 12-5. Xing W, Wang Z L, Lyu T T, et al. Biological characteristics of a db/db mouse model of type 2 diabetes[J]. Chin J Comp Med, 2017, 27(8): 12-5. |
| [11] |
Zhang H, Wei J, Xue R, et al. Berberine lowers blood glucose in type 2 diabetes mellitus patients through increasing insulin receptor expression[J]. Metabolism, 2010, 59(2): 285-92. doi:10.1016/j.metabol.2009.07.029 |
| [12] |
韩淑英, 姜妍, 王志路, 等. 荞麦花叶黄酮对2型糖尿病大鼠肝损伤及IRS-2、PI3K、NF-κB表达的影响[J]. 中国药理学通报, 2013, 29(11): 1582-6. Han S Y, Jiang Y, Wang Z L, et al. Effects of flavones of buckwheat flower and leaf on IRS-2, PI3K, NF-κB expressions and its protection on liver injury in T2DM rats[J]. Chin Pharmacol Bull, 2013, 29(11): 1582-6. doi:10.3969/j.issn.1001-1978.2013.11.025 |
| [13] |
王建行, 王妍, 刘曼, 等. 荞麦花叶发酵提取物对2型糖尿病db/db小鼠心肌损伤的影响[J]. 中国药理学通报, 2017, 33(7): 1026-31. Wang J X, Wang Y, Liu M, et al. Effects of extract from fermented buckwheat flower and leaf(EFBFL) on myocardial injury in type 2 diabetic db/db mice[J]. Chin Pharmacol Bull, 2017, 33(7): 1026-31. doi:10.3969/j.issn.1001-1978.2017.07.027 |
| [14] |
张泽生, 张梦娜, 高云峰, 等. D-手性肌醇对STZ诱导的2型糖尿病大鼠糖原合成的影响[J]. 中国食品添加剂, 2016(7): 66-71. Zhang Z S, Zhang M N, Gao F, et al. Effect of D-chiro-inositol on the glycogen synthesis in STZ induced T2DM rats[J]. Chin Food Addi, 2016(7): 66-71. doi:10.3969/j.issn.1006-2513.2016.07.003 |
| [15] |
张泽生, 董硕, 高云峰, 等. 肌醇、D-手性肌醇对大鼠酒精性脂肪肝作用的研究[J]. 中国食品添加剂, 2014(9): 85-90. Zhang Z S, Dong S, Gao Y F, et al. Effect of inositol and D-chiro-inositol on alcoholic fatty liver rats[J]. Chin Food Addi, 2014(9): 85-90. doi:10.3969/j.issn.1006-2513.2014.09.005 |