

2. 重庆市药品技术审评认证中心,重庆 401120;
3. 四川大学华西第二医院药剂科,四川 成都 610041
2. Center for Certification and Evaluation, Chongqing Food and Drug Administration, Chongqing 401120, China;
3. West China Second University Hospital, Sichuan University, Chengdu 610041, China
羟基红花黄色素A(hydroxysafflor yellow A,HSYA)是红花中的主要成分,作用广泛,可降低血压、保护心肌、抗肿瘤等,尤其对心脑血管疾病有较好的治疗效果[1-3]。HSYA具有高水溶性,但肠膜通透性特别差,稳定性低,导致口服生物利用度很低[4]。目前,只有HSYA氯化钠注射剂已被批准临床使用,但作为治疗慢性疾病药物,长期使用注射剂使用不便,又因其具有安全性差、制备复杂、成本高等缺点,因此迫切需要口服制剂。磷脂属于两亲脂质,其脂溶性和生物膜相容性均较好,药物可与磷脂结合制备成磷脂复合物,从而提高其生物利用度[5]。文献报道[6],药物与羟丙基-β-环糊精结合后,稳定性增加且生物利用度提高;纳米乳剂可以增强口服药物渗透性,减缓药物释放,促进胃肠道对药物的吸收,应用前景广阔[7]。本实验将HSYA制备成HSYA羟丙基-β-环糊精磷脂复合物后,再将复合物制备成油包水型HSYA复合物纳米乳(HSYA complex nanoemulsion,HCNE),期望结合磷脂复合物和纳米乳的优点,在低剂量给药条件下,提高HSYA的口服生物利用度。
1 材料与方法 1.1 仪器AB204S电子分析天平(瑞士Mettler Toledo仪器公司);QL-901型旋涡混合器(海门市其林贝尔仪器制造有限公司);高效液相仪(日本SHIMADZU公司)。
1.2 试药HSYA(纯度98%,浙江永宁药业股份有限公司);HCNE(实验室自制);芦丁(纯度98%,成都曼思特生物科技有限公司);甲醇、乙腈(色谱纯,美国天地有限公司),其余试剂均为分析纯。
1.3 实验动物18只SD大鼠,♂,体质量(230±20)g,购自重庆医科大学实验动物中心,许可证号:SCXK(渝)2016-0001。
2 方法 2.1 血浆样品处理方法精密量取100 μL血浆,加入1 mmol·L-1高氯酸50 μL和50 mg·L-1芦丁内标溶液10 μL,12 000 r·min-1离心10 min,取上清液进样测定。
2.2 色谱条件色谱柱:Hypersil ODS2 C18色谱柱(4.6 mm×250 mm,5 μm);检测波长:403 nm;流动相:乙腈(A)-20 mmol·L-1磷酸缓冲溶液(B,pH=3.5),梯度洗脱:0~3 min,10% A~20% A;3~13 min,20% A;流速:1 mL·min-1;进样量:20 μL。
2.3 给药方案与样品采集、处理18只SD大鼠随机分成3组,禁食12 h。其中,1、2组分别灌胃HSYA生理盐水溶液和HCNE,第3组尾静脉注射HSYA生理盐水溶液(等同于HSYA 6 mg·kg-1)。1、2组分别于给药后5、15、30、45 min,以及1、1.5、2、3、4、5、6、8、12、24、48、72 h(第3组给药后0 min,其余时间点同1、2组)眼眶采血0.3~0.5 mL于肝素化EP管中,6 000 r·min-1离心10 min后,取上清液于-80℃保存待测。
2.4 药动学研究将药代动力学数据用DAS软件(2.1.1版)进行处理,得到主要药代动力学参数,并将HSYA和HCNE的血药浓度-时间曲线下面积(area under concentration-time curve, AUC(0-72 h))和峰浓度(peak concentration, Cmax)经对数转化后,进行[1-2α] 90%可信区间考察,运用统计学分析AUC(0-72 h)、Cmax和达峰时间(peak time, Tmax)(非参数统计的Wilcoxon符号秩和检验),评价HSYA和HCNE是否具有生物等效性,检验标准α=0.05[8]。
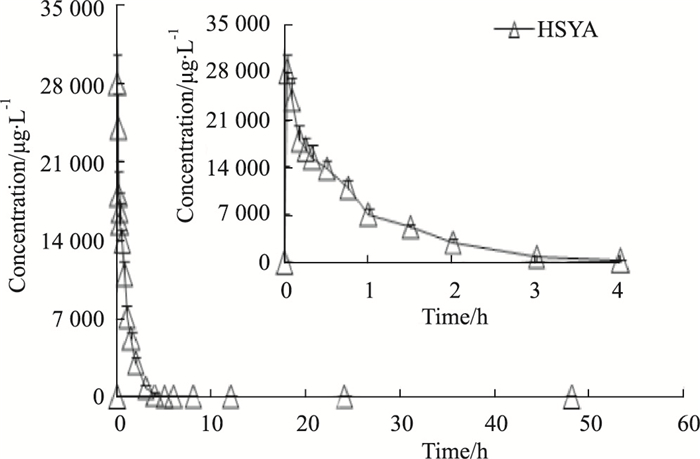
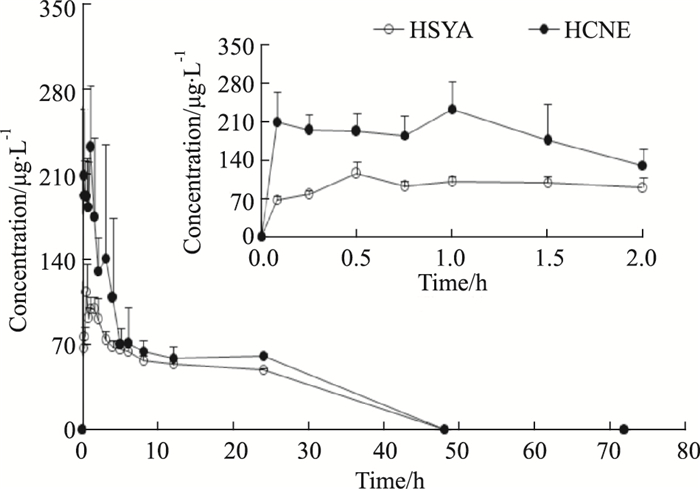
3 结果 3.1 HCNE药动学研究静脉注射的HSYA血药浓度与时间变化曲线图见Fig 1,经药代曲线从0 h开始呈下降趋势,4 h左右几乎消除殆尽。口服给予HSYA和HCNE后药代曲线如Fig 2所示,在整个药物代谢期间,HSYA血药浓度偏低,HCNE的整体血药浓度值均高于HSYA,HCNE达到最大血药浓度时间比HSYA晚约0.5 h,其中最大约为HSYA的3倍。
|
| Fig 1 Mean plasma concentration-time curve of HSYA after a single intravenous injection administration (x±s, n=6) |
|
| Fig 2 Mean plasma concentration-time curve of HSYA and HCNE after a single oral administration (x±s, n=6) |
经DAS软件(2.1.1版)对HSYA和HCNE数据计算后,得出非室模型主要药动学参数见Tab 1。分析数据可看出,给药方式为静脉注射时,HSYA的AUC和Cmax均较大,Tmax为0.03 h,说明HSYA在体内迅速达到最大血药浓度;给药方式为口服灌胃时,HSYA与HCNE相比,Cmax和AUC(0-72 h)分别增加了164.38 ng·L-1和449.28 ng·L-1·h-1,证明口服吸收增加;清除率(clearance, Cl)和表观分布容积(apparent volume of distribution, V)分别减少了1.4 L·h-1·kg-1和15.6 L·kg-1,表明体内停留时间增加。房室模型主要药动学参数见Tab 2,从AUC(0-72 h)的比较看出,与HSYA相比,HCNE的相对生物利用度约为131.71%(非房室模型)或157.14%(房室模型),HSYA的绝对生物利用度为5.94%(非房室模型)或4.99%(房室模型)。非房室模型和房室模型得出的结果几乎一致。对两种分析结果进行对比,HCNE均提高了HSYA的血药浓度,降低了清除率,提高了HSYA的口服生物利用度。
| Parameter | Injection | Oral | ||
| HSYA | HSYA | HCNE | ||
| AUC(0-72h)/ng·L-1·h-1 | 23 851.51±2 116.37 | 1 417.01±71.76 | 1 866.29±257.60 | |
| AUC(0-∞)/ng·L-1·h-1 | 27 518.48±2 506.33 | 4 602.12±2 228.62 | 5 026.91±1 472.52 | |
| MRT(0-72h)/h | 1.47±0.04 | 10.69±0.10 | 10.76±0.70 | |
| C0/Cmax/ng·L-1 | 28 072.38±2 654.76 | 120.20±12.74 | 284.58±51.09 | |
| Tmax/h | 0 | 0.92±0.67 | 1.03±1.07 | |
| Cl/L·h-1·kg-1 | 0.22±0.02 | 1.69±1.01 | 1.29±0.38 | |
| V/L·kg-1 | 16.47±12.36 | 84.98±10.97 | 69.38±12.87 | |
| Fr | - | - | 131.71% | |
| Fa | - | 5.94% | 7.82% | |
| C0: the initial concentration of injection; Fr: relative bioavailability; Fa: absolute bioavailablity | ||||
| Parameter | Injection | Oral | ||
| HSYA | HSYA | HCNE | ||
| AUC(0-72h)/ng·L-1·h-1 | 23 547.75±2 145.89 | 1 173.88±574.66 | 1 844.71±655.81 | |
| AUC(0-∞)/ng·L-1·h-1 | 28 264.71±2 183.25 | 3 592.17±2 409.19 | 5 113.41±1 612.68 | |
| MRT(0-72h)/h | 1.34±0.28 | 10.56±0.21 | 10.71±0.56 | |
| C0/Cmax/ng·L-1 | 28 072.38±2 654.76 | 120.20±12.74 | 284.58±51.09 | |
| Tmax/h | 0 | 0.92±0.67 | 1.03±1.07 | |
| Cl/L·h-1·kg-1 | 0.21±0.02 | 1.52±0.71 | 1.38±0.25 | |
| t1/2/h | 15.85±36.47 | 3.01±6.69 | 7.18±2.08 | |
| Fr | - | - | 157.14% | |
| Fa | - | 4.99% | 7.83% | |
生物等效性比较结果见Tab 3,AUC(0-72h)和Cmax分别超出规定范围80%~125%和70%~143%。统计学分别分析AUC(0-72h)、Cmax和Tmax,得出AUC(0-72h)和Tmax的P>0.05,差异无显著性,Cmax的P < 0.05,差异有显著性。综合结果表明,HSYA与HCNE二者生物不等效,后者具有较高的生物利用度。
| Formulation 1 and 2 | Parameter | 90% confidential interval calculated | Bioequivalence standard | P value | Bioequivalence |
| HSYA and HCNE | AUC(0-72h) | 111.3%~143.8% | 80%~125% | 0.56 | No |
| Cmax | 210.1%~271.7% | 70%~143% | 0.01 | No | |
| Tmax | 0.93 | Yes |
将中药制备成羟丙基-β-环糊精磷脂复合物,较单一的磷脂复合物或羟丙基-β-环糊精包合物更能促进药物的吸收,更有利于提高药物的生物利用度[9-11]。目前,生物药剂学Ⅲ类药物HSYA的研究中,暂无单独将其制备成羟丙基-β-环糊精磷脂复合物后的药代动力学文献报道,但生物药剂学Ⅱ类药物如姜黄素有相关研究。本团队前期研究了姜黄素羟丙基-β-环糊精磷脂复合物、姜黄素羟丙基-β-环糊精包合物、姜黄素磷脂复合物、姜黄素原料药在大鼠体内的药动学特征,结果表明,前三者姜黄素制剂的AUC分别为姜黄素原料药的5.89、1.49、1.17倍,证实复合制剂效果优于单一制剂[12]。故在此基础上,本研究制备了HCNE,药动学结果表明,HCNE提高了HSYA的口服生物利用度。
Lv等[13]选用自双重乳化药物递送系统(self-double-emulsifying drug delivery systems, SDEDDS)来改善HSYA的吸收,其将大豆磷脂、中链甘油三酯、油酸等辅料与HSYA混合,制备成w/o/w双层自微乳,HSYA双层自微乳相对于HSYA的生物利用度为217%。本研究制备的HCNE相对于HSYA的生物利用度为132%,两者差异可能是由于剂型与给药剂量不同。在药动学研究中,Lv等[13]制备的HSYA双层自微乳,不到10 h血药浓度几乎为零,HCNE在24 h仍保持较高血药浓度,说明HCNE缓释效应更好。再与HCNE制备工艺相比,HSYA双层自微乳制备更复杂,且SDEDDS可引起肠黏膜损伤,致一定程度的毒性,安全性有待改善;而HCNE制备简单,易于产业化。周鹏等[14]研究证明,HSYA的转运与其质量浓度和时间呈正相关,HCNE的生物利用度提高不够明显,可能与给药剂量较低有关。本实验可为后期加大给药剂量的剂型研究提供参考。
( 致谢: 本实验在重庆医科大学重庆高校药物工程研究中心完成,在此真诚感谢实验室的所有老师和同学。)
| [1] |
高海珣, 杨秀芬. 注射用红花黄色素对大鼠肝脏药物代谢酶基因表达的影响[J]. 中国药理学通报, 2017, 33(3): 441-3. Gao H X, Yang X F. Effects of safflower yellow for injection on gene expressions of drug-metabolizing enzymes in liver of rats[J]. Chin Pharmacol Bull, 2017, 33(3): 441-3. doi:10.3969/j.issn.1001-1978.2017.03.028 |
| [2] |
郝荣荣, 张译丹, 秦袖平, 等. 中药色素类成分药理活性及不良反应研究进展[J]. 中国药理学通报, 2017, 33(6): 745-9. Hao R R, Zhang Y D, Qin X P, et al. The research progress of traditional Chinese medicine pigments' pharmacological activity and its adverse reaction[J]. Chin Pharmacol Bull, 2017, 33(6): 745-9. |
| [3] |
姜华. 羟基红花黄色素A对大鼠脑缺血-再灌注损伤的保护作用及机制[J]. 中药材, 2013, 36(3): 462-4. Jiang H. The protective effect and mechanism of hydroxysafflor yellow on cerebral ischemia/reperfusion injury in rats[J]. J Chin Med Mater, 2013, 36(3): 462-4. |
| [4] |
范红晶, 虞立, 金伟锋, 等. 原儿茶醛与羟基红花黄色素A单用与合用在高脂血症大鼠体内的药动学-药效学相关性研究[J]. 中国中药杂志, 2017, 42(13): 2564-70. Fan H J, Yu L, Jin W F, et al. Pharmacokinetics-pharmacodynamics correlation of protocatechuic aldehyde and hydroxysafflor yellow A alone or their combination use in rats with hyperlipidemia[J]. Chin J Chin Mater Med, 2017, 42(13): 2564-70. |
| [5] |
马述春, 李石, 李少华, 等. 磷脂在胃粘液屏障中作用的实验研究[J]. 第二军医大学学报, 1996, 17(4): 370-3. Ma S C, Li S, Li S H, et al. Experimental study on role of phospholipid in gastric mucous barrier[J]. Acad J Sec Mil Med Univ, 1996, 17(4): 370-3. doi:10.3321/j.issn:0258-879X.1996.04.019 |
| [6] |
Aytac Z, Uyar T. Core-shell nanofibers of curcumin/cyclodextrin inclusion complex and polylactic acid: enhanced water solubility and slow release of curcumin[J]. Int J Pharm, 2017, 518(1-2): 177-84. doi:10.1016/j.ijpharm.2016.12.061 |
| [7] |
Sun L, Wan K, Hu X, et al. Functional nanoemulsion-hybrid lipid nanocarriers enhance the bioavailability and anti-cancer activity of lipophilic diferuloylmethane[J]. Nanotechnology, 2016, 27(8): 085102. doi:10.1088/0957-4484/27/8/085102 |
| [8] |
张海防, 郭健新, 黄罗生, 等. 羟基红花黄色素A在大鼠体内的药代动力学[J]. 中国药科大学学报, 2006, 37(5): 456-60. Zhang H F, Guo J X, Huang L S, et al. Pharmacokinetics of hydroxysafflor yellow A in rats[J]. J China Pharm Univ, 2006, 37(5): 456-60. doi:10.3321/j.issn:1000-5048.2006.05.015 |
| [9] |
丁冬梅, 张振海, 蒋艳荣, 等. 中药磷脂复合物的研究进展[J]. 中国中药杂志, 2013, 38(13): 2046-50. Ding D M, Zhang Z H, Jiang Y R, et al. Advance in studies on phospholipid compound of traditional Chinese medicines[J]. Chin J Chin Mater Med, 2013, 38(13): 2046-50. |
| [10] |
石明芯, 胡江波, 晏声蕾, 等. 吴茱萸碱水包油型复合物纳米乳的体内外评价[J]. 中国药学杂志, 2016, 51(19): 1678-81. Shi M X, Hu J B, Yan S L, et al. Evaluation of evodiamine complex nanoemulsion oil-in-water in vitro and in vivo[J]. Chin Pharm J, 2016, 51(19): 1678-81. |
| [11] |
袁誉铭, 陈学梁, 陈静, 等. 溴吡斯的明新型纳米乳体外释放和大鼠在体胃肠吸收[J]. 中国药理学通报, 2017, 33(2): 276-9. Yuan Y M, Chen X L, Chen J, et al. In vitro release and gastrointestinal absorption of novel pyridostigmine bromide nanoemulsion[J]. Chin Pharmacol Bull, 2017, 33(2): 276-9. doi:10.3969/j.issn.1001-1978.2017.02.024 |
| [12] |
罗见春, 胡雪原, 吴建勇, 等. 姜黄素羟丙基-β-环糊精磷脂复合物在大鼠体内药代动力学研究[J]. 中药材, 2015, 38(3): 572-5. Luo J C, Hu X Y, Wu J Y, et al. Pharmacokinetics study on curcumin hydroxypropyl-β-cyclodextrin phospholipid complex in rats[J]. J Chin Med Mater, 2015, 38(3): 572-5. |
| [13] |
Lv L Z, Tong C Q, Lv Q, et al. Enhanced absorption of hydroxysafflor yellow A using a self-double-emulsifying drug delivery system: in vitro and in vivo studies[J]. Int J Nanomed, 2012, 7: 4099-107. |
| [14] |
周鹏, 周惠芬, 何昱, 等. 羟基红花黄色素A在Caco-2细胞单层模型的转运研究[J]. 中草药, 2014, 45(14): 2030-5. Zhou P, Zhou H F, He Y, et al. Transport characteristics of hydroxysafflor yellow A across Caco-2 cell monolayer model[J]. Chin Tradit Herb Drugs, 2014, 45(14): 2030-5. doi:10.7501/j.issn.0253-2670.2014.14.014 |

