


2. 山东省医学科学院药物研究所,山东 济南 250062;
3. 国家卫生部生物技术药物重点实验室,山东 济南 250062;
4. 山东省罕少见病重点实验室,山东 济南 250062;
5. 山东省电力中心医院心内科,山东 济南 250001
 ,
LIN Gui-ming1,2,3,4,
WANG Li-ying5,
WANG Yan2,3,4,
LI Jun2,3,4,
MOU Yan-ling2,3,4
,
LIN Gui-ming1,2,3,4,
WANG Li-ying5,
WANG Yan2,3,4,
LI Jun2,3,4,
MOU Yan-ling2,3,4

2. Institute of Materia Medica, Shandong Academy of Medical Sciences, Jinan 250062, China;
3. Key Lab for Biotech-Drugs Ministry of Health, Jinan 250062, China;
4. Key Lab for Rare & Uncommon Diseases of Shandong Province, Jinan 250062, China;
5. Shandong Electric Power Center Hospital, Internal Medicine-Cardiovascular Dept, Jinan 250001, China
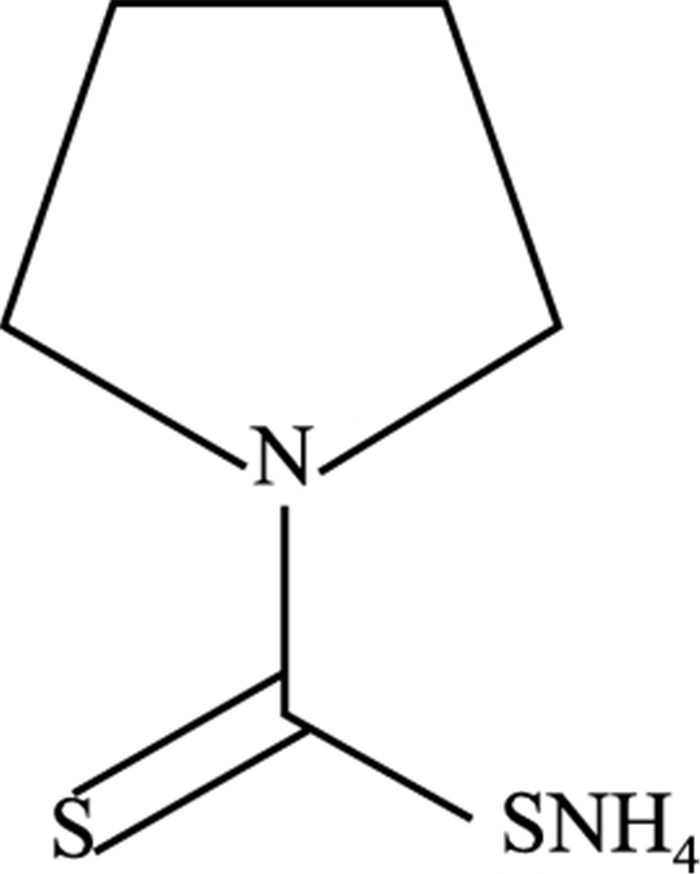
糖尿病(diabetes mellitus,DM)是心血管疾病患者发病率和死亡率升高的一个独立的风险因素,并伴随一系列的并发症[1],其中,DM心脑血管并发症的治愈率最低[2]。研究证实,NF-κB和Wnt/β-catenin两条信号通路对DM进程至关重要,其中,NF-κB通路参与调控代谢、细胞的凋亡、炎症的产生等,而Wnt/β-catenin通路则与主动脉内皮细胞生长分化等病理过程密切相关。尽管如此,这两条通路在DM主动脉病变中的研究较少。因此,本实验主要研究NF-κB及Wnt/β-catenin两条信号通路在DM发生、发展中的病理生理机制。吡咯烷二硫代氨基甲酸酯(pyrrolidine dithiocarbamate,PDTC)是一种可以通透细胞膜的NF-κB活化抑制剂(结构见Fig 1),分子式C5H9NS2·NH3,分子量164.29,其可在多种细胞中抑制NF-κB通路的激活。糖原合成酶激酶3β(glycogen synthase kinase 3β,GSK-3β)作为Wnt/β-catenin信号通路一个重要的下游信号分子,调控糖原的合成。GSK-3β的过表达可能诱发胰岛素抵抗,引起Wnt/β-catenin通路的异常,进而促使一些代谢综合症的产生[3]。研究显示[4],在1型DM大鼠主动脉病变的发生、发展过程中,Wnt/β-catenin信号通路被激活。另有研究显示[5],PDTC抑制NF-κB的活化后,能抑制DM的进程,此过程可能会通过GSK-3β这一关键点,对Wnt/β-catenin通路产生影响。本实验给予1型DM大鼠PDTC进行治疗,检测PDTC在抑制NF-κB的同时,对Wnt/β-catenin信号通路中相关蛋白表达的影响,探讨NF-κB及Wnt/β-catenin信号通路在DM主动脉病变发生、发展过程中的作用机制,为DM主动脉病变的诊断与治疗提供理论依据。
|
| Fig 1 Structure of PDTC |
健康♂SD大鼠50只,SPF级,体质量(170±20)g,购自济南朋悦实验动物有限公司,实验动物许可证号:SCXK(鲁)20140007。大鼠适应性喂养1周后,按体质量均衡的原则,随机分为对照组(10只)、DM模型组(40只)。模型组大鼠禁食16 h后,一次性腹腔注射用pH 4.5柠檬酸-柠檬酸三钠缓冲液配制的链脲佐菌素(60 mg·kg-1),对照组大鼠注射同体积柠檬酸-柠檬酸三钠缓冲液。造模72 h后,尾静脉采血测空腹血糖(fasting blood glucose, FBG),以FBG≥ 16.7 mmol·L-1,并出现多饮、多食、多尿和体质量下降者为DM模型成功。模型组造模成功大鼠随机分为4周DM模型组、4周PDTC给药组、8周DM模型组、8周PDTC给药组,每组10只。PDTC给药组剂量为100 mg·kg-1·d-1,灌胃给药(10 mL·kg-1),其余组给予同体积的蒸馏水灌胃。对照组及模型组大鼠均以普通饲料和蒸馏水继续饲养。
1.2 药物与试剂PDTC购自美国Sigma公司,纯度≥98.0%,呈白色粉末,4℃冰箱避光保存。链脲佐菌素、戊巴比妥钠(美国Sigma公司); 血糖试纸(强生中国医疗器材有限公司); 生物素标记山羊抗兔IgG/鼠IgG二抗试剂盒(北京中杉金桥生物技术有限公司); 裂解液、BCA蛋白浓度测定试剂盒(增强型),均购自碧云天生物技术研究所; 蛋白marker(美国Lonza Rockland公司); 增强型化学发光试剂(美国Millipore公司); 单克隆抗体GSK-3β、p-GSK-3β(Ser9)、β-catenin、NF-κB p65、β-actin,均购自美国Cell Signaling Technology公司; p-NF-κB p65、IκB、p-IκB抗体(Ser536),均购自Santa Cruz公司; LC3抗体(Abcam公司); PCR引物(中国BioSune); 逆转录试剂盒(日本Toyobo Life Science公司)。
1.3 仪器ASP200S型脱水机(德国LEICA公司); KL型石蜡包埋机(湖北康龙电子生产有限公司); SLEE型石蜡切片机(北京莱比信科技发展有限公司); TKY-TKB型摊烤片机(湖北泰康医疗设备有限公司); Eclipse TE 2000-S荧光显微镜(日本Nikon公司); 7300型Real Time PCR system(德国Applied Biosystems公司)。
1.4 标本收集各周期末,尾静脉采血测血糖值。大鼠麻醉,仰位固定,开胸,腹主动脉取血,每只5 mL,3 000 r·min-1离心10 min,取上清,分装到EP管,-20℃保存待测。迅速取出主动脉,用预冷生理盐水洗净,剔除脂肪组织,滤纸吸干,将主动脉分为两部分:一部分用4%多聚甲醛固定,经脱水、透明、包埋,制成主动脉石蜡组织块; 另一部分置于EP管,液氮保存待测。
1.5 HE染色取正常对照组及各时间点模型组、给药组主动脉组织,制作石蜡切片,常规脱蜡至水,苏木精染色10 min,流水稍加冲洗,体积分数1%的盐酸乙醇分化,流水冲洗数分钟,伊红染色5 min,流水稍加冲洗,梯度乙醇常规脱水,中性树胶封片。荧光显微镜拍照,观察主动脉组织病理结构的变化。
1.6 Western blot检测取各组大鼠主动脉组织,制备组织匀浆,每20 mg组织加入100~200 μL含1 mmol·L-1 PMSF的裂解液,4℃下14 000×g离心10 min,取上清,分装于EP管,-20℃保存。用BCA蛋白浓度测定试剂盒测定总蛋白浓度。40 μg总蛋白上样,10%的凝胶电泳分离。冰浴恒流(300 mA)湿法转膜2 h,体积分数5%的BSA封闭液室温封闭1 h后,与相应的一抗4℃孵育过夜。TBS-T洗液洗涤,与辣根过氧化物标记的二抗共孵育,增强型化学发光试剂显色,并用灰度分析软件定量分析。
1.7 实时荧光定量逆转录聚合酶链反应(qRT-PCR)取各组大鼠主动脉组织,每100~150 mg组织匀浆,按照TRIzol提取说明书提取主动脉组织总RNA; 按逆转录试剂盒操作说明进行逆转录,4℃保存。各目的基因的扩增引物序列见Tab 1,扩增条件:94℃变性30 s,55℃变性30 s,72℃延伸45 s,共40个循环,最后72℃延伸5 min。根据熔解曲线导出扩增的周期阈值(Ct),并计算出各组间2-ΔΔCt值,进行统计学分析。
| Gene | Forward primer (5′-3′) | Reverse primer (5′-3′) |
| NF-κB p65 | AAGATCAATGGCTACACGGG | CCTCAATGTCTTCTTTCTGC |
| IκBα | GACGAGGATTACGAGCAGAT | CCTGGTAGGTTACTCTGTTG |
| GSK-3β | CAAGCAGACACTCCCTGTGA | GTGGCTCCAAAGATCAGCTC |
| β-catenin | CATCACCACGCTGCATAATC | GAGCTTGCTTTCCTGATTGC |
| LC3 | CATGCCTTGGGACACCAGAT | ACCTTCTTCAAGTGCTGTTTGT |
| GAPDH | TCTCTGCTCCTCCCTGTTCT | ATCCGTTCACACCGACCTTC |
数据以x±s表示,应用SPSS 22.0统计软件进行数据分析,组间差异比较采用方差分析及t检验。
2 结果 2.1 DM大鼠模型建立情况实验期间,正常对照组大鼠状态良好、健壮、皮毛油亮有光泽,自主活动正常,对外界反应灵敏,无死亡。与正常对照组大鼠相比,DM模型组大鼠逐渐消瘦,精神萎靡,皮毛黯淡无光泽,腥臊臭味加重等; 且随着时间的增加,多饮、多食、多尿和消瘦加重,生存状态越来越差,甚至有死亡,其中8周DM大鼠死亡2只。与DM模型组比较,PDTC给药组大鼠体质量稍有增加,精神较DM模型组略好。
2.2 大鼠体质量、空腹血糖值变化如Tab 2所示,DM模型组大鼠与正常对照组大鼠比较,空腹血糖值明显升高,体质量明显下降; 与DM模型组比较,给予大鼠4周PDTC治疗后,PDTC组空腹血糖值及体质量无明显变化,大鼠的身体状况并没有向好的趋势发展。由此可见,4周PDTC给药组相对于DM模型组,疗效并不是很明显。但随着时间的延长,给药至8周时,与DM模型组比较,PDTC给药组的体质量明显升高,血糖值明显降低(P < 0.01)。
| Group | n | BW/g | FBG/mmol·L-1 |
| Control | 10 | 310.4±34.881 | 5.38±0.681 |
| 4 wk DM | 10 | 184.4±42.045** | 25.22±5.537** |
| 4 wk PDTC | 10 | 181.2±41.346** | 26.34±6.191** |
| 8 wk DM | 8 | 174.3±36.354** | 29.43±5.491** |
| 8 wk PDTC | 10 | 229.0±26.654**△△ | 11.19±9.398△△ |
| **P < 0.01 vs control; △△P < 0.01 vs 8 wk DM | |||
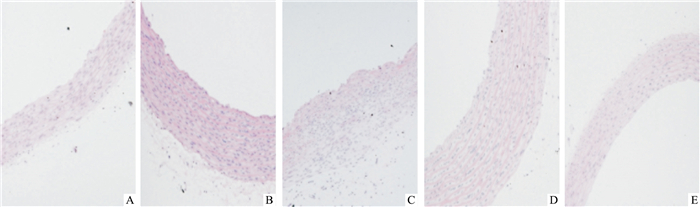
如Fig 2所示,正常对照组大鼠主动脉内皮细胞形态正常,排列整齐,细胞核分布均匀,无变形、坏死等病变。DM模型组大鼠主动脉内皮细胞胞质丰富,排列紊乱,细胞核由正常的圆形或椭圆形变为长杆状,尤其是8周DM模型组的大鼠,HE染色图片显示有不同程度的血管壁增厚,弹力膜层数增多,平滑肌细胞增生等。与DM模型组比较,PDTC给药组在8周时病变明显减轻。
|
| Fig 2 HE staining of aorta of DM rats(×400) A:Control group; B:4 wk DM; C:4 wk PDTC; D:8 wk DM; E:8 wk PDTC. |
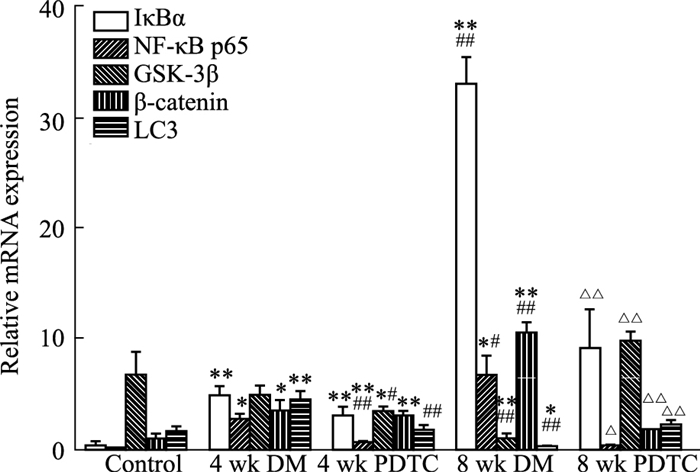
Fig 3的qPCR结果显示,与正常对照组比较,各糖尿病组大鼠主动脉组织中IκBα、β-catenin、NF-κB p65的表达明显升高,而在PDTC 8周给药组中,β-catenin、NF-κB p65、IκBα mRNA表达明显降低(P < 0.01);与正常对照组比较,DM模型组中GSK-3β mRNA表达量降低; 与DM模型组比较,PDTC给药至4周时,GSK-3β的表达较4周DM组降低,说明早期抑制Wnt/β-catenin信号通路,会使大鼠主动脉中内源性抑制剂增加,抑制GSK-3β的表达; PDTC给药至8周时,GSK-3β表达升高,可能由于随着给药时间的增加,上调了大鼠主动脉中p21蛋白,而p21蛋白表达的升高能够使p65蛋白表达略有上升,进而激活下游GSK-3β的表达。关于GSK-3β在DM大鼠主动脉中的具体表达情况,还有待进一步研究证实。
|
| Fig 3 The mRNA levels of IκBα, NF-κB p65, GSK-3β, β-catenin, LC3 in total RNA extracts of aorta from DM rats analyzed by qPCR(x±s, n=5) *P < 0.05, **P < 0.01 vs control group; #P < 0.05, ##P < 0.01 vs 4 wk DM group, △P < 0.05, △△P < 0.01 vs 8 wk DM group |
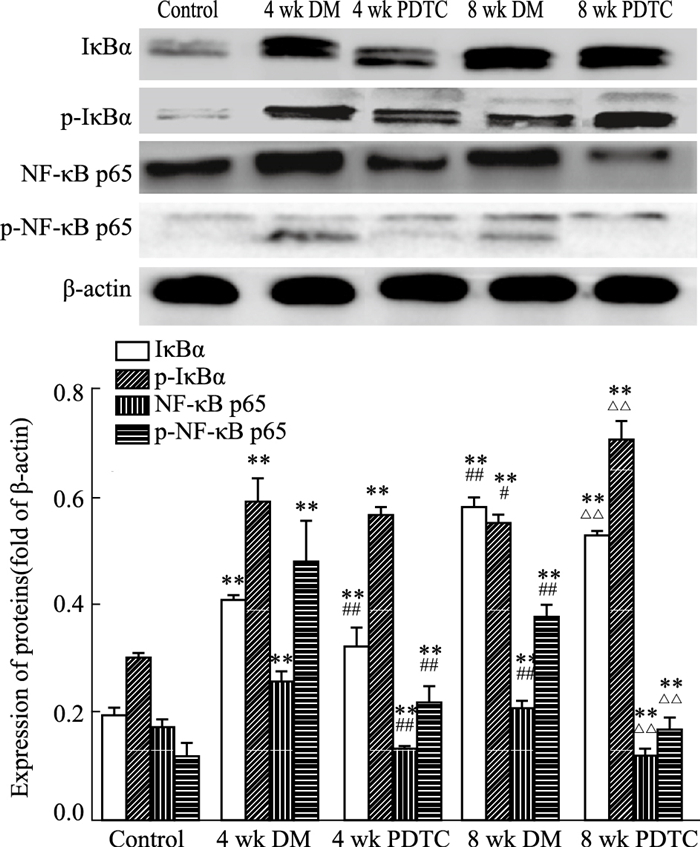
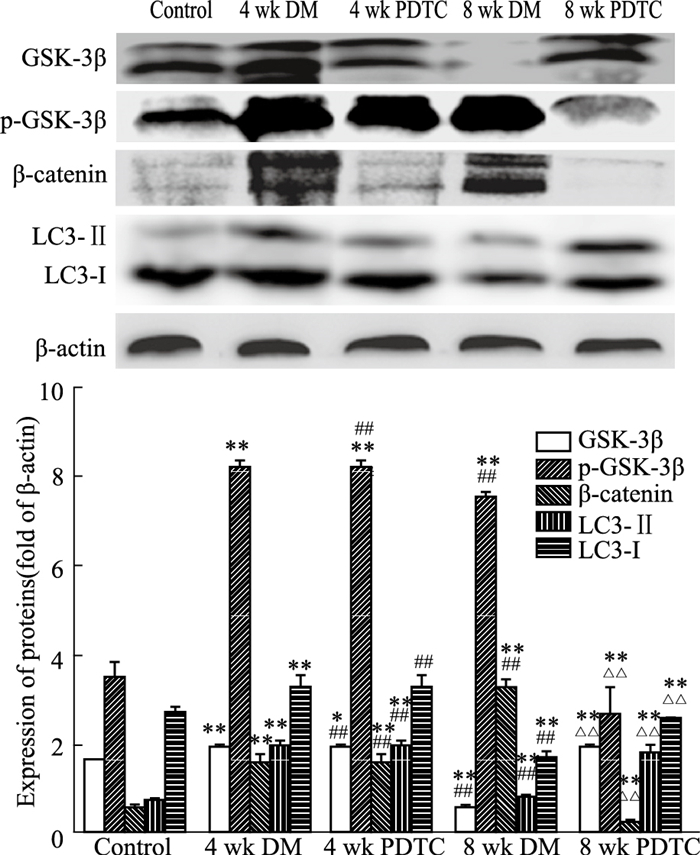
Fig 4、5的Western blot结果表明,DM模型组大鼠主动脉中IκBα、NF-κB p65、β-catenin、p-GSK-3β的表达比正常对照组明显升高(P < 0.01),PDTC给药组的IκBα、β-catenin、NF-κB p65、p-GSK-3β蛋白表达与DM模型组比较明显降低(P < 0.01)。与正常对照组比较,8周DM模型组大鼠主动脉GSK-3β、LC3的表达降低(P < 0.05);与8周DM模型组比较,PDTC给药组GSK-3β、LC3的表达升高(P < 0.01)。
|
| Fig 4 The protein levels of IκBα, p-IκBα, NF-κB p65, p-NF-κB p65 in total protein extracts of aorta from DM rats analyzed by Western blot(x±s, n=7) **P < 0.01 vs control group; #P < 0.05, ##P<0.01 vs 4 wk DM group; △△P < 0.01 vs 8 wk DM group |
|
| Fig 5 The protein levels of GSK-3β, p-GSK-3β, β-catenin, LC3 in total protein extracts of aorta from DM rats analyzed by Western blot(x±s, n=7) *P < 0.05, **P < 0.01 vs control group; ##P < 0.01 vs 4 wk DM group; △△P < 0.01 vs 8 wk DM group |
近年来,DM的发病率和死亡率愈来愈高,严重危害着人们的健康与生活。NF-κB以及Wnt/β-catenin这两条信号通路在DM的病理生理进程中至关重要,探索其对血管内皮功能异常的病理生理机制,并有效改善血管内皮功能,可能是1型DM心脑血管等疾病防治的关键点。
本实验采用一次性腹腔注射链脲佐菌素的建模方法[6],建立1型DM大鼠模型,与正常对照组比较,DM模型组大鼠空腹血糖值明显升高,并呈现持续的高血糖,体质量明显低于正常对照组,且主动脉组织中局部内皮细胞凝固性坏死; 8周DM模型组大鼠主动脉血管壁增厚,平滑肌细胞增生,弹力膜层数增多,表明DM大鼠主动脉具有不同程度的损伤。
NF-κB信号通路在心血管中的研究日益增多[7],Emadi等[8]发现,NF-κB信号通路在DM大鼠主动脉中处于被激活的状态。这种表达的异常是由NF-κB抑制剂IκB通过不同机制调节的,IκB的磷酸化以及随后IκB的降解,都会引起NF-κB p65进入细胞核[9],随后会引起大鼠血管功能的紊乱,增加促炎因子的表达,诱发大鼠主动脉炎症等病变。另有研究表明[4],Wnt/β-catenin信号通路在大鼠主动脉中也是激活的状态,在DM大血管损伤中至关重要。Wnt/β-catenin通路在DM大鼠主动脉中信号转导时,Wnt蛋白与细胞膜上的跨膜蛋白受体结合,促进β-catenin的表达及其核转移,激活下游靶基因,启动基因转录。GSK-3β作为调控血糖稳态的重要分子,参与许多DM发生发展的进程,对心血管疾病也有一定影响[10]。GSK-3β可调控NF-κB、Wnt、MAPK等多条信号通路,对DM的病理生理过程产生影响。Khan等[11]研究表明,肝癌大鼠体内NF-κB及Wnt/β-catenin信号通路的激活与GSK-3β的磷酸化有一定关联,而Wnt/β-catenin及NF-κB信号通路是如何在DM大鼠主动脉病变发生、发展过程中产生作用的,还有待进一步实验研究。
本研究中,DM大鼠主动脉中NF-κB p65、β-catenin、IκBα的表达量升高,GSK-3β的磷酸化表达也明显升高,说明NF-κB以及Wnt/β-catenin信号通路在DM大鼠主动脉中处于被激活的状态。给予DM大鼠PDTC灌胃治疗后,早期DM大鼠的基本生命指征及病理结果显示,与4周DM模型组相比,4周PDTC给药组并没有起到改善大鼠的生存状态及缓解病变的作用,可能是由于对早期DM模型大鼠给药后,PDTC激活了Akt-GSK信号通路,诱发了下游蛋白的高表达[12],进而使得DM大鼠主动脉病变并没有得到缓解。而给药至8周,大鼠的各项指标与DM模型组相比均有好转,HE染色显示,给药8周组主动脉组织中血管壁厚度相较于8周DM组有变薄的迹象,平滑肌细胞排列变均匀等,生命指征趋于正常,表明PDTC作用DM大鼠一段时间后,能够通过促进大鼠肝糖原的合成,对DM大鼠的高血糖及主动脉损伤有一定的缓解作用[13]。给药后,大鼠主动脉qPCR及Western blot结果表明,NF-κB p65、p-GSK-3β、β-catenin表达与DM模型组相比明显减少,而LC3的表达较DM模型组则呈现升高的状态,说明PDTC在蛋白及基因水平均能够通过抑制NF-κB信号通路,阻止GSK-3β发生磷酸化,进而抑制Wnt/β-catenin信号通路中相关蛋白的表达。
本实验发现,PDTC通过抑制NF-κB信号通路,抑制Wnt/β-catenin信号通路,并下调其下游相关蛋白因子的表达,参与了DM大鼠主动脉损伤的修复过程,揭示了NF-κB以及Wnt/β-catenin信号通路的激活对DM发生发展的重要作用,该结果将为DM的早期诊断及治疗提供理论依据。
| [1] | Zhang Z, Zhang D, Dou M, et al. Dendrobium officinale Kimuraet Migo attenuates diabetic cardiomyopathy through inhibiting oxidative stress, inflammation and fibrosis in streptozotocin-induced mice[J]. Biomed Pharmacother, 2016, 84: 1350-8. doi:10.1016/j.biopha.2016.10.074 |
| [2] | Elçiolu H K, Kabasakal L, Özkan N, et al. A study comparing the effects of rosiglitazone and/or insulin treatments on streptozotocin induced diabetic (type Ⅰ diabetes) rat aorta and cavernous tissues[J]. Eur J Pharmacol, 2011, 660(2-3): 476-84. doi:10.1016/j.ejphar.2011.03.030 |
| [3] | Kim J S, Piao S, Lee E, et al. Development of Akt-activated GSK3β inhibitory peptide[J]. Biochem Biophys Res Commun, 2013, 434(4): 735-9. doi:10.1016/j.bbrc.2013.03.103 |
| [4] | 尹茂山, 许淑红, 王燕, 等. 2型糖尿病大鼠主动脉Wnt/β-catenin信号通路的变化及SIRT1的调节作用[J]. 中国药理学通报, 2016, 32(3): 337-42. Yin M S, Xu S H, Wang Y, et al. Alteration of Wnt/β-catenin signaling pathway in type 2 diabetic rats' aorta and regulation of SIRT1[J]. Chin Pharmacol Bull, 2016, 32(3): 337-42. doi:10.3969/j.issn.1001-1978.2016.03.009 |
| [5] | Wang Z, Bildin V N, Yang H, et al. Dependence of corneal epithelial cell proliferation on modulation of interactions between ERK1/2 and NKCC1[J]. Cell Physiol Biochem, 2011, 28(4): 703-14. doi:10.1159/000335764 |
| [6] | Yigitturk G, Acara A C, Erbas O, et al. The antioxidant role of agomelatine and gallic acid on oxidative stress in STZ induced type Ⅰ diabetic rat testes[J]. Biomed Pharmacother, 2017, 87: 240-6. doi:10.1016/j.biopha.2016.12.102 |
| [7] | Roghanidehkordi F, Roghani M, Baluchnejadmojarad T. Diosgenin mitigates streptozotocin diabetes-induced vascular dysfunction of the rat aorta: the involved mechanisms[J]. J Cardiovasc Pharmacol, 2015, 66(6): 584-92. doi:10.1097/FJC.0000000000000308 |
| [8] | Emadi S S, Soufi F G, Khamaneh A M. MicroRNA-146a expression and its intervention in NF-κB signaling pathway in diabetic rat aorta[J]. Endocr Regul, 2014, 48(2): 103-8. doi:10.4149/endo_2014_02_103 |
| [9] | Baldwin A S Jr. The NF-kappa B and I kappa B proteins: new discoveries and insights[J]. Annu Rev Immunol, 1996, 14: 649-83. doi:10.1146/annurev.immunol.14.1.649 |
| [10] | Kerkela R, Kockeritz L, Macaulay K, et al. Deletion of GSK-3beta in mice leads to hypertrophic cardiomyopathy secondary to cardiomyoblast hyperproliferation[J]. J Clin Invest, 2008, 118(11): 3609-18. doi:10.1172/JCI36245 |
| [11] | Khan M S, Halagowder D, Devaraj S N. Methylated chrysin induces co-ordinated attenuation of the canonical Wnt and NF-κB signaling pathway and upregulates apoptotic gene expression in the early hepatocarcinogenesis rat model[J]. Chem Biol Interact, 2011, 193(1): 12-21. doi:10.1016/j.cbi.2011.04.007 |
| [12] | Nurmi A, Goldsteins G, Närväinen J, et al. Antioxidant pyrrolidine dithiocarbamate activates Akt-GSK signaling and is neuroprotective in neonatal hypoxia-ischemia[J]. Free Radic Biol Med, 2006, 40(10): 1776-84. doi:10.1016/j.freeradbiomed.2006.01.011 |
| [13] | Zhu T, Zhao R, Zhang L, et al. Pyrrolidine dithiocarbamate enhances hepatic glycogen synthesis and reduces FoxO1-mediated gene transcription in type 2 diabetic rats[J]. Am J Physiol Endocrinol Metab, 2012, 302(4): E409-16. doi:10.1152/ajpendo.00453.2011 |