

2. 沈阳药科大学生命科学与生物制药学院,辽宁 沈阳 110016
2. School of Pharmaceutical Engineering, Shengyang Pharmaceutical University, Shenyang 110016, China
肺癌是目前死亡率最高的恶性肿瘤之一,约85%的肺癌为非小细胞肺癌(non-small cell lung cancer,NSCLC)。晚期NSCLC的治疗一直是肺癌治疗领域的一个难点,随着肿瘤分子靶向治疗的开展,表皮生长因子受体(epidermal growth factor receptor, EGFR)酪氨酸激酶抑制剂为晚期NSCLC的治疗带来了新的希望[1-2]。恶性肿瘤生长失控,侵害周围组织并发生转移,这些过程在某种程度上受病理性的细胞信号转导所控制。信号传至胞内,诱导细胞增殖或抑制细胞凋亡。受体蛋白酪氨酸激酶就是其中一类过度表达的信号蛋白[3]。EGFR是一种受体蛋白酪氨酸激酶,能够介导多条信号通路的转导,将胞外信号传递至胞内,对正常细胞和肿瘤细胞的增殖、分化、凋亡均发挥重要的调节作用。因此,选择性抑制EGFR介导的信号转导途径以达到治疗肿瘤的目的,已成为近年来肿瘤治疗研究的热点。
缩氨基硫脲及其衍生物由于具有广泛的生物活性,如抗病毒、抗菌、抗肿瘤、抗结核、抗疟等,备受人们的重视[4-6]。缩氨基硫脲化合物的抗肿瘤活性是由于该化合物能够抑制DNA的合成,将核苷酸还原为脱氧核苷酸[7]。喹唑啉化合物通过抑制EGFR、血管内皮生长因子受体、血小板衍生生长因子受体等其他多个作用靶点,在抗癌、抗菌、抗真菌、抗炎、抗惊厥等药物化学领域受到广泛关注[8-9]。喹唑啉类化合物作为一种较成功的小分子EGFR酪氨酸激酶抑制剂受到了广泛的重视。研究表明,喹唑啉类化合物通过与作用位点结合,高度选择性地抑制EGFR的磷酸化,从而抑制肿瘤细胞的生长[10]。以EGFR为靶点的喹唑啉类药物,如拉帕替尼(lapatinib,LPTN)、吉非替尼和厄洛替尼已经上市,用于NSCLC的治疗[11]。
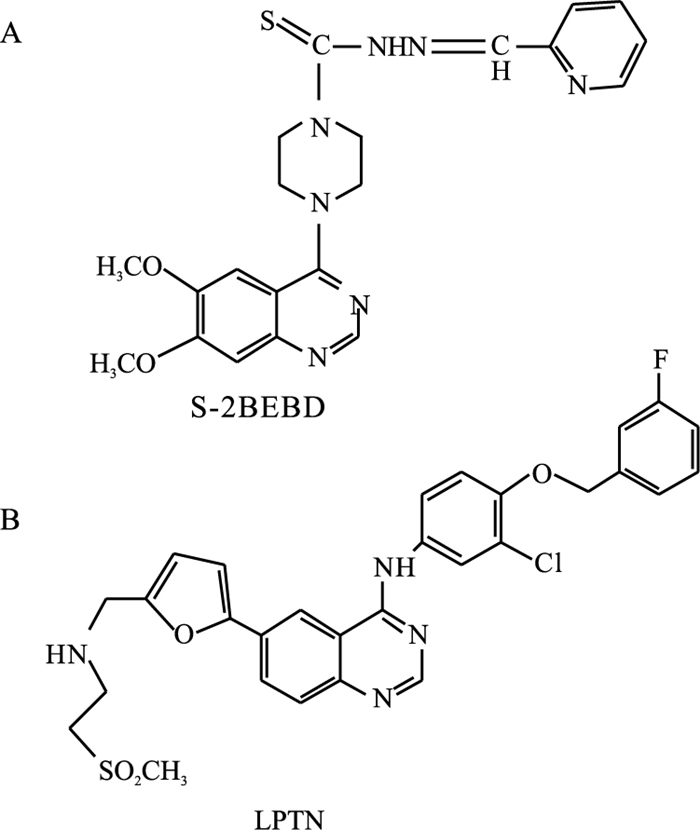
尽管对靶向的小分子抑制剂的研究已有长足进展,但目前仍有很多方面不甚了解,其更完善的作用机制、适用范围及用药方式尚待进一步研究。由于EGFR抑制剂在使用过程中逐渐出现耐药现象,因此寻找新的EGFR抑制剂显得尤为迫切。作者合成了含有缩氨基硫脲结构的喹唑啉类衍生物S-2BEBD [12-14],其结构式见Fig 1。研究发现,S-2BEBD对MCF-7、A549和PC3肿瘤细胞表现出较高的体外细胞抑制活性,并且与LPTN相比,S-2BEBD显示出更高的活性[14]。为了探索S-2BEBD的作用机制,本文从细胞凋亡形态、细胞周期、caspase-3相对活性等方面,与LPTN进行比较,研究S-2BEBD对人肺癌A549细胞增殖及凋亡的影响。
|
| Fig 1 Structures of S-2BEBD (A) and LPTN (B) |
人肺癌细胞A549购自中国科学院上海生命科学研究院细胞资源中心。S-2BEBD按文献方法[14]合成; 拉帕替尼购自百灵威公司; RPMI 1640培养基购自Gibco公司; 胎牛血清购自天津市灏洋生物制品科技有限责任公司; Western blot抗体购自Santa Cruz公司; MTT购自Ameresco公司; 吖啶橙(acridine orange,AO)、碘化丙啶(propidium iodide, PI)、核糖核酸酶A(RNaseA),均购自Sigma公司; 其他试剂均为分析纯。
1.2 仪器CJ-1F型医用净化工作台(苏州市金燕净化设备有限公司); XDS-1B型倒置显微镜(重庆光电仪器有限公司); DMLS2型正置荧光显微镜(德国Leica公司); Multiskan MK3型酶标仪(赛默飞世尔上海仪器有限公司); FACS Calibur流式细胞仪(美国Becton Dickson公司)。
1.3 细胞培养将人肺癌细胞A549接种于含有10%胎牛血清的RPMI 1640培养基中培养,置于饱和湿度、37 ℃、5% CO2培养箱中,传至3代后,待细胞状态稳定即可实验。
1.4 细胞增殖检测MTT法检测S-2BEBD和LPTN对A549细胞的增殖抑制作用。取对数生长期的A549细胞,接种于无菌96孔细胞培养板中,每孔加入180 μL的细胞悬液,培养24 h,分别加入浓度为1 000、100、10、1、0.1 μmol·L-1的LPTN和S-2BEBD两种药,每个浓度设3个复孔。培养72 h后,每孔加入浓度为5 g·L-1的MTT溶液20 μL,培养4 h,每孔加入150 μL DMSO溶液,充分震荡,酶标仪492 nm处测吸光度值(OD),计算细胞的增殖抑制率。增殖抑制率=(阴性对照组OD值-实验组OD值)/(阴性对照组OD值-空白对照组OD值)×100%。利用SPSS 16.0软件计算IC50。实验重复3次,取平均值。
1.5 倒置显微镜下观察细胞形态取对数生长期的A549细胞接种于96孔细胞培养板,每孔180 μL细胞悬液,细胞数为5×103/孔,培养24 h后,加入浓度为4.0 μmol·L-1的S-2BEBD,同时设阴性对照组(只含DMSO的培养基),药物作用24、48、72 h后,光学显微镜下观察细胞形态变化。
1.6 AO染色检测凋亡细胞取对数生长期的A549细胞接种于24孔板,5×104/孔,每孔1.0 mL培养液,培养24 h后,加入S-2BEBD(2.25、4.5、6.0 μmol·L-1),药物作用24、48、72 h后,每孔加入1 mL PBS缓冲液,10 μL AO染液,荧光显微镜下观察细胞形态。
1.7 流式细胞术检测细胞周期变化采用同上方法处理A549细胞,24 h后加入S-2BEBD(3、2.25、1.5、0.75 μmol·L-1),各瓶培养液终体积为8 mL。继续培养,于加药24、48、72 h后收集细胞,吸除培养基,PBS冲洗3次,胰酶消化,悬浮液转移至离心管,离心后,弃上清,加20 μL RNase溶液,然后再加入30 μL PI染液,流式细胞仪检测。
1.8 Western blot检测采用同上方法处理A549细胞,加入S-2BEBD 24 h后,提取细胞质蛋白进行SDS-PAGE电泳,转膜后,5%脱脂奶粉封闭,再加入相对应的一抗,4 ℃摇床孵育3 h,将膜在TBST缓冲液中漂洗3次,用封闭液稀释二抗,室温下孵育2 h后显影。检测p-EGFR、EGFR、p-Akt、Akt、p-ERK1/2、ERK1/2等蛋白表达水平。
1.9 统计学分析实验数据用x±s表示,应用SPSS 16.0统计软件处理,组间比较采用F检验。
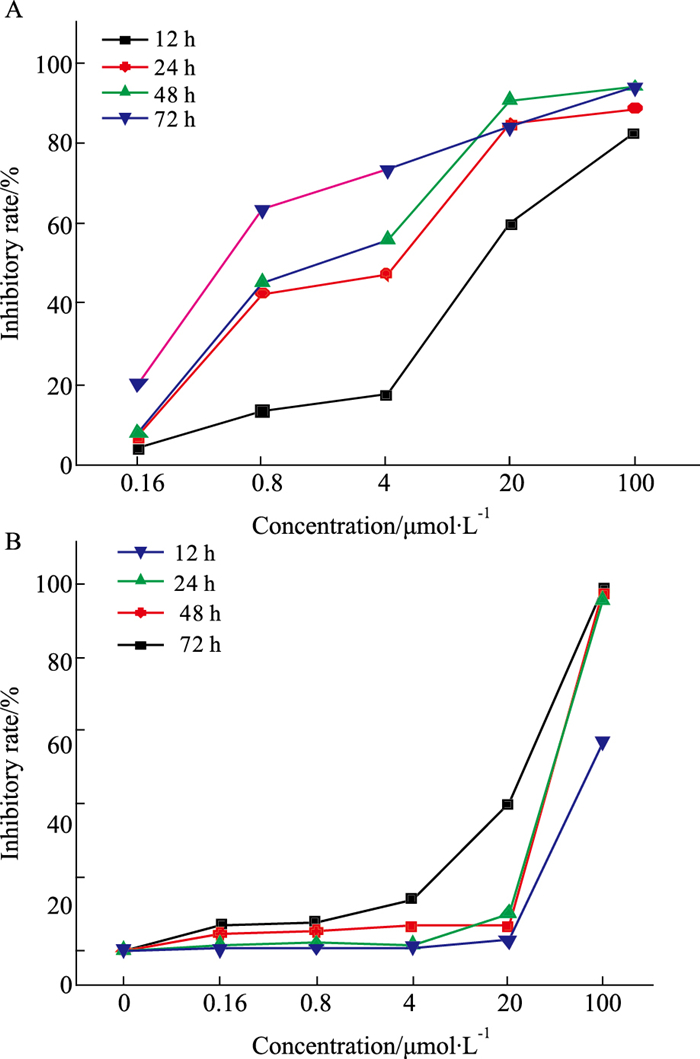
2 结果 2.1 S-2BEBD对A549细胞体外增殖抑制作用的量效、时效关系LPTN作为阳性对照药,Fig 2结果表明,S-2BEBD和LPTN对A549细胞增殖具有明显的抑制作用,S-2BEBD的抑制活性强于LPTN。S-2BEBD对A549细胞体外增殖的抑制作用明显,随着浓度的增大、时间的延长,抑制作用也明显增强。提示S-2BEBD对A549细胞体外增殖的抑制作用具有剂量和时间依赖性。
|
| Fig 2 Time and concentration-response curves of S-2BEBD (A) and LPTN (B) on A549 cells (x±s, n=3) |
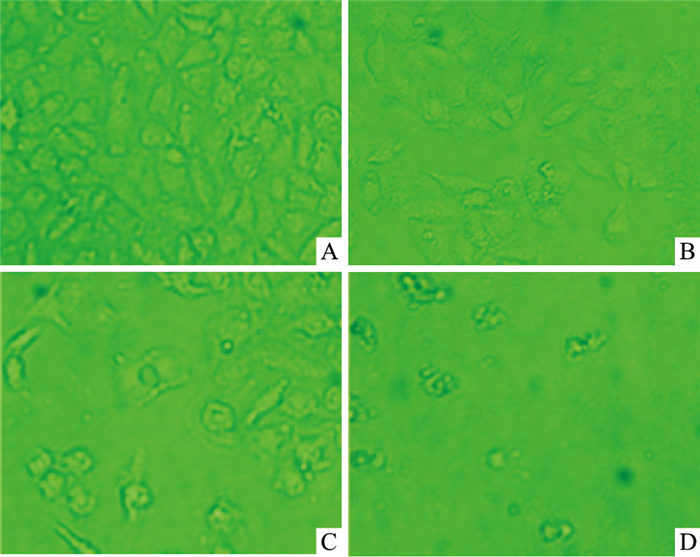
倒置显微镜观察A549细胞的形态学变化。如Fig 3所示,对照组A549细胞生长状态良好,形态规则,呈圆梭形,贴壁生长,轮廓清楚,细胞生长较旺盛。S-2BEBD 4.0 μmol·L-1处理组A549细胞均表现出细胞皱缩,细胞膜表面不光滑,贴壁能力减弱,胞质中出现颗粒状物质,染色质凝集,部分细胞形成凋亡小体。时间越长,作用效果越明显。
|
| Fig 3 Morphological changes of A549 cells after treatment with S-2BEBD (×400) A: 12 h; B: 24 h; C: 48 h; D: 72 h. |
如Fig 4所示,对照组A549细胞的核染色质着绿色,并呈正常结构,细胞结构完整,边缘清晰,而药物处理组的细胞核形状则发生了明显的改变,48 h时出现了染色质浓缩、断裂、边缘化; 72 h后出现凋亡小体等典型细胞凋亡特征,且随着S-2BEBD浓度的增高,凋亡特征越明显。提示S-2BEBD以时间和剂量依赖性的方式诱导A549细胞发生凋亡。

|
| Fig 4 Morphological changes of A549 cells after treatment with S-2BEBD by a fluorescent microscopy (×400) A: Control; B: S-2BEBD 4.5 μmol·L-1 24 h; C: S-2BEBD 4.5 μmol·L-1 48 h; D: S-2BEBD 4.5 μmol·L-1 72 h; E: Control; F: S-2BEBD 2.25 μmol·L-1 48 h; G: S-2BEBD 4.50 μmol·L-1 48 h; H: S-2BEBD 6.00 μmol·L-1 48 h. |
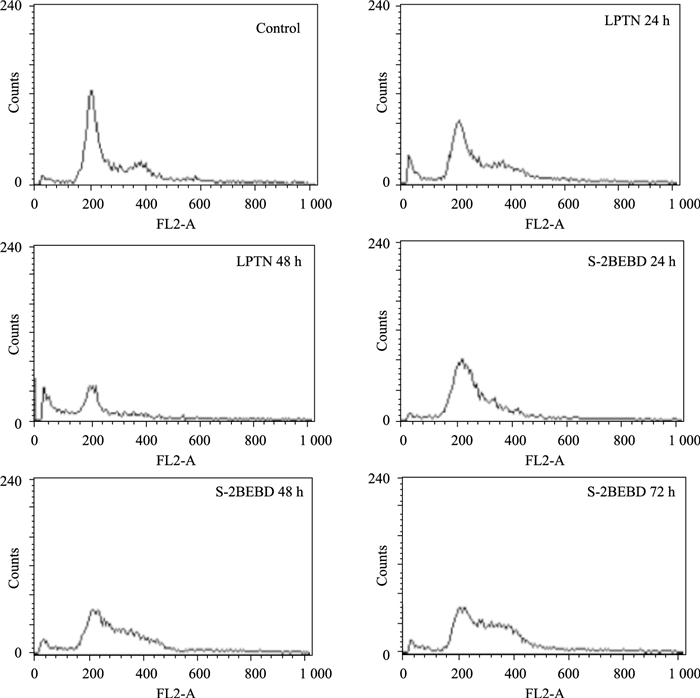
流式细胞术检测发现,20 μmol·L-1的LPTN作用A549细胞24~48 h,SubG1期细胞明显增加,柱形图上可见明显的凋亡峰,G0/G1期细胞明显减少,S期和G2/M期细胞随着时间的延长先升高,后降低。1.5 μmol·L-1的S-2BEBD作用A549细胞24~72 h,G0/G1细胞明显减少,S期细胞逐渐增加,差异有统计学意义; G2/M期细胞先升高,后又发生明显的降低(Tab 1、Fig 5)。
| Group | Time/h | SubG1/% | G0/G1/% | S/% | G2/M/% |
| Control | - | 2.67±0.56 | 57.61±4.23 | 12.05±1.77 | 18.06±2.73 |
| LPTN | 24 | 8.44±1.57** | 46.11±4.56* | 14.89±1.58 | 20.04±2.26 |
| 48 | 31.34±3.67** | 49.88±3.43* | 6.77±3.67* | 8.04±0.63** | |
| S-2BEBD | 24 | 4.24±1.07 | 40.85±3.83** | 41.71±3.28** | 8.77±1.58** |
| 48 | 4.50±1.11 | 24.14±2.57** | 33.90±2.83** | 30.44±2.69** | |
| 72 | 6.81±1.49** | 37.67±1.48** | 29.77±1.63** | 16.81±1.59 | |
| *P < 0.05,**P < 0.01 vs control | |||||
|
| Fig 5 Effect of LPTN and S-2BEBD on apoptosis and cell cycle of A549 cells |
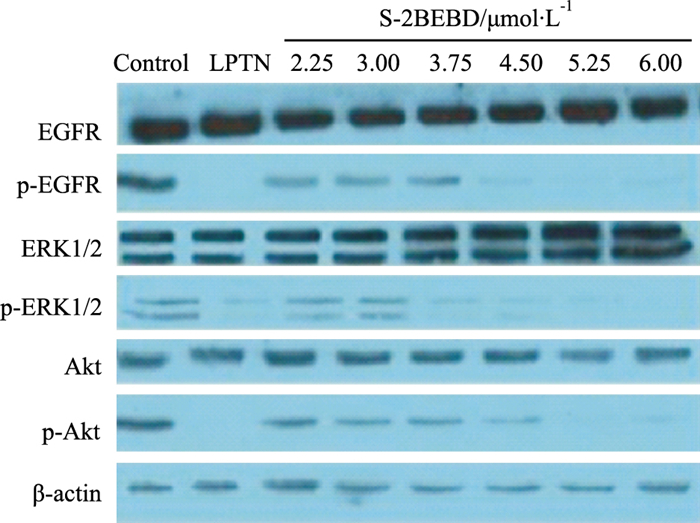
首先检测了LPTN和S-2BEBD对肺癌A549细胞中EGFR及下游信号蛋白ERK、Akt磷酸化的影响。Fig 6结果显示,与对照组相比,LPTN(20 μmol·L-1)和S-2BEBD(4.5、5.25、6.00 μmol·L-1)能够以剂量依赖性的方式明显下调p-EGFR、p-Akt、p-ERK l/2蛋白的表达,而对非磷酸化的EGFR、Akt、ERK l/2表达无明显影响。
|
| Fig 6 Effects of LPTN and S-2BEBD on phosphorylation status of EGFR, ERK1/2 and Akt in A549 cells |
Western blot检测凋亡相关蛋白的表达,Fig 7结果显示,cleaved caspase-3的表达随S-2BEBD浓度增高而增加。LPTN和S-2BEBD通过促进促凋亡蛋白Bax的激活,抑制Bcl-2的活性,诱导A549细胞的凋亡。

|
| Fig 7 Effects of LPTN and S-2BEBD on expression of caspase-3, Bcl-2 and Bax in A549 cells |
EGFR信号传导途径在肿瘤细胞的增殖、损伤修复、侵袭及新生血管形成中起重要作用,近年来,EGFR靶向药物已成为肿瘤治疗研究的新热点[15]。自20世纪90年代中期起,喹唑啉类化合物对EGFR的抑制作用,使其成为抗癌药物的主要研发对象之一。近年来,众多研究者对喹唑啉类化合物进行了更深入的构效关系和作用机制研究,显示出此类化合物的优良抗癌潜力,有望筛选出高效抗癌临床药物。前期作者合成了含有缩氨基硫脲结构的喹唑啉类衍生物,研究显示,S-2BEBD对多种肿瘤细胞表现出较高的体外抑制活性。
本实验将LPTN和S-2BEBD分别作用于肺癌A549细胞系72 h,经过MTT比色分析,表明LPTN和S-2BEBD体外抗肿瘤细胞增殖的作用具有明显的剂量和时间依赖性。分别考察了不同浓度S-2BEBD作用下细胞形态和细胞周期,发现均有明显的变化,即存在着剂量依赖性,且考察了S-2BEBD对A549细胞作用不同时间的细胞周期和细胞形态,也均有明显的变化,即存在着时间依赖性。S-2BEBD能够以剂量依赖性的方式明显下调p-EGFR、p-Akt、p-ERKl/2蛋白的表达水平,并且cleaved caspase-3的表达随S-2BEBD浓度增高而增加。同时,LPTN和S-2BEBD通过诱导Bax的激活,抑制Bcl-2的活性,诱导A549细胞的凋亡。
综上所述,S-2BEBD对肺癌细胞系A549具有抑制增殖、诱导凋亡作用,其机制可能与下调p-EGFR、p-Akt、p-ERK l/2、Bcl-2蛋白的表达水平有关。本研究表明S-2BEBD具有潜在的临床应用前景,可以为S-2BEBD对NSCLC的治疗提供一定的理论基础。
( 致谢: 本课题完成于沈阳药科大学生命科学与生物制药学院药理实验室,在此对实验室的各位老师、同学的帮助表示由衷的感谢!)
| [1] | 刘灿, 蔡天宇, 赵晓萌, 等. 罗汉果提取物诱导肺癌细胞A549凋亡的研究[J]. 中国药理学通报, 2015, 31(9): 1310-4. Liu C, Cai T Y, Zhao X M, et al. Apoptosis effect of Siraitiagrosvenorii extracts on lung cancer cells A549 and its mechanisms[J]. Chin Pharmacol Bull, 2015, 31(9): 1310-4. doi:10.3969/j.issn.1001-1978.2015.09.025 |
| [2] | 钟良瑞, 魏克民. 三叶青黄酮对肺癌A549细胞生长抑制与MAPKs通路关系的研究[J]. 中国药理学通报, 2014, 30(1): 101-4. Zhong L R, Wei K M. Radix tetrastigma hemsleyani flavone suppresses human lung carcinoma A549 cell by regulating MAPKs pathway[J]. Chin Pharmacol Bull, 2014, 30(1): 101-4. doi:10.3969/j.issn.1001-1978.2014.01.022 |
| [3] | Hunter T. Oncoprotein networks[J]. Cell, 1997, 88: 333-6. doi:10.1016/S0092-8674(00)81872-3 |
| [4] | Li M X, Zhang D, Zhang L Z, et al. Diorganotin(Ⅳ) complexes with 2-benzolypyridine and 2-acetylpyrazine N(45)-phenylthiosemicarbazones: synthesis, crystal structures and biological activities[J]. J Organomet Chem, 2011, 696: 852-8. doi:10.1016/j.jorganchem.2010.10.011 |
| [5] | Duan L P, Zhang H B. Novel thiosemicarbazones derivatives bearing aromatic iodine moiety: design, synthesis and anti-malarial activity[J]. Arabian J Chem, 2011, 4: 231-4. doi:10.1016/j.arabjc.2010.06.042 |
| [6] | Fujii N, Mallari J P, Hansell E J, et al. Discovery of potent thiosemicarbarbazone inhibitors of rhodesain and cryzain[J]. Bioorg Med Chem Lett, 2005, 15: 121-3. doi:10.1016/j.bmcl.2004.10.023 |
| [7] | Kovala-Demertzi D, Domopuolou A, Demertzi M, et al. Coordinating properties of 2-acetylpyridine thiosemicarbazone. Palladium(Ⅱ) complexes with neutral and deprotonated ligand. X-ray structure of bromo(2-acetylpyridine thiosemicarbazonato) palladium(Ⅱ)[J]. Polyhedron, 1994, 13: 1917-25. doi:10.1016/0277-5387(94)80015-4 |
| [8] | He J B, Wang X G, Zhao X Q, et al. Synthesis and antitumor activity of novel quinazoline derivatives containing thiosemicarbazide mnoiety[J]. Eur J Med Chem, 2012, 54: 925-30. doi:10.1016/j.ejmech.2012.06.003 |
| [9] | Shallal H M, Russu W A. Discovery, synthesis, and investigation of the antitumor activity of novel piperazinylpyrimnidine derivatives[J]. Eur J Med Chem, 2011, 46(6): 2043-57. doi:10.1016/j.ejmech.2011.02.057 |
| [10] | Rewcastle G W, Denny W A, Bridges A J, et al. Tyrosine kinase inhibitors. 5. Synthesis and structure-activity relationships for 4-[(phenylmethyl)amino]- and 4-(phenylamino)quinazolines as potent adenosine 5'-triphosphate binding site inhibitors of the tyrosine kinase domain of the epidermal growth factor receptor[J]. J Med Chem, 1995, 38: 3482-7. doi:10.1021/jm00018a008 |
| [11] | Wu X Q, Li M D, Tang W H, et al. Synthesis, and in vitro antitumor activity evaluation of novel 4-pyrrylamino quinazoline derivatives[J]. Chem Biol Drug Des, 2011, 78: 932-40. doi:10.1111/j.1747-0285.2011.01234.x |
| [12] | 刘海彬, 吕萍, 潘宁宁, 等. 6-氯-4-哌嗪基喹唑啉缩氨基硫脲类化合物的合成及体外抗肿瘤活性[J]. 应用化学, 2012, 29(9): 1000-5. Liu H B, Lyu P, Pan N N, et al. Synthesis and in vitro antitumor activity of 6-chloro-4-piperazinquinazoline thiosemicarbazone derivatives[J]. Chin J Appl Chem, 2012, 29(9): 1000-5. |
| [13] | 刘海彬, 徐惠娟, 吕萍, 等. 6, 7-二甲氧基-4-哌嗪喹唑啉缩氨基硫脲衍生物的合成及体外抗肿瘤活性研究[J]. 化学学报, 2012, 70(5): 674-8. Liu H B, Xu H J, Lyu P, et al. Synthesis and in vitro antitumor activities of 6, 7-dimethoxy-4-piperazinquinazoline thiosemicarbazone derivatives[J]. Acta Chim Sin, 2012, 70(5): 674-8. |
| [14] | 刘海彬, 吕萍, 潘宁宁, 等. 新型含缩氨基硫脲结构的喹唑啉衍生物的合成及其体外抗癌活性研究[J]. 高等学校化学学报, 2014, 35(5): 981-8. Liu H B, Lyu P, Pan N N, et al. Synthesis and in vitro anticancer activity of novel quinazoline derivatives containing thiosemicarbazone structure[J]. Chem J Chin Univ, 2014, 35(5): 981-8. |
| [15] | 刘刚, 李晓燕. 喹唑啉类化合物生物活性研究进展[J]. 药学进展, 2007, 31(12): 542-50. Liu G, Li X Y. Advances in the study on bioactivity of quinazoline compounds[J]. Prog Pharm Sci, 2007, 31(12): 542-50. doi:10.3969/j.issn.1001-5094.2007.12.003 |

