

CYP1A2在肝脏细胞色素P450(cytochrome P450,CYP450)药物代谢酶总含量中所占比例仅次于CYP3A和CYP2C亚家族,居于第3位,可参与多种外源性药物及内源性类固醇激素的代谢,也参与多种前毒物或前致癌物质,如芳香胺类、黄曲霉素及杂环胺类的代谢活化过程[1-2]。以往对CYP1A2代谢功能的研究多着重于该酶在化学毒物代谢中的作用及机制,而对其在病毒性肝炎、肝硬化、肝细胞癌等免疫性肝损伤过程中的作用和调控机制尚不清楚[3]。核转录因子κB (nuclear factor kappa B,NF-κB)是调节炎症和免疫反应及细胞存活的重要因子[4-5],也涉及细胞转化和肿瘤形成。炎症和组织损伤过程中,NF-κB激活,调控大量下游炎性细胞因子,可能参与损伤过程。吡咯烷二硫氨基甲酸(pyrrolidine dithiocarbamate,PDTC)可以通过抑制IκB的磷酸化,从而发挥抑制NF-κB的作用[6],因此, 可以阻止NF-κB向核内移位,减少下游细胞因子的表达。本研究以尾静脉注射卡介苗(Bacille Calmette-Guerin,BCG)制备大鼠免疫性肝损伤模型,观察CYP1A2的代谢活性蛋白表达有何变化,采用PDTC抑制NF-κB活化,观察对CYP1A2氧化代谢活力和肝功能的影响,深入探讨NF-κB在免疫性肝损伤中的作用及其作用环节,为免疫性肝损伤药物治疗提供新的靶点和思路。
1 材料与方法 1.1 实验动物与试剂清洁级♂SD大鼠,内蒙古大学动物实验中心提供,体质量(250±20)g,动物许可证号:SCXK(蒙)2005-0001。BCG冻干粉(60 mg/支,1 g·L-1),购自中国药品生物制品鉴定所,批号:2015-01;PDTC(批号:851002)、茶碱(批号:057k0691),均购自美国Sigma公司; 组织蛋白提取试剂盒、BCA蛋白定量试剂盒、SDS-PAGE凝胶制备试剂盒、CYP1A2兔抗大鼠多克隆抗体、β-actin鼠多克隆抗体,均购自武汉博士德生物工程有限公司。
1.2 仪器高效液相色谱仪(美国Waters公司); DF-D型恒压恒流电泳仪(北京市六一仪器厂); 离心机(上海安亭科学仪器厂); 快速混匀器(姜堰市新康医疗有限公司); 7600-020型自动生化分析仪(日本日立公司)。
1.3 动物分组及免疫性肝损伤模型的制备SD大鼠60只,适应性饲养2周,称重编号后,按随机数字表分为control、BCG、BCG+PDTC(50、100、200 mg·kg-1)组,每组12只。BCG、BCG+PDTC组尾静脉注射BCG 125 mg·kg-1 14 d制备免疫性肝损伤大鼠模型,Control组尾静脉注射等体积生理盐水。采用NF-κB特异性抑制剂对BCG+PDTC组进行干预(d 11、12、13的16时腹腔注射PDTC各1次,剂量分别为50、100、200 mg·kg-1)。d 14用于高效液相色谱(HPLC)法测定CYP1A2代谢活力实验,随后将大鼠颈椎脱臼处死,迅速剖取肝脏、脾脏,称重。将部分肝组织浸泡于事先配好的甲醛酒精(甲醛:酒精=1 :9)固定液中,做石蜡包埋切片,常规HE染色。称取部分肝组织用于CYP450总含量测定,另称取部分肝组织冻存,用于Western blot检测。
1.4 HPLC法测定大鼠CYP 1A2代谢活性于实验d 14,取control、BCG、BCG+PDTC(100 mg·kg-1)3组大鼠,按照40 mg·kg-1的剂量经口单次给予探针药物氨茶碱注射液,并分别于给予氨茶碱后0.25、0.5、0.75、1、1.5、2、3、4、5、7、10、12、24 h,从眼内眦静脉丛采血,每次采血0.5 mL,置于预先放有少量肝素钠的软试管中,缓慢上下颠倒3次后,立即3 500 r·min-1离心5 min,记录血浆量,并保存在-20 ℃冰箱中。根据文献方法[3],测定血浆中CYP1A2探针药物茶碱浓度的经时变化。用药物代谢动力学软件3P97对血药浓度数据进行拟合,得出AUC、
BCG刺激2周后(d 14晨),各组动物均取定量12只肝脏制备肝匀浆样本, 按1 :4比例向肝组织匀浆样本中加入预冷的0.15 mol·L-1 Tris-HCl缓冲液,通入CO气体2 min,联二亚硫酸钠还原样本后,用双光束紫外可见分光光度计测定490 nm、450 nm处光密度差值。采用BCA法测定肝匀浆样本中蛋白的含量,以牛血清白蛋白作标准曲线,计算每毫克蛋白中CYP450全酶含量。
1.6 Western blot检测肝组织CYP1A2表达肝组织称重后,匀浆制备蛋白抽提物,用BCA法蛋白定量,SDS-PAGE电泳,将蛋白质转移到硝酸纤维素膜上,放入0.02 mol·L-1 TBS缓冲液配制的5%脱脂奶粉和1%的BSA混合的封闭液内,摇床摇动,室温封闭2 h。漂洗,CYP1A2兔多克隆抗体、β-actin鼠多克隆抗体杂交,加二抗,显色,X线片曝光,用紫外透视成像系统对X线片进行光密度分析。
1.7 血清肝功能检测血清谷丙转氨酶(alanine transarninase,ALT)、谷草转氨酶(aspartate aminotransferase,AST)水平使用自动生化分析仪测定。
1.8 统计学处理实验结果用x±s表示, 采用SPSS 19.0统计软件,单因素方差分析进行组间比较。
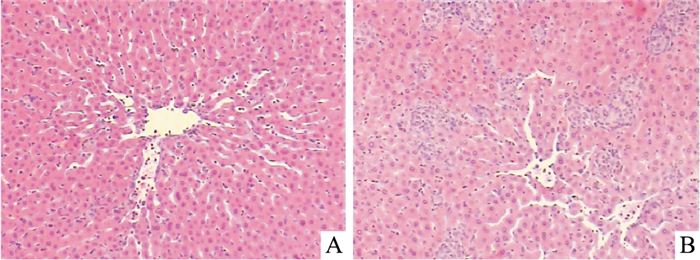
2 结果 2.1 PDTC对BCG诱导的免疫性肝损伤大鼠肝脏病理组织学、肝重/体质量、脾重/体质量、血清转氨酶含量的影响经尾静脉注射BCG 2周后,光镜下观察到肝实质及汇管区周围有大量单核细胞及淋巴细胞浸润,形成大小不等,且弥漫性分布的大量肉芽肿团块为特征的免疫性肝损伤(Fig 1)。Tab 1结果显示,肝脏重量增加(P < 0.05),脾脏重量增加,PDTC可降低肝脏、脾脏重量的增加; 血清AST、ALT均升高(P < 0.01),PDTC可抑制AST、ALT的升高。
|
| Fig 1 Pathological features of liver (HE, ×200) A: Control group; B: BCG group. |
| Group | Liver weight/body weight/% | Spleen weight/body weight/% | ALT/U·L-1 | AST/U·L-1 |
| Control | 5.1±0.7 | 0.4±0.0 | 66.5±8.6 | 84.0±9.3 |
| BCG | 8.6±0.5* | 1.2±0.2** | 196.7±12.4** | 153.9±16.8** |
| BCG+PDTC(50 mg·kg-1) | 8.2±1.1* | 1.0±0.2** | 173.4±15.5** | 146.8±14.9** |
| BCG+PDTC(100 mg·kg-1) | 7.9±0.5* | 0.8±0.1*# | 146.8±13.8*# | 137.4±14.8*# |
| BCG+PDTC(200 mg·kg-1) | 7.7±0.5* | 0.7±0.1*## | 111.2±12.9*## | 124.2±12.5*## |
| *P < 0.05, **P < 0.01 vs control; #P < 0.05, ##P < 0.01 vs BCG | ||||
Tab 2结果显示,与空白对照组相比,尾静脉注射BCG 14 d后,肝脏CYP450全酶含量明显减少(P < 0.01)。在BCG刺激的基础上给予工具药PDTC进行干预,可剂量依赖性地减缓肝脏CYP450全酶含量减少(P < 0.05)。
| Group | CYP450 content/μmol·g-1 Pro |
| Control | 1.71±0.36 |
| BCG | 0.68±0.13** |
| BCG+PDTC(50 mg·kg-1) | 0.78±0.17* |
| BCG+PDTC(100 mg·kg-1) | 0.97±0.14* |
| BCG+PDTC(200 mg·kg-1) | 1.42±0.26# |
| *P < 0.05, **P < 0.01 vs control; #P < 0.05 vs BCG | |
Control、BCG、BCG+PDTC(100 mg·kg-1)3组大鼠经口单次给予经CYP1A2代谢的探针药物茶碱(40 mg·kg-1),经HPLC测得大鼠血浆中茶碱血药浓度的经时变化。如Fig 2所示,BCG组在0.75、1、1.5、2、3、4、5、7 h时间点血药浓度均高于control组,BCG+PDTC组在0.75、1、1.5、2、3 h时间点血药浓度低于BCG组(P < 0.05)。Tab 3结果显示,BCG组Ke、CL均小于control组,A、Cmax、AUC、Tmax、T12均高于control组(P < 0.05)。BCG+PDTC组A、Ke、CL均高于BCG组,AUC、CL均低于control组(P < 0.05),而Vd在3组中不变。

|
| Fig 2 Plasma theophylline levels in all groups (x±s, n=6) *P < 0.05, **P < 0.01 vs control; #P < 0.05, ##P < 0.01 vs BCG |
| Parameter | Control | BCG | BCG+PDTC (100 mg·kg-1) |
| A/mg·L-1 | 28.00±2.30 | 38.41±3.60** | 45.26±1.60*# |
| Cmax/mg·kg-1 | 14.69±1.80 | 22.59±1.30** | 17.58±1.50# |
| AUC/mg·h·L-1 | 58.63±5.90 | 137.96±4.20** | 51.06±6.30*## |
| Ke/h-1 | 0.25±0.08 | 0.21±0.10* | 0.28±0.05# |
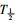 /h
/h |
2.68±0.20 | 3.18±0.10** | 2.47±0.20# |
| Tmax/h | 1.64±0.10 | 1.98±0.10* | 1.96±0.06* |
| CL/L·h-1·kg-1 | 0.47±0.10 | 0.29±0.12* | 0.37±0.10# |
| Vd/L·kg-1 | 1.52±0.30 | 1.33±0.20 | 1.34±0.30 |
| *P < 0.05, **P < 0.01 vs control; #P < 0.05, ##P < 0.01 vs BCG | |||
Fig 3的Western blot结果显示,内参β-actin可见各条带密度均一,提示蛋白定量基本准确,各组蛋白上样量基本一致。BCG组肝组织中CYP1A2蛋白的表达明显低于control组,PDTC预处理后CYP1A2蛋白的表达有所恢复。

|
| Fig 3 CYP1A2 expression in all groups (x±s, n=6) *P < 0.05, **P < 0.01 vs control; #P < 0.05, ##P < 0.01 vs BCG |
我国人群中发生的免疫性肝损伤多为病毒、原虫等微生物感染所致,免疫应答在清除病毒的同时,肝细胞也受到损伤,是病毒性肝炎、肝硬化最终发展为肝细胞癌的重要发病机制之一,严重威胁人类的健康[6]。由于人类肝炎病毒不能自然地在啮齿类动物肝脏进行复制,寻找合适的动物模型进行免疫性肝损伤研究一直是国内外学者亟待解决的问题。大鼠经尾静脉注射BCG两周后,观察到肝实质及汇管区周围有大量单核细胞及淋巴细胞浸润,大鼠肝、脾重量增加,转氨酶增加,表明免疫性肝损伤大鼠模型造模成功,与人类病毒性肝炎的病理改变颇为一致,可以用于病毒性肝炎的代谢酶变化及其调控机制的研究。
CYP1A2酶约占肝脏中CYP450酶总量的13%,参与临床约5%药物的代谢,如华法林、茶碱、氯氮平、替加氟等[3],是重要的药物代谢酶之一。本实验观察到,BCG免疫损伤刺激导致大鼠肝脏CYP450酶总含量降低,给予工具药PDTC抑制NF-κB激活,可减缓肝药酶全酶的含量降低。研究结果进一步显示,免疫损伤过程中,占CYP450酶系13%左右的CYP1A2表达和代谢活力下调,钝化NF-κB激活可抑制其下调,推测CYP1A2的下调可能与NF-κB调节有关。当临床上CYP1A2酶活力下调与经其代谢的药物联用时,将会导致被代谢药物在体内因清除率降低而蓄积,从而引发药物相互作用,产生一系列严重的不良反应。因此,研究免疫性肝损伤状态对CYP1A2酶活性的影响,进而评估药物之间是否存在相互作用,具有重要的临床意义。BCG免疫刺激可诱导肝实质细胞或肝枯否细胞表达诱导型一氧化氮合酶(inducible nitric oxide synthase,iNOS),继而生成大量NO。NO作用于CYP1A2的铁蛋白中心,使CYP1A2破坏增加,使其下调[7-8]。NF-κB能与许多细胞因子和炎性介质的基因启动子区域的固定核苷酸序列结合,启动转录因子,在机体免疫应答、炎症反应方面发挥重要作用[9]。这可能是本研究中观察到的抑制NF-κB活化,可减缓肝脏代谢酶CYP1A2的表达和代谢活力降低,缓解肝脏损伤的分子机制之一。代谢酶恢复正常,可以认为是肝功能恢复的一个方面。
炎症和免疫损伤性刺激,导致肠黏膜屏障受损,肠道通透性增加,致使内毒素血症,iNOS大量诱生,NO合成增加,内毒素可以通过结合枯否细胞上CD14受体来激活NF-κB,活性氧可能是所有刺激物激活NF-κB共同机制和LPS诱导细胞信号通路的核心,活性氧诱生能减少巯基,从而增加细胞被氧化的比例,调节NF-κB激活。NF-κB可增加氧化信号通路的敏感性,导致基因产物的增多[10-12]。iNOS既是NF-κB的激活物,同时,又受到NF-κB的调控,抑制NF-κB的活化可以减少NO的诱生,减缓CYP1A2的下调。关于免疫性肝损伤过程中CYP1A2代谢活力是否经由NF-κB转录调控,调控了下游哪些炎性细胞因子,能否通过转录调控代谢酶活力干预损伤过程,有待进一步深入研究。
| [1] | 景欣悦, 彭蕴茹, 王新敏, 段金廒. 甘遂与甘草合用对大鼠肝药酶CYP1A2、CYP2C19和CYP2E1的影响[J]. 中国药理学通报, 2015, 31(11): 1625-6. Jing X Y, Peng Y R, Wang X M, Duan J A. Combined effect of Euphorbia kansui and Glycyrrhiza uralensis on CYP1A2, CYP2C19 and CYP2E1[J]. Chin Pharmacol Bull, 2015, 31(11): 1625-6. doi:10.3969/j.issn.1001-1978.2015.11.029 |
| [2] | 张咏莉, 崔玉强, 汪向升, 等. 黄芪颗粒和黄芪注射液对CYP1A2、CYP2D、CYP2C亚酶活性影响的实验研究[J]. 中国药理学通报, 2013, 29(4): 512-9. Zhang Y L, Cui Y Q, Wang X S, et al. Experimental study on effect of Astragalus granules and Astragalus injection on enzymatic activities of CYP1A2, CYP2D and CYP2C[J]. Chin Pharmacol Bull, 2013, 29(4): 512-9. doi:10.3969/j.issn.1001-1978.2013.04.016 |
| [3] | 张艳辉, 于超, 郭延垒, 等. 黄芪甲苷通过抑制大鼠体内CYP1A2酶活性影响药物相互作用[J]. 第三军医大学学报, 2012, 34(13): 1300-3. Zhang Y H, Yu C, Guo Y L, et al. Astragaloside Ⅳ exerts drug interactions via inhibiting CYP1A2 activity in rats[J]. J Third Mil Med Univ, 2012, 34(13): 1300-3. |
| [4] | 邓丽娟, 李湛军, 罗楹, 等. Caspase抑制剂F1013对刀豆蛋白A诱导小鼠急性肝损伤的治疗作用[J]. 中国药理学通报, 2012, 28(1): 136-9. Deng L J, Li Z J, Luo Y, et al. Therapeutic effect of the caspase selective inhibitor F1013 on ConA-induced acute hepatic injury in mice[J]. Chin Pharmacol Bull, 2012, 28(1): 136-9. doi:10.3969/j.issn.1001-1978.2012.032 |
| [5] | Lee H J, Jeong Y J, Lee T S, et al. Moringa fruit inhibits LPS-induced NO/iNOS expression through suppressing the NF-κB activation in RAW264.7 cells[J]. Am J Chin Med, 2013, 5: 1109-23. |
| [6] | Li X N, Su J, Zhao L, et al. The p38 MAPK inhibitor JLU1124 inhibits the inflammatory response induced by lipopolysaccharide through the MAPK-NF-κB pathway in RAW264.7 macrophages[J]. Int Immunopharmacol, 2013, 17(3): 785-92. doi:10.1016/j.intimp.2013.09.001 |
| [7] | Ko J W, Shin J Y, Kim J W, et al. Protective effects of diallyl disulfide against acetaminophen-induced nephrotoxicity: a possible role of CYP2E1 and NF-κB[J]. Food Chem Toxicol, 2017, 102: 156-65. doi:10.1016/j.fct.2017.02.021 |
| [8] | Lin X, Huang R, Zhang S, et al. Methyl helicterate protects against CCl4-induced liver injury in rats by inhibiting oxidative stress, NF-κB activation, Fas/FasL pathway and cytochrome P450 2E1 level[J]. Food Chem Toxicol, 2012, 50(10): 3413-20. doi:10.1016/j.fct.2012.07.053 |
| [9] | Lim K H, Kim K H, Choi S I, et al. RPS3a over-expressed in HBV-associated hepatocellular carcinoma enhances the HBx-induced NF-κB signaling via its novel chaperoning function[J]. PLoS One, 2011, 6(8): e22258. doi:10.1371/journal.pone.0022258 |
| [10] | Zordoky B N, El-Kadi A O. Role of NF-κB in the regulation of cytochrome P450 enzymes[J]. Current Drug Metab, 2009, 10(2): 164-78. doi:10.2174/138920009787522151 |
| [11] | Ghose R, Omoluabi O, Gandhi A, et al. Role of high-fat diet in regulation of gene expression of drug metabolizing enzymes and transporters[J]. Life Sci, 2011, 89(1-2): 57-64. doi:10.1016/j.lfs.2011.05.005 |
| [12] | Shi L X, Wang X, Wu Q, et al. Hepatic Cyp1a2 expression reduction during inflammation elicited in a rat model of intermittent hypoxia[J]. Chin Med J (Engl), 2017, 130(21): 2585-90. doi:10.4103/0366-6999.217084 |

