

2. 武汉大学人民医院精神卫生中心,湖北 武汉 430060
2. Dept of Psychiatry, Renmin Hospital, Wuhan University, Wuhan 430060, China
近来,许多研究表明胃泌素释放肽(gastrin-releasing peptide, GRP)/胃泌素释放肽受体(gastrin-releasing peptide receptor, GRPR)通路在中枢神经系统疾病发病中起着重要的作用[1]。GRP是一种神经肽,GRPR作为GRP的受体,通过结合GRP而发挥作用,GRPR在多种哺乳动物脑内(包括人类和大、小鼠)大量表达,并且在多种哺乳动物组织和细胞中有着相似的生物学机制[2]。研究表明,在应激条件下,实验动物脑内GRPR的表达明显上调,GRPR激动剂(GRP)可诱发应激样行为学改变,而GRPR拮抗剂(RC-3095)可以逆转上述行为学改变[3]。上述研究表明,GRPR与应激引起的神经精神疾病(包括抑郁症)相关联,进一步提示GRP/GRPR通路可能成为神经精神疾病(包括抑郁症)新的治疗靶点[4]。
氟西汀(fluoxetine,FLX)是一种选择性5-羟色胺(5-hydroxy tryptamine,5-HT)再摄取抑制剂,是临床最常见的一线抗抑郁药。研究发现,氟西汀使用后可以立即升高突触间隙的5-HT浓度,然而,其抗抑郁的临床疗效却需要数周才能显现,这种不一致显示,除了单胺能神经递质系统以外,可能还有其他机制涉及氟西汀的临床抗抑郁活动[5]。
海马作为应激抑郁的重要脑区,国内外的研究表明,海马与抑郁症的发病和治疗有着重要的关联[6]。研究表明,GRPR在海马(特别是CA3区和齿状回)有广泛的分布,并参与了海马有关记忆的调节作用[7]。然而,目前尚无关于海马GRPR的表达与抑郁症发病和抗抑郁治疗机制的相关研究报道。因此,通过可靠的应激抑郁动物模型,进一步探讨海马GRPR的表达与氟西汀抗抑郁作用的关系是必要的。本研究拟在制备慢性不可预见性应激(chronic unpredictable stress, CUS)C57BL/6小鼠应激抑郁模型的基础上,研究氟西汀对CUS小鼠海马GRPR表达的影响。进一步探讨氟西汀抗抑郁作用的新机制,为抑郁症的发生和治疗的机制研究提供理论依据。
1 材料与方法 1.1 实验动物30只♂C57BL/6小鼠,SPF级,6~8周龄,体质量(19±2)g,由武汉大学动物实验中心提供,实验动物质量合格证编号:4200593324。所有小鼠正常饲养于笼中,自由进食和饮水。1周后,利用随机数字表将小鼠随机分为3组:实验对照组、CUS模型组、氟西汀处理组,每组实验动物10只。
1.2 药品与试剂氟西汀原药(上海金洹化工科技有限公司);兔多克隆抗体GRPR(MC-830, 日本MBL);兔多克隆抗体GAPDH(ab9485, 美国Abcam公司);辣根过氧化物酶标记的羊抗兔IgG(sc-2004, 美国Santa Cruz公司)。
1.3 仪器EthoVision 3.0动物行为自动跟踪系统(荷兰Noldus公司);奥林巴斯BX50显微镜(日本奥林巴斯公司);JEDA801D计算机辅助图像分析系统(捷达科技有限公司);凝胶扫描分析系统(美国Bio-Rad公司)。
1.4 方法 1.4.1 CUS模型的建立基于前期的研究,进行适当修改,建立抑郁动物模型[8]。对小鼠采用10种不同的应激刺激:4 ℃冰水游泳5 min,潮湿垫料24 h,鼠笼45°倾斜24 h,夹尾1 min,行为限制2 h,24 h昼夜颠倒,42 ℃热水游泳5 min,禁水24 h,禁食24 h,鼠笼摇晃15 min。对同一只小鼠不连续使用同样的刺激,每天刺激2次,连续35 d。对照组小鼠不进行任何处理。
1.4.2 糖水偏好实验实验前,对小鼠进行糖水适应性训练。随后禁水12 h(20:00-8:00),糖水偏好实验在每天上午8:00-9:00进行。给予小鼠事先称量好的两瓶水,一瓶质量浓度为10 g·L-1蔗糖水,一瓶为动物日常饮用水。1 h后,计算小鼠的糖水偏好:糖水偏好=糖水饮用量/总液体饮用量。
1.4.3 旷场实验旷场大小为80 cm×80 cm×40 cm,实验从早上9:00开始,将小鼠放置于旷场中心,使用动物行为自动跟踪系统进行记录,并分析小鼠在旷场内10 min的行为活动,主要观测的旷场行为学指标包括直立次数(垂直运动得分记录为两前爪腾空或攀附墙壁)、总行程、平均移动速度。每只小鼠均单独进行测试,两只小鼠实验之间,将旷场清理干净[8]。
1.4.4 氟西汀治疗实验前,将氟西汀溶解在生理盐水中。向小鼠腹腔注射氟西汀(10 mg·kg-1)[8]或等体积的生理盐水,连续使用21 d。
1.4.5 免疫印迹分析取出小鼠的海马组织,匀浆离心,采用BCA法测定蛋白质浓度。经SDS聚丙烯酰胺凝胶电泳,转移至PVDF膜。分别加入GRPR抗体(1:200)及内标GAPDH抗体(1:300),轻摇孵育过夜。洗膜后,加入辣根过氧化物酶标记的羊抗兔IgG(1:5 000), 室温轻摇1 h。充分洗膜后加ECL,胶片曝光显影。用凝胶扫描分析系统对胶片进行灰度分析。GRPR表达的相对含量变化用GRPR与GAPDH条带的灰度值的比值表示。
1.4.6 荧光定量PCR检测取出小鼠的海马组织,用TRIzol法提取总RNA后,以其为模板逆转录合成cDNA。采用荧光定量PCR检测GRPR mRNA的表达。GRPR的上游引物序列:5′-AGCTGACAGGTACAAAGCCATT-3′,下游引物序列:5′-AGGGTGTAGCTCATTGGAGTGT-3′;内参β-actin的上游引物序列:5′-CACGATGGAGGGGCCGGACTCATC-3′,下游引物序列:5′-TAAAGACCTCTATGCCAACACAGT-3′。反应体系:2×SYBR-Green Master Mix 10 μL,上、下游引物各1 μL,cDNA 1 μL,双蒸水7 μL。PCR反应条件为:50 ℃ 2 min 1个循环,95 ℃ 10 min,95 ℃ 30 s,60 ℃ 30 s,40个循环。每个样本均重复3个复孔,取平均值为最终结果,目的基因与内参基因同时进行反应。所得数据用2-ΔΔCt法计算。
1.5 统计学处理应用SPSS 21.0软件统计包对数据进行处理,结果采用x±s表示。组间差异的比较采用单因素ANOVA分析,均数间的两两比较采用Bonferroni检验。
2 结果 2.1 氟西汀对CUS小鼠行为学指标的影响 2.1.1 氟西汀治疗1周后对行为学指标的影响由Tab 1可见,氟西汀组小鼠糖水偏好、旷场行为学指标(总行程、平均移动速度和直立次数)与对照组比较明显减少(P < 0.01);其行为学指标与CUS组相比,差异无显著性(P>0.05)。说明经过1周的氟西汀干预,小鼠行为学指标无明显改善。
| Group | Sucrose preference | Open field tests | ||
| Total traveled distance/cm | Moved velocity/cm·s-1 | Frequencies of rearing | ||
| Control | 0.86±0.03 | 7 388.67±595.05 | 14.63±1.08 | 63.10±4.84 |
| CUS | 0.59±0.03** | 2 770.53±442.12** | 5.69±0.57** | 23.50±2.07** |
| FLX | 0.61±0.02** | 2 974.15±279.90** | 5.91±0.46** | 25.50±2.80** |
| **P < 0.01 vs control | ||||
由Tab 2可见,氟西汀组小鼠糖水偏好、旷场行为学指标(总行程、平均移动速度和直立次数)与对照组比较,仍明显减少(P < 0.01);其行为学指标与CUS组相比有明显改善(P < 0.01)。说明经过2周的氟西汀干预,小鼠行为学指标有一定的改善。
| Group | Sucrose preference | Open field tests | ||
| Total traveled distance/cm | Moved velocity/cm·s-1 | Frequencies of rearing | ||
| Control | 0.85±0.02 | 7 114.72±582.46 | 12.77±0.97 | 55.30±3.86 |
| CUS | 0.59±0.03** | 2 671.80±442.25** | 4.99±0.66** | 19.10±2.13** |
| FLX | 0.68±0.02**## | 4 584.21±362.96**## | 8.48±0.50**## | 38.80±4.26**## |
| **P < 0.01 vs control; ##P < 0.01 vs CUS | ||||
由Tab 3可见,氟西汀组小鼠糖水偏好、旷场行为学指标(总行程、平均移动速度和直立次数)与CUS组比较明显增加(P < 0.01);其行为学指标与对照组相比,差异无显著性(P>0.05)。说明经过3周的氟西汀干预,小鼠行为学指标已经恢复到正常水平。
| Group | Sucrose preference | Open field tests | ||
| Total traveled distance/cm | Moved velocity/cm·s-1 | Frequencies of rearing | ||
| Control | 0.82±0.02 | 7 166.33±582.16 | 12.88±0.86 | 64.20±4.94 |
| CUS | 0.60±0.03** | 3 025.71±268.89** | 5.98±0.40** | 27.20±2.62** |
| FLX | 0.80±0.04## | 6 918.35±505.14## | 12.51±0.90## | 59.80±3.85## |
| **P < 0.01 vs control; ##P < 0.01 vs CUS | ||||
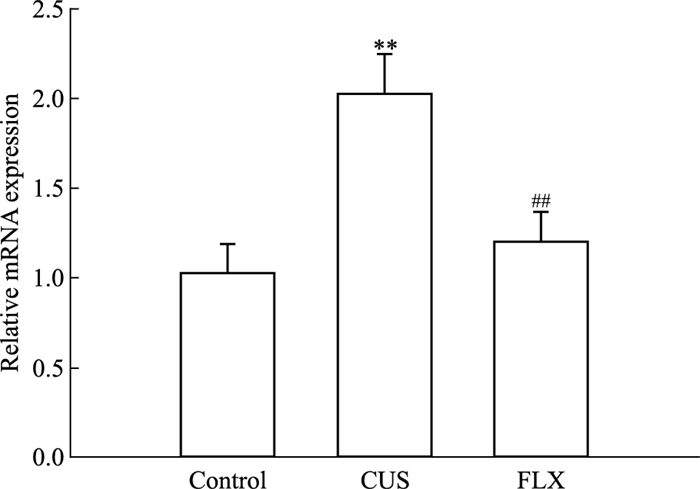
Fig 1的荧光定量PCR及Fig 2的免疫印迹结果显示,CUS组小鼠海马GRPR mRNA及蛋白的表达明显增加(P < 0.01),氟西汀明显降低GRPR mRNA和蛋白的表达(P < 0.01)。
|
| Fig 1 GRPR mRNA expression in C57BL/6mouse hippocamus as revealed by qPCR(x±s, n=10) **P < 0.01 vs control; ##P < 0.01 vs CUS |

|
| Fig 2 GRPR expression in C57BL/6 mousehippocamus as revealed by Western blot(x±s, n=10) **P < 0.01 vs control; ##P < 0.01 vs CUS |
抑郁症是目前临床上最常见的,慢性反复发作的重性精神疾病,其人群发病率有逐渐增高的趋势。目前,人们已经逐渐认识到,单胺类神经递质失调学说单独不足以解释抑郁症的发病及抗抑郁药的作用机制[9]。因此,探索抑郁症新的发病机制和可靠的药物作用靶点,成为当前抑郁症研究的重点和热点。越来越多的研究表明,GRP/GRPR通路可能在抑郁症的发病和治疗中起着重要作用[4]。
GRPR属于一类G蛋白偶联受体,其位于细胞膜上,整个分子由7个疏水跨膜区构成,GRPR由384个氨基酸构成[10]。当GRP结合GRPR后,激活G蛋白,随后启动整个细胞内的信号转导机制,包括一系列的蛋白激酶信号级联反应,如促分裂原活化蛋白激酶(mitogen-activated protein kinase, MAPK)/胞外信号调节蛋白激酶(extracellular signal-regulated kinase, ERK)和蛋白激酶C(protein kinase C, PKC)等信号通路[10]。来自临床神经精神疾病的病人和实验动物的研究显示,GRP和GRPR的表达水平在疾病状况下发生改变。Gerner等[11]报道,精神分裂症患者的脑脊液中GRP表达水平明显降低。GRP和GRPR的解剖学分布,与其在情感和应激相关障碍中的作用一致。Merali等[12]研究表明,自杀死亡的抑郁症患者脑内表现出GRP的紊乱。另外,实验动物研究显示,应激后,实验大鼠表现出持续GRP和GRPR升高等神经内分泌和行为学改变[3]。而通过脑室注射或者脑内注射系统给予GRPR激动剂后,可以产生类似于应激样的内分泌和行为学改变,其中最常见的是“理毛行为”,又称“修饰行为”,是鼠类应激状态时常见的表现[13]。
在本研究中,通过连续3周的氟西汀干预发现,CUS应激小鼠虽然在干预的第1周行为学改变不明显,但是从第2周末开始,其行为学开始有明显的好转,特别是在第3周末,CUS应激小鼠的行为学已经完全恢复,与正常组没有差异。更重要的是,这些行为上的改变同时伴有海马GRPR表达的变化。在本实验中,应激小鼠海马的GRPR mRNA及蛋白表达明显上升,经过氟西汀治疗3周后,GRPR mRNA和蛋白的表达恢复到与正常对照组无明显差异。我们前期的研究显示,经过CUS联合孤养的应激刺激后,C57BL/6小鼠下丘脑GRPR mRNA和蛋白表达明显增高,而经氟西汀干预后,GRPR的表达可以恢复到正常水平。小鼠下丘脑GRPR表达的这种动态变化与其行为学变化是一致的[14]。本研究结果与我们前期的研究具有一致性。结合以上研究,本研究结果进一步提供了GRPR在氟西汀抗抑郁治疗靶标中的潜在价值。然而,关于GRPR在氟西汀抗抑郁中的精确机制还需要进一步研究,特别是其中涉及到的第二信使系统还不明确。研究表明,氟西汀抗抑郁活动主要与G蛋白启动的cAMP蛋白激酶信号系统有关[15],而GRPR的信号转导过程也涉及到G蛋白有关的蛋白激酶系统,这两者之间细胞内分子的交集可能为解释GRPR参与氟西汀的抗抑郁活动精确机制,甚至为阐明临床抗抑郁活动的延迟效应产生的机制提供了方向。
| [1] | Qu X, Wang H, Liu R. Recent insights into biological functions of mammalian bombesin-like peptides and their receptors[J]. Curr Opin Endocrinol Diabetes Obes, 2018, 25(1): 36-41. |
| [2] | Kent P, Awadia A, Zhao L, et al. Effects of intranasal and peripheral oxytocin or gastrin-releasing peptide administration on social interaction and corticosterone levels in rats[J]. Psychoneuroendocrinology, 2016, 64: 123-30. doi:10.1016/j.psyneuen.2015.11.019 |
| [3] | Merali Z, Kent P, Anisman H. Role of bombesin-related peptides in the mediation or integration of the stress reponse[J]. Cell Mol Life Sci, 2002, 59(2): 272-87. doi:10.1007/s00018-002-8422-x |
| [4] | Roesler R, Henriques J A, Schwartsmann G. Gastrin-releasing peptide receptor as a molecular target for psychiatric and neurological disorders[J]. CNS Neurol Disord Drug Targets, 2006, 5(2): 197-204. doi:10.2174/187152706776359673 |
| [5] | Barbon A, Caracciolo L, Orlandi C, et al. Chronic antidepressant treatments induce a time-dependent up-regulation of AMPA receptor subunit protein levels[J]. Neurochem Int, 2011, 59(6): 896-905. doi:10.1016/j.neuint.2011.07.013 |
| [6] | 陈建新, 刘忠纯, 王高华, 等. 谷氨酸转运体EAAT2在抑郁症发病及治疗中的作用[J]. 中国药理学通报, 2016, 32(7): 894-7. Chen J X, Liu Z C, Wang G H, et al. Roles of glutamate transporter EAAT2 in occurrence and treatment of depression[J]. Chin Pharmacol Bull, 2016, 32(7): 894-7. doi:10.3969/j.issn.1001-1978.2016.07.002 |
| [7] | Hashimoto M, Hossain S, Katakura M, et al. Docosahexaenoic acid helps to lessen extinction memory in rats[J]. Molecules, 2018, 23(2): 451. doi:10.3390/molecules23020451 |
| [8] | 陈建新, 姚丽华, 刘忠纯, 等. 氟西汀对慢性应激大鼠前额叶谷氨酸转运体GLT-1表达的影响[J]. 中国药理学通报, 2015, 31(2): 256-60. Chen J X, Yao L H, Liu Z C, et al. Effects of fluoxetine on changes of GLT-1 in rat prefrontalcortex after chronic unpredictable stress[J]. Chin Pharmacol Bull, 2015, 31(2): 256-60. doi:10.3969/j.issn.1001-1978.2015.02.022 |
| [9] | 张笑笑, 林天炜, 张君利, 等. 淫羊霍对产前应激子代大鼠抗抑郁作用研究[J]. 中国药理学通报, 2017, 33(7): 987-91. Zhang X X, Lin T W, Zhang J L, et al. Antidepressant effects of icariin in prenatally stressed offsprings[J]. Chin Pharmacol Bull, 2017, 33(7): 987-91. doi:10.3969/j.issn.1001-1978.2017.07.020 |
| [10] | Roesler R, Kent P, Luft T, et al. Gastrin-releasing peptide receptor signaling in the integration of stress and memory[J]. Neurobiol Learn Mem, 2014, 112: 44-52. doi:10.1016/j.nlm.2013.08.013 |
| [11] | Gerner R H, van Kammen D P, Ninan P T. Cerebrospinal fluid cholecystokinin, bombesin and somatostatin in schizophrenia and normals[J]. Prog Neuropsychopharmacol Biol Psychiatry, 1985, 9(1): 73-82. doi:10.1016/0278-5846(85)90181-2 |
| [12] | Merali Z, McIntosh J, Anisman H. Role of bombesin-related peptides in the control of food intake[J]. Neuropeptides, 1999, 33(5): 376-86. doi:10.1054/npep.1999.0054 |
| [13] | Gmerek D E, Cowan A. Studies on bombesin-induced grooming in rats[J]. Peptides, 1983, 4(6): 907-13. doi:10.1016/0196-9781(83)90089-X |
| [14] | Yao L H, Chen J X, Liu Z C, et al. Hypothalamic gastrin-releasing peptide receptor mediates an antidepressant-like effect in a mouse model of stress[J]. Am J Transl Res, 2016, 8(7): 3097-105. |
| [15] | Thome J, Sakai N, Shin K, et al. cAMP response element-mediated gene transcription is upregulated by chronic antidepressant treatment[J]. J Neurosci, 2000, 20(11): 4030-6. doi:10.1523/JNEUROSCI.20-11-04030.2000 |

