

2. 安徽医科大学药学院,安徽 合肥 230032
2. College of Pharmacy, Anhui Medical University, Hefei 230032, China
据了解,很大比例的新药都是因为心血管毒性而在临床前阶段就被迫终止研发,提高药物早期心脏毒性筛选的预测能力,可降低研发成本,提高研发成功率。随着干细胞研究的不断深入,干细胞诱导分化的心肌细胞成为心脏毒性体外评价研究的新热点。胚胎干细胞(embryonic stem cell, ESC)以其具有体外无限增殖能力和发育全能性,以及对药物作用反应迅速、敏感性高、干扰因素少等优点,已被用于药物毒性评价研究中,且备受关注。但目前对ESC经外界扰动后,其细胞内部的小分子代谢物(如糖、氨基酸、脂肪等)的动态变化研究较少。代谢组学利用核磁共振或者质谱联用技术,以及化学统计学方法,对生物体系中内源性小分子代谢物进行检测和解析。将ESC技术和代谢组学技术联合、优势互补,整合用于毒性筛选、靶器官毒性等毒理学和安全性评价研究中,将大有裨益。建立干细胞代谢组学技术分析平台,用于药物研发的早期评价,是未来药物研究发展的趋势。本研究旨在前人的研究基础上,以经典的心脏毒性药物多柔比星(doxorubicin,DOX)为工具药,弱胚胎、心脏毒性药物二甲双胍(metformin,Met)为参比药,将干细胞和代谢组学技术结合,重演心脏发育过程中,心脏毒性药物攻击的可能代谢途径,筛选出可能的代谢标志物,进一步探索架构干细胞代谢组学技术分析平台。
1 材料 1.1 细胞株小鼠胚胎干细胞(mouse embryonic stem cell,mESC)D3细胞,购自中国科学院典型培养物保藏委员会细胞库。
1.2 实验动物7~8周龄C57BL/6♀鼠和C3H/HeN♂鼠,购自北京维通利华实验动物技术有限公司,许可证号:SCXK(京)2012-0001。
1.3 药物与试剂DOX、Met、维生素C(vitamin C,VC)、丝裂霉素C、β-巯基乙醇,均购自Solarbio;Knock out DMEM、ES-FBS、双抗、非必需氨基酸(non-essential amino acid,NEAA)、L-谷氨酰胺、胰酶,均购自Gibco公司;PE标记的抗小鼠心肌肌钙蛋白T(cardiac troponin T,cTnT)抗体,购自BD公司;白血病抑制因子(leukemia inhibitory factor,LIF),购自Millipore公司。
1.4 仪器Waters ACQUITY UPLC/Q-TOF-MS Premier超高效液相色谱/四级杆-飞行时间串联质谱仪,Masslynx工作站和MarkerLynx数据预处理软件,UPLC BEH C18色谱柱(2.1 mm×100 mm,1.7 μm),美国Waters公司;MCO-19AIC型CO2培养箱,日本SANYO公司;TS100-F型倒置荧光显微镜,日本Nikon公司;MS2漩涡混匀器,广州仪科实验室技术有限公司;VELOCITY 14R台式冷冻离心机,澳大利亚Dynamica公司。
2 方法 2.1 实验分组将mESC分为对照组、DOX(3.40、0.17 μmol·L-1)处理组和Met(905.7 μmol·L-1)处理组。药物浓度依前期实验结果设计[1]。
2.2 饲养层细胞的制备及培养将♀、♂鼠合笼交配,当♀鼠怀孕12~15 d时,脱颈处死孕鼠,无菌条件下取出胎鼠,留躯干部分剪碎,加入0.05%胰酶-EDTA消化制备单细胞悬液,并培养于含10% FBS的DMEM培养液中,记为P0代,置于37 ℃、5% CO2培养箱中培养。每2 d换液,4~5 d用0.25%胰酶处理传代。临用前,加入丝裂霉素C(终浓度为10 mg·L-1)孵育2.5~3 h,灭活细胞制备饲养层,饲养层细胞使用P2~P4代。
2.3 mESC的培养培养mESC于饲养层上,使用Knock out DMEM培养液,含15% ES-FBS、1%双抗、1%谷氨酰胺、1% NEAA、0.125 mmol·L-1 β-巯基乙醇、1 000 kU·L-1 LIF。置于37 ℃、5% CO2培养箱培养,每2 d换液,4~5 d传代。
2.4 mESC的心肌定向分化将mESC细胞悬液转移至空白培养瓶中预贴壁1 h,利用贴壁速度的差异,消除大部分已分化的mESC和饲养层细胞的干扰,收集悬浮细胞,加入基础分化培养液(不含LIF,其余成分与mESC培养液相同),调整细胞密度至108·L-1,以每滴20 μL,逐滴滴在培养皿盖上,培养皿中加入3 mL PBS,将铺满液滴的皿盖盖上培养皿进行培养,记为分化第0天(d 0)。悬滴培养2 d(d 2)后,可见悬滴内细胞团形成,即拟胚体(embryoid body,EB),将EBs逐个转移至24孔板中,1个/孔,培养2 d(d 4)贴壁后,换成诱导分化培养液(含VC 0.1 g·L-1,其余成分与基础分化培养液相同)。
2.5 加药及一般观察EBs诱导分化2 d(d 6)后,换用含药诱导分化培养液作用,每组24个EBs,每2 d换液,并随时观察EBs的生长情况,记录拟胚体自主节律搏动首次出现的时间、搏动频率等,当对照组超过80%的EBs搏动后,结束培养,行后续实验。
2.6 心肌细胞鉴定采用免疫细胞化学方法测定EBs中cTnT表达,方法简述如下:弃去培养上清,2%多聚甲醛固定20 min,弃液洗涤后,0.1%皂素室温破膜10 min,PBS洗涤,5%牛血清白蛋白封闭20 min,PE-cTnT(40倍稀释)2~8 ℃孵育过夜,PBS洗涤,无水乙醇脱水5 min。
2.7 代谢组学检测将EBs消化至悬浮,离心收集细胞团块,PBS洗涤后,加入200 μL预冷至-80 ℃的甲醇,-80℃保存,共独立收集样本4次。检测时,样本涡旋3 min,4 ℃、13 000 r·min-1离心10 min,取上清5 μL进样。色谱条件:流动相A:乙腈;流动相B为0.1%甲酸水。柱温30 ℃,流速400 μL·min-1,采用梯度洗脱方式:0~10 min,A相2%~90%;10~12 min,A相90%;12~14 min,A相90%~2%;14~16 min,A相2%。质谱条件:电喷雾电离源,正负离子电离模式。离子源温度120 ℃,脱溶剂温度350 ℃,脱溶剂氮气流600 L·h-1,锥孔反吹氮气50 L·h-1。正、负离子模式毛细管电离电压分别为3.0 kV和2.5 kV,取样锥孔电压为27 eV,萃取锥孔4 eV,四极杆扫描范围m/z:50~1 500。
2.8 数据处理检测cTnT时,荧光显微镜拍照,每组随机选取5个拟胚体以ImageJ软件计算cTnT阳性表达面积(Area)、累积光密度(integrated optical density,IOD)、平均光密度(mean optical density,MOD),经LSD-t检验。代谢组学结果取4次的平均值,差异代谢组分入选标准:s < x/2,药物干预组与对照组的差异倍数(fold change,FC)>2.0,VIP>1.0,且经LSD-t检验P < 0.05。之后依据筛选所得结果,返检数据,以点带面,分析数据所涉及的通路及代谢途径。
3 结果 3.1 一般观察结果mESC在饲养层上呈集落、“克隆岛”状贴壁生长,“岛内”细胞紧密排列,界限不清。分化阶段,mESC由于重力作用形成EBs,呈球形或近球形,中央细胞比较致密,多层,透光率低,体积逐渐增大成熟,膨胀为囊状胚体,胚体中央可有囊腔,腔内存在液体,d 8~10近中央区域心肌细胞可出现自发性搏动。对照组于d 8~10发现首个自发搏动EB,至d 12~14自发搏动EBs逐渐增多至超过80%,1个搏动中心者居多,搏动缓慢而有力,频率约为每分钟40~80次,搏动区域较小。与对照组比较,DOX高浓度对EBs的生长产生了明显抑制,EBs基本不发育,贴壁不牢,甚至逆生长,仅见零星散在细胞;DOX低浓度对EBs的生长未产生明显影响(镜下观察,并MTT法测定,结果未列出),首次搏动出现的时间与对照组相同,但至d 12~14搏动EBs的比例明显高于对照组,搏动中心以2个者居多,搏动迅速,搏动区域也大,频率明显高于对照组,约为每分钟90~150次;Met对EBs的生长分化未产生明显影响,各项指标与对照组比较差异均无统计学意义。见Tab 1、Fig 1。
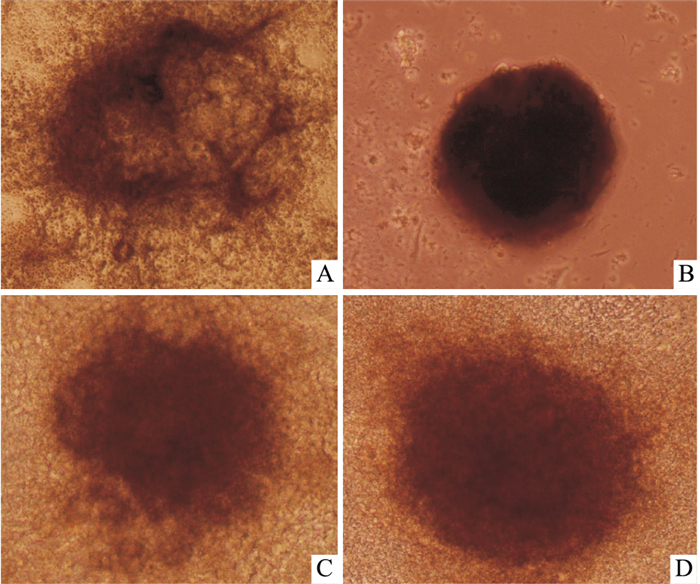
|
| Fig 1 EBs morphological observation(scale bar=200 μm) The results of EBs morphological observation, when the EBs were treated with DOX and Met for 4 d (differentiated culture for 10 d, d 10). A: Control EBs; B: EBs treated with DOX 3.40 μmol·L-1; C: EBs treated with DOX 0.17 μmol·L-1; D: EBs treated with Met 905.7 μmol·L-1. |
| Group | Time of first pulsation/d | Beating rate/min-1 | Percentage of beating EBs/% |
| Control | 7±1 | 64±17 | 84.9±4.3 |
| DOX 3.40 μmol·L-1 | 0 | 0 | 0.0 |
| DOX 0.17 μmol·L-1 | 7±1 | 124±21** | 98.5±2.6** |
| Met 905.7 μmol·L-1 | 7±1 | 60±8 | 75.7±9.8 |
| The results of first pulsation time, beating rate, and percentage of beating EBs, when the EBs were treated with DOX and Met for 6 d (differentiated culture for 12 d, d 12). **P < 0.01 vs control. | |||
除形态学变化外,进一步分析特异性心肌cTnT的表达,发现各组EBs均有cTnT的阳性表达,且主要集中于囊状胚体区,周边细胞少见cTnT表达,且该阳性区域与一般观察中搏动区域相对应。与对照组比较,各加药组IOD无明显变化,DOX高浓度组Area明显降低、MOD明显升高,DOX低浓度组和Met组Area、MOD无明显变化。见Fig 2、3。

|
| Fig 2 cTnT expression of EBs affected by DOX and Met(x±s, n=5) Differences of area, IOD, MOD of cTnT expression tested by immunocytochemical method, when the EBs were treated with DOX and Met for 6 d (differentiated culture for 12 d, d 12). **P < 0.01 vs control. |
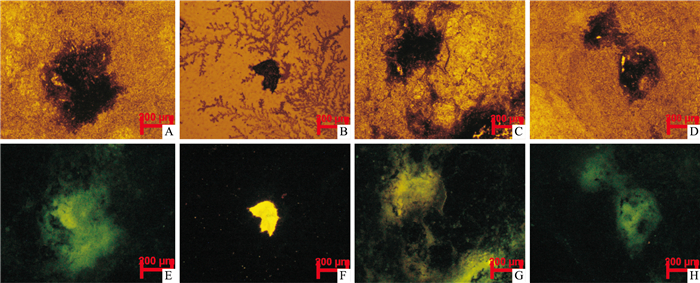
|
| Fig 3 cTnT expression of EBs affected by DOX and Met(scale bar=200 μm) A, E: Control EBs; B, F: EBs treated with DOX 3.40 μmol·L-1; C, G: EBs treated with DOX 0.17 μmol·L-1; D, H: EBs treated with Met 905.7 μmol·L-1. The upper diagrams were the observation results via ordinary optical microscope, and the lower diagrams were that via fluorescence microscopy. |
从OPLS-DA模型散点图(Fig 4)中可以看出,DOX 0.17 μmol·L-1和Met 905.7 μmol·L-1处理组与对照组可以明显分开,且DOX与Met处理组也可以明显分开,说明药物处理组EBs的生理及物质代谢状况存在明显差异,且不同药物的处理对EBs的代谢影响也不尽相同。综合PLS-DA图、VIP值以及t检验结果等因素,得到了多种差异生物标志物,且发现DOX和Met对某些代谢物的影响一致,提示这些内源性代谢物可能与心脏发育损伤密切相关,且更为敏感,为诱导EBs分化时心脏毒性的生物标志物,得到的部分结果见Tab 2。通过标准质谱数据库检索对Tab 2所涉标志物进行了指认,潜在标志物名称、变化趋势和代谢通路见Tab 3。
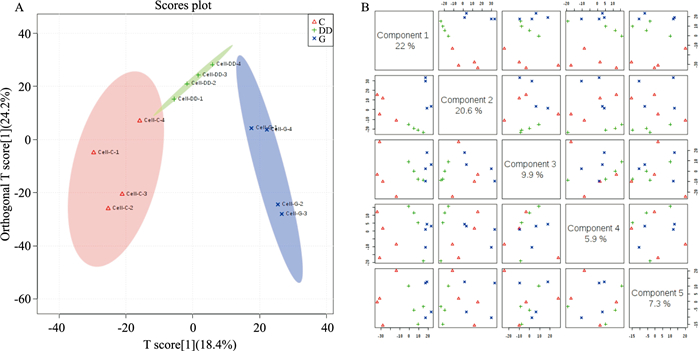
|
| Fig 4 The OPLS-DA(A) and PLS-DA(B) profiles of metabolites in cells(n=4) C: Control EBs; DD: EBs treated with DOX 0.17 μmol·L-1; G: EBs treated with Met 905.7 μmol·L-1. The development of EBs in DOX 3.40 μmol·L-1 treatment group was significantly inhibited, and the sufficient cell samples could not be obtained. |
| No. | m/z | T/min | VIP | FC | |
| DOX 0.17 | Met 905.7 | ||||
| 1 | 628.5 | 15.7 | 1.53 | +4.04 | +3.23 |
| 2 | 742.6 | 10.5 | 2.28 | +7.51 | +12.79 |
| 3 | 793.6 | 13.5 | 1.99 | +3.06 | +5.02 |
| 4 | 122.1 | 16.8 | 1.67 | -1.54 | -3.59 |
| 5 | 136.1 | 14.6 | 2.11 | -2.60 | -8.99 |
| 6 | 171.1 | 15.8 | 2.05 | -3.34 | -7.83 |
| 7 | 246.2 | 4.3 | 1.50 | -16.46 | -4.05 |
| 8 | 281.1 | 13.3 | 1.89 | -5.12 | -4.59 |
| 9 | 307.1 | 0.9 | <1 | -38.70 | -1.17 |
| 10 | 329.3 | 13.6 | 1.79 | -11.78 | -7.07 |
| 11 | 370.3 | 13.3 | 1.80 | -3.51 | -3.82 |
| 12 | 393.3 | 15.5 | 1.98 | -3.74 | -3.88 |
| 13 | 441.3 | 15.0 | 1.60 | -2.34 | -2.43 |
| 14 | 445.1 | 14.0 | 1.74 | -2.66 | -2.40 |
| 15 | 505.9 | 14.3 | 1.84 | -6.52 | -10.78 |
| 16 | 527.4 | 14.1 | 1.89 | -4.34 | -6.74 |
| 17 | 569.4 | 15.2 | 1.66 | -2.22 | -2.28 |
| 18 | 724.5 | 16.5 | 2.12 | -3.45 | -9.70 |
| 19 | 733.6 | 14.1 | 1.93 | -3.16 | -3.70 |
| 20 | 789.6 | 13.3 | 1.80 | +#DIV | +#DIV |
| +represented upregulation, - represented down-regulation, #DIV represented that the values of the control groups were lower than the detection limit. No. 4, 9, 13, 14 were the data added after the review. | |||||
| Formula weight | Potential biomarker | Trend | Pathway/function |
| 121.158 | Cysteine | ↓ | Cysteine metabolism |
| 136.073 | L-Homocysteine | ↓ | Cysteine and methionine metabolism |
| 246.241 | β-Alanyl-L-arginine | ↓ | β-Alanine and arginine metabolism |
| 307.323 | Glutathione | ↓ | Energy metabolism, antioxygenation |
| 330.583 | 3', 5'-Cyclic AMP | ↓ | Purine metabolism |
| 441.403 | Folic acid | ↓ | folatemetabolism |
| 445.435 | Tetrahydrofolic acid | ↓ | folatemetabolism |
| 733.228 | FeTMPyP | ↓ | Energy metabolism, antioxygenation |
| 789.260 | 5, 10-Methylene tetrahydromethanopterin | ↑ | Methane and folatemetabolism |
DOX作为常见的抗肿瘤药对心肌有严重的损伤作用,这一特点在本研究中得到进一步的证实。既往研究显示,DOX可造成心律失常,且多发生在DOX心脏毒性早期,主要表现为心电图异常、期前收缩和心动过速[2-3],甚至出现心力衰竭[4]。DOX高浓度下可能促进cTnT表达,与研究结果一致[5],此时也未见“心脏跳动”,众所周知,临床上cTnT的高表达与心肌梗死导致细胞坏死呈密切正相关,提示大部分细胞可能已死亡,当然不会有搏动出现。而低浓度对该蛋白表达的影响不明显,但“心率”明显增快,可能与心肌细胞的缺氧状况有关,是EBs为生存下去表现出来的病理生理现象,提示EBs仍具有一定的代偿能力,后续将详细讨论。综上,cTnT表达变化对心肌细胞损伤的表征缺乏敏感性,可能并不是最敏感的心脏毒性标志物。
Met在一般观察、cTnT阳性表达方面均未发现明显异常,与DOX明显不同,提示Met可能是弱心脏毒性药物。而代谢组学技术具有高灵敏性,利用该技术仍检测到了其对心脏分化发育的影响,多种代谢组分的胞内水平发生了明显变化,与DOX存异亦存同,现有研究结果体现的问题主要集中在氧化呼吸代谢方面,以DOX为例分析讨论。
心肌细胞因能量需求而富含线粒体,而DOX恰恰在细胞核和线粒体内有特异蓄积[6-7]。本研究发现,DOX可使铁卟啉(FeTMPyP)水平明显降低,FeTMPyP是过氧化物酶的催化活性中心,具有强力清除羟自由基和超氧阴离子的能力[8]。DOX一方面经酶类作用生成氧自由基,而心脏中含有抗氧化酶本身就较少,致使过氧化物酶类耗竭,活性氧堆积,引起线粒体和微粒体的脂质过氧化,引发能量代谢障碍;另一方面,DOX与Fe3+形成复合物,造成FeTMPyP的“原材料”减少,使FeTMPyP生成不足,加重氧化应激反应,且DOX-Fe3+本身也是强氧化剂,DOX-Fe3+和DOX-Fe2+的反复转化,形成大量自由基,导致细胞器膜功能损伤,心肌细胞功能进一步丧失[9]。
本研究还发现,同型半胱氨酸(L-homocysteine,Hcy)的胞内水平明显下降,与临床血中Hcy升高是心血管疾病的危险因素明显相悖。查阅KEGG代谢数据库可知,Hcy可经胱硫醚转化为半胱氨酸,而半胱氨酸是合成谷胱甘肽的重要原料之一,由此返查实验结果发现,半胱氨酸及谷胱甘肽水平均有不同程度的降低,提示抗氧化酶体系(包含谷胱甘肽)的高消耗[10],引起“原材料”的短缺,可能是造成Hcy水平降低的主要原因。另外,心肌细胞受到DOX攻击后,一氧化氮合酶高表达[11],NO过度释放,又可进一步加重氧化应激反应,从而抑制心肌细胞呼吸链,损害线粒体能量代谢,使心脏受损,精氨酸作为NO的前体,在该过程中大量消耗,这可能导致与之相关的代谢过程全部向生成精氨酸的方向进行,从而致使β-丙氨酰-L-精氨酸(β-alanyl-L-arginine)水平下降。
同时本研究还发现,5, 10-亚甲基四氢甲烷蝶呤(5, 10-methylene tetrahydromethanopterin,MTHMPT)水平升高,且环磷酸腺苷(cAMP)水平下降。MTHMPT是一碳单位代谢途径的中间产物之一,一碳单位是合成核苷酸和氨基酸转化的重要材料,在体内主要以四氢叶酸为载体,返检数据恰好发现叶酸和四氢叶酸(tetrahydrofolic acid,THF)均有不同程度的下调,提示MTHMPT的上调与心脏发育异常密切相关。有研究显示[12-13],叶酸具有抗凋亡活性,对心脏具有一定的保护作用。在这一过程中叶酸被大量消耗,使代谢过程全部“流向”叶酸生成过程,本为辅助的叶酸生成途径激活,从而造成中间产物MTHMPT水平升高蓄积。cAMP是调节细胞的生理活动与物质代谢关键分子,作为第二信使参与多种信号通路,cAMP的生理功能研究已比较透彻,简言之,cAMP水平的降低,直接或间接地影响到了心肌细胞的能量代谢,导致能量缺乏、线粒体肿胀溶蚀以及相关功能的不可逆损害[14]。
在分子水平,DOX和Met对氨基酸、维生素、能量代谢均产生了不同程度的不利影响,而DOX作为典型的心脏毒性药物亦在细胞水平、组织水平都表现出毒性作用。目前认为, Met是弱心脏毒性药物,虽在宏观水平未见明显的毒性作用,但已证实[15],Met可抑制线粒体呼吸链酶复合体I,会引起线粒体有氧呼吸功能减弱、ATP生成减少,使细胞从合成代谢状态转换为分解代谢状态,这一药理作用在心脏发育阶段是不利因素,与本研究结果相一致,表明物质代谢变化要先于蛋白、细胞、组织水平的异常,敏感性更强。另外,本研究支持DOX诱发心脏毒性的氧化损伤自由基学说[23],并提供了进一步的证据。
干细胞代谢组学技术分析平台对药物反应迅速、敏感性高,在本研究中得到印证。本实验室初步建立了早期、快速、灵敏及特异性强的分析平台,可用于药物的心脏毒性评价筛选。Hcy、FeTMPyP、Cysteine等具有成为心脏毒性敏感标志物的潜力,后续研究中将综合多个方面研究结果,全面考察,完善该评价体系。
( 致谢: 本实验于天津药物研究院新药评价有限公司实验室完成,在此对本实验做出贡献的所有人员给予诚挚的感谢。)
| [1] | 李黎, 申秀萍, 钱鑫, 等. 体外心肌毒性代谢组学研究中模型药物多柔比星浓度及受试时间筛选[J]. 药物评价研究, 2016, 39(3): 398-402. Li L, Shen X P, Qian X, et al. Selection of test concentrations and test times of model drugs for metabonomic studies of in vitro cardiotoxicity[J]. Drug Eval Res, 2016, 39(3): 398-402. |
| [2] | 顾觉奋. 多柔比星毒副作用机制及其防治研究进展[J]. 国外医药抗生素分册, 2017, 38(4): 145-51. Gu J F. Current views on the mechanism of doxorubicin-induced cardiotoxicity and its prevention[J]. World Notes Antibiot, 2017, 38(4): 145-51. doi:10.3969/j.issn.1001-8751.2017.04.001 |
| [3] | 徐鸿洁, 魏大军. 蒽环类化疗药物心脏毒性及其治疗研究进展[J]. 中国城乡企业卫生, 2015(4): 37-9. Xu H J, Wei D J. Progress on anthracycline cardiotoxicity and treatment[J]. Chin J Urban Rural Ind Hyg, 2015(4): 37-9. |
| [4] | 吴运香, 张野, 谢春林, 等. SD大鼠阿霉素慢性心力衰竭模型的建立与评价[J]. 中国药理学通报, 2011, 27(8): 1170-3. Wu Y X, Zhang Y, Xie C L, et al. Establishment and evaluation of adriamycin-induced chronic heart failure model in SD rats[J]. Chin Pharmacol Bull, 2011, 27(8): 1170-3. doi:10.3969/j.issn.1001-1978.2011.08.032 |
| [5] | 孙凤姣, 张译丹, 张密霞, 等. β-AR/PKA/CaMK Ⅱ信号通路在阿霉素诱导大鼠心肌细胞凋亡中的作用[J]. 中国药理学通报, 2017, 33(3): 360-5. Sun F J, Zhang Y D, Zhang M X, et al. Roles of β-AR/PKA/CaMK Ⅱ signaling pathway in cardiomyocyte apoptosis induced by adriamycin in rats[J]. Chin Pharmacol Bull, 2017, 33(3): 360-5. doi:10.3969/j.issn.1001-1978.2017.03.014 |
| [6] | Anderson A B, Arriaga E A. Subcellular metabolite profiles of the parent CCRF-CEM and the derived CEM/C2 cell lines after treatment with doxorubicin[J]. J Chromatogr B Analyt Technol Biomed Life Sci, 2004, 808(2): 295-302. doi:10.1016/j.jchromb.2004.05.017 |
| [7] | 从文娟, 刘清飞, 梁琼麟, 等. 基于血清代谢组学的吡柔比星注射剂的累积毒性作用研究[J]. 中国药理学通报, 2012, 28(9): 1294-9. Cong W J, Liu Q F, Liang Q L, et al. Serum metabolites of commerical pirarubicin injections[J]. Chin Pharmacol Bull, 2012, 28(9): 1294-9. doi:10.3969/j.issn.1001-1978.2012.09.025 |
| [8] | Kang J L, Lee H S, Pack I S, et al. Iron tetrakis(n-methyl-4′-pyridyl) porphyrinato (FeTMPyP) is a potent scavenging antioxidant and an inhibitor of stimulant-induced NF-kappaB activation of RAW 264.7 macrophages[J]. J Toxicol Environ Health A, 2001, 64(4): 291-310. doi:10.1080/152873901316981295 |
| [9] | Nawara K, Beeckman H, Krysiński P, Blanchard G J. Structure-dependent complexation of Fe3+ by anthracyclines. 2. The roles of methoxy and daunosamine functionalities[J]. J Phys Chem B, 2013, 117(23): 6868-73. doi:10.1021/jp4023508 |
| [10] | 彭琳, 唐小海, 严伟, 等. 果胶阿霉素对大鼠心脏毒性的研究[J]. 中国药理学通报, 2016, 32(8): 1075-80. Peng L, Tang X H, Yan W, et al. Study of pectin-adriamycin conjugate to cardiac toxicity in rats[J]. Chin Pharmacol Bull, 2016, 32(8): 1075-80. doi:10.3969/j.issn.1001-1978.2016.08.009 |
| [11] | 阳冠明, 孙胜涛, 李树全, 等. β-胡萝卜素对阿霉素致大鼠心肌组织的超氧化物歧化酶、谷胱甘肽过氧化物酶mRNA表达改变的影响[J]. 中国药理学通报, 2006, 22(4): 465-70. Yang G M, Sun S T, Li S Q, et al. Effect of beta-carotene on adriamycin induced changes of expression of mRNA of superoxide dismutase and glutathione peroxidase in myocardial tissue of rats[J]. Chin Pharmacol Bull, 2006, 22(4): 465-70. doi:10.3321/j.issn:1001-1978.2006.04.019 |
| [12] | 张辰, 骆海燕, 高小博, 等. 叶酸对阿霉素诱导心脏毒性的拮抗作用研究[J]. 中国计划生育学杂志, 2017, 25(3): 159-63. Zhang C, Luo H Y, Gao X B, et al. The study of folic acid against doxorubicin-induced cardiotoxicity[J]. Chin J Fam Plann, 2017, 25(3): 159-63. |
| [13] | Sahu B D, Kumar J M, Kuncha M, et al. Baicalein alleviates doxorubicin-induced cardiotoxicity via suppression of myocardial oxidative stress and apoptosis in mice[J]. Life Sci, 2016, 144: 8-18. doi:10.1016/j.lfs.2015.11.018 |
| [14] | Zhou S, Starkov A, Froberg M K, et al. Cumulative and irreversible cardiac mitochondrial dysfunction induced by doxorubicin[J]. Cancer Res, 2001, 61(2): 771-7. |
| [15] | 薛朝军, 刘克辛. 二甲双胍抗肿瘤机制的研究进展[J]. 药学学报, 2015, 50(10): 1210-6. Xue C J, Liu K X. Advances of the anti-tumor research of metformin[J]. Acta Pharm Sin, 2015, 50(10): 1210-6. |

