


慢性肾脏病(chronic kidney disease,CKD)已成为世界公共卫生关注的重大问题,我国CKD的发病率已高达10.8%,患病人群数量接近1.2亿。肾间质纤维化(renal interstitial fibrosis,RIF)是各种病因导致的CKD进展至终末期肾病的共同病理机制[1]。RIF被认为是CKD发展的关键因素,造成正常肾单位的丢失,导致肾小球硬化和RIF,最终可能造成肾功能丧失等严重后果。自噬是细胞分解自身构成成分的一种生理现象,广泛存在于真核细胞的蛋白降解过程中,它可将损伤的或过剩的细胞构成成分分解成基本的活性成分,使之可再次得到利用[2]。自噬对肾纤维化的作用和机制引起科研人员极大的兴趣[3]。Kim等[4]研究发现,Akt/mTOR信号通路激活自噬,自噬在肾小管损伤和肾纤维化方面起到保护作用。大黄素(emodin,EM)是中药大黄蒽醌类物质,Ma等[5]研究发现,大黄中大黄蒽醌类活性成分EM可改善肾损伤功能。本文通过转化生长因子β1(transforming growth factor β1,TGF-β1)刺激人肾小管上皮细胞(HK-2)模型[6],研究EM对模型细胞形态改变,肾纤维化标志蛋白TGF-β1、Ⅰ型胶原蛋白(collagen Ⅰ,COLⅠ)、纤连蛋白(fibronectin,FN),自噬标志性蛋白LC3、Beclin-1表达的影响,探讨EM保护肾纤维化的机制。
1 材料与方法 1.1 细胞株HK-2细胞购自中科院上海细胞库,用含10%胎牛血清的DMEM/F12(1:1)培养基培养,其中加入100 kU·L-1的青霉素和链霉素双抗,在37 ℃、5% CO2培养箱中培养[10]。
1.2 药物与试剂EM(纯度大于98%),购自中国食品药品检定研究院,溶于含10%胎牛血清的DMEM/F12培养液。TGF-β1细胞因子(Cat:100-21,美国Peprotech公司);兔抗COL Ⅰ多克隆抗体(Proteintech公司);兔抗LC3单克隆抗体、兔抗Beclin-1多克隆抗体(美国CST公司);鼠抗β-actin单克隆抗体(美国Santa Cruz公司);CCK-8试剂盒(日本Dojindo Laboratories)。
1.3 仪器371型CO2培养箱(美国Thermo公司);IX71型倒置显微镜(日本Olympus公司);C2+激光扫描共聚焦(日本Nikon公司);Powerpac电泳仪、CFX96TM Real-Time PCR Detection System、ChemiDocTM XRS型化学发光成像系统(美国Bio-Rad公司)。
2 方法 2.1 细胞模型的建立按上述方法进行细胞培养,将细胞接种在6孔板中,细胞生长至60%~70%时,换成无血清的培养基24 h后,治疗组加入EM,30 min后,治疗组和模型组均加入10 μg·L-1的TGF-β1刺激24 h。实验分为以下3组:① Control(正常对照组);② TGF-β1(模型组);③ TGF-β1+EM(治疗组)。所有实验组同步一式4份培养,然后收集细胞用于免疫荧光、免疫印迹和qPCR分析。
2.2 EM浓度筛选按照CCK-8实验说明书操作,细胞按照5×103个/孔的密度接种在96孔板,在37 ℃、5% CO2培养箱中培养。每孔加入10 μL CCK-8溶液,孵育2 h后,在波长450 nm处测定EM(20、40、60、80、100 μmol·L-1)的光密度(OD)值[11]。每组有3个复孔,至少重复4次。
2.3 EM对HK-2细胞形态的影响用8 cm培养皿培养细胞,加入含10%胎牛血清的DMEM/F12培养液,过夜待细胞贴壁,按照模型制作流程操作,显微镜拍照。
2.4 细胞免疫荧光实验弃细胞培养液,用预冷的PBS轻洗3遍;置于冰上4%多聚甲醛固定15 min,TBST摇洗5 min×3次;0.3% Triton 100通透化处理15 min,TBST摇洗5 min×3次;山羊血清封闭30 min;4 ℃孵育一抗过夜;TBST摇洗5 min×3次;避光孵育荧光二抗1 h;0.1% DAPI染色6 min,TBST摇洗5 min×3次;用防淬灭封片剂封片;暗室激光扫描共聚焦拍照。
2.5 Western blot根据目的蛋白的分子质量,选择不同浓度的SDS凝胶电泳进行分离,转膜,5%脱脂奶粉(溶在TBST中)封闭1 h。一抗4 ℃孵育过夜,TBST洗膜,10 min×3次。室温孵育二抗1 h,TBST洗膜10 min×3次。显色,使用ImageJ软件进行图像分析,分析条带灰度值,根据目的蛋白/β-actin计算相对灰度比值,得到目的蛋白的相对表达量。
2.6 Real time PCR测定按TaKaRa试剂盒流程提取RNA检测。逆转录反应,取5×Primer Script Master Mix 2 μL,Total RNA 1 μL,RNase Free H2O 7 μL,总体积10 μL。按以下条件进行反应:37 ℃,15 min;85 ℃,5 s;4 ℃,1 h;得到cDNA液,储存在-20 ℃备用。PCR反应扩增程序,反应条件:预变性95 ℃,30 s,进入循环,变性95 ℃,5 s,退火60 ℃,34 s,循环40次,延伸95 ℃ 15 s,60 ℃ 60 s,95 ℃ 15 s。引物序列见Tab 1。
| Gene | Forward primer | Reverse primer |
| TGF-β1 | 5′-CGCATCCTAGACCCTTTCT CCTC-3′ | 5′-GGTGTCTCAGTATCCCACGGAAAT-3′ |
| FN | 5′-CTAGGCAATGCGTTGGTTT GTA-3′ | 5′-ACGCTCATAAGTGTCACCCACTC-3′ |
| LC3 | 5′-CCCCAGTGGATTAGGCAGAG -3′ | 5′-CCAAAAGAGCAACCCGAACA -3’ |
| Beclin-1 | 5′-GGGTCACCATCCAGGAACTCA-3′ | 5′-CACCATCCTGGCGAGTTTCA-3′ |
| β-actin | 5′-TGGCACCCAGCACAATG AA -3′ | 5′-CTAAGTCATAGTCCGCC TAGAAGCA -3′ |
使用统计软件SPSS 20.0进行分析。所有计量结果均采用x±s表示。多组均数之间比较采用单因素方差分析,组间差异比较采用t检验。
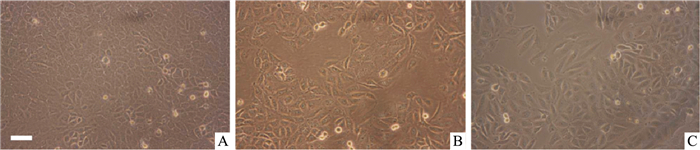
3 结果 3.1 EM对维持细胞形态的作用Control组HK-2细胞呈铺路石样,细胞状态良好,贴壁生长。TGF-β1模型组细胞形状改变明显,细胞间隙加大,拉长增大呈梭形,在形态上趋向于成纤维细胞,生长缓慢。与TGF-β1组相比,TGF-β1+EM组细胞形态改善明显,梭状形态减少,更接近Control组的细胞形态(Fig 1)。
|
| Fig 1 Cell morphology (scale bar:200 μm) A:Control; B:TGF-β1;C:TGF-β1+EM |
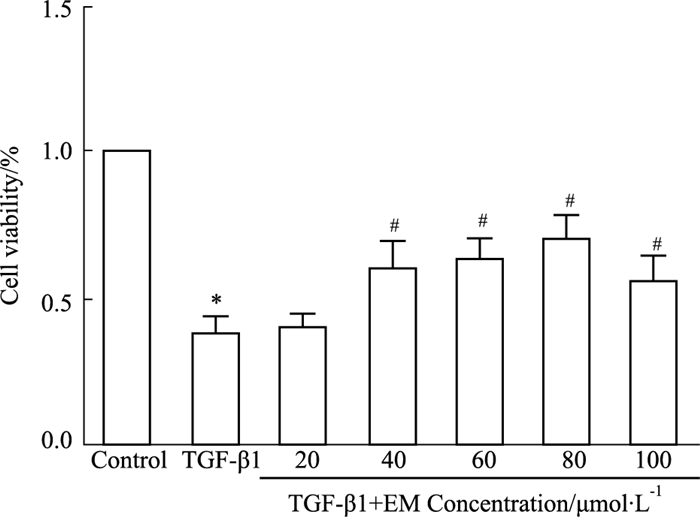
检测EM不同浓度对TGF-β1(10 μg·L-1)诱导HK-2细胞模型活性的影响。如Fig 2所示,TGF-β1组较Control组细胞活性明显下降(P < 0.05)。不同浓度的EM给药组中,EM 20 μmol·L-1与TGF-β1组差异无统计学意义,EM(40、60、80、100 μmol·L-1)与TGF-β1组相比,差异有统计学意义,而EM 40 μmol·L-1与EM 60 μmol·L-1组对细胞活性的影响,差异无统计学意义,故在后期的实验中均选用40 μmol·L-1的浓度。
|
| Fig 2 Ability of cell proliferation increased in HK-2 cells as indicated by CCK-8 assay (x±s, n=4) *P < 0.05 vs control group; #P < 0.05 vs TGF-β1 group |
如Fig 3所示,与Control组相比,TGF-β1刺激HK-2细胞组TGF-β1和COL Ⅰ的蛋白表达水平升高(P < 0.01)。与TGF-β1组相比,TGF-β1+EM组TGF-β1和COL Ⅰ的蛋白表达水平降低(P < 0.05)。

|
| Fig 3 Effect of EM on expression of TGF-β1 and COL Ⅰ in HK-2 cells detected by Western blot (x±s, n=4) **P < 0.01 vs control group; #P < 0.05 vs TGF-β1 group |
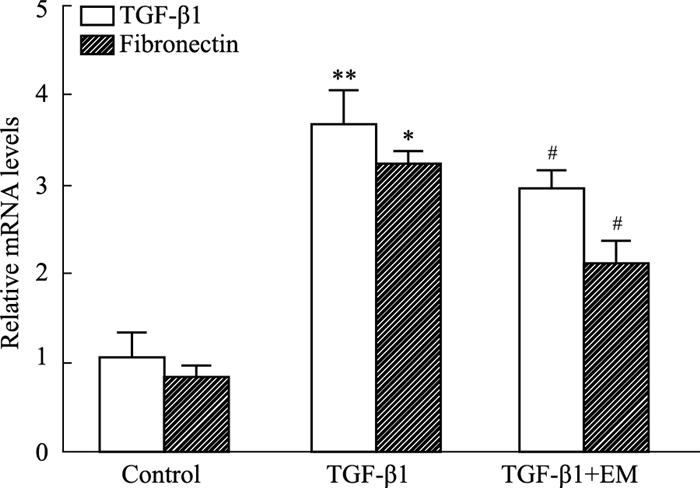
Fig 4的qPCR结果显示,与Control组相比,TGF-β1组纤维化相关分子TGF-β1、FN mRNA表达水平升高(P < 0.05)。与TGF-β1组相比,TGF-β1+EM组纤维化相关分子TGF-β1、FN mRNA表达水平降低(P < 0.05)。提示EM可以通过调控肾纤维化相关因子的表达,发挥抗纤维化作用。
|
| Fig 4 mRNA expression of TGF-β1 and FN in control, TGF-β1 and TGF-β1+EM groups by qPCR analysis(x±s, n=4~8) *P < 0.05, **P < 0.01 vs control group; #P < 0.05 vs TGF-β1 group |
Fig 5的免疫荧光结果显示,与Control组相比,TGF-β1组FN表达增加;与TGF-β1组相比,TGF-β1+EM组FN表达减少。说明EM可以减少TGF-β1刺激的HK-2细胞中纤维化相关蛋白的表达。

|
| Fig 5 Immunofluorescent staining images for FN in control, TGF-β1 and TGF-β1+EM groups as showed by representative micrographs(scale bar: 50 μm) |
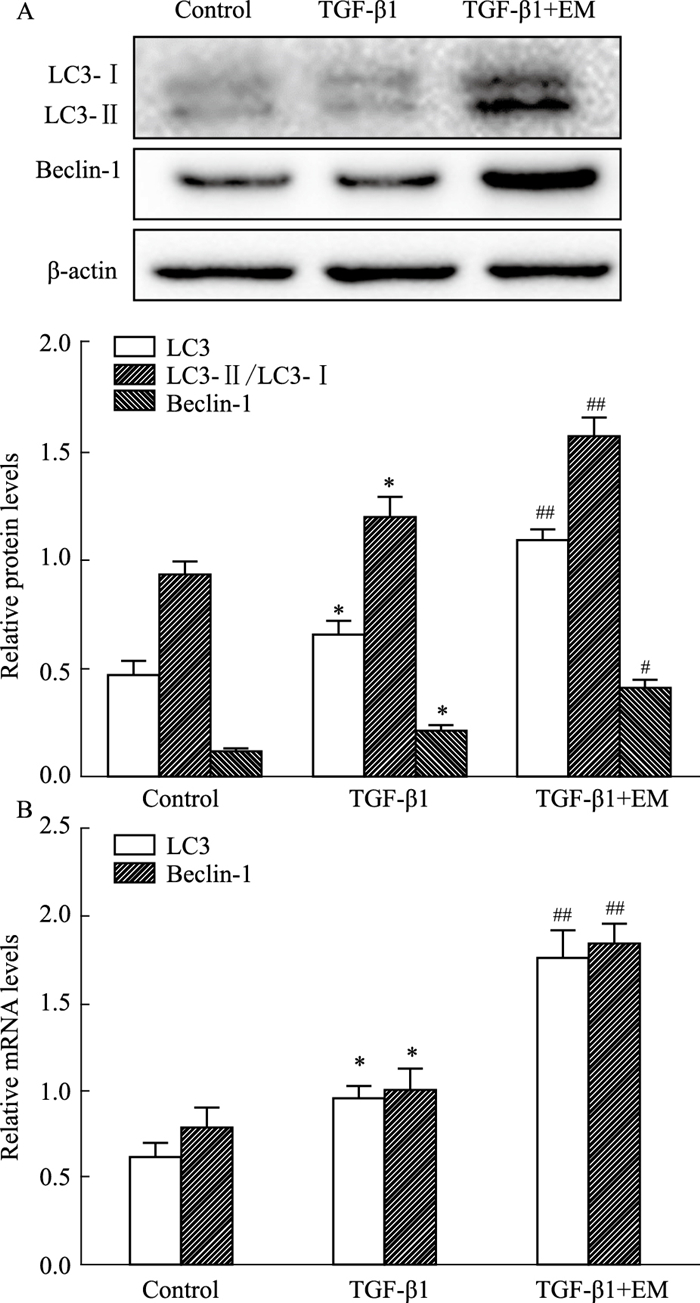
Fig 6的Western blot和qPCR结果显示,与Control组相比,TGF-β1组自噬标志性蛋白LC3、LC3-Ⅱ/LC3-Ⅰ、Beclin-1表达水平增加(P < 0.05)。与TGF-β1组相比,TGF-β1+EM组LC3、LC3-Ⅱ/LC3-Ⅰ、Beclin-1蛋白的表达水平增加,差异有统计学意义(P < 0.05,P < 0.01)。表明EM激活TGF-β1刺激HK-2细胞模型中的自噬。
|
| Fig 6 Expression of autophagy markers LC3 and Beclin-1 expression in HK-2 cells (x±s, n=4) A: Protein expression of LC3 and Beclin-1; B: mRNA levels of LC3 and Beclin-1. *P < 0.05 vs control group; #P < 0.05, ##P < 0.01 vs TGF-β1 group. |
TGF-β是公认的促肾纤维化细胞因子,能够通过多种途径参与肾纤维化的进展。Casalena等[7]发现,TGF-β能够直接增强肾小管上皮细胞-间充质细胞转分化,导致RIF。Piera等[8]发现,TGF-β能够引起细胞外基质的异常堆积,肾小球基底膜的增厚,进而加重RIF。本研究Western blot和qPCR结果表明,EM可以减轻TGF-β1刺激HK-2细胞引起的纤维化。因此,本研究对EM保护TGF-β1诱导的HK-2细胞模型的机制进行探讨。前期已有研究初步证实了大黄提取物及其药效成分的肾保护作用,本课题主要针对其肾损伤保护作用及可能机制进行探索,因此本研究未设阳性对照药物。
细胞内基础性自噬在正常生理状态下水平很低,起到了维持胞内稳态的作用,但在外界较强刺激下,自噬水平会增强,保护细胞及组织免受损伤[9]。自噬对肾脏细胞的稳态和存活起着关键作用,而自噬失调可能导致肾脏疾病的发展[10]。自噬对肾纤维化的作用机制引起科研人员极大的兴趣[11]。调控自噬,对肾脏生理功能以及疾病发展过程具有重要意义[12]。Kaushal等[13]发现在急性肾损伤中,敲除肾小管上皮细胞自噬相关基因,进一步加重肾纤维化。自噬和肾纤维化的研究,目前还处在初始阶段,自噬在纤维化中的作用存在争议,但随着更深入的研究,自噬可能成为一个新的防治和缓解肾纤维化的治疗靶点。
LC3-Ⅰ转化成LC3-Ⅱ是自噬小体形成的必需步骤,被认为是自噬小体形成的标志,LC3-Ⅱ/ LC3-Ⅰ的比值可反映自噬水平[14]。Western blot实验结果显示,LC3-Ⅱ条带比LC3-Ⅰ更明显,可能是因为LC3-Ⅰ比LC3-Ⅱ更不稳定,并且对抗体检测不太敏感。Western blot和qPCR实验结果证实,EM干预后,可以增加蛋白LC3、LC3-Ⅱ/LC3-Ⅰ、Beclin-1的表达,激活自噬。体外实验结果证实,EM干预后可以通过激活细胞自噬,改善细胞损伤。
本课题应用分子生物学技术和体外细胞模型,探究EM对细胞模型肾损伤的保护作用及分子机制,为EM有效防治肾纤维化提供实验依据。后期研究中,课题将对大黄组分EM临床应用以及EM药物剂型方面的优化进一步研究,以开发其在临床的应用价值。
( 致谢: 诚挚感谢第四军医大学西京医院病理科肖丽娜、张倩等,对实验给予的支持与帮助。)
| [1] | Webster A C, Nagler E V, Morton R L, Masson P. Chronic kidney disease[J]. Lancet, 2017, 389(10075): 1238-52. doi:10.1016/S0140-6736(16)32064-5 |
| [2] | Tooze S A, Abada A, Elazar Z. Endocytosis and autophagy: exploitation or cooperation[J]. Cold Spring Harb Perspect Biol, 2014, 6(5): a018358. doi:10.1101/cshperspect.a018358 |
| [3] | 杜春阳, 肖夏, 王鑫贵, 等. 鞘氨醇激酶1在肾间质纤维化中的作用及机制研究[J]. 中国药理学通报, 2017, 33(2): 212-8. Du C Y, Xiao X, Wang X G, et al. Role of SphK1 in renal tubulointerstitial fibrosis and its mechanism[J]. Chin Pharmacol Bull, 2017, 33(2): 212-8. doi:10.3969/j.issn.1001-1978.2017.02.014 |
| [4] | Kim W Y, Nam S A, Song H C, et al. The role of autophagy in unilateral ureteral obstruction rat model[J]. Nephrology, 2012, 17(2): 148-59. doi:10.1111/nep.2012.17.issue-2 |
| [5] | Ma L, Li H, Zhang S, et al. Emodin ameliorates renal fibrosis in rats via TGF-beta1/Smad signaling pathway and function study of Smurf 2[J]. Int Urol Nephrol, 2018, 50(2): 373-82. doi:10.1007/s11255-017-1757-x |
| [6] | Yang R, Xu X, Li H, et al. p53 induces miR199a-3p to suppress SOCS7 for STAT3 activation and renal fibrosis in UUO[J]. Sci Rep, 2017, 7: 43409. doi:10.1038/srep43409 |
| [7] | Casalena G, Daehn I, Bottinger E. Transforming growth factor-beta, bioenergetics, and mitochondria in renal disease[J]. Semin Nephrol, 2012, 32(3): 295-303. doi:10.1016/j.semnephrol.2012.04.009 |
| [8] | Piera V S, Li Z, Jimenez S A. Role of endothelial-mesenchymal transition (EndoMT) in the pathogenesis of fibrotic disorders[J]. Am J Pathol, 2011, 179(3): 1074-80. doi:10.1016/j.ajpath.2011.06.001 |
| [9] | Kaushal G P. Autophagy protects proximal tubular cells from injury and apoptosis[J]. Kidney Int, 2012, 82(12): 1250-3. doi:10.1038/ki.2012.337 |
| [10] | Yamamoto N K, Koike M, Asanuma K, et al. Cathepsin D in podocytes is important in the pathogenesis of proteinuria and CKD[J]. J Am Soc Nephrol, 2016, 27(9): 2685-700. |
| [11] | Lenoir O, Tharaux P L, Huber T B. Autophagy in kidney disease and aging: lessons from rodent models[J]. Kidney Int, 2016, 90(5): 950-64. doi:10.1016/j.kint.2016.04.014 |
| [12] | Kimura T, Isaka Y, Yoshimori T. Autophagy and kidney inflammation[J]. Autophagy, 2017, 13(6): 997-1003. doi:10.1080/15548627.2017.1309485 |
| [13] | Kaushal G P, Shah S V. Autophagy in acute kidney injury[J]. Kidney Int, 2016, 89(4): 779-91. doi:10.1016/j.kint.2015.11.021 |
| [14] | Jacquin E, Leclerc M S, Judon C, et al. Pharmacological modulators of autophagy activate a parallel noncanonical pathway driving unconventional LC3 lipidation[J]. Autophagy, 2017, 13(5): 854-67. doi:10.1080/15548627.2017.1287653 |

