


2. 天津市心血管重塑与靶器官损伤重点实验室,天津 300162;
3. 武警后勤学院附属医院心血管内科,天津 300162;
4. 武警后勤学院病原生物学教研室,天津 300309
2. Tianjin Key Lab of Cardiovascular Remodeling and Target Organ Injury, Logistics University of the Chinese People's Armed Police Force, Tianjin 300162, China;
3. Dept of Cardiology, the Affiliated Hospital of Logistics University of the Chinese People's Armed Police Force, Tianjin 300162, China;
4. Dept of Pathogen Biology, Logistics University of the Chinese People's Armed Police Force, Tianjin 300309, China
动脉粥样硬化(atherosclerosis,AS)是严重危害健康的常见心血管疾病,主要病理表现为动脉管壁内脂质沉积,进而形成粥样斑块。AS斑块破裂又可导致一系列严重后果,如心绞痛、心肌梗死、脑血管破裂,甚至猝死。近年研究发现,中性粒细胞可以释放核酸到细胞核外,与组蛋白和髓过氧化物酶等形成网状纤维结构,即中性粒细胞胞外陷阱(neutrophil extracellular traps,NETs),参与AS的病程进展[1-2]。此外,单核细胞的变化也贯穿AS发生、发展全过程,并与NETs的形成关系密切。鉴于NETs与单核细胞以及两者的交互影响在AS病程进展中的重要作用,对其进一步深入研究已成为防治AS的新方向。曲美他嗪(trimetazidine,TMZ)是临床常用的抗心绞痛药物,我们前期首次发现,TMZ可明显抑制小鼠缺血/再灌注损伤引发的左心室结构改变和功能障碍,改善缺血心肌的能量代谢,从而保护心肌组织损伤[3],但其能否通过调节NETs以及单核细胞亚群,影响AS进程尚未见报道。本研究初步探讨TMZ对AS的干预作用及潜在机制,为扩展TMZ的临床适应症,揭示其更多的药理学作用机制提供参考。
1 材料与方法 1.1 试剂与仪器TMZ、油红O购自Sigma公司;辛伐他汀购自广州南新制药有限公司(批号:BN 3139234);小鼠抗CD11b-PE、Ly6G-PerCP/Cy5.5、Ly6C-FITC抗体、Ly6G-PE抗体,均购自eBioscience公司;刺激剂(Leukocyte Activation Cocktail)购自BD公司;HistoneH3、羊抗兔IgG、髓过氧化物酶(myeloperoxidase,MPO)抗体、Hoechst 33258,均购自Abcam公司;甘油三酯(triglyceride, TG)、总胆固醇(total cholesterol, TC)检测分析试剂盒,购自南京建成生物工程研究所。小动物超声仪Vevosonic2100(加拿大Fujifilm VisualSonics公司);流式细胞仪Cytomics FC 500和BD FACSAriaTM Ⅲ(Beckman Coulter公司);冰冻切片机CM1850(德国Leica公司);显微镜ECLIPSE 80i(日本Nikon公司);荧光定量PCR仪ABI 7300(美国Applied Biosystems公司)。
1.2 实验动物8周龄♂ApoE-/-小鼠40只,C57BL/6小鼠10只,体质量(22.5±3.5)g,均购自天津市奥臣实验动物销售有限公司,动物批号:1601826。ApoE-/-小鼠实验前经DNA检测为纯合子。
1.3 动物模型的制备及药物干预所有实验动物适应性喂养1周。C57BL/6小鼠作为对照组,给予普通饮食;ApoE-/-小鼠给予高脂饮食(高脂饲料购自南通特洛菲饮食饲料科技有限公司,饲料代码:TP26303),饲养8周后,ApoE-/-小鼠随机分为4组(每组10只),依据以下分组,给予相应剂量的药物进行干预,分别为模型组(0.9% NaCl)、辛伐他汀组(3 mg·kg-1·d-1)、TMZ低、高剂量组(10、20 mg·kg-1·d-1)。连续灌胃12周后取材。
1.4 血脂含量检测实验结束后,各组小鼠2.5%异氟烷气体麻醉,眼球取血,静置30 min,3 000 r·min-1离心15 min,取上清,-80℃储存备用。根据试剂盒说明书,采用分光光度计检测各组小鼠血清TG和TC含量。
1.5 油红O染色各组小鼠以PBS灌流心脏,于主动脉根部上2 mm处留取心脏,沿左、右心耳下缘连线平行向下2 mm处去掉心尖部,留取心底部分,于30%的蔗糖溶液中脱水下沉后,OCT包埋,冰冻切片,厚度8 μm,常规油红O染色,光学显微镜下观察主动脉窦斑块面积及主动脉窦狭窄程度,使用Image-Pro Plus 6.0软件计算斑块面积及主动脉狭窄程度。
1.6 小动物超声检测主动脉弓内-中膜厚度(intima-media thickness,IMT)2.5%异氟烷气体麻醉小鼠后,将其固定于超声加热板,脱毛膏脱掉胸部绒毛,涂抹耦合剂,采用小动物超声检测内膜回声至中膜-外膜回声之间的垂直距离[4],于动脉收缩期测量3次,求平均值。
1.7 流式细胞术检测循环单核细胞抗凝EP管收集各组小鼠外周血,50 μL抗凝全血加入Ly6G-PerCP/Cy5.5、Ly6C-FITC、CD11b-PE,细胞染色缓冲液吹打混匀,室温避光孵育15 min,加入600 μL红细胞裂解液,流式细胞仪迅速上机检测,使用CXP2.0软件分析数据。
1.8 流式细胞术检测NETs水平[5]取100 μL外周血,500×g离心5 min后,弃上清,加入红细胞裂解液,2 min后,离心弃上清,用含2% BSA的DPBS重悬细胞,加入刺激剂,在37℃、5% CO2条件下孵育5 h,多聚甲醛固定,用含2% BSA的DPBS封闭过夜,复温后,加抗Histone H3在37℃孵育30 min,离心弃上清,重悬细胞,加入二抗IgG、MPO-FITC、Hoechst-DAPI、Ly6G-PE抗体,37℃孵育30 min,流式细胞仪检测,使用FlowJo 7.6.1软件分析结果。
1.9 qRT-PCR检测小鼠脾脏IL-1β、IL-18基因表达TRIzol法提取小鼠脾脏RNA,按照反转录cDNA合成试剂盒(Roche公司)说明书,将总RNA反转录为cDNA,取反转录后cDNA作为模板,使用SYBR Green Master进行定量PCR。扩增条件为:95 ℃预变性5 min,95 ℃变性15 s,60 ℃退火20 s,72 ℃延伸30 s,40个循环。以β-actin作为内参。每个样品分别设3个平行孔,反应总体系为20 μL,引物序列如下,β-actin:F 5′-CTAAGGCCAACCGT GAAAAG-3′, R 5′-ACCAGAGGCATACAGGGACA-3′; IL-1β:F 5′-AACGTGTGGGGGATGAATTG-3′, R 5′-CATACTCATCAAAGCAATGT-3′; IL-18:F 5′-ACTACCTCAACCGTTCCACG-3′, R 5′-TTCCCTCCGCATTGACACAG-3′。
1.10 统计学分析所有数据以x±s表示,GraphPad Prism 6软件进行统计学分析,组间对比采用单因素方差分析。
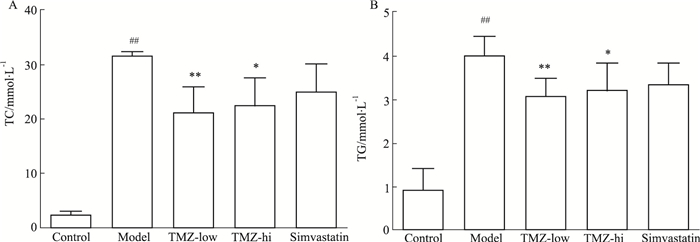
2 结果 2.1 TMZ对血脂水平的影响与普通饮食组小鼠相比,高脂饮食组小鼠体质量增长明显;给药后,小鼠体质量增长有一定程度减轻(数据未显示)。如Fig 1所示,与对照组相比,模型组TC、TG水平均明显升高(P < 0.05),TMZ干预后,模型鼠血脂水平明显降低(P < 0.01,P < 0.05)。
|
| Fig 1 Effects of trimetazidine on lipid TC(A) and TG(B) (x±s, n=10) ##P < 0.01 vs control; *P < 0.05, **P < 0.01 vs model |
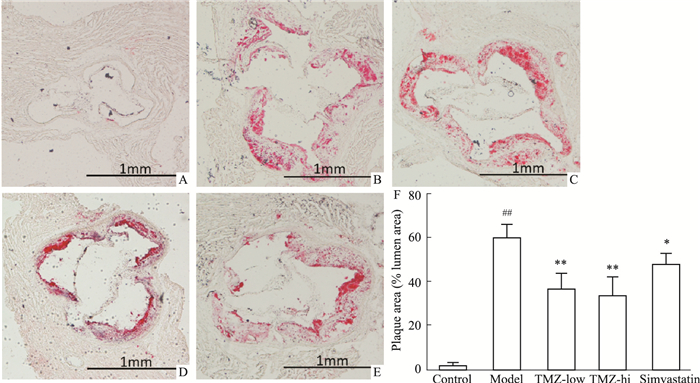
Fig 2的油红O染色结果显示,与对照组相比,模型组斑块负荷明显增多(P < 0.01),TMZ及辛伐他汀干预组均明显减少主动脉窦斑块负荷,与模型组相比差异具有显著性(P < 0.05),其中,TMZ低、高剂量组斑块负荷减少明显。
|
| Fig 2 Effects of trimetazidine on atherosclerotic lesions (x±s, n=10) A: Control group; B: Model group; C: Low-dose trimetazidine group; D: High-dose trimetazidine group; E: Simvastatin group; F: The area of plaque in aortic root. ##P < 0.01 vs control; *P < 0.05, **P < 0.01 vs model. |
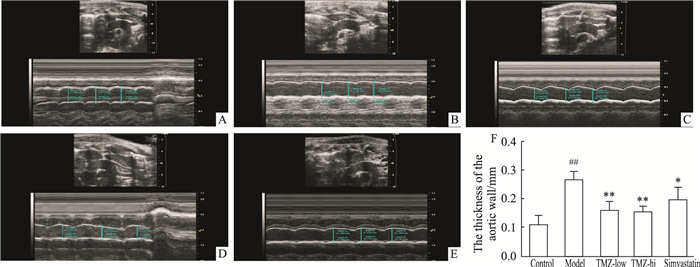
Fig 3的小动物超声检测结果显示,与对照组相比,模型组小鼠主动脉弓部血管IMT明显增加(P < 0.01);TMZ低、高剂量及辛伐他汀干预后,小鼠主动脉弓部血管IMT明显降低(P < 0.05),且TMZ低、高剂量组小鼠IMT减小程度相比辛伐他汀组更明显。
|
| Fig 3 Effects of trimetazidine on aortic IMT (x±s, n=10) A: Control group; B: Model group; C: Low-dose trimetazidine group; D: High-dose trimetazidine group; E: Simvastatin group; F:The thickness of the aortic wall. ##P < 0.01 vs control; *P < 0.05, **P < 0.01 vs model. |
如Fig 4所示,与对照组小鼠比较,模型组Ly6G-CD116+Ly6Chi单核细胞亚群比例明显增加(P < 0.01);TMZ低、高剂量组及辛伐他汀组明显降低小鼠Ly6G-CD116+Ly6Chi单核细胞亚群比例(P < 0.05),且TMZ高剂量组比低剂量组降低趋势更明显。

|
| Fig 4 Effects of trimetazidine on peripheral blood monocytes subset proportion (x±s, n=10) A: Gate strategy; B: Representative picture in each group; C: Percentage of monocyte subsets. ##P < 0.01 vs control; *P < 0.05, **P < 0.01 vs model. |
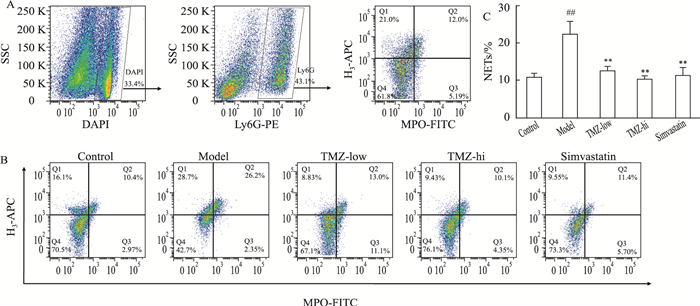
如Fig 5所示,与对照组小鼠比较,模型组小鼠NETs水平明显增加(P < 0.01);TMZ低、高剂量组及辛伐他汀组均明显降低模型小鼠NETs水平(P < 0.01),但TMZ不同剂量间量效关系不明显。
|
| Fig 5 Effects of trimetazidine on NETs (x±s, n=10) A: Gate strategy; B: Representative picture in each group; C: Percentage of NETs. ##P < 0.01 vs control; **P < 0.01 vs model. |
Fig 6实时定量PCR结果显示,与对照组相比,模型组小鼠IL-1β、IL-18基因表达明显上调(P < 0.01);与模型组相比,TMZ低、高剂量组及辛伐他汀组小鼠IL-1β、IL-18基因表达水平均明显下降(P < 0.01,P < 0.05)。

|
| Fig 6 Effects of trimetazidine on gene expression levels of IL-1β and IL-18 (x±s, n=10) ##P < 0.01 vs control; *P < 0.05, **P < 0.01 vs model |
AS是由血脂异常引起,并由固有免疫和适应性免疫反应介导的慢性炎症性疾病。炎症反应是AS进展各个阶段的关键因素,其中促炎细胞因子加速AS进展,抗炎细胞因子改善疾病。因此,抑制免疫激活及其介导的炎症反应是针对AS的重要治疗策略。单核细胞作为AS进展中重要的炎症免疫反应细胞早已被证实,通常可分为促炎M1型和抑炎M2型两种经典表型,分别对应于小鼠的Ly6Chi和Ly6Clo细胞亚群。Ly6Chi单核细胞被认为是炎症状态下巨噬细胞和树突状细胞的前体,Ly6Clo单核细胞代表组织巨噬细胞的稳态前体细胞。研究发现,脂质代谢紊乱会使单核细胞向促炎型偏移,外周单核细胞亦可经C-C基序趋化因子配体2(CCL2)与其受体CCR2相互作用,穿过内皮屏障,朝炎症部位募集[6],从而参与或加重AS的病程进展。我们前期亦证实,ApoE-/-小鼠模型中,炎症性单核细胞亚群比例随AS病变的加重而升高[7]。
AS中另一种重要的炎症相关固有免疫细胞中性粒细胞可通过NETs介导炎症反应,NETs形成过程中释放的MPO、DNA、抗微生物肽LL37等,可形成LL37-DNA复合物,并进入单核细胞,刺激DNA传感器分泌干扰素α(interferon α,IFN-α),也会激活NF-κB通路,进一步产生大量炎症因子,如IL-1β、TNF-α。因此,NETs已经成为炎症性心血管疾病血管新的监测指标[8]。新近研究表明,NETs与单核细胞在AS过程中能够相互作用,放大炎症反应。例如,在AS早期阶段,中性粒细胞可通过释放类似导管素的刺激素,促进经典单核细胞聚集,Cl-Amidine(脱氨活性抑制剂)处理抑制肽精氨酸脱亚胺酶,能预防中性粒细胞形成NETs,从而降低AS斑块负荷,延缓颈动脉内血栓形成[9]。炎症因子中,IL-18、IL-1β属于相同结构家族。单核细胞是IL-1β的主要来源,IL-1β在单核细胞中会增强炎症反应,并促进AS斑块的不稳定性[10]。此外,AS中的胆固醇晶体亦能引发中性粒细胞释放NETs,进而诱导巨噬细胞释放炎症因子IL-1β等,并激活T细胞,促进AS斑块中的免疫细胞募集[11]。多效促炎因子IL-18可以在IFN-γ诱导下,由单核细胞产生[12],并参与AS进展和斑块破裂,且在AS斑块中明显高表达。ApoE-/-小鼠给予IL-18可加速AS进展,IL-18结合蛋白(一种内源性IL-18抑制剂)的过度表达则抑制AS发生。特别是中性粒细胞浸润以及NETs的形成,也会刺激IL-1β和IL-18分泌,加速AS病程进展[11]。可见,IL-18、IL-1β与单核细胞和NETs关系密切,能够共同影响AS的发生、发展。
TMZ是一种促进心肌能量代谢的药物,在心肌缺血时可以通过调节脂肪酸和葡萄糖的氧化,提高心脏功能。近年发现,TMZ还具有良好的抗炎活性,例如,心衰动物模型给予TMZ治疗后,可使血浆C反应蛋白、TNF-α、IL-6等炎症因子水平明显下降[13]。在糖尿病大鼠模型中,TMZ能增强心脏舒张功能,其对心脏保护作用的机制可能与抑制炎症因子TNF-α,改善氧化应激损伤等有关[14]。此外,TMZ还能有效抑制炎症反应、膜破坏和氧化应激,减轻巨噬细胞浸润,从而明显改善脂多糖诱导的败血症、心肌功能障碍和心肌细胞凋亡。进一步机制研究显示,TMZ通过作用于Sirt1、AMPK、PPARα等信号通路,减轻巨噬细胞介导的炎症反应[15],但其是否能通过抗炎活性,发挥对AS的保护作用尚不明确。
本研究中,我们以高脂饮食诱导ApoE-/-小鼠为研究对象,首次应用TMZ进行干预。结果显示,TMZ及辛伐他汀都明显降低小鼠TC和TG的水平,抑制主动脉弓IMT增加,减少斑块面积,提示TMZ能够有效减轻AS斑块负荷,实验条件下,甚至优于辛伐他汀阳性对照组。此外,TMZ在明显减少NETs水平的同时,明显下调外周血Ly6Chi单核细胞比例,并且明显抑制炎症因子IL-1β、IL-18的基因表达。提示TMZ通过减少NETs表达,抑制单核细胞的炎症性偏移,从而减轻中性粒细胞和单核细胞介导的炎症反应,改善AS的病程进展。需要说明的是,本研究只是在动物水平上初步探讨了TMZ对AS的干预作用,并证实其通过调控NETs及炎症性单核细胞亚群,发挥抗AS效应,但对其具体的作用环节和分子机制等问题,仍需进一步研究阐明。
综上所述,TMZ作为游离脂肪酸氧化抑制剂,在临床上主要用于治疗缺血性心脏病和慢性心力衰竭,改善心室功能,尚未见其在AS治疗中的应用。本研究结果表明,TMZ不仅能有效改善AS的脂质代谢失衡,还明显抑制炎症性单核细胞亚群,调节NETs水平,为进一步拓展其临床应用提供了依据。
( 致谢: 本实验在天津市心血管重塑与靶器官损伤重点实验室完成,感谢各位老师和同学的支持!)
| [1] | Jorch S K, Kubes P. An emerging role for neutrophil extracellular traps in noninfectious disease[J]. Nat Med, 2017, 23(3): 279-87. doi:10.1038/nm.4294 |
| [2] | Döring Y, Soehnlein O, Weber C. Neutrophil extracellular traps in atherosclerosis and atherothrombosis[J]. Circ Res, 2017, 120(4): 736-43. doi:10.1161/CIRCRESAHA.116.309692 |
| [3] | 王婷, 毕莹, 陈泽富, 等. 曲美他嗪对小鼠急性心肌缺血再灌注损伤的保护作用[J]. 中华实用诊断与治疗杂志, 2017, 31(5): 427-30. Wang T, Bi Y, Chen Z F, et al. The protective effect of trimetazidine on acute myocardial ischemia-reperfusion injury in mice[J]. J Chin Integr Tradit Nephrol, 2017, 31(5): 427-30. |
| [4] | Qin M, Luo Y, Meng X B, et al. Myricitrin attenuates endothelial cell apoptosis to prevent atherosclerosis: an insight into PI3K/Akt activation and STAT3 signaling pathways[J]. Vasc Pharmacol, 2015, 70: 23-34. doi:10.1016/j.vph.2015.03.002 |
| [5] | Gavillet M, Martinod K, Renella R, et al. Flow cytometric assay for direct quantification of neutrophil extracellular traps in blood samples[J]. Am J Hematol, 2015, 90(12): 1155-8. doi:10.1002/ajh.24185 |
| [6] | 姜懿纳, 陈乃宏. CCL2/MCP-1在其相关疾病的机制研究[J]. 中国药理学通报, 2016, 32(12): 1634-8. Jiang Y N, Chen N H. Mechanism of CCL2/MCP-1 in related disease[J]. Chin Pharmacol Bull, 2016, 32(12): 1634-8. doi:10.3969/j.issn.1001-1978.2016.12.002 |
| [7] | 李宵, 周欣, 姬文婕, 等. 载脂蛋白E基因敲除小鼠动脉粥样硬化病变进展过程中循环单核细胞亚群和斑块内增殖巨噬细胞的动态变化[J]. 中国动脉硬化杂志, 2015, 23(1): 24-8. Li X, Zhou X, Ji W J, et al. Dynamic changes of circulating monocyte subpopulations and proliferating macrophages in the progression of atherosclerosis lesions in apolipoprotein E knockout mice[J]. Chin J Arterioscler, 2015, 23(1): 24-8. |
| [8] | 贾庆龄, 杨琨, 唐莎, 等. 中性粒细胞胞外诱捕网对单核细胞分泌炎症介质的影响[J]. 中国中西医结合肾病杂志, 2017, 18(5): 389-92. Jia Q L, Yang K, Tang S, et al. Effects of extracellular trapping network of neutrophils on the secretion of inflammatory mediators by monocytes[J]. Chin J Integr Tradit Nephrol, 2017, 18(5): 389-92. doi:10.3969/j.issn.1009-587X.2017.05.006 |
| [9] | Montecucco F, Liberale L, Bonaventura A, et al. The role of inflammation in cardiovascular outcome[J]. Curr Atheroscler Rep, 2017, 19(3): 11. doi:10.1007/s11883-017-0646-1 |
| [10] | Sieve I, Ricke-Hoch M, Kasten M, et al. A positive feedback loop between IL-1β, LPS and NEU1 may promote atherosclerosis by enhancing a pro-inflammatory state in monocytes and macrophages[J]. Vascul Pharmacol, 2018, 103-105: 16-28. doi:10.1016/j.vph.2018.01.005 |
| [11] | Westerterp M, Fotakis P, ouimet M, et al. Cholesterol efflux pathways suppress inflammasome activation, NETosis and atherogenesis[J]. Circulation, 2018. pii: CIRCULATIONAHA.117.032636. doi: 10.1161/CIRCULATIONAHA.117.032636. http://www.ncbi.nlm.nih.gov/pubmed/29588315 |
| [12] | Bhat O M, Kumar P U, Rao K R, et al. Terminalia arjuna prevents interleukin-18-induced atherosclerosis via modulation of NF-kappaB/PPAR-gamma-mediated pathway in ApoE-/- mice[J]. Inflammopharmacology, 2018, 26(2): 583-98. doi:10.1007/s10787-017-0357-9 |
| [13] | 潘霭青, 黄润坚, 邝锦波. 曲美他嗪对慢性心力衰竭患者血清炎症因子水平及心功能的影响[J]. 广州医药, 2017, 48(2): 79-81. Pan A Q, Huang R J, Kuang J B. Effect of trimetazidine on serum inflammatory factors and cardiac function in patients with chronic heart failure[J]. Guangzhou Med J, 2017, 48(2): 79-81. doi:10.3969/j.issn.1000-8535.2017.02.022 |
| [14] | 赵云跃, 钟钧琳, 谢冬梅, 等. 曲美他嗪降低1型糖尿病大鼠心肌组织炎症反应和氧化应激水平[J]. 中山大学学报(医学科学版), 2016, 37(3): 390-5. Zhao Y Y, Zhong J L, Xie D M, et al. Trimetazidine reduces myocardial inflammation and oxidative stress in type 1 diabetic rats[J]. J Sun Yat-sen Univ (Med Sci), 2016, 37(3): 390-5. |
| [15] | 陈静.曲美他嗪通过Sirt1缓解巨噬细胞介导的脓毒症心肌病及其机制研究[D].武汉: 华中科技大学, 2016. Chen J. Relief of macrophage mediated sepsis cardiomyopathy by trimetazidine through Sirt1[D]. Wuhan: Huazhong University of Science and Technology, 2016. http://www.wanfangdata.com.cn/details/detail.do?_type=degree&id=D01077741 |

