

2. 贵州医科大学省部共建药用植物功效与利用国家重点实验室,贵州 贵阳 550014;
3. 贵州省人民医院干医科,贵州 贵阳 550002;
4. 贵州省中国科学院天然产物化学重点实验室,贵州 贵阳 550014;
5. 贵州师范大学化学与材料科学学院,贵州 贵阳 550001
2. State Key Lab of Functions and Applications of Medicinal Plants, Guizhou Medical University, Guiyang 550014, China;
3. General Ward, Guizhou Provincial People's Hospital, Guiyang 550002, China;
4. Key Lab of Chemistry for Natural Products, Guizhou Province and Chinese Academy of Science, Guiyang 550014, China;
5. School of Chemistry & Material Science, Guizhou Normal University, Guiyang 550001, China
血管内皮细胞功能的损伤与动脉粥样硬化、冠心病、糖尿病、慢性肾功能衰竭、肿瘤等疾病的病理过程直接相关[1-2],因此,血管内皮细胞保护是防治相关疾病的关键环节。多种因素可以导致血管内皮细胞损伤,其中补体过度激活所产生的物质会作用于内皮细胞,从而引发细胞结构、功能等改变[3],导致内皮细胞产生炎症反应和功能失调。槲皮素类化合物是一种多羟基黄酮类化合物,具有抗炎、镇痛、抗癌、抗缺氧损伤、抗血小板凝聚、降血压、保护动脉粥样硬化等作用[4-7]。本实验室前期实验筛选发现,槲皮素对补体旁路激活血管内皮细胞具有保护作用,为了进一步了解槲皮素类化合物的保护作用,我们选择了槲皮素(1)及其衍生物槲皮苷(2)、异槲皮素(3)、芦丁(4)、金丝桃苷(5)、异鼠李素(6)6种化合物(结构见Fig 1),采用补体旁路激活产物诱导微血管内皮细胞发生炎症反应的细胞模型,考察了上述槲皮素类衍生物对内皮细胞炎症反应的干预作用。

|
| Fig 1 Structures of quercetin derivatives(1~6) |
永生的人微血管内皮细胞株(human microvascular endothelial cell, HMEC)、眼镜蛇毒因子(cobra venom factor, CVF),均由本课题组提供,其中CVF的分离纯化和检测方法参照文献[8];RPMI 1640培养基(美国Gibco公司);四氮唑盐购自美国Sigma公司;胎牛血清(fetal bovine serum,FBS)(天津灏洋生物科技);pRL-TK质粒、pGL 4.32(luc2P/NF-κB-RE/Hygro)质粒、双萤光素酶报告基因检测试剂盒(美国Promega公司);质粒抽提试剂盒、Lipofecter脂质体转染试剂(江苏碧云天生物技术研究所);人细胞间黏附分子1(intracellular cell adhesion molecule 1, ICAM-1)、血管细胞黏附分子1(vascular cell adhesion molecule 1, VCAM-1)、E-选择素(E-selectin)、肿瘤坏死因子α(tumor necrosis factor α, TNF-α)等ELISA试剂盒(武汉博士德生物工程有限公司);槲皮素、槲皮苷、异槲皮素、金丝桃苷、芦丁等化合物(成都普瑞法科技有限公司);正常人血清(normal human serum, NHS)由本实验室健康志愿者献血提供,经补体活性检测后,分装,-80 ℃冻存备用;NHS在56 ℃水浴孵育30 min,制备灭活人血清(inactivated normal human serum,INHS);其余试剂均为符合要求的实验分析纯。
1.2 仪器CO2培养箱、超低温冰箱(美国Thermo公司);倒置相差显微镜(日本Nikon公司);5810R冷冻离心机(德国Eppendorf公司);连续波长酶标仪(美国Molecular Devices公司);超纯水系统(美国Millipore公司)。
1.3 方法 1.3.1 细胞培养HMEC由本课题组传代培养,用含15%胎牛血清的RPMI 1640培养基,在37 ℃、5% CO2饱和湿度培养箱内培养,收集对数生长期细胞进行实验。
1.3.2 补体旁路激活产物的制备CVF与NHS按一定比例混合,37 ℃水浴30 min,制备NHS与CVF激活产物(CVF activated complement,CAC)。同时设置对照组INHS与CVF的孵育产物。
1.3.3 样品对HMEC细胞活力的影响将HMEC以每孔1×104个接种于96孔细胞培养板,细胞培养24 h后,损伤组加入10 μL的槲皮素及其衍生物(终浓度为1×10-10、1×10-11 mol·L-1),正常对照组加入10 μL生理盐水。培养24 h后,每孔加入5 g·L-1 MTT 20 μL,培养4 h后,每孔加入三联液50 μL,24 h后,在570 nm处测定OD值。
1.3.4 样品对CAC刺激的HMEC中ICAM-1、VCAM-1、E-selectin的影响参照文献[9-10]方法,HMEC以每孔1×104个接种于96孔细胞培养板,继续培养24 h后弃上清,干预组分别加入10 μL槲皮素及其衍生物(浓度为1×10-10、1×10-11 mol·L-1),正常对照组和模型组加入10 μL生理盐水,培养2 h后,损伤组和模型组加入30 μL CAC,各孔培养体系总体积为100 μL,继续培养6 h后,取上清液,离心,分装,-80 ℃冻存备用。
1.3.5 样品对CAC刺激的HMEC中TNF-α的影响参照文献[9-10]方法,HMEC以每孔1×104个接种于96孔细胞培养板,培养24 h后弃上清,干预组分别加入20 μL槲皮素及其衍生物(终浓度为1×10-10、1×10-11 mol·L-1),正常对照组和损伤组加入20 μL生理盐水,培养2 h后,损伤组和模型组加入60 μL CAC,各孔培养体系总体积为200 μL,继续培养24 h后,取上清液,离心,分装,-80 ℃冻存备用。
1.3.6 样品对CAC刺激HMEC诱导NF-κB核内转录活性上调的影响 1.3.6.1 质粒制备取1 μL重组质粒(1 ng)加入到100 μL感受态DH5α悬液中,混匀,冰水浴30 min,42 ℃水浴90 s,取出,再冰水浴3 min,然后加入900 μL LB培养基,置于37 ℃振荡培养45 min,取菌液100 μL均匀涂布于筛选平板上,置37 ℃培养过夜,挑取白色菌落进行扩增,按说明书抽提质粒。
1.3.6.2 双萤光素报告基因检测参照文献[11]方法,HMEC以每孔1×104个接种于96孔板,培养24 h后弃上清,用无血清RPMI 1640培养基洗2次,然后加入90 μL含血清RPMI 1640培养基,按Lipofecter脂质体转染试剂说明书进行转染。具体如下:将一定量NF-κB表达质粒和内参质粒,以及脂质体试剂与无血清RPMI 1640培养基混匀,20~25 ℃孵育20 min。然后,每孔加入该转染混合液10 μL,转染20 h后去除上清,干预组分别加入10 μL槲皮素及其衍生物(终浓度为1×10-10、1×10-11 mol·L-1),正常对照组和模型组加入10 μL生理盐水,37 ℃、5% CO2培养箱中孵育2 h,弃30 μL上清,加入30 μL CAC,使各孔培养体系总体积为100 μL,同时设置CVF与INHS的孵育物作对照,继续培养4 h,按双萤光素酶报告基因检测试剂盒说明书检测萤光强度,通过计算得到各组的相对核转录活性。
1.3.7 统计学分析实验数据以x±s表示,采用GraphPad Prism 5软件作图,组间比较采用SPSS 18.0进行单因素方差分析(LSD法)。
2 结果 2.1 槲皮素及其衍生物对细胞活力的影响Fig 2结果表明,不同浓度的化合物(1~6)作用于内皮细胞24 h后,与相同时间内的对照组比较无明显差异,说明在这些浓度下,槲皮素及其衍生物对细胞无明显毒性。
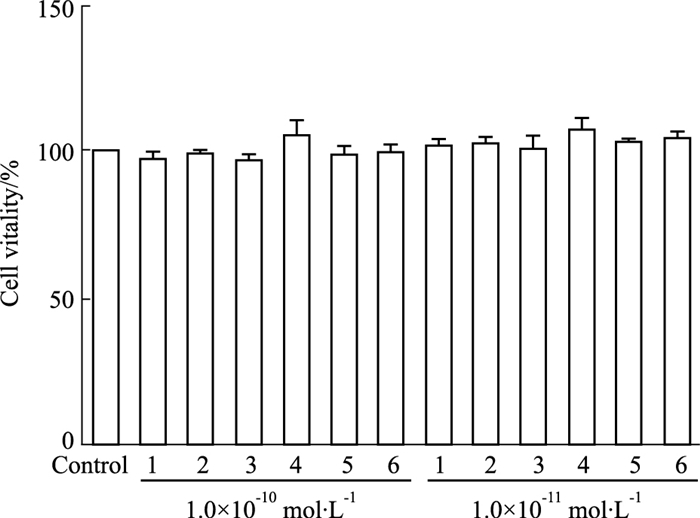
|
| Fig 2 Effects of compounds 1~6 on endothelial cell activity (x±s, n=3) |
如Fig 3所示,化合物1~6预处理内皮细胞后,在1×10-10 mol·L-1浓度下,均可不同程度地降低内皮细胞ICAM-1水平。降低样品浓度到1×10-11 mol·L-1,槲皮苷(2)、芦丁(4)和异鼠李素(6)对内皮细胞ICAM-1水平依然有明显的抑制作用(P < 0.05)。

|
| Fig 3 Effects of compounds 1~6 on ICAM-1 level in HMEC induced by CAC for 6 h(x±s, n=3) *P < 0.05, **P < 0.01 vs model; ##P < 0.01 vs control |
如Fig 4所示,在1×10-10 mol·L-1浓度下,槲皮素及其衍生物均可不同程度地降低内皮细胞VCAM-1水平,其中,槲皮苷(2)对内皮细胞VCAM-1水平有明显的抑制作用(P < 0.01),芦丁(4)对VCAM-1的抑制作用较为明显(P < 0.05)。

|
| Fig 4 Effects of compounds 1~6 on VCAM-1 level in HMEC induced by CAC for 6 h(x±s, n=3) *P < 0.05, **P < 0.01 vs model; ##P < 0.01 vs control |
如Fig 5所示,1×10-10 mol·L-1的槲皮素及其衍生物预处理内皮细胞后,可一定程度降低E-selectin水平。其中,1×10-10 mol·L-1的槲皮苷(2)和芦丁(4)对E-selectin水平的抑制作用较为明显(P < 0.05)。
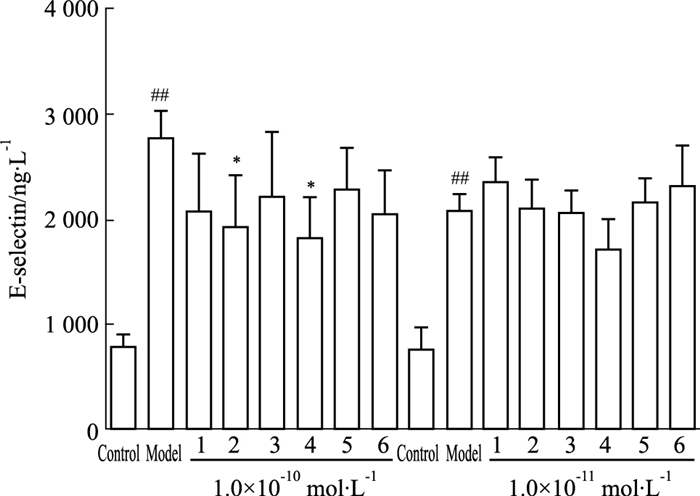
|
| Fig 5 Effects of compounds 1~6 on E-selectin level in HMEC induced by CAC for 6 h(x±s, n=3) *P < 0.05 vs model; ##P < 0.01 vs control |
如Fig 6所示,在1×10-10 mol·L-1浓度下,槲皮素及其衍生物均可不同程度地降低内皮细胞TNF-α水平。其中,槲皮素(1)、槲皮苷(2)、异槲皮素(3)、金丝桃苷(5)、异鼠李素(6)对TNF-α水平的抑制作用明显(P < 0.01)。在1×10-11 mol·L-1浓度下,各组TNF-α水平均低于模型组,但差异无显著性。

|
| Fig 6 Effects of compounds 1~6 on TNF-α level in HMEC induced by CAC for 24 h(x±s, n=3) **P < 0.01 vs model; ##P < 0.01 vs control |
如Fig 7所示,化合物1~6对内皮细胞因补体旁路激活产物引起的NF-κB核内转录活性上调,均表现出抑制作用(P < 0.01)。其中,槲皮苷和金丝桃苷的抑制作用最明显。

|
| Fig 7 Effects of compounds 1~6 on NF-κB transcriptional activity in HMEC induced by CAC (x±s, n=3) **P < 0.01 vs model; ##P < 0.01 vs control |
槲皮素及其衍生物均为黄酮类化合物,已报道具有多种生物活性[12-14]。基于前期研究,我们选择槲皮素和5种槲皮素的衍生物,考察了这些化合物对CAC诱导血管内皮细胞炎症反应的保护作用。结果显示,这些化合物对CAC诱导的内皮细胞炎症反应都有不同程度的保护作用,能明显下调由于CAC诱导炎症反应引起的炎症指标。在一定浓度时,槲皮苷(2)、芦丁(4)和异槲皮素(3)都表现出了明显抑制黏附因子ICAM-1水平的作用,其中,槲皮苷和芦丁还较明显地降低了VCAM-1、E-selectin的水平。同时,这些化合物均能下调因CAC诱导而明显升高的HMEC中NF-κB转录活性,提示槲皮素及其衍生物可能通过调节NF-κB信号通路,发挥其抗炎作用。
槲皮素(1)是一种典型的黄酮醇,其C-3位置的羟基引入1个鼠李糖后,转化为槲皮苷(2),而引入葡萄糖基团,就是异槲皮素(3),异槲皮素的葡萄糖基上再引入1个鼠李糖基后,就得到了芦丁(4)。化合物2~4都表现出了与槲皮素相当或更为明显的抗炎作用,说明在3-OH位置引入糖基进行糖苷化,有利于其抗炎活性提高,特别是糖链末端为鼠李糖基,影响最为明显,说明糖基的种类有较大影响,如金丝桃苷的糖基为半乳糖基,其对炎症介质的调节作用与槲皮素相比,没有明显变化。
槲皮素及其衍生物,特别是槲皮素的3-O-糖苷,已经逐步被证实具有明显的生理活性,特别是在心血管功能方面,发挥着重要的作用[15]。调节血管内皮细胞功能,可能是槲皮素及其衍生物发挥心血管保护作用的重要机制。而通过优化槲皮素衍生物的结构特征,是增强槲皮素衍生物生物利用度和活性强度的重要途径。本研究结果提示,3-O-糖基的种类对调节槲皮素衍生物的抗炎活性有一定的影响,其中,末端的鼠李糖基可能具有较好的增强抗炎作用。
( 致谢: 本研究在贵州省中国科学院天然产物化学重点实验室孙黔云研究员课题组完成,在此表示感谢。)
| [1] | Perez-Vizcaino F, Duarte J, Andriantsitohaina R. Endothelial function and cardiovascular disease: effects of quercetin and wine polyphenols[J]. Free Radic Res, 2006, 40(10): 1054-65. doi:10.1080/10715760600823128 |
| [2] | Rajendran P, Rengarajan T, Thangavel J, et al. The vascular endothelium and human diseases[J]. Int J Biol Sci, 2013, 9(10): 1057-69. doi:10.7150/ijbs.7502 |
| [3] | Bergseth G, Lambris J D, Mollnes T E, Lappegrd K T. Artificial surface-induced inflammation relies on complement factor 5: proof from a deficient person[J]. Ann Thorac Surg, 2011, 91(2): 527-33. doi:10.1016/j.athoracsur.2010.10.084 |
| [4] | Tong F, Liu S, Yan B, et al. Quercetin nanoparticle complex attenuated diabetic nephropathy via regulating the expression level of ICAM-1 on endothelium[J]. Int J Nanomedicine, 2017, 12: 7799-813. doi:10.2147/IJN |
| [5] | Stewart L K, Soileau J L, Ribnicky D, et al. Quercetin transiently increases energy expenditure but persistently decreases circulating markers of inflammation in C57BL/6J mice fed a high-fat diet[J]. Metabolism, 2008, 57(7 Suppl 1): S39-46. |
| [6] | Olaleye M T, Crown O O, Akinmoladun A C, Akindahunsi A A. Rutin and quercetin show greater efficacy than nifedipin in ameliorating hemodynamic, redox, and metabolite imbalances in sodium chloride-induced hypertensive rats[J]. Hum Exp Toxicol, 2014, 33(6): 602-8. doi:10.1177/0960327113504790 |
| [7] | Lin W, Wang W, Wang D, Ling W. Quercetin protects against atherosclerosis by inhibiting dendritic cell activation[J]. Mol Nutr Food Res, 2017, 61(9). doi:10.1002/mnfr.201700031 |
| [8] | 孙黔云, 李敏, 李红玲, 叶巧玲. 补体旁路激活导致内皮细胞的活化和损伤[J]. 中国药理学通报, 2012, 28(7): 925-9. Sun Q Y, Li M, Li H L, Ye Q L. Endothelial cell activation and injury induced by complement alternative pathway[J]. Chin Pharmacol Bull, 2012, 28(7): 925-9. doi:10.3969/j.issn.1001-1978.2012.07.010 |
| [9] | 路青瑜, 李敏, 孙黔云. 补体旁路激活致内皮细胞纤溶凝血相关分子表达变化及干预研究[J]. 中国药理学通报, 2015, 31(8): 1142-6. Lu Q Y, Li M, Sun Q Y. Expression of coagulation-and fibrinolysis-related molecules of endothelial cells induced by activated complement alternative pathway and intervention[J]. Chin Pharmacol Bull, 2015, 31(8): 1142-6. doi:10.3969/j.issn.1001-1978.2015.08.023 |
| [10] | 李朝胜, 孙黔云. 三种化学小分子对补体旁路激活致内皮细胞黏附分子表达的干预及机制研究[J]. 中国药理学通报, 2015, 31(10): 1421-6. Li C S, Sun Q Y. Effect of three chemical molecules on adhesion molecules expression in HEMCs induced by activated complement alternative pathway[J]. Chin Pharmacol Bull, 2015, 31(10): 1421-6. doi:10.3969/j.issn.1001-1978.2015.10.019 |
| [11] | 李敏, 孙玲, 孙黔云, 李红玲. 阿托伐他汀减轻氧化型低密度脂蛋白导致的人微血管内皮细胞活化和损伤[J]. 中国药理学通报, 2014, 30(5): 679-83. Li M, Sun L, Sun Q Y, Li H L. Atorvastatin attenuates activation and injury of human microvascular endothelial cells induced by oxidized low density lipoprotein[J]. Chin Pharmacol Bull, 2014, 30(5): 679-83. doi:10.3969/j.issn.1001-1978.2014.05.020 |
| [12] | Miladpour B, Rasti M, Owji A A, et al. Quercetin potentiates transdifferentiation of bone marrow mesenchymal stem cells into the beta cells in vitro[J]. J Endocrinol Invest, 2017, 40(5): 513-21. doi:10.1007/s40618-016-0592-8 |
| [13] | Oh Y S. Plant-derived compounds targeting pancreatic beta cells for the treatment of diabetes[J]. Evid Based Complement Alternat Med, 2015, 2015: 629863. |
| [14] | Fan Y F, Chen Z W, Guo Y, et al. Cellular mechanisms underlying hyperin-induced relaxation of rat basilar artery[J]. Fitoterapia, 2011, 82(4): 626-31. doi:10.1016/j.fitote.2011.01.023 |
| [15] | Terao J. Factors modulating bioavailability of quercetin-related flavonoids and the consequences of their vascular function[J]. Biochem Pharmacol, 2017, 139: 15-23. doi:10.1016/j.bcp.2017.03.021 |

