


2. 哈尔滨商业大学生命科学与环境科学研究中心,黑龙江 哈尔滨 150076
 ,
BAI Xue-lian1,2,
YANG Shu-xian1,
HAN Jia-yuan1,
ZHAO Qing-zhou1,
BAO Xiao-wei1,2,
LI Li-yong1,
CAO Li1
,
BAI Xue-lian1,2,
YANG Shu-xian1,
HAN Jia-yuan1,
ZHAO Qing-zhou1,
BAO Xiao-wei1,2,
LI Li-yong1,
CAO Li1

2. Research Center of Life Sciences and Environment Sciences, Harbin University of Commerce, Harbin 150076, China
人横纹肌肉瘤(rhabdomyosarcoma,RMS)来源于横纹肌细胞或向横纹肌细胞分化的间叶细胞,分化程度低而恶性程度高[1]。其发病率仅次于恶性纤维组织细胞瘤和脂肪肉瘤,位居软组织肉瘤的第3位。RMS主要分为3个亚型,分别为胚胎型横纹肌肉瘤(embryonal rhabdomyosarcomas,ERMS)、腺泡型横纹肌肉瘤(alveolar rhabdomyosarcoma,ARMS)和多形性横纹肌肉瘤(pleomorphic rhabdomyosarcoma,PRMS)[2]。ERMS好发于婴儿及儿童期,平均发病年龄为5岁,约占RMS的2/3。而ARMS好发于青少年,PRMS多发于成年。ERMS是儿童期最常见的一种高度恶性的软组织肉瘤,若手术能够完全切除,可达到较好的效果,但由于多种因素限制,仅有10%的患者能够完全切除。且ERMS易发生转移,在手术切除后必须结合后续治疗,目前,临床上仍采用放疗和细胞毒药物化疗等手段,对儿童的生长发育极为不利,需要寻找新的治疗药物。
注射用核糖核酸Ⅱ是一种上市多年的核酸类抗肿瘤药物,主要成分为牛胰脏组织提取的高纯度低分子RNA,广泛用于胰腺癌、肝癌、胃癌、肺癌、乳腺癌、软组织肉瘤等多种癌症的治疗。目前,关于注射用核糖核酸Ⅱ的文献报道多来自临床病例,关于其作用机制的研究依然缺乏。前期在多种细胞系的筛选实验中发现,人白血病K562细胞、人恶性胚胎横纹肌瘤RD细胞对注射用核糖核酸Ⅱ较为敏感,对于K562细胞的作用已有相关研究文献[3],而对于RD细胞的研究尚未见报道。因此,本研究探讨注射用核糖核酸Ⅱ对RD细胞的作用。
1 材料 1.1 药物与试剂注射用核糖核酸Ⅱ(规格50 mg)由吉林敖东药业提供;MTT(美国Sigma公司);Hoechst 33258、JC-1、细胞周期与细胞凋亡检测试剂盒(碧云天生物科技有限公司);吖啶橙(AO)/溴化乙锭(EB)双染试剂盒(美国Amresco公司);RIPA高效裂解液、PMSF、BCA蛋白检测试剂盒、DMEM高糖培养基(北京索莱宝科技有限公司);特级胎牛血清(加拿大Wisent公司);ECL显色试剂盒(康为世纪生物技术有限公司);β-actin、p-Akt、Bax、Bcl-2、caspase-8、caspase-3、羊抗兔IgG抗体(美国CST公司);p-JNK、p21、周期蛋白依赖性激酶2(cyclin-dependent kinase 2,CDK2)、CDK4抗体(美国Santa Cruz公司)。
1.2 仪器CO2细胞培养箱(日本Panasonic公司);Infinite M200 PRO酶标仪(瑞士Tecan公司);台式高速冷冻离心机(湘仪离心机仪器有限公司);荧光显微镜(Life公司);高内涵成像系统(美国Molecular Devices公司);流式细胞分析仪(美国Becton-Dickinson公司);垂直电泳仪(上海天能科技有限公司);凝胶成像系统(美国Bio-Rad公司)。
2 方法 2.1 细胞培养RD细胞购自中国医学科学院基础医学研究所细胞资源中心,培养在含有10%胎牛血清的DMEM培养基中,每天换液1次,2~3 d传代1次。
2.2 注射用核糖核酸Ⅱ贮备液的配制每次加药前,将1支注射用核糖核酸Ⅱ(50 mg冻干粉针剂)溶于5 mL的无菌DEPC水中,配制成浓度为10 g·L-1的贮备液,备用。
2.3 MTT法检测RD细胞存活率将处于对数生长期且状态良好的RD细胞,用0.25%胰蛋白酶-EDTA消化液消化,充分吹打混匀后计数,并用完全培养基将其稀释至8×107·L-1,以每孔0.1 mL接种到96孔板中,继续培养24 h后,用完全培养基对注射用核糖核酸Ⅱ贮备液进行稀释,各孔按组别加药0.1 mL(每组设4个复孔,下同),使药物终浓度分别为0、50、100、200、400、800 mg·L-1,作用24 h后,每孔加入5 g·L-1的MTT溶液10 μL,小心混匀,充分反应4 h后,弃去细胞上清液,加入150 μL DMSO,酶标仪震荡120 s,570 nm处测定吸光度(A)值,计算细胞存活率。根据细胞存活率结果计算半数抑制浓度(IC50),并确定给药浓度。细胞存活率=(A给药组-A空白组)/(A正常组-A空白组)×100%。
2.4 Hoechst 33258染色法检测RD细胞凋亡取处于对数生长期的RD细胞,胰酶消化,吹匀计数后,将细胞悬液稀释至5×108·L-1,以每孔1 mL接种于6孔板中,24 h后,分别加入不同浓度的含药完全培养基1 mL,使终浓度为125、250、500 mg·L-1,药物作用24 h,PBS洗2次,加入Hoechst 33258染色液0.5 mL,避光染色15 min,PBS洗掉多余染料。置于荧光显微镜下,观察并拍照。
2.5 AO/EB双染法检测RD细胞凋亡按照“2.4”项下同样的方法,接种细胞并给药,药物作用24 h后,PBS洗2次,加入AO :EB=1 :1的混合染色液0.5 mL,轻柔混匀,避光染色15 min,置于荧光显微镜下观察并拍照。
2.6 JC-1法检测RD细胞内线粒体膜电位严格按照JC-1试剂盒说明书配制各工作液。按照“2.3”项下同样的方法接种细胞,24 h后,分别加入不同浓度的含药完全培养基0.1 mL,使终浓度为125、250、500 mg·L-1,药物作用24 h后,加入0.1 mL的JC-1染色工作液,充分混匀,37 ℃避光孵育20 min后,弃去上清,用JC-1染色缓冲液洗涤2次。用荧光酶标仪检测荧光强度,490 nm/530 nm检测绿色荧光,525 nm/590 nm检测红色荧光,线粒体膜电位结果以红色/绿色荧光信号强度的比值表示。采用高内涵成像系统拍照。
2.7 流式细胞术检测RD细胞周期分布按照“2.4”项下同样的方法接种细胞并给药,24 h后,用胰蛋白酶消化收集细胞,与细胞上清液合并,1 500 r·min-1离心5 min,预冷的PBS洗2次,用体积分数为70%的冰乙醇小心混匀,-20 ℃固定过夜。离心,弃去乙醇固定液,PBS洗2次,弃上清,加入按照说明书配制好的碘化丙啶染色液0.5 mL,37 ℃避光染色30 min后,用流式细胞仪检测细胞周期。
2.8 Western blot检测RD细胞蛋白表达变化按照“2.4”项下同样的方法接种细胞并给药,24 h后,用胰蛋白酶消化收集各组细胞,与细胞上清液合并,1 500 r·min-1离心5 min,PBS洗2次。按体积比为RIPA :PMSF :蛋白磷酸酶抑制剂=98 :1 :1的比例配制裂解液,适量加入细胞中,充分涡旋,置于冰上,裂解40 min,20 min时重复涡旋混匀1次,12 000 r·min-1离心10 min,上清液即为细胞总蛋白,采用BCA法进行蛋白定量。按每孔45 μg上样,80 V进行SDS-PAGE凝胶电泳,300 mA恒流将已分离的蛋白条带转移到PVDF膜上,在质量分数5%的脱脂牛奶中封闭2 h,分别以1 :2 000稀释p-Akt、Bax、Bcl-2、caspase-8、caspase-3、β-actin抗体,以1 :500稀释p-JNK、p21、CDK2、CDK4抗体,置4 ℃孵育过夜。TBST洗3次后,二抗孵育2 h,TBST洗3次,加入ECL试剂使条带充分显色,于凝胶成像系统进行扫描并拍照,配套软件检测灰度值,各条带灰度值与对应β-actin灰度值的比值为该蛋白相对表达量。
2.9 统计学方法采用SPSS 21.0版,进行数据的统计分析,结果以x±s表示,组间比较采用单因素方差分析,LSD法检验组间差异。采用GraphPad Prism 5.0版作图。
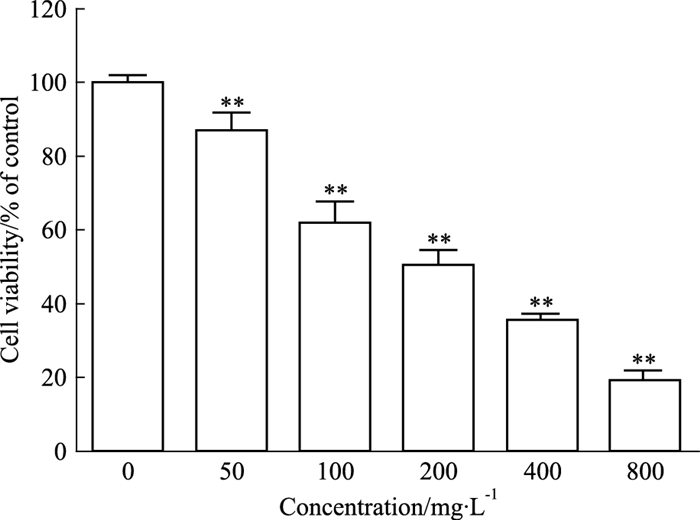
3 结果 3.1 注射用核糖核酸Ⅱ抑制RD细胞的增殖如Fig 1所示,注射用核糖核酸Ⅱ给药24 h后,与正常组(即给药浓度为0 mg·L-1)相比,各给药组细胞存活率明显降低(P < 0.01),且细胞存活率与给药浓度呈负相关,表明注射用核糖核酸Ⅱ对RD细胞增殖有明显抑制作用,且呈浓度依赖性。经计算,IC50为222 mg·L-1。因此,确定后续实验低、中、高给药组浓度分别为125、250、500 mg·L-1。
|
| Fig 1 Inhibitory effect on RD cells afterribonucleic acid Ⅱ treatment for 24 h(x±s, n=4) **P < 0.01 vs control |
如Fig 2所示,注射用核糖核酸Ⅱ给药24 h后,正常组细胞呈现正常的蓝色荧光,而各给药组细胞蓝色荧光出现不同程度的致密浓染,颜色发白,提示细胞进入凋亡状态。

|
| Fig 2 RD cell apoptosis detected by Hoechst 33258 staining A: 0 mg·L-1; B: 125 mg·L-1; C: 250 mg·L-1; D: 500 mg·L-1. |
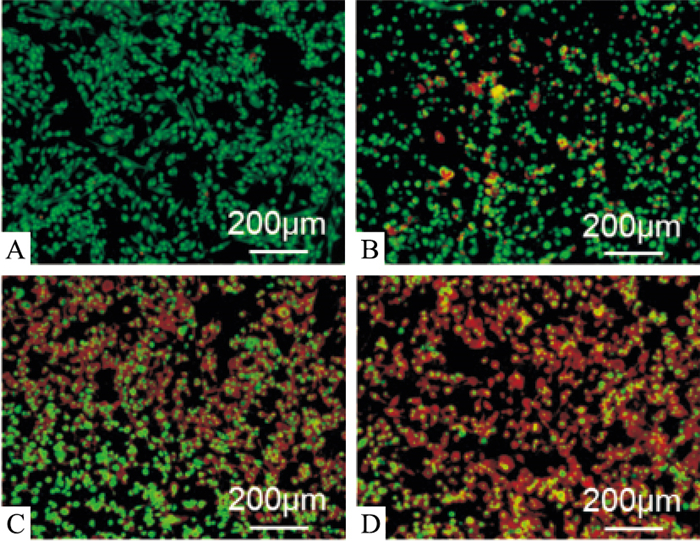
如Fig 3所示,注射用核糖核酸Ⅱ给药24 h后,正常组细胞的胞核呈现有层次的绿色荧光,细胞形态完整,未见凋亡。各给药组细胞荧光强度增加,呈均匀一致的圆状、团块状结构,出现明显的橘红色荧光,随着浓度的增加,橘红色荧光比例同时增加,表明注射用核糖核酸Ⅱ能够浓度依赖性地诱导RD细胞凋亡。
|
| Fig 3 RD cell apoptosis detected by AO/EB staining A: 0 mg·L-1; B: 125 mg·L-1; C: 250 mg·L-1; D: 500 mg·L-1. |
JC-1拍照(200倍)及线粒体膜电位统计结果见Fig 4,与正常组相比,随着给药浓度的增加,各给药组绿色荧光相应增强,红色荧光相应减弱,红色/绿色荧光强度比值明显降低(P < 0.01),表明注射用核糖核酸Ⅱ能够明显降低RD细胞线粒体膜电位,且呈浓度依赖性。

|
| Fig 4 Results of mitochondrion membrane potential(×200) A: 0 mg·L-1; B: 125 mg·L-1; C: 250 mg·L-1; D: 500 mg·L-1.**P < 0.01 vs control. |
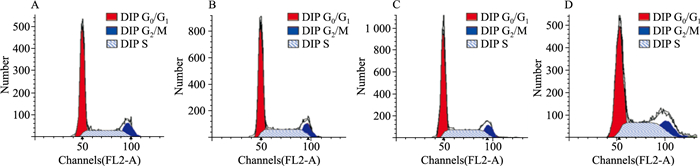
流式细胞术检测细胞周期分布的结果见Fig 5,各时期细胞所占比例见Tab 1。与正常组相比,给药24 h后,各给药组G0/G1期细胞比例明显降低,S期细胞比例明显增加(P < 0.01),表明注射用核糖核酸Ⅱ将RD细胞的染色体复制过程阻滞在S期。
|
| Fig 5 Effect of ribonucleic acid Ⅱ on RD cell cycle distribution A: 0 mg·L-1; B: 125 mg·L-1; C: 250 mg·L-1; D: 500 mg·L-1. |
| Concentration/mg·L-1 | G0/G1/% | S/% |
| 0 | 56.70±1.06 | 28.81±1.01 |
| 125 | 53.72±1.00* | 33.58±0.74** |
| 250 | 52.74±1.29** | 34.12±1.12** |
| 500 | 52.63±1.88** | 34.26±0.16** |
| *P < 0.05, **P < 0.01 vs control | ||
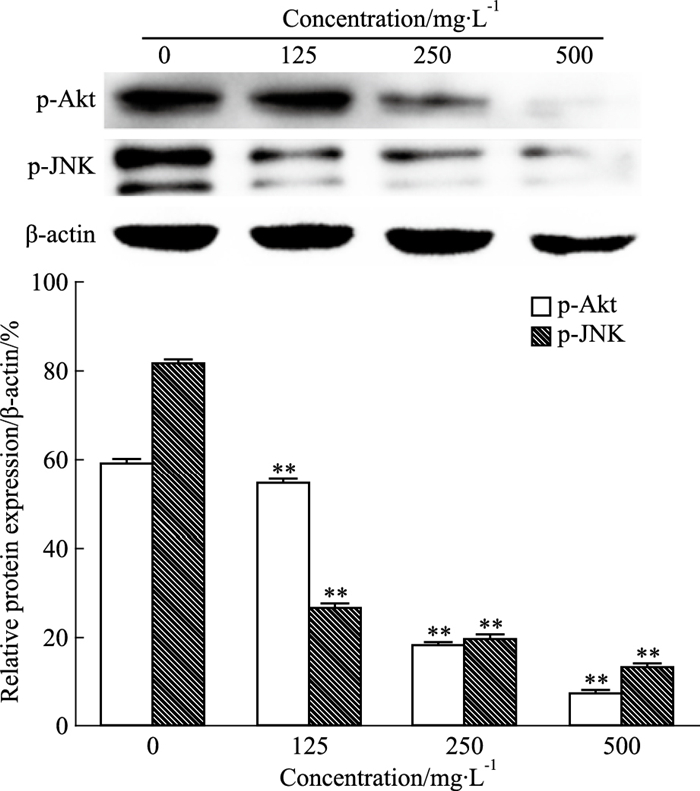
细胞周期相关蛋白表达结果见Fig 6。注射用核糖核酸Ⅱ对G1/S期关键蛋白信号通路发挥调控作用,与正常组相比,药物明显上调周期阻滞蛋白p21的表达,并下调CDK2、CDK4的表达,将细胞周期阻滞在G1/S期。如Fig 7所示,与正常组相比,注射用核糖核酸Ⅱ使RD细胞Akt、JNK磷酸化水平明显降低,表明RD细胞的生长发育过程受到抑制。

|
| Fig 6 Cell cycle-related protein expression after ribonucleicacid Ⅱ treatment for 24 h(x±s, n=3) **P < 0.01 vs control |
|
| Fig 7 Proliferation-related protein expression afterribonucleic acid Ⅱ treatment for 24 h(x±s, n=3) **P < 0.01 vs control |
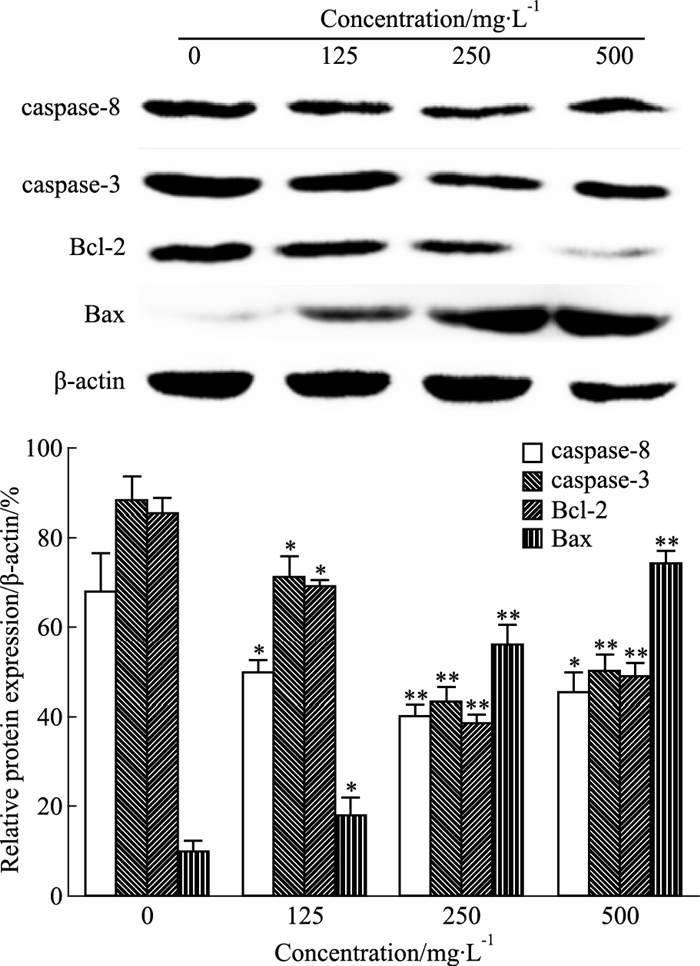
凋亡相关蛋白表达结果见Fig 8。与正常组相比,注射用核糖核酸Ⅱ明显下调抑凋亡蛋白Bcl-2表达,并上调促凋亡蛋白Bax的表达,caspase-8、caspase-3前体含量明显降低(P < 0.01),表明二者被大量激活,RD细胞发生凋亡。
|
| Fig 8 Apoptosis-related protein expression afterribonucleic acid Ⅱ treatment for 24 h(x±s, n=3) *P < 0.05, **P < 0.01 vs control |
在临床中,注射用核糖核酸Ⅱ单用或联合其他化疗药用于多种肿瘤治疗,可改善癌症患者生活质量,减轻由于放化疗导致的不良反应及免疫细胞数量下降[4]。据报道,注射用核糖核酸Ⅱ可增强小鼠腹腔巨噬细胞的吞噬能力,改善顺铂导致的外周血白细胞数量减少,提升脾脏T细胞的增殖能力,且与顺铂协同抑制小鼠腹水瘤S180细胞的增殖[5];通过抑制血管内皮生长因子(vascular endothelial growth factor,VEGF),抑制血管新生[6];通过上调p53调控Bcl-2/Bax的功能,激活线粒体凋亡通路,诱导人白血病K562细胞凋亡[3];降低周期调控关键蛋白cyclin D1的表达,将肝癌细胞的周期阻滞在G0/G1期,并下调基质金属蛋白酶-3(matrix metalloproteinase 3,MMP-3),抑制肝癌细胞的侵袭和迁移[7]。
几乎所有肿瘤的发生都与细胞周期相关,细胞周期的失控,导致肿瘤的发生。周期依赖性蛋白激酶(cyclin-dependent kinases,CDKs)是调控细胞周期的核心之一,其中以CDK4为主要因子,注射用核糖核酸Ⅱ对CDK4的下调直接导致了细胞周期的阻滞。p21是p53基因下游的CDKs抑制因子,注射用核糖核酸Ⅱ明显下调了p21的表达,CDK2的表达随之降低。CDK2、CDK4作为细胞周期信号通路的两个节点蛋白,二者表达量降低直接影响了整个通路的信息传递,导致细胞周期被阻滞在G1/S期。流式细胞术结果也显示,注射用核糖核酸Ⅱ主要将RD细胞阻滞在S期。
JNK是MAPK家族的成员之一,其主要的生物学功能为促进细胞的增殖发育,而不同细胞中JNK的生理功能有所不同。据报道,许多疾病的发生是由于JNK对正常细胞的促凋亡作用,如心肌细胞、神经细胞[8-10]等。而在一些肿瘤细胞中,JNK处于持续激活状态[11-12], 能够促进肿瘤细胞的增殖。注射用核糖核酸Ⅱ通过抑制Akt、JNK的磷酸化,抑制了肿瘤细胞的增殖,对RD细胞生长发育产生抑制作用。
正常生理状态下,Bcl-2可通过阻止该家族促凋亡蛋白Bax、Bak引起的DNA损伤,维持线粒体的完整性。实验结果表明,注射用核糖核酸Ⅱ明显下调了Bcl-2的表达,而Bax的表达量随之上调,Bcl-2/Bax比值明显降低,线粒体完整性被破坏。膜系统崩溃后,线粒体膜电位降低(与JC-1结果一致),生命活动受到抑制,细胞进入凋亡早期[13],随后,线粒体基质内大量的凋亡因子释放到细胞内。Caspase-8和caspase-3作为线粒体凋亡的起始者和执行者,其前体含量较正常组明显降低,意味着二者已被大量激活,促进细胞凋亡的发生。
综上,注射用核糖核酸Ⅱ通过上调p21的表达,抑制CDK2、CDK4的作用,将RD细胞的复制阻滞在S期;并通过调控Bcl-2/Bax,激活caspase-8、caspase-3,促进RD细胞凋亡,发挥抗人恶性胚胎横纹肌瘤的作用。实验中,注射用核糖核酸Ⅱ对一些信号分子的调控,可能是通过上游因子产生影响,也可能是直接产生调控作用,若要寻找其关键的作用位点,应排除因子间的相互干扰。另外,注射用核糖核酸Ⅱ为混合物,其具体的作用靶点仍未明确,就现有报道来看,其可能作用于肿瘤生长发育的多个环节,而其具体的作用靶点仍需进一步探究。
( 致谢: 本研究在中国医学科学院药用植物研究所药理毒理中心曹丽课题组实验室完成,衷心感谢实验室各位给予的帮助!)
| [1] | Rossi S, Stoppani E, Puri P L, et al. Differentiation of human rhabdomyosarcoma RD cells is regulated by reciprocal, functional interactions between myostatin, p38 and extracellular regulated kinase signalling pathways[J]. Eur J Cancer, 2011, 47(7): 1095-105. doi:10.1016/j.ejca.2010.12.010 |
| [2] | Parham D M, Barr F G. Classification of rhabdomyosarcoma and its molecular basis[J]. Adv Anat Pathol, 2013, 20(6): 387-97. doi:10.1097/PAP.0b013e3182a92d0d |
| [3] | 郭珮, 冉建华, 李静, 等. 注射用核糖核酸Ⅱ上调p53诱导人白血病细胞凋亡[J]. 中国药理学通报, 2016, 32(12): 1729-34. Guo P, Ran J H, Li J, et al. Ribonucleic acid Ⅱ induces apoptosis in human leukemia cells by up-regulating p53[J]. Chin Pharmacol Bull, 2016, 32(12): 1729-34. doi:10.3969/j.issn.1001-1978.2016.12.018 |
| [4] | 夏爱坤.注射用核糖核酸Ⅱ质量检测方法的研究[D].上海: 上海医药工业研究院, 2017. Xia A K. Study on quality inspection method of ribonucleic acidⅡfor injection[D]. Shanghai: Shanghai Institute of Pharmaceutical Industry, 2017. http://cdmd.cnki.com.cn/Article/CDMD-85901-1017203769.htm |
| [5] | 霍小位, 王灿红, 马晓玲, 等. 注射用免疫核糖核酸Ⅱ的免疫调节及对顺铂的增效减毒作用[J]. 中国医药生物技术, 2016, 11(1): 32-7. Huo X W, Wang C H, Ma X L, et al. Effects of BP on modulating sensitivity and toxicity of cisplatin and regulating immune function in S180 tumor-bearing mice[J]. Chin Med Biotechnol, 2016, 11(1): 32-7. doi:10.3969/j.issn.1673-713X.2016.01.007 |
| [6] | 牛晓晓, 金良昆. BP素在肿瘤治疗中的临床应用价值[J]. 医学综述, 2012, 18(2): 221-3. Niu X X, Jin L K. Clinical value of BP in tumor treatment[J]. Med Recap, 2012, 18(2): 221-3. doi:10.3969/j.issn.1006-2084.2012.02.022 |
| [7] | 吕晓婷, 郭珮, 宋丹, 等. 上调miR-320a对注射用核糖核酸Ⅱ诱导的肝癌Bel-7402细胞凋亡和迁移的影响[J]. 中国药理学通报, 2017, 33(11): 1503-10. Lyu X T, Guo P, Song D, et al. Effect of miR-320a up-regulation on apoptosis and migration of Bel-7402 cells induced by ribonucleic acid Ⅱ[J]. Chin Pharmacol Bull, 2017, 33(11): 1503-10. doi:10.3969/j.issn.1001-1978.2017.11.007 |
| [8] | Lai B, Pu H, Cao Q, et al. Activation of caspase-3 and c-Jun NH2-terminal kinase signaling pathways involving heroin-induced neuronal apoptosis[J]. Neurosci Lett, 2011, 502(3): 209-13. doi:10.1016/j.neulet.2011.07.046 |
| [9] | Anand S S, Babu P P. c-Jun N terminal kinases (JNK) are activated in the brain during the pathology of experimental cerebral malaria[J]. Neurosci Lett, 2011, 488(2): 118-22. doi:10.1016/j.neulet.2010.11.012 |
| [10] | Wang T, Gu J, Wu P F, et al. Protection by tetrahydroxystilbene glucoside against cerebral ischemia: involvement of JNK, SIRT1, and NF-kappaB pathways and inhibition of intracellular ROS/RNS generation[J]. Free Radic Biol Med, 2009, 47(3): 229-40. doi:10.1016/j.freeradbiomed.2009.02.027 |
| [11] | Xia H H, He H, De Wang J, et al. Induction of apoptosis and cell cycle arrest by a specific c-Jun NH2-terminal kinase(JNK) inhibitor, SP-600125, in gastrointestinal cancers[J]. Cancer Lett, 2006, 241(2): 268-74. doi:10.1016/j.canlet.2005.10.031 |
| [12] | Benoit M, Dormond-Meuwly A, Demartines N, et al. Targeting the JNK signaling pathway potentiates the antiproliferative efficacy of rapamycin in LS174T colon cancer cells[J]. J Surg Res, 2011, 167(2): e193-8. doi:10.1016/j.jss.2011.01.015 |
| [13] | Rostovtseva T K, Tan W, Colombini M. On the role of VDAC in apoptosis: fact and fiction[J]. J Bioenerg Biomembr, 2005, 37(3): 129-42. doi:10.1007/s10863-005-6566-8 |