

2. 中国药科大学药学院,江苏 南京 211198;
3. 中国药科大学基础医学与临床药学学院,江苏 南京 211198
 分别为(2.41±0.62) h、(2.81±1.16) h。与对照组相比,糖尿病大鼠肝脏中CYP3A1 mRNA和蛋白表达均明显增加。结论
硝苯地平在糖尿病大鼠体内的药代动力学发生明显改变,提示临床注意硝苯地平在糖尿病患者中安全、合理用药问题。
分别为(2.41±0.62) h、(2.81±1.16) h。与对照组相比,糖尿病大鼠肝脏中CYP3A1 mRNA和蛋白表达均明显增加。结论
硝苯地平在糖尿病大鼠体内的药代动力学发生明显改变,提示临床注意硝苯地平在糖尿病患者中安全、合理用药问题。2. School of Pharmacy, China Pharmaceutical University, Nanjing 211198, China;
3. School of Basic Medicine and Clinical Pharmacy, China Pharmaceutical University, Nanjing 211198, China
 was (2.41±0.62) h and (2.81±1.16) h, respectively. Compared with normal rats, the CYP3A1 protein expression and mRNA levels were significant higher in liver of diabetic rats.
Conclusion
The pharmacokinetics of nifedipine after oral administration were significantly changed in diabetic rat model compared to normal controls, which should be taken into consideration in clinical medication.
was (2.41±0.62) h and (2.81±1.16) h, respectively. Compared with normal rats, the CYP3A1 protein expression and mRNA levels were significant higher in liver of diabetic rats.
Conclusion
The pharmacokinetics of nifedipine after oral administration were significantly changed in diabetic rat model compared to normal controls, which should be taken into consideration in clinical medication.
硝苯地平是二氢吡啶类钙离子拮抗剂,临床广泛用于高血压和心绞痛的治疗,对心血管疾病临床症状的改善发挥重要作用。硝苯地平口服吸收迅速完全,血浆蛋白结合率高(90%左右),在体内主要由肝脏CYP3A4代谢,80%经肾排泄,20%经粪便排出。硝苯地平血药浓度与药理作用相关,对于高血压患者,其理想治疗浓度为10~100 μg·L-1[1],血药浓度波动易引起其降压效果改变及不良反应的发生。
糖尿病是一种慢性代谢性疾病,很多生理生化指标与蛋白功能发生改变,从而影响药物的吸收、分布、代谢、排泄过程,导致一些药物在糖尿病患者和糖尿病动物体内的药代动力学发生改变[2]。然而,尚未有研究报道硝苯地平在糖尿病状态下的药代动力学特征,因此,本研究比较正常及糖尿病状态下大鼠体内硝苯地平的药代动力学差异。
1 材料 1.1 实验动物SD大鼠,♂,体质量(170±10)g,由浙江省实验动物中心提供,许可证编号:SCXK(浙)2014-0001。
1.2 药物与试剂硝苯地平对照品(批号:100338-0001)、内标地西泮对照品(批号:171225-200302),均购于中国食品药品检定研究院;链脲佐菌素(streptozotocin,STZ),购于美国Sigma公司;一水柠檬酸(99.5%,批号:H1624005)、二水柠檬酸钠(≥99.0%,批号:C1624081),购于中国阿拉丁公司;抗CYP3A1抗体(货号:ab22724),购于英国Abcam公司;TRIzol购自美国Invitrogen公司;SYBRGreen realtime PCR master mix plus QPK212试剂盒,购自日本TOYOBO公司。
1.3 仪器API4000三重四级杆检测器、操作软件Analyst 1.5.1(美国应用生物系统有限公司产品);高效液相色谱系统(日本岛津公司产品);低温超速离心机5430R(德国Eppendorf公司产品);Vortex-Genie2涡旋震荡仪(美国Scientific Industries公司产品);StepOnePlus荧光定量PCR仪(美国ABI公司产品)。
2 方法 2.1 糖尿病大鼠模型的建立大鼠随机分为糖尿病模型组及正常对照组。大鼠适应性饲养3 d后,禁食不禁水12 h,模型组大鼠腹腔注射STZ 65 mg·kg-1,对照组大鼠注射溶媒(0.1 mol·L-1柠檬酸-柠檬酸钠缓冲液,pH 4.5)。3 d后测定大鼠空腹血糖,空腹血糖高于11.1 mmol·L-1的大鼠选入糖尿病模型组。在造模后的35 d进行实验。
2.2 生化指标的检测全自动生化分析仪检测血清葡萄糖(glucose,GLU)、总胆固醇(total cholesterol,TC)、三酰甘油(triacylglycerol,TG)、高密度脂蛋白胆固醇(high density lipoprotein cholesterol,HDL-C)和低密度脂蛋白胆固醇(low density lipoprotein cholesterol,LDL-C)水平[3]。
2.3 糖尿病大鼠灌胃硝苯地平后的药代动力学研究造模35 d后的模型组和对照组大鼠,按10 mg·kg-1体质量灌胃给予硝苯地平(硝苯地平用0.5%羧甲基纤维素钠溶液配制成1 g·L-1的混悬液,给药体积为10 mL·kg-1),于给药前和给药后15 min、30 min、45 min、1 h、1.5 h、2 h、4 h、8 h、12 h,眼底静脉丛取血0.3 mL,置肝素处理的EP管中,离心10 min,取血浆,-80 ℃保存待测。
2.4 大鼠血浆中硝苯地平浓度的测定[4] 2.4.1 样本处理精密吸取血浆样品50 μL,置于1.5 mL EP管中,加入50 μL乙腈,再加入100 μL含500 μg·L-1内标(地西泮)的乙腈,涡旋振荡5 min,于12 000 r·min-1离心10 min,取上清液10 μL进样分析,所用操作均在避光条件下进行。
2.4.2 HPLC-MS/MS测定方法使用前期建立的HPLC-MS/MS方法检测大鼠血浆中硝苯地平浓度[4]。色谱条件:岛津Shim-pack VP-ODS C18色谱柱(2.0 mm×150 mm,5 μm);流动相A:0.1%甲酸-水,流动相B:纯乙腈;流速:0.35 mL·min-1;柱温:40 ℃;进样体积:10 μL。采用梯度洗脱:0~0.5 min,A:B=90:10(V/V),0.5~2.0 min,A:B=20:80(V/V),2.0~4.0 min,A:B=20:80(V/V),4.0~4.3 min,A:B=90:10(V/V),4.3~5.5 min,A:B=90:10(V/V)。质谱条件:电喷雾离子源(ESI),正离子检测方式,喷雾电压5500 V,离子源温度450 ℃;气帘气为10 kPa;鞘气20 kPa;辅助气:20 kPa;硝苯地平和地西泮的去簇电压(DP)分别为33、100 V;碰撞能量(CE)分别为11、40 eV。扫描方式为多级反应监测(MRM),用于定量分析的离子反应分别为m/z 347.2→315.3(硝苯地平)和m/z 285.3→154.2(内标地西泮)。硝苯地平在2~1 000 μg·L-1范围内线性良好,定量下限为2 μg·L-1。该方法精密度、回收率、基质效应及稳定性均满足方法学要求。
2.5 Real-time PCR法测定CYP3A1 mRNA表达按TRIzol一步法提取大鼠肝组织的总RNA。逆转录操作按照试剂盒说明书进行,样品保存在-80 ℃。PCR反应体系参照荧光定量试剂盒说明书,以β-actin为内参基因,2-ΔΔCt法计算CYP3A1 mRNA的相对表达量变化倍数。CYP3A1引物序列为上游:5′-TGAAAGAAGTGTTTGGTGCCTAC-3′,下游:5′-ACTACTGACAAGAACAACGGATC-3′; β-actin引物序列为上游:5′-CATCAAGAAGGTGGTGAAGCA-3′,下游:5′-TCAAAGGTGGAGGAGTGGGT-3′。
2.6 Western blot测定CYP3A1蛋白表达大鼠肝组织(正常组和糖尿病组)均按照蛋白提取说明书提取总蛋白样本。经核酸定量仪测定后,100 ℃、5 min变性。加入5×SDS上样缓冲液,8% SDS-PAGE电泳80 V 50 min, 100 V 2.5 h转膜,10%脱脂奶粉37 ℃封闭1 h。TBST清洗10 min×3次,加入CYP3A1一抗(1: 500稀释) 37 ℃孵育2 h。TBST清洗10 min×3次,加入二抗(1:2 000)孵育1.5 h,再用TBST清洗10 min×3次。蛋白用ECL显影,于Bio-Rad化学发光成像分析仪中曝光。采用Quantity One图像分析软件分析结果,测得条带的灰度值,计算目的条带CYP3A1和内参GAPDH的比值。
2.7 数据分析血浆中硝苯地平的峰浓度(Cmax)和达峰时间(Tmax)由实测数据直接得出,其它参数如血药浓度-时间曲线下面积(AUC)、半衰期(
大鼠腹腔注射STZ造模35 d后,呈现非常明显的糖尿病症状(Tab 1):多饮、多食、多尿,体重明显下降,而血糖明显升高,是对照组的6.2倍(P < 0.01),表明糖尿病大鼠造模成功。此外,糖尿病大鼠血清中TC、TG、HDL-C和LDL-C水平均明显增加,分别是正常大鼠的4.1倍(P < 0.01)、13.1倍(P < 0.01)、1.7倍(P < 0.05)、8.3倍(P < 0.05)。
| Control | DM | |
| Body weight/g | 360.50±24.56 | 220.50±11.82** |
| GLU/mmol·L-1 | 5.16±1.27 | 32.08±3.04** |
| TC/mmol·L-1 | 1.75±0.51 | 7.11±2.14** |
| TG/mmol·L-1 | 1.50±0.57 | 19.62±9.13** |
| HDL-C/mmol·L-1 | 0.73±0.11 | 1.21±0.30* |
| LDL-C/mmol·L-1 | 0.11±0.03 | 0.91±0.35* |
| *P < 0.05, **P < 0.01 vs control group | ||
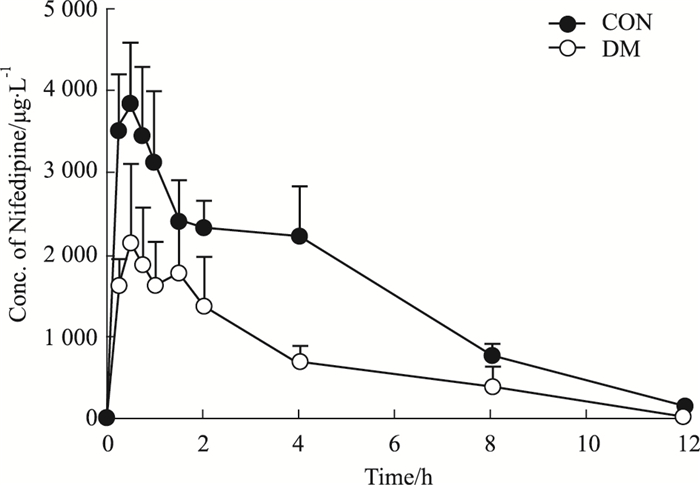
糖尿病组和对照组大鼠分别给予硝苯地平(10 mg·kg-1)灌胃后,测定不同时间点血浆中硝苯地平的浓度,平均血药浓度-时间曲线如Fig 1所示。糖尿病组大鼠硝苯地平各时间点的血药浓度均低于对照组大鼠。
|
| Fig 1 Plasma concentration-time curves of nifedipine after oral administration of nifedipine in diabetic and control group (n=6) |
糖尿病组和对照组大鼠的硝苯地平主要药代动力学参数见Tab 2。统计分析显示,糖尿病大鼠硝苯地平Cmax、AUC0-t及AUC0-∞明显低于对照组大鼠,CL/F和Vd/F明显增加,而Tmax和
| Parameter | Control | DM |
| Cmax/μg·L-1 | 3875.00±720.24 | 2295.00±875.00** |
| Tmax/h | 0.50±0.16 | 0.83±0.61 |
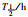 |
2.81±1.16 | 2.41±0.62 |
| CL/F/L·h-1·kg-1 | 0.53±0.09 | 1.25±0.36** |
| Vd/F/L·kg-1 | 2.11±0.68 | 4.41±1.88* |
| AUC0-t/μg·h·L-1 | 18072.42±2456.72 | 8377.54±2148.57** |
| AUC0-∞/μg·h·L-1 | 19180.21±3101.79 | 8514.22±2147.71** |
| *P < 0.05, **P < 0.01 vs control group | ||
如Fig 2、3所示,与对照组相比,糖尿病大鼠肝脏中CYP3A1 mRNA和蛋白表达均明显增加,CYP3A1 mRNA表达水平是对照组的1.77倍(P < 0.05),CYP3A1蛋白表达水平是对照组的1.84倍(P < 0.01)。

|
| Fig 2 Effect of diabetes on CYP3A1 mRNA level in rat liver (x±s, n=4) *P < 0.05 vs control group |

|
| Fig 3 Effect of diabetes on CYP3A1 protein expression in rat liver (x±s, n=4) **P < 0.01 vs control group |
大量研究表明,糖尿病以多种方式,如影响胃肠道转运时间、水和电解质平衡、血浆蛋白水平、组织血流速率、药物代谢酶和转运体等因素,导致药物的吸收、分布、代谢、排泄过程发生改变,从而影响一些药物的药代动力学。
本研究结果表明,糖尿病对硝苯地平在大鼠体内的药代动力学有较大的影响,使硝苯地平药物暴露量降低(Cmax、AUC明显下降)。CYP3A是一种重要的CYP450酶系,它在肝脏和肠道中含量最为丰富,临床上60%以上的药物都由其代谢。硝苯地平在人体内主要由CYP3A4代谢,在大鼠体内主要由CYP3A1/2代谢。有文献报道,糖尿病大鼠肝脏中药物代谢酶的功能与表达发生明显改变,其中CYP3A1/2的功能与表达与正常对照大鼠相比均明显升高[5]。本研究结果显示,糖尿病大鼠肝脏中CYP3A1 mRNA和蛋白表达均明显增加,这可能是导致硝苯地平在糖尿病大鼠体内代谢增加,清除加快,暴露减少的原因之一。此外,硝苯地平也是外排转运体P-gp的底物。P-gp在体内多种组织中高度表达,如肝、肠道、肾脏、大脑等,可以将药物逆浓度梯度从细胞内转运至细胞外,因此对药物的吸收和分布具有重要作用。有研究报道,糖尿病状态下,大鼠P-gp的功能及表达呈组织特异性改变[6]。可推测糖尿病状态下,P-gp的改变也会影响硝苯地平在体内吸收和分布。此外,硝苯地平在体内主要经肾排泄,糖尿病大鼠多饮、多尿可能也会对硝苯地平的排泄具有一定影响。糖尿病影响硝苯地平体内代谢过程的多个环节,各种影响因素的叠加,最终导致硝苯地平的血药浓度发生明显变化。
有关硝苯地平在糖尿病患者体内的药代动力学研究报道非常有限,近期1篇文献研究了妊娠合并2型糖尿病、高血压患者口服硝苯地平的药代动力学,发现在血糖得到控制的妊娠合并高血压患者中,2型糖尿病对硝苯地平的药代动力学没有影响[7]。动物实验和临床实验结果的不一致可能与糖尿病的种类、血糖是否控制、研究对象的种属、性别等因素有关,还有待进一步探索。
( 致谢: 本实验在中国药科大学基础医学与临床药学学院临床药代动力学研究室完成,对本实验的参与人员表示感谢。)
| [1] | 张新慧, 刘群, 褚志杰, 等. 硝苯地平口服制剂药代动力学影响因素[J]. 药学研究, 2016, 35(8): 475-8. Zhang X H, Liu Q, Chu Z J, et al. The influencing factors of pharmacokinetics of nifedipine oral preparation[J]. J Pharm Res, 2016, 35(8): 475-8. |
| [2] | Dostalek M, Akhlaghi F, PuzanovovaM. Effect of diabetes mellitus on pharmacokinetic and pharmacodynamic properties of drugs[J]. Clin Pharmacokinet, 2012, 51(8): 481-99. doi:10.1007/BF03261926 |
| [3] | 麦云珮, 张淑允, 窦纪梁, 等. 香芹酚对STZ诱导的1型糖尿病小鼠糖脂代谢的影响[J]. 中国药理学通报, 2016, 32(9): 1306-10. Mai Y P, Zhang S Y, Dou J L, et al. Effect of CAR on STZ-induced type 1 diabetic mice[J]. Chin Pharmacol Bull, 2016, 32(9): 1306-10. doi:10.3969/j.issn.1001-1978.2016.09.023 |
| [4] | 胡楠, 鲁晓雨, 赵娣, 等. LC-MS/MS法测定大鼠血浆中硝苯地平及其代谢物氧化硝苯地平的浓度[J]. 中国临床药理杂志, 2017, 33(23): 101-5. Hu N, Lu X Y, Zhao D, et al. Determination the concentration of nifedipine and its metabolite dehydronifedipine in rat plasma by LC-MS/MS[J]. Chin J ClinPharmacol, 2017, 33(23): 101-5. |
| [5] | Lee J H, Yang S H, Oh J M, et al. Pharmacokinetics of drugs in rats with diabetes mellitus induced by alloxan or streptozocin: comparison with those in patients with type Ⅰ diabetes mellitus[J]. J Pharm Pharmacol, 2010, 62(1): 1-23. doi:10.1211/jpp.62.01.0001 |
| [6] | Zhang L L, Lu L, Jin S, et al. Tissue-specific alterations in expression and function of P-glycoprotein in streptozotocin-induced diabetic rats[J]. Acta Pharmacol Sin, 2011, 32(7): 956-66. doi:10.1038/aps.2011.33 |
| [7] | Filgueira G C O, Filgueira O A S, Carvalho D M, et al. Effect of type 2 diabetes mellitus on the pharmacokinetics and transplacental transfer of nifedipine in hypertensive pregnant women[J]. Br J Clin Pharmacol, 2017, 83(7): 1571-9. doi:10.1111/bcp.v83.7 |

